某种牛奶的营养成分表如下所示(NRV%是指每100g食品中营养素的含量占该营养素每日摄入量的比例)。
回答下列问题。
(1)成分表中含有的元素有Na、Ca、H、C、N、O,其中位于同周期的元素是___________ (填元素名称)。
(2)Na在元素周期表中的位置是___________ ,它与氧元素形成的常见化合物中含有非极性共价键,其电子式为___________ 。
(3)比较下列物质的性质,用“>”或“<”填空。
①半径:r(Na+)___________ r(O2-);②沸点:NH3___________ CH4
(4)设计实验证明Ca、Mg都能与水反应,且比较它们与水反应的难易程度。
(限选试剂与仪器:烧杯、小试管、胶头滴管、酚酞、蒸馏水、钙、镁条、砂纸)
| 营养成分表 | ||
| 项目 | 每100g | NRV% |
| 能量 | 309kJ | 4% |
| 蛋白质 | 3.6g | 4% |
| 脂肪 | 4.4g | 7% |
| 碳水化合物 | 5.0g | 2% |
| 钠 | 65mg | 3% |
| 钙 | 120mg | 15% |
(1)成分表中含有的元素有Na、Ca、H、C、N、O,其中位于同周期的元素是
(2)Na在元素周期表中的位置是
(3)比较下列物质的性质,用“>”或“<”填空。
①半径:r(Na+)
(4)设计实验证明Ca、Mg都能与水反应,且比较它们与水反应的难易程度。
(限选试剂与仪器:烧杯、小试管、胶头滴管、酚酞、蒸馏水、钙、镁条、砂纸)
| Ca | Mg | |
| 操作 | 取绿豆大小的一块钙投入盛有水的 | 将打磨后的镁条投入盛有冷水的试管中。 |
| 现象 | 钙先沉入水中,表面产生大量气体,一段时间后上浮,溶液变浑浊。 | 一段时间后,镁条表面有细小气泡产生。 |
| 描述或推测 | ①钙密度比水大; ②溶液中产生的沉淀主要是 | 由细小气泡猜测Mg可能与水发生反应,还需要补充的实验操作及现象是 |
| 结论 | 钙能与水反应生成沉淀和氢气,且反应剧烈。 | 镁能与水缓慢反应,化学方程式为 |
更新时间:2023-07-07 07:20:20
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】如图是元素周期表的一部分,回答下列问题。
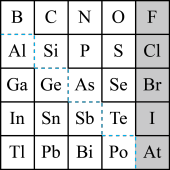
(1)元素 在元素周期表中的位置为
在元素周期表中的位置为_______ (写明周期数和族序数)。
(2) 的最高正价为
的最高正价为_______ , 的最高价氧化物为
的最高价氧化物为_______ (填化学式)。
(3)根据元素周期律推断:
①阴影部分元素最容易与氢气化合的是_______ (填元素符号)。
②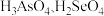 的酸性强弱:
的酸性强弱:
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
③氢化物的还原性:
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(4)可在图中分界线(虚线部分)附近寻找_______(填序号)。
(5)① 常用作溶剂,其电子式为
常用作溶剂,其电子式为_______ 。
②镓( )的化合物氮化镓(
)的化合物氮化镓( )和砷化镓(
)和砷化镓( )作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。下列说法正确的是
)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。下列说法正确的是_______ (填序号)。
A.原子半径: B.N的非金属性比O强
B.N的非金属性比O强
C. 的金属性比
的金属性比 弱 D.
弱 D. 和
和 的氧化物可能是两性氧化物
的氧化物可能是两性氧化物
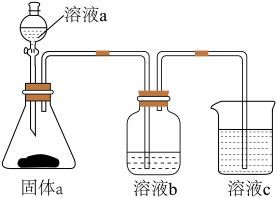
(6)用如图装置证明酸性: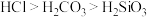 ,则溶液b为
,则溶液b为_______ 。下列事实可用于比较元素C与 非金属性相对强弱的是
非金属性相对强弱的是_______ (填序号)。
A.最高正化合价
B. 的氢化物比C的简单氢化物稳定
的氢化物比C的简单氢化物稳定
C. 的氢化物比C的简单氢化物沸点高
的氢化物比C的简单氢化物沸点高
D.最高价氧化物对应的水化物的酸性: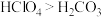

(1)元素
 在元素周期表中的位置为
在元素周期表中的位置为(2)
 的最高正价为
的最高正价为 的最高价氧化物为
的最高价氧化物为(3)根据元素周期律推断:
①阴影部分元素最容易与氢气化合的是
②
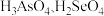 的酸性强弱:
的酸性强弱:
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。③氢化物的还原性:

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(4)可在图中分界线(虚线部分)附近寻找_______(填序号)。
| A.农药 | B.合金材料 | C.半导体材料 | D.优良的催化剂 |
 常用作溶剂,其电子式为
常用作溶剂,其电子式为②镓(
 )的化合物氮化镓(
)的化合物氮化镓( )和砷化镓(
)和砷化镓( )作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。下列说法正确的是
)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。下列说法正确的是A.原子半径:
 B.N的非金属性比O强
B.N的非金属性比O强C.
 的金属性比
的金属性比 弱 D.
弱 D. 和
和 的氧化物可能是两性氧化物
的氧化物可能是两性氧化物(6)用如图装置证明酸性:
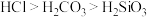 ,则溶液b为
,则溶液b为 非金属性相对强弱的是
非金属性相对强弱的是
A.最高正化合价

B.
 的氢化物比C的简单氢化物稳定
的氢化物比C的简单氢化物稳定C.
 的氢化物比C的简单氢化物沸点高
的氢化物比C的简单氢化物沸点高D.最高价氧化物对应的水化物的酸性:
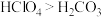
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素周期表和元素周期律的应用
(1)根据同周期、同主族元素性质的递变规律判断元素性质的_______________ 。
(2)应用于_______________ 元素的相互推断。
(3)预测新元素
为新元素的发现及预测它们的_______________ 提供线索。
(4)寻找新物质
①在金属与非金属分界线附近寻找_______________ 。
②研究_______________ 附近元素,制造新农药。
③在_______________ 中寻找催化剂和耐高温、耐腐蚀的合金材料。
(1)根据同周期、同主族元素性质的递变规律判断元素性质的
(2)应用于
(3)预测新元素
为新元素的发现及预测它们的
(4)寻找新物质
①在金属与非金属分界线附近寻找
②研究
③在
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据要求填空(所涉及元素均为前20号)
(1)A元素的原子M层有5个电子,则其原子结构示意图为__________________ ;最高价氯化物的化学式_______________________ 。
(2)C元素原子最外层电子是最内层电子的3倍,其形成的离子与Ar元素有相同的电子结构,请写出C离子的结构示意图和电子式:________________ 、_________ 。
(3)标出下列反应的电子转移方向和数目,并填写有关内容:
KClO3+6HCl→3Cl2↑+3H2O+KCl、___________
氧化剂______________ ;氧化产物______________ ;还原剂______________ ;还原产物______________ ;被氧化的元素______________ ;HCl的作用______________ .
(1)A元素的原子M层有5个电子,则其原子结构示意图为
(2)C元素原子最外层电子是最内层电子的3倍,其形成的离子与Ar元素有相同的电子结构,请写出C离子的结构示意图和电子式:
(3)标出下列反应的电子转移方向和数目,并填写有关内容:
KClO3+6HCl→3Cl2↑+3H2O+KCl、
氧化剂
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)在③~⑦元素中,原子半径最大的元素是________ ,其离子结构示意图为________
(2)元素的最高价氧化物对应的水化物中酸性最强的物质是________ ,碱性最强的物质是_______ ,呈两性的氢氧化物是________ ;
(3)按要求写出下列两种物质的电子式:①的氢化物________ ;⑨的最高价氧化物对应的水化物________ ;
(4)在⑦与⑩的单质中,化学性质较活泼的是_______ ,可用什么化学反应说明该事实(写出反应的化学方程式):_____________ .
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
(2)元素的最高价氧化物对应的水化物中酸性最强的物质是
(3)按要求写出下列两种物质的电子式:①的氢化物
(4)在⑦与⑩的单质中,化学性质较活泼的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】水泥是人类最伟大的发明之一,主要成分为硅酸三钙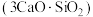 。将其与适量的水反应,形成相互交联的结构,发生的反应为
。将其与适量的水反应,形成相互交联的结构,发生的反应为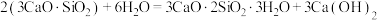 。回答下列问题:
。回答下列问题:
(1)为了加快硅酸三钙与水的反应速率,可采用的方式为_______ (填一种即可)。
(2)Si在元素周期表中的位置为_______ 。
(3) 的电子式为
的电子式为_______ , 的空间结构为
的空间结构为_______ 。
(4)元素C、O、Si、Ca的原子半径由大到小的顺序为_______ 。
(5)带有玻璃塞的磨口玻璃瓶不能用来盛装NaOH溶液的原因为_______ (用化学方程式表示)。
(6)写出 在农业上的一种用途:
在农业上的一种用途:_______ 。
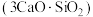 。将其与适量的水反应,形成相互交联的结构,发生的反应为
。将其与适量的水反应,形成相互交联的结构,发生的反应为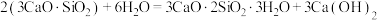 。回答下列问题:
。回答下列问题:(1)为了加快硅酸三钙与水的反应速率,可采用的方式为
(2)Si在元素周期表中的位置为
(3)
 的电子式为
的电子式为 的空间结构为
的空间结构为(4)元素C、O、Si、Ca的原子半径由大到小的顺序为
(5)带有玻璃塞的磨口玻璃瓶不能用来盛装NaOH溶液的原因为
(6)写出
 在农业上的一种用途:
在农业上的一种用途:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表为元素周期表的一部分,表中所列的字母分别代表一种化学元素。
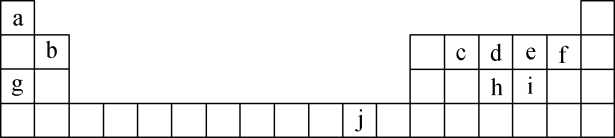
回答下列问题:
(1)写出元素f的基态原子核外电子排布式:____ 。
(2)写出元素h的基态原子核外电子轨道表示式:________ 。
(3)基态b原子电子占据最高能级的电子云轮廓图为_________
(4)ce2分子的电子式为____ 。
(5)d、g、h的原子半径由小到大的顺序是_______ (用元素符号表示)
(6)用一个化学方程式证明e、i的非金属性的强弱_________ 。
(7)d的简单氢化物比h的简单氢化物沸点____ (填“高”或“低”),请分析其原因____ ,写出j的原子结构示意图_____________

回答下列问题:
(1)写出元素f的基态原子核外电子排布式:
(2)写出元素h的基态原子核外电子轨道表示式:
(3)基态b原子电子占据最高能级的电子云轮廓图为
(4)ce2分子的电子式为
(5)d、g、h的原子半径由小到大的顺序是
(6)用一个化学方程式证明e、i的非金属性的强弱
(7)d的简单氢化物比h的简单氢化物沸点
您最近一年使用:0次
【推荐1】干冰晶体中,每个CO2周围等距且紧邻的CO2有___________ 个。在冰的结构模型中,每个水分子最多与相邻的___________ 个水分子相连接。同为分子晶体,但干冰中CO2的配位数(即一个分子周围最邻近的分子的数目)大于冰中水分子的配位数,其原因是___________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
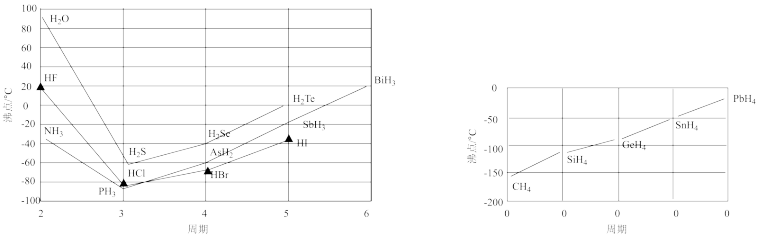
【推荐2】下列现象与氢键有关的是_____________
①乙醇、乙酸可以和水以任意比互溶
②NH3的熔沸点比PH3的熔沸点高
③稳定性:HF>HCl
④邻羟基苯甲酸的熔沸点比对羟基苯甲酸的低
⑤水分子高温下也很稳定
①乙醇、乙酸可以和水以任意比互溶
②NH3的熔沸点比PH3的熔沸点高
③稳定性:HF>HCl
④邻羟基苯甲酸的熔沸点比对羟基苯甲酸的低
⑤水分子高温下也很稳定
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】为探究 溶液中的离子平衡和离子反应,某小组同学进行了如下实验。
溶液中的离子平衡和离子反应,某小组同学进行了如下实验。
(1)配制:50 mL 1.0 mol⋅L-1的 溶液,测其pH约为0.7,即
溶液,测其pH约为0.7,即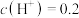 mol⋅L-1。用离子方程式解释
mol⋅L-1。用离子方程式解释 溶液呈酸性的原因:
溶液呈酸性的原因:___________ 。
(2)小组同学利用上述 溶液探究其与足量锌粉的反应。实验操作及现象如表:
溶液探究其与足量锌粉的反应。实验操作及现象如表:
已知:Zn的性质与Al相似,能发生反应:
①红褐色沉淀是:___________ (填化学式),结合实验现象和平衡移动原理解释出现红褐色沉淀的原因:___________ 。
②反应后溶液为浅绿色,写出相关反应的离子方程式:___________ 。
③分离出黑色固体,经下列实验证实了其中含有的主要物质。
ⅰ.黑色固体可以被磁铁吸引;
ⅱ.向黑色固体中加入足量的NaOH溶液,产生气泡;
ⅲ.将ⅱ中剩余固体用蒸馏水洗涤后,加入稀盐酸,产生大量气泡;
ⅳ.向ⅲ反应后的溶液中滴加KSCN溶液,无变化。
a.黑色固体中一定含有的物质是___________ 。
b.小组同学认为上述实验无法确定黑色固体中是否含有 ,理由是
,理由是___________ 。
(3)为进一步探究上述1.0 mol⋅L-1 溶液中
溶液中 和
和 氧化性的相对强弱,继续实验并观察到反应开始时现象如表:
氧化性的相对强弱,继续实验并观察到反应开始时现象如表:
小组同学得出结论:在1.0 mol⋅L-1  溶液中,
溶液中, 的氧化性比
的氧化性比 更强。
更强。
 溶液中的离子平衡和离子反应,某小组同学进行了如下实验。
溶液中的离子平衡和离子反应,某小组同学进行了如下实验。(1)配制:50 mL 1.0 mol⋅L-1的
 溶液,测其pH约为0.7,即
溶液,测其pH约为0.7,即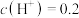 mol⋅L-1。用离子方程式解释
mol⋅L-1。用离子方程式解释 溶液呈酸性的原因:
溶液呈酸性的原因:(2)小组同学利用上述
 溶液探究其与足量锌粉的反应。实验操作及现象如表:
溶液探究其与足量锌粉的反应。实验操作及现象如表:| 操作 | 现象 |
向反应瓶中加入6.5 g锌粉,然后加入50 mL 1.0 mol·L 的 的 溶液,搅拌 溶液,搅拌 | 溶液温度迅速上升,稍后出现红褐色沉淀,同时出现少量气泡;反应一段时间后静置,上层溶液为浅绿色,反应瓶底部有黑色固体 |
| 收集检验反应过程中产生的气体 | 集气管口靠近火焰,有爆鸣声 |

①红褐色沉淀是:
②反应后溶液为浅绿色,写出相关反应的离子方程式:
③分离出黑色固体,经下列实验证实了其中含有的主要物质。
ⅰ.黑色固体可以被磁铁吸引;
ⅱ.向黑色固体中加入足量的NaOH溶液,产生气泡;
ⅲ.将ⅱ中剩余固体用蒸馏水洗涤后,加入稀盐酸,产生大量气泡;
ⅳ.向ⅲ反应后的溶液中滴加KSCN溶液,无变化。
a.黑色固体中一定含有的物质是
b.小组同学认为上述实验无法确定黑色固体中是否含有
 ,理由是
,理由是(3)为进一步探究上述1.0 mol⋅L-1
 溶液中
溶液中 和
和 氧化性的相对强弱,继续实验并观察到反应开始时现象如表:
氧化性的相对强弱,继续实验并观察到反应开始时现象如表:| 操作 | 现象 |
将5 mL 1.0 mol⋅L-1的 溶液与0.65 g锌粉混合 溶液与0.65 g锌粉混合 | 溶液温度迅速上升,开始时几乎没有气泡 |
| 将 | 溶液中立即产生大量气泡 |
 溶液中,
溶液中, 的氧化性比
的氧化性比 更强。
更强。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】学习小组设计实验探究C、Si、S、Br四种元素的非金属性强弱。回答下列问题:
(1)小组同学根据元素周期表和元素周期律可分析判定非金属性强弱:C_______ Si(填写“>”或“<”,下同),Si_______ S。
(2)小组同学设计如图实验装置比较C、Si、S的非金属性强弱。
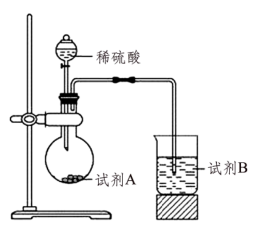
①设计此实验的依据是_______ 。
②试剂A的名称是_______ 。
③实验开始后,试剂B发生反应的离子方程式为_______ 。
(3)小组同学通过化学实验证明了非金属性:Br>S。(供选择的试剂:氯水、溴水、溴化钠溶液、新制Na2S溶液、四氯化碳、酚酞溶液。)
①完成实验需要的最合适试剂为_______ 。
②完成实验所需要的最合适仪器有_______ 。
③实验现象为_______ 。
(1)小组同学根据元素周期表和元素周期律可分析判定非金属性强弱:C
(2)小组同学设计如图实验装置比较C、Si、S的非金属性强弱。

①设计此实验的依据是
②试剂A的名称是
③实验开始后,试剂B发生反应的离子方程式为
(3)小组同学通过化学实验证明了非金属性:Br>S。(供选择的试剂:氯水、溴水、溴化钠溶液、新制Na2S溶液、四氯化碳、酚酞溶液。)
①完成实验需要的最合适试剂为
②完成实验所需要的最合适仪器有
③实验现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某小组同学探究Na2CO3的性质,请你与他们一起完成,并回答下列问题。
(1)观察:描述Na2CO3的颜色、状态:____ 。
(2)预测:从物质的类别来看,Na2CO3属于____ 类,可以与____ 等类别的物质发生反应。
(3)设计实验并得出结论:
(4)问题和讨论:①对实验II的离子方程式原理,你能再找出一个与它解释相同的化学反应吗____ ?
②在实验室中,如何鉴别Na2CO3和NaHCO3____ ?
③该组同学在探究Na2CO3的性质时的思路是什么____ ?用了什么方法____ ?
(1)观察:描述Na2CO3的颜色、状态:
(2)预测:从物质的类别来看,Na2CO3属于
(3)设计实验并得出结论:
| 实验步骤 | 实验现象 | 结论或解释(用离子方程式) |
| I.向盛有Na2CO3溶液的试管中滴加澄清石灰水 | ||
| II.向盛有Na2CO3溶液的试管中滴加CaCl2溶液 | ||
| III.向盛有Na2CO3溶液的试管中滴加稀盐酸 | 开始无气泡产生,一段时间后产生气泡 | ①CO +H+=HCO +H+=HCO ② |
②在实验室中,如何鉴别Na2CO3和NaHCO3
③该组同学在探究Na2CO3的性质时的思路是什么
您最近一年使用:0次