水泥是人类最伟大的发明之一,主要成分为硅酸三钙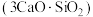 。将其与适量的水反应,形成相互交联的结构,发生的反应为
。将其与适量的水反应,形成相互交联的结构,发生的反应为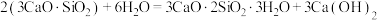 。回答下列问题:
。回答下列问题:
(1)为了加快硅酸三钙与水的反应速率,可采用的方式为_______ (填一种即可)。
(2)Si在元素周期表中的位置为_______ 。
(3) 的电子式为
的电子式为_______ , 的空间结构为
的空间结构为_______ 。
(4)元素C、O、Si、Ca的原子半径由大到小的顺序为_______ 。
(5)带有玻璃塞的磨口玻璃瓶不能用来盛装NaOH溶液的原因为_______ (用化学方程式表示)。
(6)写出 在农业上的一种用途:
在农业上的一种用途:_______ 。
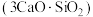 。将其与适量的水反应,形成相互交联的结构,发生的反应为
。将其与适量的水反应,形成相互交联的结构,发生的反应为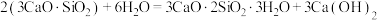 。回答下列问题:
。回答下列问题:(1)为了加快硅酸三钙与水的反应速率,可采用的方式为
(2)Si在元素周期表中的位置为
(3)
 的电子式为
的电子式为 的空间结构为
的空间结构为(4)元素C、O、Si、Ca的原子半径由大到小的顺序为
(5)带有玻璃塞的磨口玻璃瓶不能用来盛装NaOH溶液的原因为
(6)写出
 在农业上的一种用途:
在农业上的一种用途:
更新时间:2023-06-07 23:13:27
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】请根据所学知识回答下列问题:
(1)已知反应Fe+H2SO4=FeSO4+H2↑。若要加快该反应的速率,在其他条件不变的情况下,下列措施可行的是______ (填字母)。
(2)近年来,科学家致力于将二氧化碳和氢气转化为甲醇(CH3OH)的技术研究,为解决环境与能源问题提供了新途径。某温度下在2L的恒容密闭容器中,充入4molCO2和4molH2,发生如下反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。
CH3OH(g)+H2O(g)。
①能判断该反应已达到化学反应限度的是______ (填字母)。
A.容器内压强保持不变
B.容器中CO2浓度与H2浓度之比为1:3
C.容器中CO2的物质的量分数保持不变
D.CO2的生成速率与CH3OH的生成速率相等
②现测得H2的浓度随时间变化如图所示。从反应开始经过12min达到平衡,则0~5min内CO2的平均反应速率v(CO2)=______ ,第12min时,甲醇的物质的量浓度为______ 。

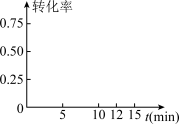
③请在图中画出0~15min内H2转化率随时间变化的示意图______ 。
(3)燃料电池能有效提高能源利用率,写出甲醇(CH3OH)空气燃料电池在碱性条件(KOH溶液)中的负极电极反应式______ 。
(1)已知反应Fe+H2SO4=FeSO4+H2↑。若要加快该反应的速率,在其他条件不变的情况下,下列措施可行的是
| A.升高温度 | B.改稀硫酸为98%的浓硫酸 |
| C.将纯铁改为生铁 | D.往稀硫酸中加入少量Na2SO4(s) |
 CH3OH(g)+H2O(g)。
CH3OH(g)+H2O(g)。①能判断该反应已达到化学反应限度的是
A.容器内压强保持不变
B.容器中CO2浓度与H2浓度之比为1:3
C.容器中CO2的物质的量分数保持不变
D.CO2的生成速率与CH3OH的生成速率相等
②现测得H2的浓度随时间变化如图所示。从反应开始经过12min达到平衡,则0~5min内CO2的平均反应速率v(CO2)=

③请在图中画出0~15min内H2转化率随时间变化的示意图

(3)燃料电池能有效提高能源利用率,写出甲醇(CH3OH)空气燃料电池在碱性条件(KOH溶液)中的负极电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】废电池中的锌皮常用于实验室制氢气,废锌皮和纯锌粒分别与同浓度的稀硫酸反应,产生氢气速率较大的是___________ ,若用过量的纯锌粒与一定量的稀硫酸反应,为了加快反应速率又不影响产生氢气的量,下列措施可行的是___________ (填序号)。
A.微热B.加入适量氧化铜C.加入少量硫酸铜溶液D.加水E.加入少量氢氧化钡溶液
A.微热B.加入适量氧化铜C.加入少量硫酸铜溶液D.加水E.加入少量氢氧化钡溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】一定温度下,向一容积为5L的恒容密闭容器中充入0.4molSO2和0.2molO2,发生反应:2SO2(g)+O2(g) 2SO3(g)ΔH=-196kJ·mol-1。当反应达到平衡时,容器内压强变为起始时的
2SO3(g)ΔH=-196kJ·mol-1。当反应达到平衡时,容器内压强变为起始时的 。请回答下列问题:
。请回答下列问题:
(1)判断该反应达到平衡状态的标志是___ (填字母)。
a.SO2、O2、SO3三者的浓度之比为2∶1∶2
b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.SO3的物质的量不再变化
e.SO2的生成速率和SO3的生成速率相等
(2)平衡时SO2的转化率为___ ;反应放出的热量为___ 。
(3)其他条件不变时,下列条件的改变引起该反应的反应速率的变化是什么(在横线上填“加快”、“减慢”或“不变”)
A.缩小体积使压强增大。___
B.体积不变充入氩气使压强增大。___
C.压强不变充入氩气使体积增大。___
D.升高温度。___
 2SO3(g)ΔH=-196kJ·mol-1。当反应达到平衡时,容器内压强变为起始时的
2SO3(g)ΔH=-196kJ·mol-1。当反应达到平衡时,容器内压强变为起始时的 。请回答下列问题:
。请回答下列问题:(1)判断该反应达到平衡状态的标志是
a.SO2、O2、SO3三者的浓度之比为2∶1∶2
b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.SO3的物质的量不再变化
e.SO2的生成速率和SO3的生成速率相等
(2)平衡时SO2的转化率为
(3)其他条件不变时,下列条件的改变引起该反应的反应速率的变化是什么(在横线上填“加快”、“减慢”或“不变”)
A.缩小体积使压强增大。
B.体积不变充入氩气使压强增大。
C.压强不变充入氩气使体积增大。
D.升高温度。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】请在表中画出元素周期表的轮廓,并在表中按要求完成下列问题:
①标出族序数;②填入1~20元素的元素符号;③)填入稀有气体元素的原子序数以及每周期的元素种类;④画出主族与副族边界线。
_______

①标出族序数;②填入1~20元素的元素符号;③)填入稀有气体元素的原子序数以及每周期的元素种类;④画出主族与副族边界线。

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】结合元素周期表回答下列问题:
(1)表中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界______ 。

(2)表中所列元素,属于短周期元素的有______ ,属于主族元素的有______ ;g元素位于第______ 周期______ 族;i元素位于第______ 周期______ 族。
(3)元素f是第______ 周期______ 族元素,请在下边方框中按氦元素的式样写出该元素的原子序数、元素符号、元素名称、相对原子质量______ 。

(1)表中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界

(2)表中所列元素,属于短周期元素的有
(3)元素f是第

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表中所列的字母分别代表某一化学元素。完成下列填空:
(1)h的最外层有____ 种运动状态的电子。a、b、c三种元素形成的化合物电子式为________ 。
(2)d单质溶于i的最高价氧化物对应水化物的溶液时发生反应的离子方程式为____________ 。
(3) 元素e与f元素相比,非金属性较强的是__________ (写元素符号),下列表述中能证明这一事实的是__________ (选填序号)。
a. e的阴离子还原性强于f的阴离子 b. f的氢化物酸性强于e的氢化物
c. e单质的熔点高于f单质 d. e和f形成的化合物中,e显正价,f显负价
(4)元素X(非a~i元素)是所在周期原子半径最大的非金属元素,它的气态氢化物为三角锥形极性分子,写出X在周期表中的位置_______________________________ 。
| a | |||||||||||||||||
| b | |||||||||||||||||
| c | d | e | f | ||||||||||||||
| g | |||||||||||||||||
| h | |||||||||||||||||
| i | |||||||||||||||||
(1)h的最外层有
(2)d单质溶于i的最高价氧化物对应水化物的溶液时发生反应的离子方程式为
(3) 元素e与f元素相比,非金属性较强的是
a. e的阴离子还原性强于f的阴离子 b. f的氢化物酸性强于e的氢化物
c. e单质的熔点高于f单质 d. e和f形成的化合物中,e显正价,f显负价
(4)元素X(非a~i元素)是所在周期原子半径最大的非金属元素,它的气态氢化物为三角锥形极性分子,写出X在周期表中的位置
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】比较下列元素的性质(用“>”、“<”表示)
(1)金属性:Li_______ Na;
(2)非金属性:F_______ Cl;
(3)根据元素在周期表中的位置,判断下列各组化合物的酸、碱性强弱:Al(OH)3_______ Mg(OH)2;
(4)原子半径:N_______ O。
(1)金属性:Li
(2)非金属性:F
(3)根据元素在周期表中的位置,判断下列各组化合物的酸、碱性强弱:Al(OH)3
(4)原子半径:N
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】元素周期表与元素周期律在化学学习研究中有很重要的作用。下表是元素周期表的一部分
(1)写出④和⑨组成的化合物的电子式_______ ,⑧的简单离子结构示意图_______ 。
(2)元素①、②、⑦简单氢化物的稳定性最强的是_______ (用化学式表示)。
(3)元素③、⑤、⑨的简单离子半径由大到小的顺序(用离子符号表示)_______ 。
(4)写出元素④、⑤最高价氧化物对应水化物相互反应的化学方程式_______ 。
(5)元素非金属性强弱比较有很多方法,其中比较⑧和⑨的非金属性强弱的研究方案中不可行的是:_______(填序号)。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | |||||||
| 2 | ① | ② | ③ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)元素①、②、⑦简单氢化物的稳定性最强的是
(3)元素③、⑤、⑨的简单离子半径由大到小的顺序(用离子符号表示)
(4)写出元素④、⑤最高价氧化物对应水化物相互反应的化学方程式
(5)元素非金属性强弱比较有很多方法,其中比较⑧和⑨的非金属性强弱的研究方案中不可行的是:_______(填序号)。
| A.比较两种单质的颜色 | B.比较两种单质与H2化合的难易程度 |
| C.依据两元素在周期表中的位置 | D.比较氧化物对应水化物的酸性强弱 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】A、B、C、D、E五种短周期元素,原子序数依次增大,其中只有C为金属元素。A、C原子序数之和等于E的原子序数,D与B同主族且D原子序数是B原子序数的2倍。AB2和DB2溶于水得到酸性溶液,C2D溶于水得到碱性溶液。
(1)E元素在周期表中的位置为_____ ;工业上制取C单质的化学方程式为______ 。
(2)A的最低负价氢化物的空间构型为____ ;C、D、E的简单离子的离子半径由大到小的顺序是_____ (用离子符号表示)。
(3)在低温下,将E的单质通入饱和NaHCO3溶液中,反应后得到一种微绿色气体E2B、CE和另外一种无色气体。则该反应中E2B、CE这两种产物的物质的量之比n(E2B):n(CE)=_______ 。已知E2B溶于水生成一种具有漂白性的弱酸,该弱酸分子的结构式为__________ 。
(4)化合物C2 D3中,各原子(或离子)最外层均达到8电子稳定结构,则C2D3的电子式为_________ ,该化合物的水溶液在空气中久置后变质,生成一种单质,所得溶液呈强碱性,用化学方程式表示这一变化过程__________ 。
(1)E元素在周期表中的位置为
(2)A的最低负价氢化物的空间构型为
(3)在低温下,将E的单质通入饱和NaHCO3溶液中,反应后得到一种微绿色气体E2B、CE和另外一种无色气体。则该反应中E2B、CE这两种产物的物质的量之比n(E2B):n(CE)=
(4)化合物C2 D3中,各原子(或离子)最外层均达到8电子稳定结构,则C2D3的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】臭氧有强氧化性能在一定条件下将烟气中的SO2、NOx分别氧化为SO42- 和NO3 -。臭氧可用于净化空气,饮用水消毒,处理工业废物和作为漂白剂。
(1)NO3-中心原子轨道的杂化类型为___________ ;SO42- 的空间构型为_____________ (用文字描述)。
(2)Fe3+基态核外外层电子排布式为__________________ 。
(3)臭氧可用于含CN一碱性电镀废水的处理。第i步:CN一转化为OCN-;第ii步: OCN一继续转化为CO32一及两种单质气体。若第ii步转化时,O3与OCN-物质的质量之比为3∶2,该步反应的离子方程式为_______ 。
(4)为测定大气中臭氧(O3)含量,将0℃、1.01×105Pa的空气VL慢慢通过足量KI溶液,使臭氧完全反应;然后将所得溶液用amL cmol/L的Na2S2O3溶液进行滴定恰好到达终点。
(已知:2Na2S2O3+I2=Na2S4O6+2NaI)
①O3与KI溶液反应生成两种单质,则反应的化学方程式__________________________ 。
②该滴定实验中除烧杯、锥形瓶外,还需要的玻璃仪器是_____________ ;
③该实验中可选用_______ (填物质名称)作指示剂。空气中臭氧的体积分数为_______ 。
④甲同学认为在滴定前应微热溶液,以排除溶液中溶解的O3和O2,不然会使滴定结果偏_____ (填“低”或“高”)。
(1)NO3-中心原子轨道的杂化类型为
(2)Fe3+基态核外外层电子排布式为
(3)臭氧可用于含CN一碱性电镀废水的处理。第i步:CN一转化为OCN-;第ii步: OCN一继续转化为CO32一及两种单质气体。若第ii步转化时,O3与OCN-物质的质量之比为3∶2,该步反应的离子方程式为
(4)为测定大气中臭氧(O3)含量,将0℃、1.01×105Pa的空气VL慢慢通过足量KI溶液,使臭氧完全反应;然后将所得溶液用amL cmol/L的Na2S2O3溶液进行滴定恰好到达终点。
(已知:2Na2S2O3+I2=Na2S4O6+2NaI)
①O3与KI溶液反应生成两种单质,则反应的化学方程式
②该滴定实验中除烧杯、锥形瓶外,还需要的玻璃仪器是
③该实验中可选用
④甲同学认为在滴定前应微热溶液,以排除溶液中溶解的O3和O2,不然会使滴定结果偏
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】两个或两个以上的分子(包括带有电荷的分子离子)它们的原子数相同,分子中的电子数目也相同。这些分子(称等电子体)具有相似的几何结构和物理性质。O 的等电子体是
的等电子体是___________ ; N 分子的几何构型是
分子的几何构型是___________ 。(BN) n晶体(n是一个很大的数目)结构类似于___________ 。
 的等电子体是
的等电子体是 分子的几何构型是
分子的几何构型是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】我国有丰富的海水资源,海水中的元素共含有80多种,总储量很大。常量元素包括H、B、C、O、F、Na、Mg、S、Cl、K、Ca、Br、Sr等13种元素,同时还含有Cr、Mn、Fe、Ni、Cu、Zn等微量元素,因此开发利用海水资源具有非常广阔的前景。
(1)Sr元素在元素周期表中的位置是___ 。
(2)上述元素能形成众多微粒,其中CO 的中心原子价层电子对数为
的中心原子价层电子对数为___ 对,SO 的空间构型为
的空间构型为___ ,CH3COOH中C的杂化方式为___ 。
(3)已知钠的晶胞棱长为apm,NA为阿伏加德罗常数的值,钠的晶胞结构如图,则其密度为___ g/cm3。

(1)Sr元素在元素周期表中的位置是
(2)上述元素能形成众多微粒,其中CO
 的中心原子价层电子对数为
的中心原子价层电子对数为 的空间构型为
的空间构型为(3)已知钠的晶胞棱长为apm,NA为阿伏加德罗常数的值,钠的晶胞结构如图,则其密度为

您最近一年使用:0次



