某化学兴趣小组欲探究a,b,c,d四种金属的活动性大小顺序,利用实验室现有材料和试剂进行实验,组装了如图所示的装置(电流表指针偏向正极,电解质溶液足量)。请回答下列问题:
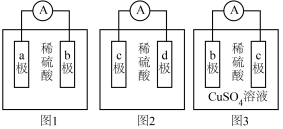
(1)观察到图1装置中的电流表指针偏向b极,说明a极为______ (填“正极”或“负极”),b极上发生的电极反应为______ 。
(2)观察到图2装置中的c极上有气泡生成,可观察到d极上的现象为______ 。
(3)图3装置中的电流表指针偏向c极,若b极为Fe电极,则b极上发生的电极反应为______ ,当该电路中转移0.4mole-时,______ (填“b”或“c”)极质量增重______ g。
(4)通过以上实验装置______ (填“能”或“不能”)比较出四种金属的活动性大小顺序,理由是______ 。

(1)观察到图1装置中的电流表指针偏向b极,说明a极为
(2)观察到图2装置中的c极上有气泡生成,可观察到d极上的现象为
(3)图3装置中的电流表指针偏向c极,若b极为Fe电极,则b极上发生的电极反应为
(4)通过以上实验装置
更新时间:2023-06-03 12:48:38
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】据图回答下列问题:
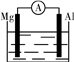
(1)如图①,若烧杯中溶液为稀硫酸,则观察到的现象是
________________________________________________________________________ ;
若烧杯中溶液为氢氧化钠溶液,则负极的电极反应式为____________________ 。
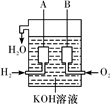
(2)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如图②所示:A、B两个电极均由多孔的碳块组成。该电池的正极为________ (填“A”或“B”);
如果将图②装置中通入的H2改成CH4气体也可以组成一个原电池装置电池的总反应方程式为CH4+2O2+2KOH===K2CO3+3H2O,则该电池的负极反应式为__________________________ 。
①
(1)如图①,若烧杯中溶液为稀硫酸,则观察到的现象是
若烧杯中溶液为氢氧化钠溶液,则负极的电极反应式为
②
(2)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如图②所示:A、B两个电极均由多孔的碳块组成。该电池的正极为
如果将图②装置中通入的H2改成CH4气体也可以组成一个原电池装置电池的总反应方程式为CH4+2O2+2KOH===K2CO3+3H2O,则该电池的负极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)如图所示,若C为浓硝酸,电流表指针发生偏转,B电极材料为Fe ,A电极材料为Cu,则B电极的电极反应式为___________ ,A电极的电极反应式为_______ ;反应进行一段时间后溶液C的pH将___ (填“升高”“降低”或“基本不变”)。____ ,负极反应为___________ ;正极反应为_____________________________ 。
(3)熔盐电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650 ℃下工作的燃料电池,完成有关电池反应式。负极反应式为2CO+2CO32--4e-=4CO2,正极反应式为___________ ,电池总反应式为_______ 。

(3)熔盐电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650 ℃下工作的燃料电池,完成有关电池反应式。负极反应式为2CO+2CO32--4e-=4CO2,正极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氢气是一种十分熟悉的物质,在许多反应中既可作为反应物,也可作为生成物。
(1)电解饱和食盐水可制取氢气,反应的化学方程式____ 。
(2)在氢气还原氧化铜的反应中,标出电子转移的方向及数目。____
H2+CuO Cu+H2O
Cu+H2O
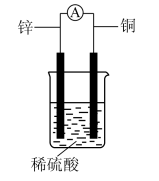
(3)在铜锌原电池中,如图,在铜极附近看到的现象是____ ;电子流向从___ 。
(4)氢气作为燃料,有1g氢气燃烧生成液态水放出142.8kJ热量,表示该反应的热化学方程式_____ 。
(5)实验室用锌与稀硫酸反应制取氢气,某学校实验员为了提高制氢的速度,在此溶液中加入少量硫酸铜溶液,你认为合理吗?为什么?____ 。
(1)电解饱和食盐水可制取氢气,反应的化学方程式
(2)在氢气还原氧化铜的反应中,标出电子转移的方向及数目。
H2+CuO
 Cu+H2O
Cu+H2O(3)在铜锌原电池中,如图,在铜极附近看到的现象是

(4)氢气作为燃料,有1g氢气燃烧生成液态水放出142.8kJ热量,表示该反应的热化学方程式
(5)实验室用锌与稀硫酸反应制取氢气,某学校实验员为了提高制氢的速度,在此溶液中加入少量硫酸铜溶液,你认为合理吗?为什么?
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:
A.NaOH+HCl=NaCl+H2O;B.Zn+H2SO4=ZnSO4+H2↑
判断能否设计成原电池A._____ ,B._____ 。(填“能”或“不能”)
(2)将纯锌片和纯铜片按图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:

①下列说法正确的是____________ 。
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲________ 乙(填“>”、“<“或“=”)。
③请写出图中构成原电池的负极电极反应式_________________________ 。
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,氢气为燃料,采用氢氧化钠溶液为电解液;则氢气应通入__ 极(填a或b),电子从____ (填a或b)极流出。
(1)现有如下两个反应:
A.NaOH+HCl=NaCl+H2O;B.Zn+H2SO4=ZnSO4+H2↑
判断能否设计成原电池A.
(2)将纯锌片和纯铜片按图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:

①下列说法正确的是
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲
③请写出图中构成原电池的负极电极反应式
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,氢气为燃料,采用氢氧化钠溶液为电解液;则氢气应通入
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.已知Sn与稀硫酸能发生反应:Sn+H2SO4 =SnSO4+H2↑
(1)若要使该反应的反应速率加快,下列措施可行的是_______ (填字母)。
(2)若将上述反应设计成原电池,石墨棒为原电池某一极材料, 则石墨棒为_______ 极(填“正”或“负”)。原电池工作时溶液中的SO 向
向_______ 极移动(填“正”或“负”)。
(3)实验后同学们经过充分讨论,观察原电池反应特点,认为符合某些要求的化学反应都可以通过原电池来实现。下列化学反应在理论上可以设计成原电池的是_______ 。
A. CO2+H2O=H2CO3 B. NaOH+HCl=NaCl+H2O
C.2H2+O2 =2H2O D. CuO+H2SO4= CuSO4+H2O
以KOH为电解质溶液,将所选反应设计成原电池,该电池负极的电极反应为:_______ 。
II.有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6mol·L-1的H2SO4溶液中,乙同学将电极放入6mol·L-1的NaOH溶液中,如图所示。
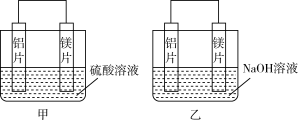
(4)写出甲中正极的电极反应式:_______ 。
(5)写出乙中负极的电极反应式:_______ 。
(1)若要使该反应的反应速率加快,下列措施可行的是_______ (填字母)。
| A.改锡片为锡粉 | B.加入少量醋酸钠固体 |
| C.滴加少量CuSO4 | D.将稀硫酸改为98%的浓硫酸 |
 向
向(3)实验后同学们经过充分讨论,观察原电池反应特点,认为符合某些要求的化学反应都可以通过原电池来实现。下列化学反应在理论上可以设计成原电池的是
A. CO2+H2O=H2CO3 B. NaOH+HCl=NaCl+H2O
C.2H2+O2 =2H2O D. CuO+H2SO4= CuSO4+H2O
以KOH为电解质溶液,将所选反应设计成原电池,该电池负极的电极反应为:
II.有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6mol·L-1的H2SO4溶液中,乙同学将电极放入6mol·L-1的NaOH溶液中,如图所示。

(4)写出甲中正极的电极反应式:
(5)写出乙中负极的电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列电化学问题:
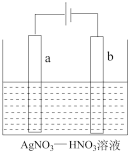
(1)如图为电解精炼银的示意图,___ (填“a”或“b”)极为含有杂质的粗银,若b极有少量红棕色气体产生,则生成该气体的电极反应式为_________________ 。
(2)通过NOx传感器可监测NOx的含量,其工作原理示意图如图所示:
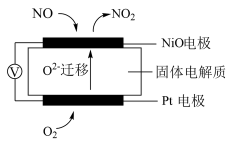
①Pt电极上发生的是________ 反应(填“氧化”或“还原”),
②写出NiO电极的电极反应式:______________________ 。
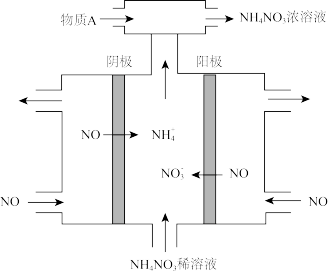
(3)电解NO制备NH4NO3的工作原理如图所示,其中阳极的电极反应式:_____________ ,为使电解产物全部转化为NH4NO3,需补充物质A,则A可以是______ 。
(1)如图为电解精炼银的示意图,

(2)通过NOx传感器可监测NOx的含量,其工作原理示意图如图所示:

①Pt电极上发生的是
②写出NiO电极的电极反应式:
(3)电解NO制备NH4NO3的工作原理如图所示,其中阳极的电极反应式:

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】利用化学反应为人类生产生活提供能量。
(1)下列反应中,属于放热反应的是___________ (填序号,下同),属于吸热反应的是___________ 。
①生石灰和水反应 ②二氧化碳与炽热的炭反应 ③氢氧化钠溶于水 ④炸药爆炸 ⑤碳酸钙高温分解 ⑥葡萄糖的缓慢氧化 ⑦ 和
和 反应
反应
(2)如图是某同学设计的一个简易的原电池装置。

①若a电极为碳,b溶液为 溶液,则正极的电极反应式
溶液,则正极的电极反应式___________ ,当有3.2g的负极材料溶解时,导线中转移的电子数目___________ 。
②若a电极为Fe,b溶液为 溶液,当导线中转移0.2mol电子时,电解质溶液减少的质量为
溶液,当导线中转移0.2mol电子时,电解质溶液减少的质量为___________ 。
③若a电极为铁,b溶液为稀硫酸,电池工作时铜电极附近的溶液pH将___________ (填“增大”、“不变”或“减小”)。
(1)下列反应中,属于放热反应的是
①生石灰和水反应 ②二氧化碳与炽热的炭反应 ③氢氧化钠溶于水 ④炸药爆炸 ⑤碳酸钙高温分解 ⑥葡萄糖的缓慢氧化 ⑦
 和
和 反应
反应(2)如图是某同学设计的一个简易的原电池装置。

①若a电极为碳,b溶液为
 溶液,则正极的电极反应式
溶液,则正极的电极反应式②若a电极为Fe,b溶液为
 溶液,当导线中转移0.2mol电子时,电解质溶液减少的质量为
溶液,当导线中转移0.2mol电子时,电解质溶液减少的质量为③若a电极为铁,b溶液为稀硫酸,电池工作时铜电极附近的溶液pH将
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】请根据有关知识,填写下列空白:
(1)已知拆开1 mol H-H键、1 mol I-I、1 mol H-I键分别需要吸收的能量为436 kJ、151 kJ、299 kJ,则由1 mol氢气和1 mol碘反应生成HI会放出_______ kJ的热量
(2)某同学做如下实验,以检验反应中的能量变化。

①在实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是_______ 热反应;
②根据能量守恒定律,(b)中反应物的总能量应该_______ 其生成物的总能量(填“>”或“<”)。
(3)下列过程中不一定放热的是_______ (填字母)。
a.铝热反应 b.炸药爆炸 c.燃料燃烧 d.分解反应 e.酸碱中和
(4)分别按下图 A、B、C 所示装置进行实验,三个烧杯里的溶液为同浓度的稀硫酸。回答下列问题:
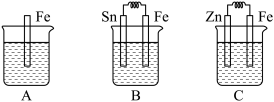
①下列叙述中,正确的是_______ 。
A.B 、C 中铁片均是为负极 B.三个烧杯中铁片表面均无气泡产生
C.产生气泡的速率 A 中比B中慢 D.C 溶液中SO 向Fe片电极移动
向Fe片电极移动
②若把Ba(OH)2·8H2O 晶体与 NH4Cl晶体反应设计成原电池,你认为是否可行?_______ (填“是”或“否”)。
(1)已知拆开1 mol H-H键、1 mol I-I、1 mol H-I键分别需要吸收的能量为436 kJ、151 kJ、299 kJ,则由1 mol氢气和1 mol碘反应生成HI会放出
(2)某同学做如下实验,以检验反应中的能量变化。

①在实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是
②根据能量守恒定律,(b)中反应物的总能量应该
(3)下列过程中不一定放热的是
a.铝热反应 b.炸药爆炸 c.燃料燃烧 d.分解反应 e.酸碱中和
(4)分别按下图 A、B、C 所示装置进行实验,三个烧杯里的溶液为同浓度的稀硫酸。回答下列问题:

①下列叙述中,正确的是
A.B 、C 中铁片均是为负极 B.三个烧杯中铁片表面均无气泡产生
C.产生气泡的速率 A 中比B中慢 D.C 溶液中SO
 向Fe片电极移动
向Fe片电极移动②若把Ba(OH)2·8H2O 晶体与 NH4Cl晶体反应设计成原电池,你认为是否可行?
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】物质发生化学反应时,常常伴随有能量变化。某学习小组用如图所示装置A、B分别探究金属锌与稀硫酸的反应,实验过程中A烧杯内的溶液温度升高,B烧杯的电流计指针发生偏转,请回答以下问题。
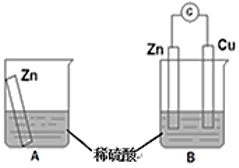
(1)A烧杯中反应的离子方程式为___________ 。
(2)B中Zn板是___________ 极,发生反应的电极反应式是___________ 。
(3)从能量转化的角度来看,A、B中反应物的总能量___________ (填“大于”、“小于”或“等于”)生成物总能量,A中是将化学能转变为___________ ,B中是将化学能转变为___________ 。
(4)该小组同学反思原电池的原理,其中观点正确的是___________(填字母序号)。

(1)A烧杯中反应的离子方程式为
(2)B中Zn板是
(3)从能量转化的角度来看,A、B中反应物的总能量
(4)该小组同学反思原电池的原理,其中观点正确的是___________(填字母序号)。
| A.原电池反应的过程中一定有电子转移 |
| B.原电池装置需要2个电极 |
| C.电极一定都参加反应 |
| D.氧化反应和还原反应可以拆开在两极发生 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
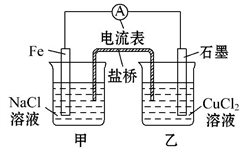
【推荐1】(1)如图为某实验小组依据氧化还原反应(用离子方程式表示)________ 设计的原电池装置。反应前,电极质量相等,一段时间后,两电极质量相差12 g,导线中通过________ mol电子。
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H= - 24.8kJ/mol
3Fe2O3(s)+ CO(g)=2Fe3O4(s)+ CO2(g) △H= - 47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe 固体和CO2气体的热化学反应方程式:__________ 。
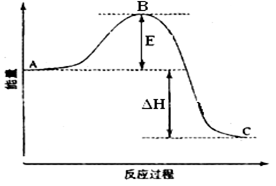
(3)2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。该反应通常用V2O5作催化剂,加V2O5会使图中B点_________ (填“升高”还是“降低”),△H______ (填“变大”、“变小”或“不变”)。

(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H= - 24.8kJ/mol
3Fe2O3(s)+ CO(g)=2Fe3O4(s)+ CO2(g) △H= - 47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe 固体和CO2气体的热化学反应方程式:
(3)2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。该反应通常用V2O5作催化剂,加V2O5会使图中B点

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】人们利用原电池原理制作了多种电池,以满足日常生活、生产和科学技术等方面的需要。请根据题中提供的信息,回答下列问题。
(1)铅蓄电池在放电时的电池反应为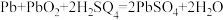 则其负极的电极反应为
则其负极的电极反应为_________________
(2) 溶液腐蚀印刷电路板时发生反应:
溶液腐蚀印刷电路板时发生反应: 。若将此反应设计成原电池,则负极材料是
。若将此反应设计成原电池,则负极材料是_______ ;当电路中转移 电子时,被腐蚀的铜的质量为
电子时,被腐蚀的铜的质量为_______  。
。
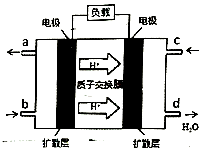
(3)已知甲醇燃料电池的工作原理如图所示。该电池工作时, 口通入的主要物质为
口通入的主要物质为_______ ,发生的电极反应为_____________ 。
(1)铅蓄电池在放电时的电池反应为
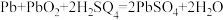 则其负极的电极反应为
则其负极的电极反应为
(2)
 溶液腐蚀印刷电路板时发生反应:
溶液腐蚀印刷电路板时发生反应: 。若将此反应设计成原电池,则负极材料是
。若将此反应设计成原电池,则负极材料是 电子时,被腐蚀的铜的质量为
电子时,被腐蚀的铜的质量为 。
。(3)已知甲醇燃料电池的工作原理如图所示。该电池工作时,
 口通入的主要物质为
口通入的主要物质为
您最近一年使用:0次

 如图
如图 ,则此原电池中锌电极上发生的是
,则此原电池中锌电极上发生的是 电子通过时,负极质量会变化
电子通过时,负极质量会变化 向
向


