氢气是一种十分熟悉的物质,在许多反应中既可作为反应物,也可作为生成物。
(1)电解饱和食盐水可制取氢气,反应的化学方程式____ 。
(2)在氢气还原氧化铜的反应中,标出电子转移的方向及数目。____
H2+CuO Cu+H2O
Cu+H2O
(3)在铜锌原电池中,如图,在铜极附近看到的现象是____ ;电子流向从___ 。
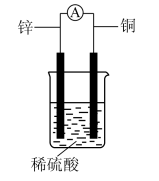
(4)氢气作为燃料,有1g氢气燃烧生成液态水放出142.8kJ热量,表示该反应的热化学方程式_____ 。
(5)实验室用锌与稀硫酸反应制取氢气,某学校实验员为了提高制氢的速度,在此溶液中加入少量硫酸铜溶液,你认为合理吗?为什么?____ 。
(1)电解饱和食盐水可制取氢气,反应的化学方程式
(2)在氢气还原氧化铜的反应中,标出电子转移的方向及数目。
H2+CuO
 Cu+H2O
Cu+H2O(3)在铜锌原电池中,如图,在铜极附近看到的现象是

(4)氢气作为燃料,有1g氢气燃烧生成液态水放出142.8kJ热量,表示该反应的热化学方程式
(5)实验室用锌与稀硫酸反应制取氢气,某学校实验员为了提高制氢的速度,在此溶液中加入少量硫酸铜溶液,你认为合理吗?为什么?
更新时间:2019-11-07 08:13:50
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】按要求填空。
(1)用双线桥表示CaH2+2H2O=Ca(OH)2+2H2↑反应电子转移情况:_______ 。
(2)某元素的一种同位素X的质量数为A,含N个中子,它与1H原子组成 分子。在a克
分子。在a克 中所含质子的物质的量是
中所含质子的物质的量是_______ mol。
(3)10.8 g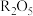 中氧原子的数目为
中氧原子的数目为 ,则元素R的摩尔质量为
,则元素R的摩尔质量为_______ 。
(4)质量相等的HCl、 、
、 、
、 四种气体中,含有分子数目最少的是
四种气体中,含有分子数目最少的是_______ 。
(5)将34. 2 g Al2(SO4)3固体溶于水配成100 mL溶液。从该溶液中取出10 mL,其中SO42-的物质的量浓度为_______ 。
(1)用双线桥表示CaH2+2H2O=Ca(OH)2+2H2↑反应电子转移情况:
(2)某元素的一种同位素X的质量数为A,含N个中子,它与1H原子组成
 分子。在a克
分子。在a克 中所含质子的物质的量是
中所含质子的物质的量是(3)10.8 g
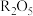 中氧原子的数目为
中氧原子的数目为 ,则元素R的摩尔质量为
,则元素R的摩尔质量为(4)质量相等的HCl、
 、
、 、
、 四种气体中,含有分子数目最少的是
四种气体中,含有分子数目最少的是(5)将34. 2 g Al2(SO4)3固体溶于水配成100 mL溶液。从该溶液中取出10 mL,其中SO42-的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)分析反应5NH4NO3=2HNO3+4N2↑+9H2O的电子转移方向和数目_______________ 。
(2)在上述反应中发生氧化反应的氮原子与发生还原反应的氮原子的个数比是________ 。
(3)在上述反应中每生成1mol硝酸生成N2的体积为________ L。(标准状况)
(2)在上述反应中发生氧化反应的氮原子与发生还原反应的氮原子的个数比是
(3)在上述反应中每生成1mol硝酸生成N2的体积为
您最近一年使用:0次
【推荐3】储氢纳米碳管研究成功体现了科技的进步。但用电弧法合成的碳纳米管常伴有大量的杂质——碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应方程式为3C+2K2Cr2O7+8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4) 3+8H2O。请回答下列问题:
(1)用单线桥法标明上述反应方程式中电子转移的方向和数目_______ (仅写出氧化剂和还原剂即可)。
(2)上述反应中氧化剂是_______ ,被氧化的元素是_______ (填元素符号) 。
(3)H2SO4在上述反应中表现出来的性质是_______(填标号)。
(4)请配平下列离子方程式_______ 。
_______Fe2+ + _______H+ +_______ = _______Fe3+ + _______N2O↑ + _______H2O
= _______Fe3+ + _______N2O↑ + _______H2O
(1)用单线桥法标明上述反应方程式中电子转移的方向和数目
(2)上述反应中氧化剂是
(3)H2SO4在上述反应中表现出来的性质是_______(填标号)。
| A.酸性 | B.氧化性 | C.氧化性和酸性 | D.还原性和酸性 |
_______Fe2+ + _______H+ +_______
 = _______Fe3+ + _______N2O↑ + _______H2O
= _______Fe3+ + _______N2O↑ + _______H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】1,2-二氯丙烷(CH2ClCHClCH3)是重要的化工原料,工业上可用丙烯加成法生产,主要副产物为3-氯丙烯(CH2=CHCH2C1) ,反应原理为
i. CH2=CHCH,3(g)+Cl2(g) CH2ClCHClCH3(g) ΔH1= -134 kJ• mol-1
CH2ClCHClCH3(g) ΔH1= -134 kJ• mol-1
ii. CH2=CHCH,3(g)+Cl2(g) CH2=CHCH2Cl (g)+HCl(g) ΔH2= -l02 kJ • mol-1
CH2=CHCH2Cl (g)+HCl(g) ΔH2= -l02 kJ • mol-1
已知:相关化学键的键能数据如下表所示:
请回答下列问题:
(1)由反应i计算出表中x=_____________ 。
(2)一定温度下,密闭容器中发生反应i和反应ii,达到平衡后增大压强,CH2C1CHClCH3的产率____________ (填“增大”“减小”或“不变”),理由是_________________________________ 。
(3)T1℃时,向10L恒容的密闭容器中充入1 mol CH2=CHCH2C1和2 mol HCl,只发生反应CH2=CH CH2Cl (g)+HCl(g) CH2ClCHClCH3(g) ΔH3。5min反应达到平衡,测得 0〜5 min内,用CH2ClCHClCH3表示的反应速率 v(CH2ClCHClCH3)=0.016 mol·L-1 • min-1。
CH2ClCHClCH3(g) ΔH3。5min反应达到平衡,测得 0〜5 min内,用CH2ClCHClCH3表示的反应速率 v(CH2ClCHClCH3)=0.016 mol·L-1 • min-1。
①平衡时,HCl的体积分数为__________________ (保留三位有效数字)。
②保持其它条件不变,6 min时再向该容器中充入0. 6 mol CH2=CHCH2Cl、0.2molHCl和0.1mol CH2ClCHClCH3,则起始反应速率 v正(HCl)______________ (填“>”“<”或“=”)V逆(HCl).
(4)一定压强下,向密闭容器中充入一定量的CH2=CHCH3和C12发生反应ii。设起始的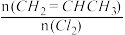 =w,平衡时Cl2的体积分数(φ)与温度(T)、w的关系如图甲所示。W=1时,正、逆反应的平衡常数(K)与温度(T)的关系如图乙所示。
=w,平衡时Cl2的体积分数(φ)与温度(T)、w的关系如图甲所示。W=1时,正、逆反应的平衡常数(K)与温度(T)的关系如图乙所示。

①图甲中,w2__________ (填“>”“<”或“=”)1
②图乙中,表示正反应平衡常数的曲线为____________ (填“A”或“B”),理由为________________ 。
③T1K下,平衡时a(Cl2)=________________ 。
(5)起始时向某恒容绝热容器中充入1 mol CH2 =CHCH3和1 mol Cl2发生反应ii,达到平衡时,容器内气体压强_________________ (填“增大”“减小”或“不变”)。
i. CH2=CHCH,3(g)+Cl2(g)
 CH2ClCHClCH3(g) ΔH1= -134 kJ• mol-1
CH2ClCHClCH3(g) ΔH1= -134 kJ• mol-1ii. CH2=CHCH,3(g)+Cl2(g)
 CH2=CHCH2Cl (g)+HCl(g) ΔH2= -l02 kJ • mol-1
CH2=CHCH2Cl (g)+HCl(g) ΔH2= -l02 kJ • mol-1 已知:相关化学键的键能数据如下表所示:
| 化学键 | C—C | C—C | C—Cl | Cl—Cl |
| E/( kJ • mol-1) | 611 | x | 328 | 243 |
请回答下列问题:
(1)由反应i计算出表中x=
(2)一定温度下,密闭容器中发生反应i和反应ii,达到平衡后增大压强,CH2C1CHClCH3的产率
(3)T1℃时,向10L恒容的密闭容器中充入1 mol CH2=CHCH2C1和2 mol HCl,只发生反应CH2=CH CH2Cl (g)+HCl(g)
 CH2ClCHClCH3(g) ΔH3。5min反应达到平衡,测得 0〜5 min内,用CH2ClCHClCH3表示的反应速率 v(CH2ClCHClCH3)=0.016 mol·L-1 • min-1。
CH2ClCHClCH3(g) ΔH3。5min反应达到平衡,测得 0〜5 min内,用CH2ClCHClCH3表示的反应速率 v(CH2ClCHClCH3)=0.016 mol·L-1 • min-1。①平衡时,HCl的体积分数为
②保持其它条件不变,6 min时再向该容器中充入0. 6 mol CH2=CHCH2Cl、0.2molHCl和0.1mol CH2ClCHClCH3,则起始反应速率 v正(HCl)
(4)一定压强下,向密闭容器中充入一定量的CH2=CHCH3和C12发生反应ii。设起始的
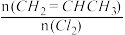 =w,平衡时Cl2的体积分数(φ)与温度(T)、w的关系如图甲所示。W=1时,正、逆反应的平衡常数(K)与温度(T)的关系如图乙所示。
=w,平衡时Cl2的体积分数(φ)与温度(T)、w的关系如图甲所示。W=1时,正、逆反应的平衡常数(K)与温度(T)的关系如图乙所示。
①图甲中,w2
②图乙中,表示正反应平衡常数的曲线为
③T1K下,平衡时a(Cl2)=
(5)起始时向某恒容绝热容器中充入1 mol CH2 =CHCH3和1 mol Cl2发生反应ii,达到平衡时,容器内气体压强
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】热化学方程式中的化学计量数为_______ 。故化学计量数可以是_______ ,也可以是_______ 。当化学计量数改变时,其 也
也_______ 的改变。
 也
也
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.键能是指拆开1mol共价键所需要吸收的能量或形成1mol共价键所放出的能量。
(1)已知键能:H-H键为436 ;H-F键为565
;H-F键为565 ;H-Cl键为431
;H-Cl键为431 ;H-Br键为366
;H-Br键为366 。则下列分子受热时最稳定的是___________。
。则下列分子受热时最稳定的是___________。
(2)能用键能大小解释的是___________。
Ⅱ.下表列出了一些化学键的键能E:
请回答下列问题:
(3)反应
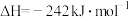 ,
,
___________ 。
(4)历史上曾用“地康法”制 ,这一方法是用
,这一方法是用 做催化剂,在450°条件下,用空气中的氧气跟氯化氢反应制氯气,若反应生成液态水,请写出该反应的热化学方程式为
做催化剂,在450°条件下,用空气中的氧气跟氯化氢反应制氯气,若反应生成液态水,请写出该反应的热化学方程式为___________ 。
(5)若忽略温度和压强对反应热的影响,根据上题中的有关数据,计算当反应中有1mol电子转移时,反应的能量变化为___________ 。
Ⅲ.关于 ,已知1mol
,已知1mol  (g)被氧化为1mol
(g)被氧化为1mol  (g)的
(g)的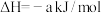
 。回答下列问题:
。回答下列问题:
(6)在一定温度下,将2mol 和1mol
和1mol  放在一密闭容器中,在催化剂作用下充分反应。测得反应放出的热量
放在一密闭容器中,在催化剂作用下充分反应。测得反应放出的热量___________ (填“等于”、“大于”或“小于”)2akJ。
(7) 的催化循环机理可能为:
的催化循环机理可能为: 氧化
氧化 时,自己被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式:
时,自己被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式:
①___________ ;②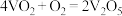
(8)已知固态单质硫的燃烧热为b kJ/mol,计算由S(s)生成3mol (g)的
(g)的
___________ 。
(1)已知键能:H-H键为436
 ;H-F键为565
;H-F键为565 ;H-Cl键为431
;H-Cl键为431 ;H-Br键为366
;H-Br键为366 。则下列分子受热时最稳定的是___________。
。则下列分子受热时最稳定的是___________。| A.HF | B.HCl | C.HBr | D. |
| A.氮气的化学性质比氧气稳定 | B.常温常压下溴呈液态,碘呈固态 |
| C.稀有气体一般很难发生化学反应 | D.硝酸易挥发而硫酸难挥发 |
Ⅱ.下表列出了一些化学键的键能E:
| 化学键 | H—H | Cl—Cl | O=O | C—Cl | C—H | O—H | H—Cl |
E/( ) ) | 436 | 247 | x | 330 | 413 | 463 | 431 |
请回答下列问题:
(3)反应

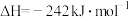 ,
,
(4)历史上曾用“地康法”制
 ,这一方法是用
,这一方法是用 做催化剂,在450°条件下,用空气中的氧气跟氯化氢反应制氯气,若反应生成液态水,请写出该反应的热化学方程式为
做催化剂,在450°条件下,用空气中的氧气跟氯化氢反应制氯气,若反应生成液态水,请写出该反应的热化学方程式为(5)若忽略温度和压强对反应热的影响,根据上题中的有关数据,计算当反应中有1mol电子转移时,反应的能量变化为
Ⅲ.关于
 ,已知1mol
,已知1mol  (g)被氧化为1mol
(g)被氧化为1mol  (g)的
(g)的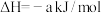
 。回答下列问题:
。回答下列问题:(6)在一定温度下,将2mol
 和1mol
和1mol  放在一密闭容器中,在催化剂作用下充分反应。测得反应放出的热量
放在一密闭容器中,在催化剂作用下充分反应。测得反应放出的热量(7)
 的催化循环机理可能为:
的催化循环机理可能为: 氧化
氧化 时,自己被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式:
时,自己被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式:①
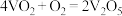
(8)已知固态单质硫的燃烧热为b kJ/mol,计算由S(s)生成3mol
 (g)的
(g)的
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】一个完整的氧化还原反应方程式可以拆写成两个“半反应式”,如2Fe3++Cu = 2Fe2++Cu2+,可拆写为氧化反应式:Cu-2e- = Cu2+,还原反应式:2Fe3++2e- = 2Fe2+。并由此实现了化学能与电能的相互转化。据此,回答下列问题。
(1)将反应Zn+2H+= Zn2++H2↑拆写为两个“半反应式”,氧化反应式为:___________ ,还原反应式为:___________ 。
(2)由题(1)反应,设计成原电池如图所示:
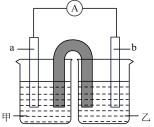
若电极a为Zn,电极b可选择材料:___________ (只填一种);电解质溶液甲是___________ ;电极b处的电极反应式:___________ 。
(3)由反应2H2+O2 2H2O,设计出以稀硫酸为电解质溶液的原电池电极反应式:负极
2H2O,设计出以稀硫酸为电解质溶液的原电池电极反应式:负极___________ ,正极:___________ 。
(1)将反应Zn+2H+= Zn2++H2↑拆写为两个“半反应式”,氧化反应式为:
(2)由题(1)反应,设计成原电池如图所示:

若电极a为Zn,电极b可选择材料:
(3)由反应2H2+O2
 2H2O,设计出以稀硫酸为电解质溶液的原电池电极反应式:负极
2H2O,设计出以稀硫酸为电解质溶液的原电池电极反应式:负极
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题
(1)根据已具备的氧化还原反应知识和电化学知识,结合图示回答下列问题:

①该原电池负极材料是______________ 。
②写出电极反应式:正极:__________________ ;负极:__________________ 。
③若电路中转移了 ,则析出的
,则析出的 的质量为
的质量为____________ 。
(2)燃料电池是利用燃料与氧气反应从而将化学能转化为电能的装置。以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。

①A为生物燃料电池的_____________ (填“正”或“负”)极。
②正极反应式为_________ 。
③放电过程中,H+由_________ 极区向______ 极区迁移(填“正”或“负”)。
(1)根据已具备的氧化还原反应知识和电化学知识,结合图示回答下列问题:

①该原电池负极材料是
②写出电极反应式:正极:
③若电路中转移了
 ,则析出的
,则析出的 的质量为
的质量为(2)燃料电池是利用燃料与氧气反应从而将化学能转化为电能的装置。以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。

①A为生物燃料电池的
②正极反应式为
③放电过程中,H+由
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】银制器皿表面日久因生成Ag2S而变黑,可进行如下处理:将表面发黑的银器浸入盛有食盐水的铝质容器中(如图),一段时间后黑色褪去。回答下列问题:
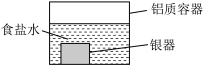
(1)银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故,该现象属于__________ 腐蚀(填“化学”或“电化学”)。
(2)铝质容器作为__________ 极,银器的电极反应式为____________ 。
(3)处理过程中总反应的化学方程式为_______________ 。
(4)若将铝质容器中的食盐水用浓硝酸代替,则铝质容器极的电极反应式为____________ 。

(1)银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故,该现象属于
(2)铝质容器作为
(3)处理过程中总反应的化学方程式为
(4)若将铝质容器中的食盐水用浓硝酸代替,则铝质容器极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】利用下列反应: 设计一个原电池,请选择适当的材料和试剂。
设计一个原电池,请选择适当的材料和试剂。
I. 请写出你选用的正极材料、负极材料、电解质溶液
请写出你选用的正极材料、负极材料、电解质溶液 写化学式
写化学式 :正极为
:正极为_____________ ,电解质溶液:_____________ ;
 负极反应式:
负极反应式: ____________________ ;
 溶液中
溶液中 向
向 __________ 极移动。
II.A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
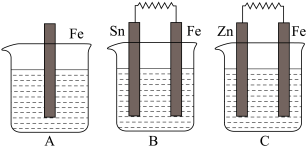
(1)B中Sn极的电极反应式为_________________ 。
(2)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是_____________________ 。
 设计一个原电池,请选择适当的材料和试剂。
设计一个原电池,请选择适当的材料和试剂。I.
 请写出你选用的正极材料、负极材料、电解质溶液
请写出你选用的正极材料、负极材料、电解质溶液 写化学式
写化学式 :正极为
:正极为 负极反应式:
负极反应式:  溶液中
溶液中 向
向 II.A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。

(1)B中Sn极的电极反应式为
(2)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的项重大贡献。
(1)某课外实验小组欲探究铝和铜的金属性(原子失电子能力)强弱,同学们提出了如下实验方案:
A.比较铝和铜的硬度和熔点
B.比较二者在稀硫酸中的表现
C.用铝片、铜片、硫酸铝溶液、硫酸铜溶液,比较二者的活动性
D.分别做铝片、铜片与NaOH溶液反应的实验
E.将铝片、铜片用导线连接后共同投入稀盐酸中接入电流计,观察电流方向
上述方案中能达到实验目的的是_________________ 。
(2)现有如下两个反应:A.NaOH+HCl=NaCl+H2O B.Zn+H2SO4=ZnSO4+H2↑。上述反应中能设计成原电池的是________ (填字母代号),作负极的物质发生了________ 反应(填“氧化”或“还原”)。
(3)将纯锌片和纯铜片按如图所示方式插入100mL相同浓度的稀硫酸一段时间,回答下列问题:
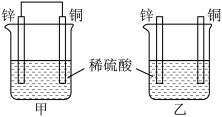
①下列说法正确的是________ (填字母代号)。
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的酸性均减弱
②在相同时间内,两烧杯中产生气泡的速度:甲________ 乙(填“>”、“<”或“=”)。原因是________ 。
③当甲中产生1.12L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1L,测得溶液中c(H+)=0.1mol/L(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为____________ 。
(1)某课外实验小组欲探究铝和铜的金属性(原子失电子能力)强弱,同学们提出了如下实验方案:
A.比较铝和铜的硬度和熔点
B.比较二者在稀硫酸中的表现
C.用铝片、铜片、硫酸铝溶液、硫酸铜溶液,比较二者的活动性
D.分别做铝片、铜片与NaOH溶液反应的实验
E.将铝片、铜片用导线连接后共同投入稀盐酸中接入电流计,观察电流方向
上述方案中能达到实验目的的是
(2)现有如下两个反应:A.NaOH+HCl=NaCl+H2O B.Zn+H2SO4=ZnSO4+H2↑。上述反应中能设计成原电池的是
(3)将纯锌片和纯铜片按如图所示方式插入100mL相同浓度的稀硫酸一段时间,回答下列问题:

①下列说法正确的是
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的酸性均减弱
②在相同时间内,两烧杯中产生气泡的速度:甲
③当甲中产生1.12L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1L,测得溶液中c(H+)=0.1mol/L(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某学生为探究锌与盐酸反应过程中的速率变化,在 时,向100 mL 2 mol·L-1盐酸中加入过量的锌粉,测得氢气体积(已换算成标准状况)累计值如下:
时,向100 mL 2 mol·L-1盐酸中加入过量的锌粉,测得氢气体积(已换算成标准状况)累计值如下:
(1)①在2~3 min时间段内,用盐酸的浓度变化表示的反应速率为_______ .
②在0~5min内,反应速率最大的时间段是___ (填 “1~2 min”、“2~3 min”或“3~4 min”)。
(2)若完全反应后放出15.2 kJ的热量,则反应Zn(s) + 2HCl(aq)=ZnCl2(aq) + H2(g)的△H=____
(3)为了减缓反应速率但不减少产生气体的量,可向反应物中分别加入等体积的下列液体,你认为可行的是_______ (填字母)。
a. 蒸馏水 b. Na2CO3溶液 c. NaNO3溶液
(4)为了加快反应速率但不减少产生气体的量,某同学向反应物中加入了少量CuSO4固体,该同学操作____ (填 “合理”或“不合理”),理由是_______
 时,向100 mL 2 mol·L-1盐酸中加入过量的锌粉,测得氢气体积(已换算成标准状况)累计值如下:
时,向100 mL 2 mol·L-1盐酸中加入过量的锌粉,测得氢气体积(已换算成标准状况)累计值如下:| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
②在0~5min内,反应速率最大的时间段是
(2)若完全反应后放出15.2 kJ的热量,则反应Zn(s) + 2HCl(aq)=ZnCl2(aq) + H2(g)的△H=
(3)为了减缓反应速率但不减少产生气体的量,可向反应物中分别加入等体积的下列液体,你认为可行的是
a. 蒸馏水 b. Na2CO3溶液 c. NaNO3溶液
(4)为了加快反应速率但不减少产生气体的量,某同学向反应物中加入了少量CuSO4固体,该同学操作
您最近一年使用:0次



