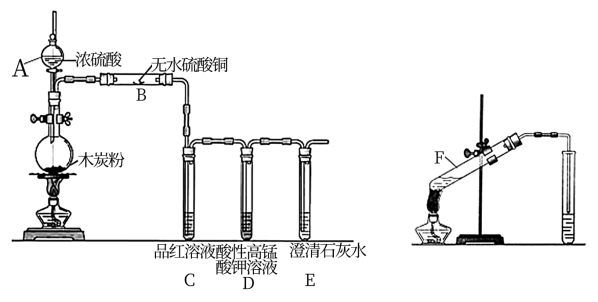
浓硫酸与木炭在加热条件下可发生化学反应,为检验反应的产物,某同学设计了如图所示的实验。请据此回答下列问题:
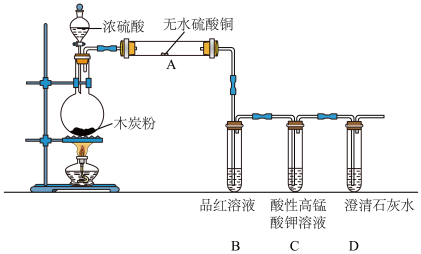
(1)圆底烧瓶内发生反应的化学方程式为______ 。
(2)A装置现象是______ ,证明产物中______ 生成(填写化学式,下同)。
(3)B装置证明产物中有______ 生成,现象是______ 。
(4)D装置证明产物中有______ 生成,现象是______ 。
(5)C装置的作用是______ ,发生反应的离子方程式是______ 。

(1)圆底烧瓶内发生反应的化学方程式为
(2)A装置现象是
(3)B装置证明产物中有
(4)D装置证明产物中有
(5)C装置的作用是
更新时间:2023-06-10 17:17:53
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】以高铁脱硫渣(主要成分为Fe2O3、Fe3O4、Al2O3等)为原料,可制备高纯度七水合硫酸亚铁(FeSO4•7H2O)和草酸亚铁晶体(FeC2O4•2H2O)。
(1)制备高纯硫酸亚铁晶体
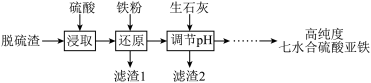
如表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1mol·L-1计算)。
①“浸取”中Fe3O4发生反应的离子方程式为____ 。实验表明,“浸取”中所用硫酸浓度不宜过高,其原因可能是____ 。
②用生石灰调节溶液pH约5.0,所得“滤渣2”的主要成分为____ (填化学式)。
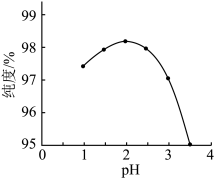
③获得高纯度七水合硫酸亚铁晶体前须要在硫酸亚铁溶液中先用硫酸调节pH,实验测得其他条件相同时溶液pH对产品纯度的影响如图所示,当pH>2.0时,硫酸亚铁晶体纯度下降的原因是____ 。
(2)制备高纯草酸亚铁晶体
实验方案:将一定量的高纯度七水合硫酸亚铁晶体溶于水配成溶液,在搅拌条件下将氨水加入上述纯净硫酸亚铁溶液中,____ (实验中还须使用的试剂有:草酸溶液,水,氯化钡溶液)。已知:草酸亚铁晶体难溶于水,受热易分解。
(1)制备高纯硫酸亚铁晶体

如表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1mol·L-1计算)。
| 金属 | 离子开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.9 | 3.2 |
| Al3+ | 3.4 | 4.7 |
| Fe2+ | 7.0 | 9.0 |
②用生石灰调节溶液pH约5.0,所得“滤渣2”的主要成分为
③获得高纯度七水合硫酸亚铁晶体前须要在硫酸亚铁溶液中先用硫酸调节pH,实验测得其他条件相同时溶液pH对产品纯度的影响如图所示,当pH>2.0时,硫酸亚铁晶体纯度下降的原因是

(2)制备高纯草酸亚铁晶体
实验方案:将一定量的高纯度七水合硫酸亚铁晶体溶于水配成溶液,在搅拌条件下将氨水加入上述纯净硫酸亚铁溶液中,
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】铁合金有下列数据:
取15g某碳素钢样品,按下列实验流程进行操作;
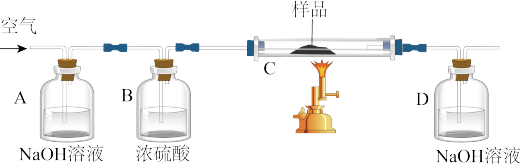
请回答:
(1)A、B的作用分别为_______ ,_______ 。
(2)D中的发生反应的离子方程式为_______ 。
(3)充分加热完全反应后,D装置质量增加0.022g,该样品含碳量为_______ ,属于_______ 碳铜。(填“低”、“中”、“高”)
(4)没有A装置,实验结果_______ (填“偏高”、“偏低”成“不影响”)
| 碳素钢(Fe、C、Mn、Si) | ||
| 低碳钢 | 中碳钢 | 高碳钢 |
| 含碳量<0.3% | 含碳量0.3%-0.6% | 含碳量>0.6% |

请回答:
(1)A、B的作用分别为
(2)D中的发生反应的离子方程式为
(3)充分加热完全反应后,D装置质量增加0.022g,该样品含碳量为
(4)没有A装置,实验结果
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】硫铁矿的主要成分为FeS2,工业上常用硫铁矿在空气中煅烧产气来制备硫酸,该过程中的烧渣可用于制备铁红、绿矾等。现以硫铁矿烧渣(主要成分为Fe2O3,FeO,还含有少量的Al2O3、SiO2杂质)为原料、氨水为沉淀剂制备铁红颜料的流程如图所示:
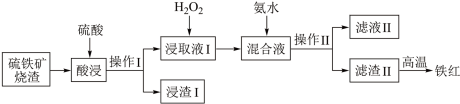
根据所学知识,回答下列问题:
(1)已知FeS2高温煅烧生成Fe2O3和SO2,请写出化学方程式:_______ ,其中氧化产物为_______ (填化学式)。
(2)“浸取液I”中加入H2O2的目的是_______ 。
(3)进行操作I所需的玻璃仪器有_______ 。
(4)在加入氨水沉淀时,调节pH可使得Fe3+沉淀而Al3+不沉淀。“滤液Ⅱ”中溶质的主要成分为_______ (填化学式)。写出获得“滤渣Ⅱ”的离子方程式:_______ 。检验滤液Ⅱ中是否存在Fe3+,应用_______ 试剂。

根据所学知识,回答下列问题:
(1)已知FeS2高温煅烧生成Fe2O3和SO2,请写出化学方程式:
(2)“浸取液I”中加入H2O2的目的是
(3)进行操作I所需的玻璃仪器有
(4)在加入氨水沉淀时,调节pH可使得Fe3+沉淀而Al3+不沉淀。“滤液Ⅱ”中溶质的主要成分为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】有关物质的转化关系如下图所示(部分物质已略去)。A、C都是金属氧化物,其中C为淡黄色,B是一种常见的强酸(图中为高浓度B),D是最常见的无色液体,E、F、H都是常见的气体,且E、F都可用于漂白,H是空气中主要成分之一,I、J都是由三种相同元素(短周期元素)组成的盐。

请回答下列问题:
(1)G的电子式为___________ 。
(2)I的化学式为___________ 。
(3)写出反应①的化学方程式___________ 。

请回答下列问题:
(1)G的电子式为
(2)I的化学式为
(3)写出反应①的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】二氧化硫性质探究
| 实验操作 | (1)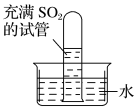 (2)测溶液pH | 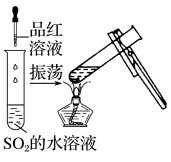 |
| 实验现象 | (1)试管中 (2)pH试纸呈 | 振荡后 |
| 结论 | SO2 |
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】如表是元素周期表的一部分,其中X,Y、Z、Q、W、R为短周期元素,Q元素的周期数和主族序数相同。用具体的元素符号表示物质来回答下列问题:
(1)T的最高价氧化物的化学式为______ ,Q在元素周期表中的位置是______ 。
(2)Q的单质与烧碱溶液反应的离子方程式为______ 。
(3)YZ2在碱性溶液(含NaOH)中可被NaClO氧化,该反应的化学方程式为______ 。
(4)H3WZ2是一种极易溶于水的一元弱酸,其与过量NaOH溶液反应的离子方程式为_____ 。
(5)写出由上述两种元素形成的具有漂白性的物质的化学式:______ 。
(6)X、Y、Z、Q、W、R的原子半径由大到小的顺序为______ (填化学式)。
| X | Y | Z | |
| Q | W | R | |
| T |
(2)Q的单质与烧碱溶液反应的离子方程式为
(3)YZ2在碱性溶液(含NaOH)中可被NaClO氧化,该反应的化学方程式为
(4)H3WZ2是一种极易溶于水的一元弱酸,其与过量NaOH溶液反应的离子方程式为
(5)写出由上述两种元素形成的具有漂白性的物质的化学式:
(6)X、Y、Z、Q、W、R的原子半径由大到小的顺序为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】某兴趣小组为探究铜与浓硫酸的反应,设计如图所示装置进行实验。请回答有关问题:

(1)装置A中盛放浓硫酸的仪器名称是_______ ,其中反应的化学方程式为_______ 。
(2)实验过程中,根据装置C、D内产生的现象分别说明了SO2具有的性质是_______ 和_______ 。若加热装置D,可观察到的现象是_______ 。
(3)装置B的作用是储存多余的气体。当装置D处有明显现象后,关闭K,移去酒精灯,但由于余热的作用,装置A处仍有气体产生,此时装置B中的现象是_______ 。装置B中应放置的液体是_______ (填字母)。
a.水 b.酸性KMnO4溶液 c.浓溴水 d.饱和NaHSO3溶液

(1)装置A中盛放浓硫酸的仪器名称是
(2)实验过程中,根据装置C、D内产生的现象分别说明了SO2具有的性质是
(3)装置B的作用是储存多余的气体。当装置D处有明显现象后,关闭K,移去酒精灯,但由于余热的作用,装置A处仍有气体产生,此时装置B中的现象是
a.水 b.酸性KMnO4溶液 c.浓溴水 d.饱和NaHSO3溶液
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】Ⅰ.兴趣小组1组同学利用如图所示装置(夹持装置已略去)探究SO2的性质,并制取一种常用食品抗氧化剂焦亚硫酸钠(Na2S2O5)。(实验前已除去装置中的空气)
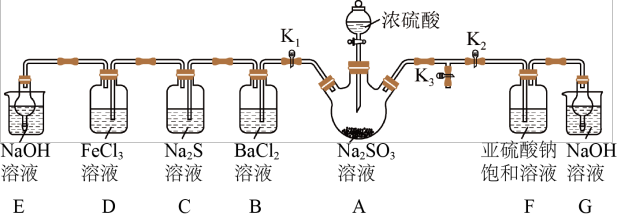
(1)A中发生反应的化学方程式为______ 。
(2)关闭K2、K3,打开K1。
①装置B中的现象是______ 。
②装置C中出现淡黄色浑浊,说明SO2具有______ 性。
③装置E和G中NaOH溶液的作用是______ 。
(3)关闭K1、K3,打开K2。一段时间后F中有Na2S2O5晶体析出,装置F中发生反应的化学方程式_______ 。
(4)Na2S2O5晶体久置空气中易被氧化为Na2SO4,检验其在空气中已被氧化的操作和现象:取少量Na2S2O5晶体于试管中,加适量水溶解,______ 。
Ⅱ.兴趣小组2组同学用如图所示装置测定某硫酸厂附近空气中二氧化硫的含量。
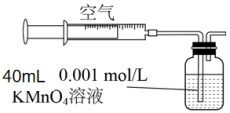
(5)当注入标准状况下200mL空气时,酸性KMnO4溶液恰好褪色,停止实验。该空气中SO2的体积分数为_____ 。(已知反应原理为:5SO2+2MnO +2H2O=2Mn2++5SO
+2H2O=2Mn2++5SO +4H+)
+4H+)

(1)A中发生反应的化学方程式为
(2)关闭K2、K3,打开K1。
①装置B中的现象是
②装置C中出现淡黄色浑浊,说明SO2具有
③装置E和G中NaOH溶液的作用是
(3)关闭K1、K3,打开K2。一段时间后F中有Na2S2O5晶体析出,装置F中发生反应的化学方程式
(4)Na2S2O5晶体久置空气中易被氧化为Na2SO4,检验其在空气中已被氧化的操作和现象:取少量Na2S2O5晶体于试管中,加适量水溶解,
Ⅱ.兴趣小组2组同学用如图所示装置测定某硫酸厂附近空气中二氧化硫的含量。

(5)当注入标准状况下200mL空气时,酸性KMnO4溶液恰好褪色,停止实验。该空气中SO2的体积分数为
 +2H2O=2Mn2++5SO
+2H2O=2Mn2++5SO +4H+)
+4H+)
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】某化学兴趣小组为了探究SO2的性质以及硫酸型酸雨的形成设计了如图的实验。

请回答下列问题:
(1)装置a中可观察到的现象为__ ,说明SO2具有的性质是___ 。
(2)装置b中产生的现象为__ ,写出其反应的离子方程式:___ 。
(3)装置c的作用是___ 。
(4)若按图d所示,将一定量的SO2通入水中,测得所得溶液的pH___ (填“>”或“<”)7,然后每隔1h测定其pH,发现pH逐渐__ (填“变大”或“变小”),直至恒定。解释其原因:__ (用化学方程式表示)。
(5)SO2形成酸雨的另一途径为SO2与空气中O2在飘尘的作用下反应生成SO3,SO3溶于降水生成H2SO4,则在此过程中的飘尘是作为___ (填“催化剂”或“氧化剂”)。

请回答下列问题:
(1)装置a中可观察到的现象为
(2)装置b中产生的现象为
(3)装置c的作用是
(4)若按图d所示,将一定量的SO2通入水中,测得所得溶液的pH
(5)SO2形成酸雨的另一途径为SO2与空气中O2在飘尘的作用下反应生成SO3,SO3溶于降水生成H2SO4,则在此过程中的飘尘是作为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】某小组同学利用下图所示装置完成碳与浓硫酸反应的实验,开验证所得全部产物。请完成下列空白。

(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:_____ 。
(2)如果用图中的装置检验上述反应的全部产物,写出下面标号所表示的仪器中应加入的试剂的名称及其作用:
A中加入的试剂_____ ,作用是_____ 。
B中加入的试剂_____ ,作用是_____ 。
D中加入的试剂_____ ,作用是_____ 。
(3)实验时,C中应观察到的现象是紫色_____ (“消失”或“变浅不消失”),原因是_____ 。

(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:
(2)如果用图中的装置检验上述反应的全部产物,写出下面标号所表示的仪器中应加入的试剂的名称及其作用:
A中加入的试剂
B中加入的试剂
D中加入的试剂
(3)实验时,C中应观察到的现象是紫色
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
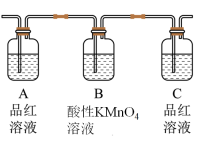
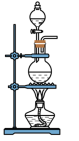
【推荐2】某研究性学习小组欲开展一次以化学为主题的活动,确定的课题是“研究浓硫酸与木炭粉在加热条件下反应的产物”。根据小组成员的推测,浓硫酸与木炭粉在加热条件下反应的产物可能有CO2、SO2,为了验证推测,小组讨论用以下装置进行实验:
请回答:
⑴ 实验时可观察装置a中A瓶溶液褪色,C瓶溶液不褪色。则A瓶溶液的作用___ ,C瓶溶液的作用_____ ;
⑵ 装置b中所加的液体是________ ,装置b可验证的产物是________ ;
⑶ 甲、乙两位同学分别设计了两套不同装置。甲的装置顺序:c→b→a,乙的装置顺序:c→a→b。你认为合理的是(填“甲”或“乙”)__ ;
⑷写出装置c中发生的化学方程式:__________
编号 | a | b | c |
装置 |
|
|
|
⑴ 实验时可观察装置a中A瓶溶液褪色,C瓶溶液不褪色。则A瓶溶液的作用
⑵ 装置b中所加的液体是
⑶ 甲、乙两位同学分别设计了两套不同装置。甲的装置顺序:c→b→a,乙的装置顺序:c→a→b。你认为合理的是(填“甲”或“乙”)
⑷写出装置c中发生的化学方程式:
您最近一年使用:0次

 的名称是
的名称是 中的现象为
中的现象为 作用为
作用为 中首先加入的试剂是
中首先加入的试剂是

