我国政府承诺2030年前实现“碳达峰”,使二氧化碳的排放不再增长,达到峰值之后逐步降低。CO2的减排已经引起国际社会的广泛关注,我国科学家实现了CO2高选择性、高稳定性加氢合成甲醇(CH3OH)。设NA为阿伏加德罗常数的值。
(1)CH3OH的摩尔质量为___________ g·mol-1。
(2)0.2molH2O中所含原子的数目为___________ ,所含质子数为___________ 。
(3)___________ g水中所含氢原子的数目与1molCH3OH所含氢原子数相同。
(4)含0.1NA个O原子的CO2中所含电子数为___________ 。
(5)16gCH3OH完全燃烧生成CO2和H2O,消耗O2的体积为___________ (标准状况)。
(1)CH3OH的摩尔质量为
(2)0.2molH2O中所含原子的数目为
(3)
(4)含0.1NA个O原子的CO2中所含电子数为
(5)16gCH3OH完全燃烧生成CO2和H2O,消耗O2的体积为
2023高三·全国·专题练习 查看更多[1]
(已下线)考点06 物质的量 气体摩尔体积(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
更新时间:2023-08-12 10:36:18
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】计算填空:
(1)某气体标准状况下的密度为 1.43g/L,该气体的相对分子质量是___________ 。
(2)1.204×1024 个 NH3 分子所含的氢原子数与___________ mol CH4 含有的氢原子数相同。
(3)ag H2SO4 中含有 b 个氧原子,则阿伏加德罗常数可以表示为___________ 。
(4)12.4 g Na2R 含 Na+0.4 mol,则 Na2R 的摩尔质量为___________ ,R 的相对原子质量为___________ 。
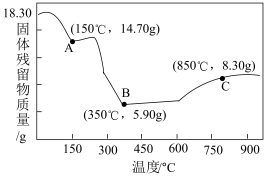
(5)CoC2O42H2O (M=183g/mol)热分解的质量变化过程如图所示,其中600C 之前是隔绝空气加热,600C 之后是在空气中加热,A、B、C 三点时的产物均为纯净物。用化学方程式表示从 A 点到 B 点的物质转化:___________________ , C 点时产物的化学式是_____________ 。
(1)某气体标准状况下的密度为 1.43g/L,该气体的相对分子质量是
(2)1.204×1024 个 NH3 分子所含的氢原子数与
(3)ag H2SO4 中含有 b 个氧原子,则阿伏加德罗常数可以表示为
(4)12.4 g Na2R 含 Na+0.4 mol,则 Na2R 的摩尔质量为
(5)CoC2O42H2O (M=183g/mol)热分解的质量变化过程如图所示,其中600C 之前是隔绝空气加热,600C 之后是在空气中加热,A、B、C 三点时的产物均为纯净物。用化学方程式表示从 A 点到 B 点的物质转化:

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】等物质的量的CO和CO2所含的原子个数之比是____ ;3molNH3分子中所含原子数与____ molH2O分子中所含原子数相等;19g某二价金属的氯化物ACl2中含有0.4molCl-,A的摩尔质量是____ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如图是可用于测量阿伏加德罗常数的装置示意图,其中A是纯铜片、B是石墨,插在100mLCuSO4稀溶液中,铜片、石墨与引出导线相连,引出端分别为X、Y。
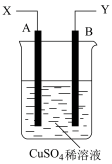
(1)当以IA的电流电解6min后,测得铜片A的质量减少了2.56g,则图装置中的X端应与直流电的____ 极相连。
(2)电解后将电源反接,2IA的电流电解6min后,假设溶液体积不变,测得溶液中CuSO4物质的量浓度为0.1mol/L,则原溶液中CuSO4物质的量浓度_________ mol/L。溶液中H+的物质的量浓度为___________ mol/L。
(3)列式计算实验测得的阿伏加德罗常数NA(用I表示)____________ mol-1。(已知电子电量e=1.60×10–19C)

(1)当以IA的电流电解6min后,测得铜片A的质量减少了2.56g,则图装置中的X端应与直流电的
(2)电解后将电源反接,2IA的电流电解6min后,假设溶液体积不变,测得溶液中CuSO4物质的量浓度为0.1mol/L,则原溶液中CuSO4物质的量浓度
(3)列式计算实验测得的阿伏加德罗常数NA(用I表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)标准状况下,1.7gNH3与___ LH2S气体含有的氢原子数相同。
(2)标准状况,NH3与CH4组成的混合气体的平均密度为0.75g·L-1,该混合气体的平均摩尔质量为___ ,NH3的体积分数为___ 。
(3)常温下,在27.9g水中溶解12.1gCu(NO3)2·3H2O,恰好达到饱和。设该溶液密度为1.20g·cm-3。
求:①溶质的质量分数为___ 。
②该溶液中NO 的物质的量浓度为
的物质的量浓度为___ 。
③取出20.0mL该溶液,配成浓度为1.00mol·L-1的稀溶液,则稀释后溶液的体积是___ mL。
④将一根质量为100g的铁棒插入到该溶液中,一段时间后取出,洗净、干燥后称量,铁棒的质量变为100.2g,此时溶液中Fe(NO3)2的物质的量浓度是___ (忽略溶液体积的变化)。
(1)标准状况下,1.7gNH3与
(2)标准状况,NH3与CH4组成的混合气体的平均密度为0.75g·L-1,该混合气体的平均摩尔质量为
(3)常温下,在27.9g水中溶解12.1gCu(NO3)2·3H2O,恰好达到饱和。设该溶液密度为1.20g·cm-3。
求:①溶质的质量分数为
②该溶液中NO
 的物质的量浓度为
的物质的量浓度为③取出20.0mL该溶液,配成浓度为1.00mol·L-1的稀溶液,则稀释后溶液的体积是
④将一根质量为100g的铁棒插入到该溶液中,一段时间后取出,洗净、干燥后称量,铁棒的质量变为100.2g,此时溶液中Fe(NO3)2的物质的量浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求填空。
(1)下列物质中:①稀硫酸②液氯③熔融氯化钠④Fe⑤二氧化碳⑥乙醇⑦BaSO4,属于电解质的是______ (填序号,下同);能直接导电的是______ 。
(2)请写出下列反应的离子方程式。
①盐酸除去铁锈(主要成分为氧化铁)______ 。
②溴水与NaI溶液反应______ 。
③FeCl2溶液与新制氯水反应______ 。
(3)1.204×1024个H2SO4分子的质量为______ g,共含______ 个氢原子。
(4)工业废水中含有有毒的重铬酸根离子( ),必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)还原
),必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)还原 得Cr3+和Fe3+,再通过沉淀处理法来处理该污水。写出该过程中Fe2+还原
得Cr3+和Fe3+,再通过沉淀处理法来处理该污水。写出该过程中Fe2+还原 的离子方程式
的离子方程式______ 。
(1)下列物质中:①稀硫酸②液氯③熔融氯化钠④Fe⑤二氧化碳⑥乙醇⑦BaSO4,属于电解质的是
(2)请写出下列反应的离子方程式。
①盐酸除去铁锈(主要成分为氧化铁)
②溴水与NaI溶液反应
③FeCl2溶液与新制氯水反应
(3)1.204×1024个H2SO4分子的质量为
(4)工业废水中含有有毒的重铬酸根离子(
 ),必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)还原
),必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)还原 得Cr3+和Fe3+,再通过沉淀处理法来处理该污水。写出该过程中Fe2+还原
得Cr3+和Fe3+,再通过沉淀处理法来处理该污水。写出该过程中Fe2+还原 的离子方程式
的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】根据所学知识填空:
(1)___________ mol H2O中含有的氧原子数与1.5 mol CO2中含有的氧原子数相等。
(2)标准状况下,4.48L NH3中N原子质量为___________ g,H原子数目为___________ 。
(3)已知a g A和b g B恰好完全反应生成0.2 mol C和d g D,则C的摩尔质量为___________ (用含a、b、d的表达式表示)。
(4)NA为阿伏加德罗常数,标准状况下,m g某气体中含有b个分子,则n g该气体在相同状态下的体积为___________ L(用含m、n、b、NA的表达式表示)
(5)将80.0 g无水硫酸铁溶于水配制成500 mL溶液,若从中取出50 mL,用水稀释到100 mL,所得溶液中Fe3+的物质的量浓度为___________ 。
(1)
(2)标准状况下,4.48L NH3中N原子质量为
(3)已知a g A和b g B恰好完全反应生成0.2 mol C和d g D,则C的摩尔质量为
(4)NA为阿伏加德罗常数,标准状况下,m g某气体中含有b个分子,则n g该气体在相同状态下的体积为
(5)将80.0 g无水硫酸铁溶于水配制成500 mL溶液,若从中取出50 mL,用水稀释到100 mL,所得溶液中Fe3+的物质的量浓度为
您最近一年使用:0次



