短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示,其中A为地壳中含量最高的金属元素。请用化学用语回答下列问题:
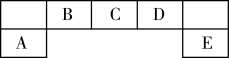
(1)D元素在周期表中的位置___________ 。
(2) A、D、E元素简单离子半径由大到小的顺序为:______> _____>_______________ 。(填微粒符号)
(3)F与D同主族且相邻,二者气态氢化物稳定性的大小关系为______>___________ 。(填微粒符号)
(4)用高能射线照射含有10电子的D元素氢化物分子时,一个分子能释放一个电子,同时产生一种具有较高氧化性的阳离子,试写出该阳离子的电子式___________ ,该阳子中存在的化学键有___________ 。
(5)C元素的简单氢化物与E元素的最高价氧化物的水化物反应,生成化合物K,则鉴别K中的阳离子的离子方程式___________ 。

(1)D元素在周期表中的位置
(2) A、D、E元素简单离子半径由大到小的顺序为:______> _____>_______
(3)F与D同主族且相邻,二者气态氢化物稳定性的大小关系为______>_____
(4)用高能射线照射含有10电子的D元素氢化物分子时,一个分子能释放一个电子,同时产生一种具有较高氧化性的阳离子,试写出该阳离子的电子式
(5)C元素的简单氢化物与E元素的最高价氧化物的水化物反应,生成化合物K,则鉴别K中的阳离子的离子方程式
更新时间:2023-07-05 18:23:16
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】a、b、c、d、e是原子序数依次增大的短周期主族元素,a、d在周期表中的相对位置如下表:a元素最低负化合价的绝对值与其原子最外层电子数相等:b的简单氢化物的水溶液显碱性;c是地壳中含量最多的金属元素。
(1)d元素在元素周期表中的位置为_______ 。
(2)化合物ad2的结构式为_______ 。
(3)用电子式表示化合物be3的形成过程_______ 。
(4)a的单质与b的最高价氧化物对应水化物的浓溶液共热反应的化学方程式为_______ 。
(5)在微电子工业中,b的简单氢化物的水溶液可作刻蚀剂H2O2的清除剂,反应的产物不污染环境,其化学方程式为_______ 。
| a | ||||
| d |
(2)化合物ad2的结构式为
(3)用电子式表示化合物be3的形成过程
(4)a的单质与b的最高价氧化物对应水化物的浓溶液共热反应的化学方程式为
(5)在微电子工业中,b的简单氢化物的水溶液可作刻蚀剂H2O2的清除剂,反应的产物不污染环境,其化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】如表列出了①~⑨九种元素在周期表中的位置。
请按要求回答下列问题:
(1)元素⑦的离子结构示意图______ ,①、④按原子个数比为1∶1组成的分子的结构式______ 。
(2)④⑤⑥三种元素的离子半径由大到小的顺序是______ (填化学符号),⑧和⑨两种元素的最高价氧化物对应的水化物中酸性较弱的是______ (填化学式)。
(3)元素⑤的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应水化物反应,其离子方程式为______ 。
(4)②的最高价氧化物的电子式______ ,其分子的空间构型为______ 。
(5)⑥⑨组成的化合物为______ (离子化合物或共价化合物),用电子式表示的其形成过程______ 。
族 周期 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ④ | ||||||
3 | ⑤ | ⑥ | ⑦ | ③ | ⑧ | ⑨ |
请按要求回答下列问题:
(1)元素⑦的离子结构示意图
(2)④⑤⑥三种元素的离子半径由大到小的顺序是
(3)元素⑤的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应水化物反应,其离子方程式为
(4)②的最高价氧化物的电子式
(5)⑥⑨组成的化合物为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】干冰的外观很像冰,硬度也跟冰相似,但结构特征上却有明显差异。
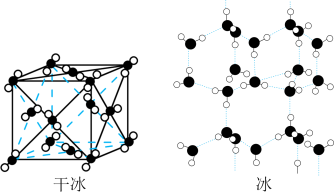
(1)干冰中分子采取密堆积方式排列。
①1个CO2分子周围等距且最近的CO2分子有_______ 个。
②下列事实能解释干冰的密度比冰大的是_______ (填字母序号)。
a.二氧化碳分子的质量大于水分子
b.干冰晶胞中二氧化碳分子堆积得更密集
c.水分子极性强,分子间作用力大
d.冰中氢键存在方向性,晶体有较大空隙,空间利用率低
(2)冰晶体中水分子采取非密堆积方式排列。
①每个水分子最多与相邻的_______ 个水分子相连接。
②对于水分子中的共价键,依据原子轨道重叠的方式判断,属于_______ 键;依据O与H的电负性判断,属于_______ 共价键。
③水分子中,氧原子的价层电子对数为_______ ,杂化轨道类型为_______ 。
④下列事实可用“水分子间存在氢键”解释的是_______ (填字母序号)。
a.常压下,4℃时水的密度最大
b.水的沸点比硫化氢的沸点高160℃
c.水的热稳定性比硫化氢强
⑤酸溶于水可形成H3O+,H3O+的电子式为_______ ;由于成键电子对和孤电子对之间的斥力不同,会对微粒的空间结构产生影响,据此判断H3O+和H2O的键角大小:H3O+_______ H2O(填“>”或“<”)。

(1)干冰中分子采取密堆积方式排列。
①1个CO2分子周围等距且最近的CO2分子有
②下列事实能解释干冰的密度比冰大的是
a.二氧化碳分子的质量大于水分子
b.干冰晶胞中二氧化碳分子堆积得更密集
c.水分子极性强,分子间作用力大
d.冰中氢键存在方向性,晶体有较大空隙,空间利用率低
(2)冰晶体中水分子采取非密堆积方式排列。
①每个水分子最多与相邻的
②对于水分子中的共价键,依据原子轨道重叠的方式判断,属于
③水分子中,氧原子的价层电子对数为
④下列事实可用“水分子间存在氢键”解释的是
a.常压下,4℃时水的密度最大
b.水的沸点比硫化氢的沸点高160℃
c.水的热稳定性比硫化氢强
⑤酸溶于水可形成H3O+,H3O+的电子式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】 是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如表:
是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如表:
(1)W位于元素周期表第_______ 周期第_______ 族; 中,形成化合物种类最多的元素名称是
中,形成化合物种类最多的元素名称是_______ 。
(2) 化学键类型为
化学键类型为_______ ;Y能形成多种单质,其中常用于漂白以及水体杀菌消毒的单质是_______ (填分子式),X的氢化物中,含氢量最大的是_______ (填分子式)。
(3)向Z单质与过量盐酸反应后的无色溶液中滴加 溶液,边滴加边振荡,直至过量,能观察到的现象是
溶液,边滴加边振荡,直至过量,能观察到的现象是_______ ;W的单质与氢氟酸反应生成两种无色气体,该反应的化学方程式是_______ 。
(4)工业上,用X在高温下还原W的氧化物可以得到W的单质,该反应的化学方程式为_______ 。
 是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如表:
是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如表:| 元素 | 相关信息 |
| X | X的最高价氧化物对应的水化物化学式为 |
| Y | Y是地壳中含量最高的元素 |
| Z | Z的最外层电子数等于所在周期数 |
| W | W的一种核素的质量数为28,中子数为14 |
 中,形成化合物种类最多的元素名称是
中,形成化合物种类最多的元素名称是(2)
 化学键类型为
化学键类型为(3)向Z单质与过量盐酸反应后的无色溶液中滴加
 溶液,边滴加边振荡,直至过量,能观察到的现象是
溶液,边滴加边振荡,直至过量,能观察到的现象是(4)工业上,用X在高温下还原W的氧化物可以得到W的单质,该反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表列出了ah八种元素在周期表中的位置
根据表中所列元素回答下列问题:
(1)b元素在周期表中的位置是___________ (请标明周期和族),b与a形成的最简单的化合物的空间构型为___________ 。
(2)最稳定的元素是___________ (填写元素符号)。
(3)将元素d、e、g的原子半径按从小到大的顺序排列:___________ (填写元素符号)。
(4)d原子结构示意图为___________ 。
(5)g的单质与水反应的化学方程式________ 。
(6)f元素的最高价氧化物在常温下跟d的最高价氧化物的水化物发生反应的化学反应方程式是___________ 。
(7)已知元素硒( )与元素c同主族,位于第4周期,则硒元素原子的最外层电子数为
)与元素c同主族,位于第4周期,则硒元素原子的最外层电子数为________ ,根据硒在元素周期表中的位置推测,下列叙述可能成立的是________ 。
A.其单质常温下为气态B. 既有氧化性又有还原性
既有氧化性又有还原性
C.最高价对应的氧化物的水化物的化学式为 D.气态氢化物比
D.气态氢化物比 稳定
稳定
族 周期 | IA | 0 | ||||||
1 | a | IIA | IIIA | IVA | VA | VIA | VIIA | |
2 | b | c | ||||||
3 | d |
|
|
|
| |||
(1)b元素在周期表中的位置是
(2)最稳定的元素是
(3)将元素d、e、g的原子半径按从小到大的顺序排列:
(4)d原子结构示意图为
(5)g的单质与水反应的化学方程式
(6)f元素的最高价氧化物在常温下跟d的最高价氧化物的水化物发生反应的化学反应方程式是
(7)已知元素硒(
 )与元素c同主族,位于第4周期,则硒元素原子的最外层电子数为
)与元素c同主族,位于第4周期,则硒元素原子的最外层电子数为A.其单质常温下为气态B.
 既有氧化性又有还原性
既有氧化性又有还原性C.最高价对应的氧化物的水化物的化学式为
 D.气态氢化物比
D.气态氢化物比 稳定
稳定
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】X、Y、Z、W代表四种短周期元素,
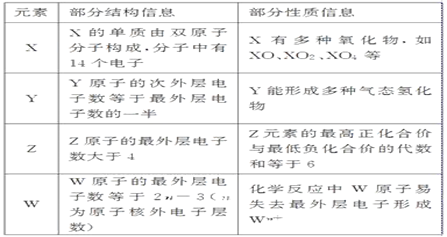
有关它们的部分结构信息及性质信息如表所示。请按要求回答下列问题:
(1)Z在元素周期表中的位置是________________ 。
(2)X、Y的气态氢化物的稳定性由强到弱的顺序是______________ (用化学式表示)。
(3)X、Y、Z三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序是____________________ (用化学式表示)。
(4)实验室用X的气态氢化物的水溶液制取W的氢氧化物的方法是______________________ (用离子方程式表示)。
(5)写出Z的单质与二氧化硫的混合气体通入水中所发生反应的离子方程式__________________ 。

有关它们的部分结构信息及性质信息如表所示。请按要求回答下列问题:
(1)Z在元素周期表中的位置是
(2)X、Y的气态氢化物的稳定性由强到弱的顺序是
(3)X、Y、Z三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序是
(4)实验室用X的气态氢化物的水溶液制取W的氢氧化物的方法是
(5)写出Z的单质与二氧化硫的混合气体通入水中所发生反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、W是短周期元素,原子序数依次递增。X与Z位于同一主族,Y元素的单质既能与盐酸反应也能与NaOH溶液反应,Z原子的最外层电子数是次外层电子数的一半,Y、Z、W原子的最外层电子数之和为14。
(1) HWO的结构式为____ 。
(2) ①X、Y、Z、W原子半径由大到小依次是____ (填元素符号)。
②X、Z、W最高价氧化物水化物酸性由强到弱依次是_________ 。(填化学式)。
(3) W同族上一周期元素单质不能把W元素从其钠盐的水溶液中置换出来,用化学方程式解释____________________ 。
(4) ①家用“管道通”的有效成分是烧碱和Y的单质,使用时需加入一定量的水,此时发生反应的化学方程式为_________________________ 。
②含Y元素的盐与小苏打溶液可用作泡沫灭火剂,写出灭火时发生反应的离子方程式__________________________________ 。
(5) NW3是黄色油状液体,无漂白性,在热水中会发生水解。NW3的电子式为____ 。若取该液体滴入50℃左右的热水中,片刻后取该热水溶液滴到干燥的红色石蕊试纸上,试纸先变蓝后褪色。写出NW3在热水中发生水解的化学方程式__________________________ 。
(1) HWO的结构式为
(2) ①X、Y、Z、W原子半径由大到小依次是
②X、Z、W最高价氧化物水化物酸性由强到弱依次是
(3) W同族上一周期元素单质不能把W元素从其钠盐的水溶液中置换出来,用化学方程式解释
(4) ①家用“管道通”的有效成分是烧碱和Y的单质,使用时需加入一定量的水,此时发生反应的化学方程式为
②含Y元素的盐与小苏打溶液可用作泡沫灭火剂,写出灭火时发生反应的离子方程式
(5) NW3是黄色油状液体,无漂白性,在热水中会发生水解。NW3的电子式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)利用如图装置可验证同主族元素非金属性的变化规律:仪器A的名称为_____ ,装置D的作用_____ 。

(2)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4,C中加淀粉碘化钾混合溶液,观察到C中溶液____ 的现象,即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用____ 溶液吸收尾气。
(3)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加____ 溶液,观察到C中溶液____ 的现象,即可证明。
(4)但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有____ 溶液的洗气瓶。
(1)利用如图装置可验证同主族元素非金属性的变化规律:仪器A的名称为

(2)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4,C中加淀粉碘化钾混合溶液,观察到C中溶液
(3)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加
(4)但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】研究性学习小组设计了几组实验验证元素周期律。
I.甲组同学在A、B、C,D四只烧杯中分别加入50mL冷水,再各滴加几滴酚酞试液,依次加入大小相同的钠(Na)、镁(Mg)、铝(Al)、钾(K)金属块(镁、铝已除去氧化膜),观察现象。
(1)甲组同学实验的目的:验证同一主族从上到下金属元素原子失电子能力逐渐_______ (填“增强”或“减弱”,下同);同一周期主族元素从左到右金属元素原子失电子能力逐渐_______ 。
(2)实验中发现B、C两只烧杯中几乎没有什么现象,要想达到实验目的,请你帮助选择下列合适的方法:_______(填字母)。
II.乙组同学设计实验探究碳、硅元素非金属性的相对强弱,实验装置如图所示。

(3)仪器A的名称为_______ 。
(4)实验步骤:①连接仪器,②_______ ,③加入固体、液体药品,④打开A的活塞滴入浓硫酸,⑤加热,观察现象。
(5)问题探究:[已知酸性:亚硫酸(H2SO3)>碳酸(H2CO3)]
①铜与浓硫酸反应的化学方程式为_______ ;装置E中酸性 溶液的作用是
溶液的作用是_______ 。
②能说明碳元素的非金属性比硅元素的强的实验现象是_______ 。
③该实验能否证明S的非金属性强于C的非金属性?______ (填“能”或“不能”),理由是______ 。
I.甲组同学在A、B、C,D四只烧杯中分别加入50mL冷水,再各滴加几滴酚酞试液,依次加入大小相同的钠(Na)、镁(Mg)、铝(Al)、钾(K)金属块(镁、铝已除去氧化膜),观察现象。
(1)甲组同学实验的目的:验证同一主族从上到下金属元素原子失电子能力逐渐
(2)实验中发现B、C两只烧杯中几乎没有什么现象,要想达到实验目的,请你帮助选择下列合适的方法:_______(填字母)。
| A.将烧杯中的冷水换成等量的98%浓硫酸 |
| B.将烧杯中的冷水换成热水 |
C.将烧杯中的冷水换成等量的 的盐酸 的盐酸 |
D.将烧杯中的冷水换成等量的 的 的 溶液 溶液 |
II.乙组同学设计实验探究碳、硅元素非金属性的相对强弱,实验装置如图所示。

(3)仪器A的名称为
(4)实验步骤:①连接仪器,②
(5)问题探究:[已知酸性:亚硫酸(H2SO3)>碳酸(H2CO3)]
①铜与浓硫酸反应的化学方程式为
 溶液的作用是
溶液的作用是②能说明碳元素的非金属性比硅元素的强的实验现象是
③该实验能否证明S的非金属性强于C的非金属性?
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示。回答下列问题:
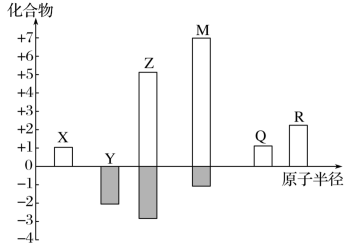
(1)Q元素位于元素周期表的第___________ 周期,Y元素原子最外层电子数为___________ 。
(2)X与Z元素所形成的常见原子团的电子式为___________ ;M与Q两种元素的最高价氧化物对应的水化物,发生反应生成盐的化学式为___________ 。
(3)M和R元素的简单离子的半径大小关系为___________ (用离子符号表示)。利用中学现有基础知识,能否判断Q和R简单离子半径的大小关系___________ (填“能”或“不能”)。M的单质与R的最高价氧化物的水化物反应的化学方程式为___________ 。

(1)Q元素位于元素周期表的第
(2)X与Z元素所形成的常见原子团的电子式为
(3)M和R元素的简单离子的半径大小关系为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A、E在元素周期表中的相对位置如图,A与氧元素能形成两种无色气体,C是地壳中含量最多的元素,D是地壳中含量最多的金属元素。
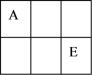
(1)D在元素周期表中的位置为___________ 。
(2)AE2的结构式为___________ 。
(3)C、E、F的简单氢化物的沸点最高的是___________ (填化学式)。
(4)C、D、E、F的简单离子半径由大到小的顺序是___________ (填离子符号)。
(5)实验室制取F2气体的主要方法的离子方程式为___________ 。
(6)在微电子工业中,B的最简单气态氢化物的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为___ 。
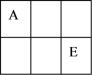
(1)D在元素周期表中的位置为
(2)AE2的结构式为
(3)C、E、F的简单氢化物的沸点最高的是
(4)C、D、E、F的简单离子半径由大到小的顺序是
(5)实验室制取F2气体的主要方法的离子方程式为
(6)在微电子工业中,B的最简单气态氢化物的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】随着原子序数的递增,8种短周期元素(用字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示。
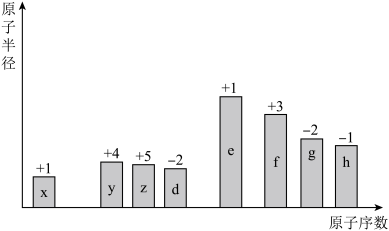
请用化学用语回答下列问题:
(1)f在元素周期表中的位置是_______ 。
(2)比较d、e常见离子的半径,半径大的是:_______ (用化学式表示,下同);g、h的最高价氧化物的水化物中酸性强的是:_______ 。
(3)d、g的单质分别与x的单质化合时,较容易的是_______ (用化学式表示,下同),形成的化合物热稳定性较差的是_______ 。x2d、x2g沸点较高的是_______ ,原因是_______ 。
(4)任选上述元素形成一种四原子共价化合物,写出其电子式:_______ 。

请用化学用语回答下列问题:
(1)f在元素周期表中的位置是
(2)比较d、e常见离子的半径,半径大的是:
(3)d、g的单质分别与x的单质化合时,较容易的是
(4)任选上述元素形成一种四原子共价化合物,写出其电子式:
您最近一年使用:0次







