含氮元素的化合物的转化关系如图所示,按要求书写化学方程式。

(1)反应①实验室制氨气:___________ 。
(2)反应②氨的催化氧化:___________ 。
(3)反应③的化学方程式为___________ 。
(4)反应④硝酸具有不稳定性:___________ 。
(5)反应⑤铜和稀硝酸反应:___________ 。

(1)反应①实验室制氨气:
(2)反应②氨的催化氧化:
(3)反应③的化学方程式为
(4)反应④硝酸具有不稳定性:
(5)反应⑤铜和稀硝酸反应:
更新时间:2023-07-05 23:54:38
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】非金属元素在化工生产中扮演着重要的角色。
(1)下列物质中,能吸收SO2的有_______ (填字母序号)。
a. 浓硫酸 b. 酸性KMnO4溶液 c. 生石灰
(2)久置在空气中的Na2SO3固体会部分变质,检验是否变质的方法是:取少量固体加水溶解,_______ (将实验操作和现象补充完整)。
(3)工业上利用氨的催化氧化制取NO,写出化学方程式_______ 。
(1)下列物质中,能吸收SO2的有
a. 浓硫酸 b. 酸性KMnO4溶液 c. 生石灰
(2)久置在空气中的Na2SO3固体会部分变质,检验是否变质的方法是:取少量固体加水溶解,
(3)工业上利用氨的催化氧化制取NO,写出化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价一物质类别关系图如下。回答下列问题:
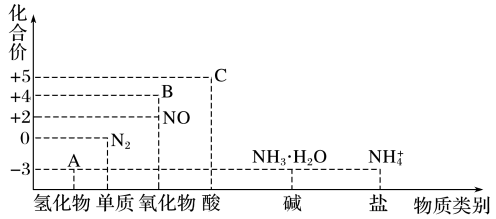
(1)已知H—H键、N—H键、N≡N键的键能分别是436kJ/mol、391kJ/mol、946kJ/mol则每生成1molNH3时,_______ (填“吸收”或“放出”)_______ kJ热量。
(2)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是_______ 。
(3)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式_______ 。
(4)实验室中,检验溶液中含有 的操作方法是
的操作方法是_______ 。
(5)物质B为红棕色气体,写出该物质与水反应的离子方程式_______ ,当反应消耗3.36L(标准状况)物质B时,转移电子的物质的量为_______ 。

(1)已知H—H键、N—H键、N≡N键的键能分别是436kJ/mol、391kJ/mol、946kJ/mol则每生成1molNH3时,
(2)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是
(3)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式
(4)实验室中,检验溶液中含有
 的操作方法是
的操作方法是(5)物质B为红棕色气体,写出该物质与水反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】结合所学内容,回答下列问题:
(1)氮元素及其化合物的转化关系如下:

①写出X的化学式:_______ ,Y的化学式:_______ 。
②图中所示,关于 转化为
转化为 的反应过程,下列说法正确的是
的反应过程,下列说法正确的是_______ 。
a.氮元素的化合价不发生变化
b.若用 与
与 反应制取
反应制取 ,另一种生成物可能是
,另一种生成物可能是
c.该转化过程中, 既是氧化剂,又是还原剂
既是氧化剂,又是还原剂
(2) 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:
催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:

① 技术中的氧化剂为
技术中的氧化剂为_______ 。
②当NO2与NO的物质的量之比为1∶1时,与足量氨气在一定条件下发生反应,该反应的化学方程式为_______ 。
(3)某同学利用如图所示的装置,进行氨气的喷泉实验,回答下列问题:

①仪器A的名称是_______ 。
②写出实验室用NH4Cl和Ca(OH)2制取氨气的化学方程式:_______ 。
③喷泉实验前需要在仪器A中充满干燥的氨气,可用_______ (填“向上”或“向下”)排空气法收集氨气:可用_______ (填“浓硫酸”或“碱石灰”)干燥氨气。
④引发喷泉实验的操作是_______ 。
(1)氮元素及其化合物的转化关系如下:

①写出X的化学式:
②图中所示,关于
 转化为
转化为 的反应过程,下列说法正确的是
的反应过程,下列说法正确的是a.氮元素的化合价不发生变化
b.若用
 与
与 反应制取
反应制取 ,另一种生成物可能是
,另一种生成物可能是
c.该转化过程中,
 既是氧化剂,又是还原剂
既是氧化剂,又是还原剂(2)
 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:
催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:
①
 技术中的氧化剂为
技术中的氧化剂为②当NO2与NO的物质的量之比为1∶1时,与足量氨气在一定条件下发生反应,该反应的化学方程式为
(3)某同学利用如图所示的装置,进行氨气的喷泉实验,回答下列问题:

①仪器A的名称是
②写出实验室用NH4Cl和Ca(OH)2制取氨气的化学方程式:
③喷泉实验前需要在仪器A中充满干燥的氨气,可用
④引发喷泉实验的操作是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】 硅酸盐具有特殊的性质与应用,回答下列问题:
(1) 硅酸盐材料是传统无机非金属材料,下列产品属于硅酸盐的是___________ (填序号)。
①玻璃 ②陶瓷 ③水晶 ④硅芯片 ⑤光导纤维 ⑥水泥 ⑦高岭石 ⑧云母 ⑨沙
(2)SiO2是一种酸性氧化物。
①盛装NaOH溶液的试剂瓶___________ (填“能”“不能”)用玻璃塞,原因是什么___________ (填化学方程式)。
②熔化烧碱应选用的坩埚应该___________ (填字母)
A.瓷坩埚 B.铁坩埚 C.玻璃坩埚 D.石英坩埚
(3)某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。

请回答:
①实验室制备氨气的化学方程式为___________
②检验氨气常用的方法有___________
③用热毛巾热敷圆底烧瓶并打开装置B中的止水夹c,若观察到烧瓶内产生了红色喷泉,则说明氨气具有的性质是___________
④为防止污染环境,以下装置(盛放的液体均为水)可用于吸收多余氨气的是___________ (填序号)

(1) 硅酸盐材料是传统无机非金属材料,下列产品属于硅酸盐的是
①玻璃 ②陶瓷 ③水晶 ④硅芯片 ⑤光导纤维 ⑥水泥 ⑦高岭石 ⑧云母 ⑨沙
(2)SiO2是一种酸性氧化物。
①盛装NaOH溶液的试剂瓶
②熔化烧碱应选用的坩埚应该
A.瓷坩埚 B.铁坩埚 C.玻璃坩埚 D.石英坩埚
(3)某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。

请回答:
①实验室制备氨气的化学方程式为
②检验氨气常用的方法有
③用热毛巾热敷圆底烧瓶并打开装置B中的止水夹c,若观察到烧瓶内产生了红色喷泉,则说明氨气具有的性质是
④为防止污染环境,以下装置(盛放的液体均为水)可用于吸收多余氨气的是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用下图中的装置可以实现该反应(夹持仪器略去)。
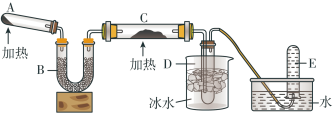
(1)A中装有氯化铵和氢氧化钙的混合物,发生反应的化学方程式是___________ ;
(2)B中加入的是碱石灰,其作用是___________ ;
(3)实验时C中观察到的现象是___________ ,发生反应的化学方程式是_____________ ;
(4)试管D中收集到的物质是___________ ,向其中滴加酚酞试液,溶液变_____ 色,原因是___________________ (用电离方程式表示)。

(1)A中装有氯化铵和氢氧化钙的混合物,发生反应的化学方程式是
(2)B中加入的是碱石灰,其作用是
(3)实验时C中观察到的现象是
(4)试管D中收集到的物质是
您最近一年使用:0次
【推荐1】在铜跟稀硝酸的反应中,如果有1 mol硝酸被还原,则被氧化的铜的物质的量为_______ mol。若将产生的气体(NO)和一定量的O2混合通入水中,恰好完全溶解,求需要O2_______ L。(气体的体积都按标况下计算)
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
【推荐2】学习小组探究了铜的氧化过程及铜的氧化物的组成。回答下列问题:
(1)铜与浓硝酸反应的装置如下图,仪器A的名称为_______ ,装置B的作用为_______ 。

(2)铜与过量 反应的探究如下:
反应的探究如下:

实验②中Cu溶解的离子方程式为_______ ;产生的气体为_______ 。比较实验①和②,从氧化还原角度说明 的作用是
的作用是_______ 。
(3)用足量NaOH处理实验②新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干燥后的X在惰性氛围下加热,mgX完全分解为ng黑色氧化物Y,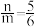 。X的化学式为
。X的化学式为_______ 。
(4)取含X粗品0.0500g(杂质不参加反应)与过量的酸性KI完全反应后,调节溶液至弱酸性。以淀粉为指示剂,用 标准溶液滴定,滴定终点时消耗
标准溶液滴定,滴定终点时消耗 标准溶液15.00mL。(已知:
标准溶液15.00mL。(已知: ,
, )标志滴定终点的现象是
)标志滴定终点的现象是_______ ,粗品中X的相对含量为_______ 。
(1)铜与浓硝酸反应的装置如下图,仪器A的名称为

(2)铜与过量
 反应的探究如下:
反应的探究如下:
实验②中Cu溶解的离子方程式为
 的作用是
的作用是(3)用足量NaOH处理实验②新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干燥后的X在惰性氛围下加热,mgX完全分解为ng黑色氧化物Y,
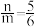 。X的化学式为
。X的化学式为(4)取含X粗品0.0500g(杂质不参加反应)与过量的酸性KI完全反应后,调节溶液至弱酸性。以淀粉为指示剂,用
 标准溶液滴定,滴定终点时消耗
标准溶液滴定,滴定终点时消耗 标准溶液15.00mL。(已知:
标准溶液15.00mL。(已知: ,
, )标志滴定终点的现象是
)标志滴定终点的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求回答下列问题:
(1)实验室制备氨气,下列方法中可以选用的是_______ 。
a.固态氯化铵加热分解 b.浓氨水中加入固体氢氧化钠
c.加热浓氨水 d.固态氯化铵与氢氧化钙混合加热
(2)氯化铵溶液显酸性,用离子方程式表示呈酸性的原因_______ 。
(3)NH3常用于检验氯气管道是否泄漏,写出反应的化学方程式_______ 。
(4)将57.6克的铜投入200毫升的硝酸溶液中恰好反应完全,产生标准状况下的NO2、NO共1.4 mol。
①写出刚开始反应的化学方程式_______ ;
②求硝酸的浓度_______ mol·L-1;
③将生成的气体收集在大试管中,然后倒扣在水中,写出二氧化氮与水反应的化学方程式_______ ,若往试管中通入氧气让液体充满试管,则通入氧气的物质的量_______ mol。
(1)实验室制备氨气,下列方法中可以选用的是
a.固态氯化铵加热分解 b.浓氨水中加入固体氢氧化钠
c.加热浓氨水 d.固态氯化铵与氢氧化钙混合加热
(2)氯化铵溶液显酸性,用离子方程式表示呈酸性的原因
(3)NH3常用于检验氯气管道是否泄漏,写出反应的化学方程式
(4)将57.6克的铜投入200毫升的硝酸溶液中恰好反应完全,产生标准状况下的NO2、NO共1.4 mol。
①写出刚开始反应的化学方程式
②求硝酸的浓度
③将生成的气体收集在大试管中,然后倒扣在水中,写出二氧化氮与水反应的化学方程式
您最近一年使用:0次




