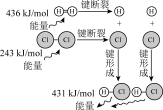
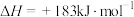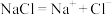研究NO2、NO、CO的污染物处理,对建设美丽中国具有重要意义。反应 的能量变化如图所示,下列说法正确的是
的能量变化如图所示,下列说法正确的是
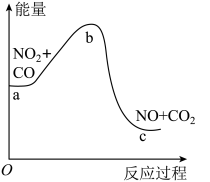
 的能量变化如图所示,下列说法正确的是
的能量变化如图所示,下列说法正确的是
| A.图中a→b为放热过程 |
| B.理论上该反应可以设计成原电池 |
| C.提高反应的温度,可以实现NO2的完全转化 |
| D.该反应中反应物的总键能大于生成物的总键能 |
更新时间:2023-07-06 12:29:18
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】科学家研究二甲醚(DME)在 分子笑(用
分子笑(用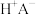 表示)上的水解反应,其反应进程中能量变化如图所示。下列说法错误的是
表示)上的水解反应,其反应进程中能量变化如图所示。下列说法错误的是
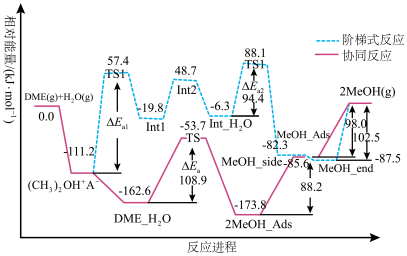
 分子笑(用
分子笑(用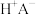 表示)上的水解反应,其反应进程中能量变化如图所示。下列说法错误的是
表示)上的水解反应,其反应进程中能量变化如图所示。下列说法错误的是
A.由于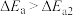 ,DME水解反应更易以阶梯式反应路径进行 ,DME水解反应更易以阶梯式反应路径进行 |
| B.根据反应图示可知,在相同的催化剂作用下,化学反应也存在多种反应途径 |
| C.升高温度,阶梯式反应路径和协同反应路径的反应速率都加快,有利于提高反应物的转化率 |
D.以阶梯式反应路径进行时, 生成Int1的反应步骤为决速步骤 生成Int1的反应步骤为决速步骤 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列过程的能量变化符合下图所示的是
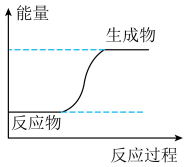
A.盐酸与NaOH溶液 | B.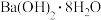 和 和  |
C.盐酸与铝条 | D.蜡烛燃烧 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
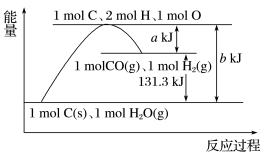
【推荐3】多相催化反应是在催化剂表面通过吸附、解吸过程进行的。我国学者发现T℃下(各物质均为气态),甲醇与水在铜基催化剂上的反应机理和能量图如图,下列说法正确的是
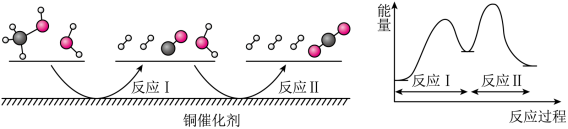

| A.CO(g)在反应中生成又消耗,CO(g)可认为是催化剂 |
| B.1molCH3OH(g)和1molH2O(g)的总能量大于1molCO2(g)和3molH2(g)的总能量 |
| C.反应Ⅱ的热化学方程式为:CO(g)+H2O(g)=H2(g)+CO2(g)△H=+a kJ/mol(a>0) |
| D.选择优良的催化剂降低反应Ⅰ和Ⅱ的活化能,有利于减少过程中的能耗 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】碘在不同状态下(固态或气态)与氢气反应的热化学方程式如下所示:①H2(g)+I2(?)⇌ 2HI(g)ΔH = -9.48kJ/mol ②H2(g)+I2(?)⇌ 2HI(g)ΔH = +26.48kJ/mol。下列判断不正确的是
| A.①中的I2为气态,②中的I2为固态 | B.②的反应物总能量比①的反应物总能量低 |
| C.①的产物与②的产物热稳定性相同 | D.1mol 固态碘升华时将吸热17kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列有关热化学方程式的叙述正确的是
| A.若C(s)+O2(g)=CO2(g)△H1,CO2(g)+C(s)=2CO(g)△H2,2CO(g)+O2(g)=2CO2(g)△H3,则反应热的关系:2△H1=△H2+△H3 |
B.若2H2(g)+O2(g)=2H2O(1)△H4,H2(g)+ O2(g)=H2O(1)△H5则反应热的关系:△H4=△H5 O2(g)=H2O(1)△H5则反应热的关系:△H4=△H5 |
| C.若2SO2(g)+O2(g)=2SO3(g)△H<0,则物质的稳定性:SO2>SO3 |
| D.若断裂1 mol H2(g)中的共价键、1 mol O2(g)中的共价键分别需要吸收436 kJ、498 kJ的能量,生成H2O(g)中的1 mol H—O键能放出463 kJ的能量,则2H2(g)+O2(g)=2H2O(g)△H=—482 kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 的 的 溶液中含 溶液中含 离子数为 离子数为 |
B. 与 与 混合反应生成 混合反应生成 ,转移电子数为 ,转移电子数为 |
C.标准状况下,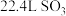 中含有的硫原子数为 中含有的硫原子数为 |
D.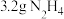 中含有共用电子对的总数为 中含有共用电子对的总数为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】一定温度下,向2L恒容密闭容器中充入0.4molNH3和0.5molO2发生反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g)。2min末,NO的物质的量为0.2mol,下列有关说法不正确的是
4NO(g)+6H2O(g)。2min末,NO的物质的量为0.2mol,下列有关说法不正确的是
 4NO(g)+6H2O(g)。2min末,NO的物质的量为0.2mol,下列有关说法不正确的是
4NO(g)+6H2O(g)。2min末,NO的物质的量为0.2mol,下列有关说法不正确的是| A.2min末,NH3 的浓度为0.1mol·L-1 |
| B.继续反应达平衡后,NO的物质的量可以达到为0.4mol |
| C.2min末,生成的水物质的量为0.3 mol |
| D.0~ 2min内,用NH3表示的平均反应速率为v(NH3)=0.05mol·L·min-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列有关反应2SO2+O2 2SO3的说法中不正确的是
2SO3的说法中不正确的是
 2SO3的说法中不正确的是
2SO3的说法中不正确的是| A.该反应为可逆反应,故在一定条件下二氧化硫与氧气不可能全部转化为三氧化硫 |
| B.达到平衡后,反应就停止了,故此时正、逆反应速率相等且均为零 |
| C.一定条件下,向某密闭容器中加入2molSO2和1molO2,则从反应开始到达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等 |
| D.在利用上述反应生产三氧化硫时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列各装置不能 构成原电池的是(电解质溶液均为稀硫酸)
A. | B.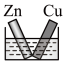 | C.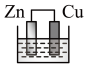 | D.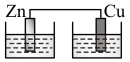 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列关于原电池的叙述中,正确的是
①构成原电池的正极和负极必须是两种不同的金属
②原电池是化学能转变为电能的装置
③在原电池中,电子流入的一极是正极,该电极被还原
④原电池放电时,电流的方向是从负极到正极
⑤原电池工作时,溶液中的阳离子向负极移动
⑥电子经溶液从负极流向正极
①构成原电池的正极和负极必须是两种不同的金属
②原电池是化学能转变为电能的装置
③在原电池中,电子流入的一极是正极,该电极被还原
④原电池放电时,电流的方向是从负极到正极
⑤原电池工作时,溶液中的阳离子向负极移动
⑥电子经溶液从负极流向正极
| A.①②⑥ | B.②③ | C.② | D.②⑥ |
您最近一年使用:0次

 与
与 反应能量变化
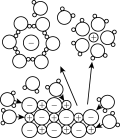
反应能量变化 溶于水
溶于水