电化学技术是有效解决CO、SO2、NOx等大气污染的重要方法,某兴趣小组以SO2为原料,采用电化学方法制取硫酸,装置如下:

(1)电解质溶液中H+向___________ (填“A极”或“B极”)移动。
(2)请写出负极电极反应式___________ 。
(3)用该原电池做电源,石墨做电极电解2 L AgNO3和KNO3混合溶液,通电一段时间,两极均产生2.24L气体(标况)。
①上述过程中转移的电子数为___________ mol。
②假设电解前后溶液体积不变,则电解后溶液中H+的浓度为___________ mol·L-1,析出Ag的质量为___________ g。

(1)电解质溶液中H+向
(2)请写出负极电极反应式
(3)用该原电池做电源,石墨做电极电解2 L AgNO3和KNO3混合溶液,通电一段时间,两极均产生2.24L气体(标况)。
①上述过程中转移的电子数为
②假设电解前后溶液体积不变,则电解后溶液中H+的浓度为
更新时间:2023-07-06 12:20:55
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下图A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。

(1)A中反应的离子方程式是____________________ 。
(2)B中Cu极的电极反应式是___________________ 。
(3)C中被腐蚀的金属是__________ (填化学式),A、B、C中铁被腐蚀的速率,由快到慢的是顺序是_____________ (用“>”表示)。

(1)A中反应的离子方程式是
(2)B中Cu极的电极反应式是
(3)C中被腐蚀的金属是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】天宫二号空间实验室已于2016 年9月15日22时04分在酒泉卫星发射中心发射成功。请回答下列问题:

(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英玻璃的成分是______ (填化学式),该物质的类别属于________ (填“碱性氧化物”或“酸性氧化物”) ,实验室中不能用玻璃塞试剂瓶盛放KOH溶液,原因是_______________ (用离子方程式表示)
(2)“碳纤维复合材料制品”应用于“天宫二号”的推进系统。碳纤维复合材料具有重量轻、可设计强度高的特点。碳纤维复合材料由碳纤维和合成树脂组成,其中合成树脂是高分子化合物,则制备合成树脂的反应类型是_____________ 。
(3)太阳能电池帆板是“天宫二号”空间运行的动力源泉,其性能直接影响到“天宫二号”的运行寿命和可靠性。
① 天宫二号使用的光伏太阳能电池,该电池的核心材料是_____ ,其能量转化方式为_____ 。
② 下图是一种全天候太阳能电池的工作原理:

太阳照射时的总反应为V3++ VO2++ H2O=V2++VO2++2H+,则负极反应式为__________ ;夜间时,电池正极为______ (填“a”或“b”)。

(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英玻璃的成分是
(2)“碳纤维复合材料制品”应用于“天宫二号”的推进系统。碳纤维复合材料具有重量轻、可设计强度高的特点。碳纤维复合材料由碳纤维和合成树脂组成,其中合成树脂是高分子化合物,则制备合成树脂的反应类型是
(3)太阳能电池帆板是“天宫二号”空间运行的动力源泉,其性能直接影响到“天宫二号”的运行寿命和可靠性。
① 天宫二号使用的光伏太阳能电池,该电池的核心材料是
② 下图是一种全天候太阳能电池的工作原理:

太阳照射时的总反应为V3++ VO2++ H2O=V2++VO2++2H+,则负极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】请回答:
(1)甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应来制备甲醇
I:CH4(g)+H2O(g) CO(g)+3H2(g) ΔH=+206.0kJ·mol-1
CO(g)+3H2(g) ΔH=+206.0kJ·mol-1
II:CO(g)+2H2(g) CH3OH(g) ΔH=-129.0kJ·mol-1
CH3OH(g) ΔH=-129.0kJ·mol-1
CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为_______ 。
(2)把a、b、c、d四种金属片浸泡在稀硫酸中,用导线两两相连,可以组成各种原电池。若a、b相连,a为正极;c、d相连,c为负极;a、c相连,c上产生气泡;b、d相连,b质量减小,则四种金属的活动性由强到弱顺序为:_______ 。
(3)甲烷燃料电池采用铂作电极催化剂,电池中的质子交换膜只允许质子(H+)和水分子通过。其工作原理的示意图如下,请回答下列问题:

①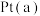 电极是电池的
电极是电池的_______ 极,电极反应式为_______ 。
②电解质溶液中的 向
向_______ (填“a”或“b”)极移动,电子流入的电极是_______ (填“a”或“b”)极。
③该电池工作时消耗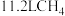 (标准状况下),则电路中通过
(标准状况下),则电路中通过_______ mol电子。
(1)甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应来制备甲醇
I:CH4(g)+H2O(g)
 CO(g)+3H2(g) ΔH=+206.0kJ·mol-1
CO(g)+3H2(g) ΔH=+206.0kJ·mol-1II:CO(g)+2H2(g)
 CH3OH(g) ΔH=-129.0kJ·mol-1
CH3OH(g) ΔH=-129.0kJ·mol-1CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为
(2)把a、b、c、d四种金属片浸泡在稀硫酸中,用导线两两相连,可以组成各种原电池。若a、b相连,a为正极;c、d相连,c为负极;a、c相连,c上产生气泡;b、d相连,b质量减小,则四种金属的活动性由强到弱顺序为:
(3)甲烷燃料电池采用铂作电极催化剂,电池中的质子交换膜只允许质子(H+)和水分子通过。其工作原理的示意图如下,请回答下列问题:

①
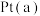 电极是电池的
电极是电池的②电解质溶液中的
 向
向③该电池工作时消耗
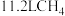 (标准状况下),则电路中通过
(标准状况下),则电路中通过
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某化学研究性学习小组欲设计实验验证Fe、Cu的金属活动性,他们提出了以下两种方案,请完成有关问题。
方案Ⅰ:将形状和大小均相同的铁片和铜片,分别同时放入100 mL 2.0 mol·L-1稀硫酸中,观察反应的情况,据此确定它们的金属活动性。
方案Ⅱ:利用Fe、Cu作电极设计成原电池,以确定它们的金属活动性。
(1)方案Ⅰ中发生反应的离子方程式为_______________ 。
(2)在方框内画出方案Ⅱ中的原电池装置图,注明电解质溶液名称和正、负极材料,标出电子流动方向,并写出电极反应式:
正极:__________________ ;
负极:__________________ 。
(3)结合你所学的知识,请你再设计一个与方案Ⅰ、Ⅱ不同的验证Fe、Cu活动性的简单实验方案:________________ ,用离子方程式表示其反应原理:____________________ 。
方案Ⅰ:将形状和大小均相同的铁片和铜片,分别同时放入100 mL 2.0 mol·L-1稀硫酸中,观察反应的情况,据此确定它们的金属活动性。
方案Ⅱ:利用Fe、Cu作电极设计成原电池,以确定它们的金属活动性。
(1)方案Ⅰ中发生反应的离子方程式为
(2)在方框内画出方案Ⅱ中的原电池装置图,注明电解质溶液名称和正、负极材料,标出电子流动方向,并写出电极反应式:
正极:
负极:
(3)结合你所学的知识,请你再设计一个与方案Ⅰ、Ⅱ不同的验证Fe、Cu活动性的简单实验方案:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图所示3套实验装置,分别回答下列问题:


(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入铁钉的玻璃筒内滴入KSCN溶液呈无色,再滴入氯水即可观察到铁钉附近的溶液变红色,表明铁被_______ (填氧化、还原);向插入碳棒的玻璃筒内滴入酚酞试液,可观察到碳棒附近的溶液变红,该电极反应为_______________ 。
(2)装置2中的石墨是_________ 极(填“正”或“负”),该装置发生的总反应的离子方程式为___________________________________ 。
(3)装置3中甲烧杯盛放100 mL 0.2 mol·L-1的NaCl溶液,乙烧杯盛放100 mL 0.5 mol·L-1的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞试液,观察到石墨电极附近首先变红。
①电源的M端为_________ 极,甲烧杯中铁电极的电极反应为________________ ;
②乙烧杯中电解反应的离子方程式为___________________________________ ;
③停止电解,取出Cu电极,洗涤、干燥、称量,电极增重0.64 g,则甲烧杯中产生的气体在标准状况下为____________ mL。


(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入铁钉的玻璃筒内滴入KSCN溶液呈无色,再滴入氯水即可观察到铁钉附近的溶液变红色,表明铁被
(2)装置2中的石墨是
(3)装置3中甲烧杯盛放100 mL 0.2 mol·L-1的NaCl溶液,乙烧杯盛放100 mL 0.5 mol·L-1的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞试液,观察到石墨电极附近首先变红。
①电源的M端为
②乙烧杯中电解反应的离子方程式为
③停止电解,取出Cu电极,洗涤、干燥、称量,电极增重0.64 g,则甲烧杯中产生的气体在标准状况下为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】研究化学反应中的能量变化,能更好地利用化学反应为生产和生活服务。
Ⅰ.探究原电池中的能量转化。图中注射器用来收集气体并读取气体体积(在标准状况下),记录实验数据如表。
______ ②(填“>”“=”或“<”),6至10min内①中产生氢气的平均速率是______ 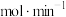 。
。
(2)有明显的气泡冒出现象的金属是______ (填“a”、“b”、“c”、“d”),当都生成56ml气体时,装置中释放的总能量①______ ②(填“>”、“=”或“<”),请对两装置温度变化不同进行解释______ 。
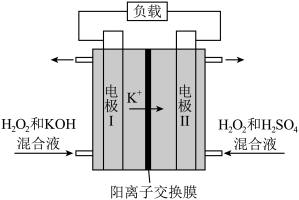
Ⅱ. 燃料电池是一种新型化学电源,工作时总反应为
燃料电池是一种新型化学电源,工作时总反应为 。
。______ 极,电极Ⅱ发生的电极反应为______ ,当电路转移电子1mol时,产生气体的体积为______ (在标准状况下)。
Ⅰ.探究原电池中的能量转化。图中注射器用来收集气体并读取气体体积(在标准状况下),记录实验数据如表。
实验数据 时间/min | ① | ② | ||
气体体积/mL | 溶液温度/℃ | 气体体积/mL | 溶液温度/℃ | |
0 | 0 | 22.0 | 0 | 22.0 |
6 | 33.6 | 24.8 | 56 | 23.8 |
10 | 56 | 26.0 | - | - |
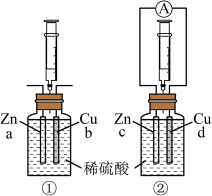
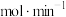 。
。(2)有明显的气泡冒出现象的金属是
Ⅱ.
 燃料电池是一种新型化学电源,工作时总反应为
燃料电池是一种新型化学电源,工作时总反应为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】结合所学知识,按要求回答问题。
(1)按要求写出电极反应式
①碱性锌锰电池的总反应为Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2,写出正极反应式___________ 。
②将2FeCl3+2KI=I2+2FeCl2+2KCl设计成双液电池:正极烧杯中盛放的溶液为___________ ,电池负极的电极反应式为___________ 。
(2)如图是以石墨为电极,电解MgCl2溶液的装置:
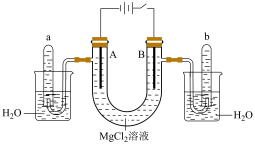
①电解时,A电极发生的电极反应为___________ 。
②检验b管中气体的方法是___________ 。
(3)某同学设计了如下图所示装置,用氢氧燃料电池作为电源探究粗铜精炼原理,根据要求回答问题:
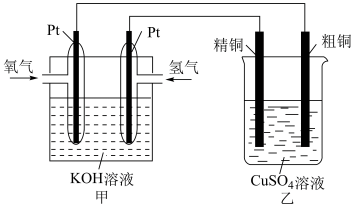
①甲装置中通入氧气的电极为___________ (填“正极”或“负极”),氧气发生的电极反应式___________ 。
②如果粗铜中含有铁、银等杂质,粗铜电极发生的电极反应式有___________ 。乙装置中反应一段时间后,CuSO4溶液的浓度___________ (填“增大”、“减小”或“不变”)。
③已知NA为阿伏加德罗常数的值。若在标准状况下,甲装置有2.24L氧气参加反应,则乙装置中阴极析出铜的质量理论上为___________ g。
(1)按要求写出电极反应式
①碱性锌锰电池的总反应为Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2,写出正极反应式
②将2FeCl3+2KI=I2+2FeCl2+2KCl设计成双液电池:正极烧杯中盛放的溶液为
(2)如图是以石墨为电极,电解MgCl2溶液的装置:

①电解时,A电极发生的电极反应为
②检验b管中气体的方法是
(3)某同学设计了如下图所示装置,用氢氧燃料电池作为电源探究粗铜精炼原理,根据要求回答问题:

①甲装置中通入氧气的电极为
②如果粗铜中含有铁、银等杂质,粗铜电极发生的电极反应式有
③已知NA为阿伏加德罗常数的值。若在标准状况下,甲装置有2.24L氧气参加反应,则乙装置中阴极析出铜的质量理论上为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.能源的开发、利用与人类社会的可持续发展息息相关,充分利用好能源是摆在人类面前的重大课题。
(1)依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是_______ (填字母)
A.C(s)+CO2(g)=2CO(g) ΔH>0
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH<0
C.2H2O(l)=2H2(g)+O2(g) ΔH>0
D.C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(l) ΔH<0
若以稀硫酸为电解质溶液,则该原电池的负极反应式为_______
Ⅱ.如图所示的装置,X、Y都是惰性电极。将电路接通后,向乙中滴入酚酞溶液,在Fe极附近显红色。试回答下列问题:
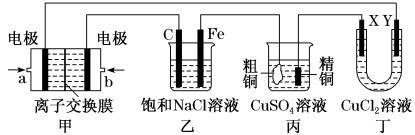
(2)甲装置是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,则a处通入的是_______ (填“CH4”或“O2”),电极上发生的电极反应是_______
(3)在乙装置中,总反应的离子方程式是_______
(4)如果丙装置中精铜电极的质量增加了6.4 g,则甲装置中消耗的CH4的质量为_______
(5)丁装置中在通电一段时间后,Y电极上发生的电极反应是_______
(1)依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是
A.C(s)+CO2(g)=2CO(g) ΔH>0
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH<0
C.2H2O(l)=2H2(g)+O2(g) ΔH>0
D.C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(l) ΔH<0
若以稀硫酸为电解质溶液,则该原电池的负极反应式为
Ⅱ.如图所示的装置,X、Y都是惰性电极。将电路接通后,向乙中滴入酚酞溶液,在Fe极附近显红色。试回答下列问题:

(2)甲装置是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,则a处通入的是
(3)在乙装置中,总反应的离子方程式是
(4)如果丙装置中精铜电极的质量增加了6.4 g,则甲装置中消耗的CH4的质量为
(5)丁装置中在通电一段时间后,Y电极上发生的电极反应是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如图是一个化学过程的示意图,回答下列问题:

(1)甲装置中通入C3H8的电极反应式为___________ ,丙装置中D极的产物是___________ (写化学式)。
(2)一段时间,当乙池中产生112mL(标准状况下)气体时,均匀搅拌丙池,所得溶液在25℃时的pH=___________ 。(已知NaCl溶液足量,假定生成的氯气完全逸出,且电解后溶液体积为200mL)。
(3)若要使乙池恢复电解前的状态,应向乙池中加入___________ (写物质化学式)。

(1)甲装置中通入C3H8的电极反应式为
(2)一段时间,当乙池中产生112mL(标准状况下)气体时,均匀搅拌丙池,所得溶液在25℃时的pH=
(3)若要使乙池恢复电解前的状态,应向乙池中加入
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】有下图所示装置:
(1)装置A中b为_______ 极,电极反应式为_______ ,a极反应式为_______ 。
(2)装置B中C为________ 极,电极反应式为________ 。
(3)当铁电极的质量变化为12.8g时,a极上消耗O2在标准状况下的体积为_______ L。
(4)若将装置B中的CuSO4溶液更换为100mL滴有酚酞的饱和NaCl溶液,电解一段时间后___ 极附近颜色变红,当装置A中消耗0.05mol氢气时,装置B中溶液的pH为______ 。
(5)若将装置B改为电解精炼铜,则粗铜作______ 极,另一极反应为_____________ 。

(1)装置A中b为
(2)装置B中C为
(3)当铁电极的质量变化为12.8g时,a极上消耗O2在标准状况下的体积为
(4)若将装置B中的CuSO4溶液更换为100mL滴有酚酞的饱和NaCl溶液,电解一段时间后
(5)若将装置B改为电解精炼铜,则粗铜作
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知图中甲池中A、B均为石墨电极,乙池中C为锌电极,D为铜电极,回答下列问题。

(1)乙池中电解质溶液为200mLCuSO4溶液,乙池为___________ (填“原电池”“电解池”),乙池中发生的化学方程式为___________ ;若把D电极换成银电极,则乙池中的反应速率会___________ 。
(2)甲池为100mLAgNO3溶液与100mLCuCl2溶液混合后的溶液,理论上两极所得气体的体积随时间变化的关系如图所示(气体体积已换算成标准状况下的体积,溶液混合过程中,体积细微变化忽略不计):

①混合前原100mLCuCl2溶液的物质的量浓度为___________ mol/L。
②t2时,甲池中所得溶液的pH=___________ ;此时乙池D增重的质量为___________ 。
③t2~t3时间段,I代表的气体为___________ 。
(3)以CH4(g)为燃料可以设计甲烷燃料电池,该电池以稀H2SO4作电解质溶液,写出该电池正极电极反应式:___________ ,已知该电池的能量转换效率为86.4%,1mol甲烷燃烧释放的热量为890.3kJ,则该电池的比能量为___________ kW·h·kg-1[结果保留1位小数,比能量= ,1kW·h=3.6×106J]。
,1kW·h=3.6×106J]。

(1)乙池中电解质溶液为200mLCuSO4溶液,乙池为
(2)甲池为100mLAgNO3溶液与100mLCuCl2溶液混合后的溶液,理论上两极所得气体的体积随时间变化的关系如图所示(气体体积已换算成标准状况下的体积,溶液混合过程中,体积细微变化忽略不计):

①混合前原100mLCuCl2溶液的物质的量浓度为
②t2时,甲池中所得溶液的pH=
③t2~t3时间段,I代表的气体为
(3)以CH4(g)为燃料可以设计甲烷燃料电池,该电池以稀H2SO4作电解质溶液,写出该电池正极电极反应式:
 ,1kW·h=3.6×106J]。
,1kW·h=3.6×106J]。
您最近一年使用:0次

 和
和 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示。若生成的乙烯和乙烷的体积比为
都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示。若生成的乙烯和乙烷的体积比为 ,则消耗的
,则消耗的


