将CO合成甲醇是实现“碳达峰、碳中和”的一项重要措施,在此过程中可能涉及以下物质:
①H2②O2③CO④He⑤H2O2⑥Na2O2⑦KOH⑧CH3OH⑨K2CO3
请判断:
(1)含有极性共价键的离子化合物有___________ (填编号)。
(2)含有非极性共价键的共价化合物有___________ (填编号)。
(3)在实验室中模拟CO合成甲醇的反应,在2L密闭容器内,400℃时发生反应:CO(g)+2H2(g)⇌CH3OH(g),体系中甲醇的物质的量n(CH3OH)随时间的变化如表:
已知每生成1molCH3OH(g),放出的热量为116kJ。计算上述反应达到平衡时放出的热量Q=___________ kJ(保留2位有效数字)。
(4)甲醇燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。电池的总反应式为:2CH3OH+3O2+4OH-=2 +6H2O。则电池放电时通入空气的电极为
+6H2O。则电池放电时通入空气的电极为___________ (“正”或“负”)极;从电极反应来看,每消耗1molCH3OH转移的电子数为___________ NA。
①H2②O2③CO④He⑤H2O2⑥Na2O2⑦KOH⑧CH3OH⑨K2CO3
请判断:
(1)含有极性共价键的离子化合物有
(2)含有非极性共价键的共价化合物有
(3)在实验室中模拟CO合成甲醇的反应,在2L密闭容器内,400℃时发生反应:CO(g)+2H2(g)⇌CH3OH(g),体系中甲醇的物质的量n(CH3OH)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 5 |
| n(CH3OH)(mol) | 0 | 0.009 | 0.012 | 0.013 | 0.013 |
(4)甲醇燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。电池的总反应式为:2CH3OH+3O2+4OH-=2
 +6H2O。则电池放电时通入空气的电极为
+6H2O。则电池放电时通入空气的电极为
更新时间:2023-08-10 16:15:39
|
相似题推荐
【推荐1】请回答下列问题:
(1)写出热化学方程式:1mol Cu(s)与适量O2(g)反应生成CuO(s),放出157.3kJ的热量___________ 。
(2)研究NO2、SO2等气体的无害化处理对治理大气污染、建设生态文明具有重要意义。
已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6kJ/mol
2SO3(g) ΔH=-196.6kJ/mol
2NO(g)+O2(g) 2NO2(g) ΔH=-113.0kJ/mol
2NO2(g) ΔH=-113.0kJ/mol
则NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH=
SO3(g)+NO(g)的ΔH=___________ kJ/mol。
(1)写出热化学方程式:1mol Cu(s)与适量O2(g)反应生成CuO(s),放出157.3kJ的热量
(2)研究NO2、SO2等气体的无害化处理对治理大气污染、建设生态文明具有重要意义。
已知:2SO2(g)+O2(g)
 2SO3(g) ΔH=-196.6kJ/mol
2SO3(g) ΔH=-196.6kJ/mol2NO(g)+O2(g)
 2NO2(g) ΔH=-113.0kJ/mol
2NO2(g) ΔH=-113.0kJ/mol则NO2(g)+SO2(g)
 SO3(g)+NO(g)的ΔH=
SO3(g)+NO(g)的ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)某一反应体系中的物质有:HCl、SnCl2、H2SnCl6、As、H3AsO3、H2O,已知:HCl是反应物之一。
①写出配平的该反应的化学方程式:_______________
②被氧化的元素是___________
(2)氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50℃时反应可生成它.CuH具有的性质有:不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;Cu+在酸性条件下发生的反应是:2Cu+==Cu2++Cu.
根据以上信息,结合自己所掌握的化学知识,回答下列问题:
①写出CuH在氯气中燃烧的化学反应方程式:___________________________________ .
②如果把CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式:__________________________________________________ .
(3)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为_________
①写出配平的该反应的化学方程式:
②被氧化的元素是
(2)氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50℃时反应可生成它.CuH具有的性质有:不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;Cu+在酸性条件下发生的反应是:2Cu+==Cu2++Cu.
根据以上信息,结合自己所掌握的化学知识,回答下列问题:
①写出CuH在氯气中燃烧的化学反应方程式:
②如果把CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式:
(3)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】生产生活中的化学反应都伴随能量的变化,请根据有关知识回答下列问题:
(1)“即热饭盒”可利用下面___________ (填字母序号)反应释放的热量加热食物。
A.生石灰和水B.浓硫酸和水C.钠和水
(2)氧、硫、硒( )、碲(
)、碲( )、钋(
)、钋(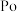 )是元素周期表中原子序数依次增大的同主族元素。
)是元素周期表中原子序数依次增大的同主族元素。
某温度时,该族单质与 反应生成气态
反应生成气态 的热化学方程式如下:
的热化学方程式如下:
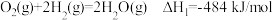
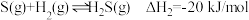
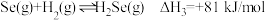
①硫和硒氢化物的热稳定性:
___________  (填“>”、“=”或“<”):判断依据是
(填“>”、“=”或“<”):判断依据是___________ 。
②写出 与
与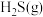 反应生成
反应生成 和
和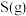 的热化学方程式
的热化学方程式___________ 。
(3)火箭发射时可以用液态肼作燃料, 作氧化剂。相关物质的能量转化关系如下。
作氧化剂。相关物质的能量转化关系如下。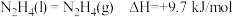 ,则
,则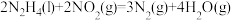 的反应热
的反应热 为
为___________  。
。
(1)“即热饭盒”可利用下面
A.生石灰和水B.浓硫酸和水C.钠和水
(2)氧、硫、硒(
 )、碲(
)、碲( )、钋(
)、钋(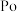 )是元素周期表中原子序数依次增大的同主族元素。
)是元素周期表中原子序数依次增大的同主族元素。某温度时,该族单质与
 反应生成气态
反应生成气态 的热化学方程式如下:
的热化学方程式如下: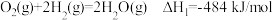
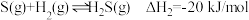
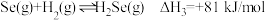
①硫和硒氢化物的热稳定性:

 (填“>”、“=”或“<”):判断依据是
(填“>”、“=”或“<”):判断依据是②写出
 与
与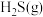 反应生成
反应生成 和
和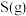 的热化学方程式
的热化学方程式(3)火箭发射时可以用液态肼作燃料,
 作氧化剂。相关物质的能量转化关系如下。
作氧化剂。相关物质的能量转化关系如下。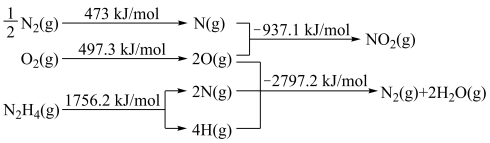
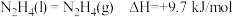 ,则
,则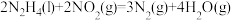 的反应热
的反应热 为
为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】I、依据氧化还原反应:2Ag+(aq)+Cu(s)==Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:
(1)电极X的材料是___________ ;(填化学式)电解质溶液Y是___________ ;X电极上发生的电极反应为________________________________ ;
(2)用两个铂丝做电极插入KOH溶液中,再分别向两极通入甲烷气体和氧气,可形成燃料电池,请写出负极的电极反应式____________________________ 在电池工作时,正极附近溶液的PH_________ ,(填,增大、减小或不变)
(3)用甲醇燃料电池作为直流电源,设计如图装置制取Cu2O,电解总反应为:2Cu+H2O=Cu2O+H2↑。铜电极为_________ (填“阳极”和“阴极”)写出铜电极的电极反应式_______________________ 。

(1)电极X的材料是
(2)用两个铂丝做电极插入KOH溶液中,再分别向两极通入甲烷气体和氧气,可形成燃料电池,请写出负极的电极反应式
(3)用甲醇燃料电池作为直流电源,设计如图装置制取Cu2O,电解总反应为:2Cu+H2O=Cu2O+H2↑。铜电极为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)表示含有20个中子的氯原子的符号为_________________________
(2)写出4核10电子分子的电子式________________________________
(3)已知一氧化碳的燃烧热 为—283kJ/mol,写出表示一氧化碳燃烧热的热化学方程式
为—283kJ/mol,写出表示一氧化碳燃烧热的热化学方程式___________________________________________________
(4)CH3OH与O2的反应可将化学能转化为电能,其工作原理如图所示,a极的电极反应式是_____ 。
(2)写出4核10电子分子的电子式
(3)已知一氧化碳的燃烧热
 为—283kJ/mol,写出表示一氧化碳燃烧热的热化学方程式
为—283kJ/mol,写出表示一氧化碳燃烧热的热化学方程式(4)CH3OH与O2的反应可将化学能转化为电能,其工作原理如图所示,a极的电极反应式是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流计的指针发生了偏转,并且三个池中的电解质溶液均足量。

请回答下列问题:
(1)甲池为_________ (填“原电池”“电解池”或“电镀池”),通入O2电极的电极反应式为__________ 。
(2)乙池B电极的电极反应式为____________ 。通电一段时间后,若使乙池恢复到通电前的状态(浓度一样),则可向其中加入适量的__________ (填化学式)物质。
(3)当丙池中D极质量增加6.40g时,则导线中通过的电子数目为_________ 。
(4)若在丙池中使铁件表面镀上铜,则C电极应改为________ 作电极(填电极的材料)。电镀前与电镀后相比:丙中溶液的pH将___ (填“增大”“减小”或“不变”)。

请回答下列问题:
(1)甲池为
(2)乙池B电极的电极反应式为
(3)当丙池中D极质量增加6.40g时,则导线中通过的电子数目为
(4)若在丙池中使铁件表面镀上铜,则C电极应改为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】⑴下列五种物质中,①Ar ②CO2 ③NaOH ④K2S ⑤NH4Cl ⑥SiO2,只存在共价键的是__________ ,(填序号,下同)只存在离子键的是__________ ,既存在离子键又存在共价键的是___________ ,不存在化学键的是___________ 。
⑵ W、X、Y、Z均为短周期主族元素,原子序数依次增加,且原子核外L电子层的电子数分别为0、6、8、8,它们的最外层电子数之和为15, W和Y的最外层电子数相同。则 ① Y、Z两元素的名称分别为______ 、_______ 。
② W2X2 的电子式为____________ ③Y2X2中存在的化学键是_____________ 。
⑵ W、X、Y、Z均为短周期主族元素,原子序数依次增加,且原子核外L电子层的电子数分别为0、6、8、8,它们的最外层电子数之和为15, W和Y的最外层电子数相同。则 ① Y、Z两元素的名称分别为
② W2X2 的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】有下列物质:①Cl2②Na2O2③NaOH④HCl⑤H2O2⑥MgF2
(1)只由离子键构成的物质是___ 。(填序号,下同)
(2)只由极性键构成的物质是___ 。
(3)只由非极性键构成的物质是___ 。
(4)由极性键和非极性键构成的物质是___ 。
(5)由离子键和极性键构成的物质是___ 。
(6)由离子键和非极性键构成的物质是___ 。
(1)只由离子键构成的物质是
(2)只由极性键构成的物质是
(3)只由非极性键构成的物质是
(4)由极性键和非极性键构成的物质是
(5)由离子键和极性键构成的物质是
(6)由离子键和非极性键构成的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】表为元素周期表中短周期元素的一部分,表中所列的字母分别代表一种元素。
(1)a、b、c、d、e、f六种元素的原子半径最大的是_______ (填元素符号)。
(2)d、e两种元素的最高价氧化物对应水化物的碱性较强的物质俗称为_______ , 、
、 的沸点较高的是
的沸点较高的是_______ (填化学式)。
(3)过量的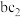 与
与 溶液能发生反应,写出反应的离子方程式:
溶液能发生反应,写出反应的离子方程式:_______ 。
(4)化学式为 的化合物属于
的化合物属于_______ (填“离子化合物”或“共价化合物”),其中含有的化学键的类型为_______ 。
| a | |||||||
| b | c | ||||||
| d | e | f |
(2)d、e两种元素的最高价氧化物对应水化物的碱性较强的物质俗称为
 、
、 的沸点较高的是
的沸点较高的是(3)过量的
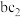 与
与 溶液能发生反应,写出反应的离子方程式:
溶液能发生反应,写出反应的离子方程式:(4)化学式为
 的化合物属于
的化合物属于
您最近一年使用:0次



