下列离子方程式正确的是________ 。
A.稀硫酸与铁丝制取氢气: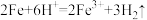
B.Cu片投入到FeCl3溶液中:Cu+2Fe3+=Cu2++2Fe2+
C.将少量Na放入水中:Na+H2O=Na++OH-+H2↑
D.氢氧化钡溶液与硫酸反应:OH-+H+=H2O
E.向澄清石灰水中通入少量二氧化碳:Ca2++2OH-+CO2=CaCO3↓+H2O
F.碳酸氢钠溶液与足量盐酸反应:2H++CO =H2O+CO2↑
=H2O+CO2↑
G.氧化钠与水反应:Na2O+H2O=2OH-+2Na+
H.将氧化钡与稀硫酸混合: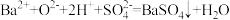
I.碳酸钙与稀盐酸制备二氧化碳:
J.CuSO4溶液中滴加Ba(OH)2溶液:Cu2++2OH-=Cu(OH)2↓
K.将铝片插入硝酸银溶液中: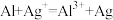
L.铁投入稀硫酸中:2Fe+6H+=2Fe3++3H2↑
A.稀硫酸与铁丝制取氢气:
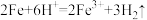
B.Cu片投入到FeCl3溶液中:Cu+2Fe3+=Cu2++2Fe2+
C.将少量Na放入水中:Na+H2O=Na++OH-+H2↑
D.氢氧化钡溶液与硫酸反应:OH-+H+=H2O
E.向澄清石灰水中通入少量二氧化碳:Ca2++2OH-+CO2=CaCO3↓+H2O
F.碳酸氢钠溶液与足量盐酸反应:2H++CO
 =H2O+CO2↑
=H2O+CO2↑G.氧化钠与水反应:Na2O+H2O=2OH-+2Na+
H.将氧化钡与稀硫酸混合:
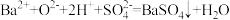
I.碳酸钙与稀盐酸制备二氧化碳:

J.CuSO4溶液中滴加Ba(OH)2溶液:Cu2++2OH-=Cu(OH)2↓
K.将铝片插入硝酸银溶液中:
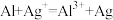
L.铁投入稀硫酸中:2Fe+6H+=2Fe3++3H2↑
2023高三上·全国·专题练习 查看更多[1]
(已下线)专题02 离子方程式(一题多问)
更新时间:2023-08-11 18:24:26
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】25℃时,有关物质的电离常数如下表:
(1)25℃时,反应 的平衡常数K=
的平衡常数K=___________ 。
(2)NaClO溶液在空气中吸收 的离子方程式为
的离子方程式为___________ 。
(3)反应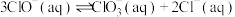 在室温下能自发进行。
在室温下能自发进行。
①T℃时,该反应的平衡常数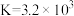 。若某混合溶液中
。若某混合溶液中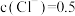
 ,
,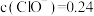
 ,
,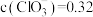
 ,则υ(正)
,则υ(正)___________ υ(逆)(填“>”“<”或“=”)。
②已知基元反应 的速率方程为
的速率方程为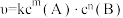 (k为只与温度有关的速率常数),一般反应的速率由基元反应中的慢反应决定。反应
(k为只与温度有关的速率常数),一般反应的速率由基元反应中的慢反应决定。反应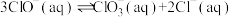 可能的机理有如下几种:
可能的机理有如下几种:
Ⅰ.
Ⅱ.(一)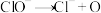 (慢)
(慢)
(二) (快)
(快)
(三) (快)
(快)
Ⅲ.(一) (慢)
(慢)
(二) (快)
(快)
则机理Ⅱ的中间体是___________ 。若反应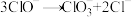 的速率方程为
的速率方程为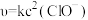 ,则该反应的历程可能是
,则该反应的历程可能是___________ (填标号)。
| 物质 | HClO |  |
| 电离常数 | 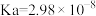 | 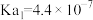 , ,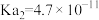 |
(1)25℃时,反应
 的平衡常数K=
的平衡常数K=(2)NaClO溶液在空气中吸收
 的离子方程式为
的离子方程式为(3)反应
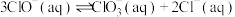 在室温下能自发进行。
在室温下能自发进行。①T℃时,该反应的平衡常数
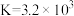 。若某混合溶液中
。若某混合溶液中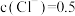
 ,
,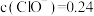
 ,
,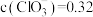
 ,则υ(正)
,则υ(正)②已知基元反应
 的速率方程为
的速率方程为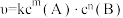 (k为只与温度有关的速率常数),一般反应的速率由基元反应中的慢反应决定。反应
(k为只与温度有关的速率常数),一般反应的速率由基元反应中的慢反应决定。反应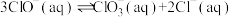 可能的机理有如下几种:
可能的机理有如下几种:Ⅰ.

Ⅱ.(一)
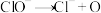 (慢)
(慢)(二)
 (快)
(快)(三)
 (快)
(快)Ⅲ.(一)
 (慢)
(慢)(二)
 (快)
(快)则机理Ⅱ的中间体是
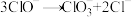 的速率方程为
的速率方程为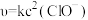 ,则该反应的历程可能是
,则该反应的历程可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下列离子方程式中正确的是______________
(1)氢氧化亚铁溶于稀硝酸中:Fe(OH)2+ 2H+= Fe2++ 2H2O
(2)过量的NaHSO4与Ba(OH)2溶液反应: Ba2++2OH-+2H++SO42-= BaSO4↓+2H2O
(3)向Ba(OH)2溶液中滴加NH4HSO4溶液至刚好沉淀完全: Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3·H2O+ H2O
(4)过量氯气通入溴化亚铁溶液中3C12+2Fe2++4Br一=6C1一+2Fe3++2Br2
(5)H218O中投入Na2O2固体:2H218O+2O22-=4OH-+18O2
(6)NH4HCO3溶液中加足量NaAlO2溶液:NH4++AlO2-+2H2O= NH3·H2O+ Al(OH)3↓
(7)0.1mol/L CuCl2溶液中加入0.1mol/L NaHS溶液:Cu2++2HS-+2H2O=Cu(OH)2↓+2H2S
(8)等物质的量的KHCO3和Ba(OH)2的溶液混合:HCO3-+Ba2++OH-= BaCO3↓+H2O
(9)向明矾溶液中逐滴加入Ba(OH)2溶液至Al3+刚好沉淀完全:Al3++SO42—+Ba2++3OH—==BaSO4↓+Al(OH)3↓
(10)NaHCO3溶液水解:HCO3-+ H2O CO32-+ H3O+
CO32-+ H3O+
(11)硫化钠水溶液呈碱性的原因:S2-+2H2O H2S↑+2OH-
H2S↑+2OH-
(12)在碳酸氢镁溶液中加入足量Ca(OH)2溶液:Mg2++HCO3-+Ca2++2OH–="=" MgCO3↓+CaCO3↓+2H2O
(13)用石墨作电极电解AlCl3溶液:2Cl-+2H2O Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
(14)向饱和碳酸钠溶液通入过量的二氧化碳气体:CO32-+CO2+H2O=2HCO3-
(1)氢氧化亚铁溶于稀硝酸中:Fe(OH)2+ 2H+= Fe2++ 2H2O
(2)过量的NaHSO4与Ba(OH)2溶液反应: Ba2++2OH-+2H++SO42-= BaSO4↓+2H2O
(3)向Ba(OH)2溶液中滴加NH4HSO4溶液至刚好沉淀完全: Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3·H2O+ H2O
(4)过量氯气通入溴化亚铁溶液中3C12+2Fe2++4Br一=6C1一+2Fe3++2Br2
(5)H218O中投入Na2O2固体:2H218O+2O22-=4OH-+18O2
(6)NH4HCO3溶液中加足量NaAlO2溶液:NH4++AlO2-+2H2O= NH3·H2O+ Al(OH)3↓
(7)0.1mol/L CuCl2溶液中加入0.1mol/L NaHS溶液:Cu2++2HS-+2H2O=Cu(OH)2↓+2H2S
(8)等物质的量的KHCO3和Ba(OH)2的溶液混合:HCO3-+Ba2++OH-= BaCO3↓+H2O
(9)向明矾溶液中逐滴加入Ba(OH)2溶液至Al3+刚好沉淀完全:Al3++SO42—+Ba2++3OH—==BaSO4↓+Al(OH)3↓
(10)NaHCO3溶液水解:HCO3-+ H2O
 CO32-+ H3O+
CO32-+ H3O+(11)硫化钠水溶液呈碱性的原因:S2-+2H2O
 H2S↑+2OH-
H2S↑+2OH-(12)在碳酸氢镁溶液中加入足量Ca(OH)2溶液:Mg2++HCO3-+Ca2++2OH–="=" MgCO3↓+CaCO3↓+2H2O
(13)用石墨作电极电解AlCl3溶液:2Cl-+2H2O
 Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-(14)向饱和碳酸钠溶液通入过量的二氧化碳气体:CO32-+CO2+H2O=2HCO3-
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)某溶液中含有下列离子中的某些离子: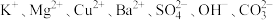 和
和 ,为确定其成分,取3份溶液分别进行如下实验:
,为确定其成分,取3份溶液分别进行如下实验:
Ⅰ.加入铝粉,有气泡产生
Ⅱ.滴入 溶液,无白色沉淀产生
溶液,无白色沉淀产生
Ⅲ.先滴加足量稀硝酸,再滴加 溶液,产生白色沉淀
溶液,产生白色沉淀
①根据以上现象判断,原溶液中肯定不存在的离子是_______ ,不能确定的离子是_______ ,若各离子浓度相等,可进一步得到的结论是_______ 。
②写出步骤Ⅲ中发生的离子反应方程式_______ 。
(2)某兴趣小组在两份相同的 溶液中,分别滴入相同浓度的
溶液中,分别滴入相同浓度的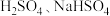 溶液,其导电能力随滴入溶液体积变化的曲线如下图所示:
溶液,其导电能力随滴入溶液体积变化的曲线如下图所示:

①图中表示 溶液中滴加
溶液中滴加 ,溶液的是曲线
,溶液的是曲线_______ (填“1”或“2”)。
② 在水溶液中的电离方程式为
在水溶液中的电离方程式为_______ 。
③下列说法错误的是_______ 。
A.曲线1中a点前导电能力不断减弱,说明生成的 不是电解质
不是电解质
B.曲线1中a点后导电能力不断增强,说明溶液中离子浓度在逐渐增大
C.曲线2中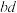 段发生的离子反应是
段发生的离子反应是
D.曲线2中d点对应的溶液显酸性
(1)某溶液中含有下列离子中的某些离子:
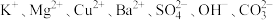 和
和 ,为确定其成分,取3份溶液分别进行如下实验:
,为确定其成分,取3份溶液分别进行如下实验:Ⅰ.加入铝粉,有气泡产生
Ⅱ.滴入
 溶液,无白色沉淀产生
溶液,无白色沉淀产生Ⅲ.先滴加足量稀硝酸,再滴加
 溶液,产生白色沉淀
溶液,产生白色沉淀①根据以上现象判断,原溶液中肯定不存在的离子是
②写出步骤Ⅲ中发生的离子反应方程式
(2)某兴趣小组在两份相同的
 溶液中,分别滴入相同浓度的
溶液中,分别滴入相同浓度的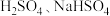 溶液,其导电能力随滴入溶液体积变化的曲线如下图所示:
溶液,其导电能力随滴入溶液体积变化的曲线如下图所示:
①图中表示
 溶液中滴加
溶液中滴加 ,溶液的是曲线
,溶液的是曲线②
 在水溶液中的电离方程式为
在水溶液中的电离方程式为③下列说法错误的是
A.曲线1中a点前导电能力不断减弱,说明生成的
 不是电解质
不是电解质B.曲线1中a点后导电能力不断增强,说明溶液中离子浓度在逐渐增大
C.曲线2中
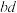 段发生的离子反应是
段发生的离子反应是
D.曲线2中d点对应的溶液显酸性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】高铁酸钠( )具有很强的氧化性,是一种优良的多功能水处理剂,工业上制备高铁酸钠有两种方法,主要反应原理如下:
)具有很强的氧化性,是一种优良的多功能水处理剂,工业上制备高铁酸钠有两种方法,主要反应原理如下:
①湿法制备:___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ (未配平)
(未配平)
②干法制备: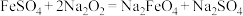
(1) 中Fe元素的化合价为
中Fe元素的化合价为___________ ,其在水溶液中的电离方程式为___________ 。
(2) 的电子式为
的电子式为___________ ,其与 反应的化学方程式为
反应的化学方程式为___________ 。
(3)配平反应①,并用“双线桥”标出中电子转移的方向和数目___________ 。该反应每生成1 mol  ,转移的电子数为
,转移的电子数为___________ 。
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________
(4)由反应②可知氧化性:
___________  (选填“<”或“>”)。
(选填“<”或“>”)。
(5) 在水中可被还原为
在水中可被还原为 ,其还原产物常用试剂
,其还原产物常用试剂___________ 检验。 可作为优良水处理剂的原因是
可作为优良水处理剂的原因是___________ 。
 )具有很强的氧化性,是一种优良的多功能水处理剂,工业上制备高铁酸钠有两种方法,主要反应原理如下:
)具有很强的氧化性,是一种优良的多功能水处理剂,工业上制备高铁酸钠有两种方法,主要反应原理如下:①湿法制备:___________
 ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ (未配平)
(未配平)②干法制备:
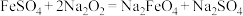
(1)
 中Fe元素的化合价为
中Fe元素的化合价为(2)
 的电子式为
的电子式为 反应的化学方程式为
反应的化学方程式为(3)配平反应①,并用“双线桥”标出中电子转移的方向和数目
 ,转移的电子数为
,转移的电子数为___________
 ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________
(4)由反应②可知氧化性:

 (选填“<”或“>”)。
(选填“<”或“>”)。(5)
 在水中可被还原为
在水中可被还原为 ,其还原产物常用试剂
,其还原产物常用试剂 可作为优良水处理剂的原因是
可作为优良水处理剂的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中Fe3+存在的试剂是________ ,证明Fe3+存在的现象是________ 。
(2)写出FeCl3溶液与金属铜发生反应的离子方程式:________ 。
(3)要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时的最佳顺序为________ 。
①加入足量氯水 ②加入足量KMnO4溶液 ③加入少量KSCN溶液
A.①③ B.③② C.③① D.①②③
(4)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:

请写出上述实验中加入或生成的有关物质的化学式④____________ 。
(5)写出向⑤的混合液中通入⑥的离子方程式:______________________ 。
(1)检验溶液中Fe3+存在的试剂是
(2)写出FeCl3溶液与金属铜发生反应的离子方程式:
(3)要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时的最佳顺序为
①加入足量氯水 ②加入足量KMnO4溶液 ③加入少量KSCN溶液
A.①③ B.③② C.③① D.①②③
(4)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:

请写出上述实验中加入或生成的有关物质的化学式④
(5)写出向⑤的混合液中通入⑥的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】铁是人类较早使用的金属之一、运用铁及其化合物的知识,完成下列问题。
(1)所含铁元素既有氧化性又有还原性的物质是____ (填字母代号)。
(2)向沸水中逐滴滴加lmol/LFeCl3溶液,至____ ,该分散系中粒子直径的范围是____ nm。
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:____ 。某校同学为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:首先取少量待测溶液﹐滴入KSCN溶液呈红色,则溶液中含有的金属阳离子是____ ,在此基础上,又进行了定量组成的测定:取50.0mL待测溶液,向其中加入足量的AgNO3溶液,得白色沉淀,____ (填实验操作,下同)、洗涤、干燥,称量沉淀质量为43.05g。则待测溶液中,FeCl3的物质的量浓度为____ 。
(4)若要验证该溶液中含有Fe2+,正确的实验方法是____ (填字母代号)。
A.向试管中加入试液,滴入KSCN溶液,若显红色,证明含有Fe2+
B.向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.向试管中加入试液,滴入氯水,再滴入KSCN溶液,若显红色,证明原溶液中含有Fe2+
(5)欲从废水中回收铜,并重新获得FeCl3溶液,设计实验方案如图:

A.请写出上述实验中加入或生成的有关物质的化学式:①____ ;②____ ;③____ ;④____ 。
B.请写出通入⑥的化学方程式:_____ 。
(1)所含铁元素既有氧化性又有还原性的物质是
| A.Fe | B.FeCl2 | C.FeSO4 | D.Fe2O3 |
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:
(4)若要验证该溶液中含有Fe2+,正确的实验方法是
A.向试管中加入试液,滴入KSCN溶液,若显红色,证明含有Fe2+
B.向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.向试管中加入试液,滴入氯水,再滴入KSCN溶液,若显红色,证明原溶液中含有Fe2+
(5)欲从废水中回收铜,并重新获得FeCl3溶液,设计实验方案如图:

A.请写出上述实验中加入或生成的有关物质的化学式:①
B.请写出通入⑥的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】铁是人类较早使用的金属之一,请按要求完成下列问题。
(1)在自然界中,铁元素主要以___ (填写“游离态”或“化合态”)形式存在
(2)下列铁的化合物中,不能直接化合得到的是___ (用字母代号填)。
A.Fe3O4 B.FeCl2 C.Fe(OH)2 D.Fe(OH)3
(3)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,与水反应可生成透明的红褐色胶体,反应原理:4FeO +10H2O=4Fe(OH)3(胶体)+3O2↑+8OH-
+10H2O=4Fe(OH)3(胶体)+3O2↑+8OH-
①Fe(OH)3胶体分散质粒子的直径范围是___ 。
②该反应中H2O是___ 。
A.氧化剂 B.还原剂 C.被氧化 D.被还原
③高铁酸钾(K2FeO4)能杀灭水中细菌的原因是___ 。
(4)电子工业常用30%左右的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得FeCl3溶液,某同学设计下列方案:
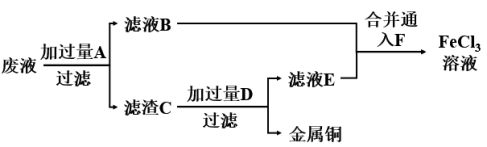
①实验室用无水氯化铁固体粗略配制30%的FeCl3溶液,需要的主要玻璃仪器除了量筒外还有___ 。
②写出FeCl3溶液与铜箔发生反应的离子方程式___ 。
③滤渣C的成分___ (填写化学式)。
④现用500g32.5%FeCl3溶液制造印刷电路板,生产后的腐蚀废液用该同学设计方案处理,最终获得氯化铁溶液中的FeCl3的质量至少为___ g。
(1)在自然界中,铁元素主要以
(2)下列铁的化合物中,不能直接化合得到的是
A.Fe3O4 B.FeCl2 C.Fe(OH)2 D.Fe(OH)3
(3)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,与水反应可生成透明的红褐色胶体,反应原理:4FeO
 +10H2O=4Fe(OH)3(胶体)+3O2↑+8OH-
+10H2O=4Fe(OH)3(胶体)+3O2↑+8OH-①Fe(OH)3胶体分散质粒子的直径范围是
②该反应中H2O是
A.氧化剂 B.还原剂 C.被氧化 D.被还原
③高铁酸钾(K2FeO4)能杀灭水中细菌的原因是
(4)电子工业常用30%左右的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得FeCl3溶液,某同学设计下列方案:

①实验室用无水氯化铁固体粗略配制30%的FeCl3溶液,需要的主要玻璃仪器除了量筒外还有
②写出FeCl3溶液与铜箔发生反应的离子方程式
③滤渣C的成分
④现用500g32.5%FeCl3溶液制造印刷电路板,生产后的腐蚀废液用该同学设计方案处理,最终获得氯化铁溶液中的FeCl3的质量至少为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】印刷电路板是由高分子材料和铜箔复合而成。刻制印刷线路时,要用过量的氯化铁溶液作为腐蚀液,使铜转化为氯化铜,所得废液经处理后可循环利用。请完成下列空白
(1)在FeCl3溶液腐蚀铜的反应中离子方程式为_______ 。
(2)从保护环境和节约资源的角度考虑,废液A不应作为废液排放。某化学兴趣小组的同学向废液A中加入某种足量的金属粉末,充分反应后,过滤,回收了铜,得到废液B,此过程中有关反应的离子方程式为_______ 、_______ 。该小组的同学为了重新得到腐蚀液,又向废液B中通入一种气体,该气体参与反应的化学方程式是_______ 。
(3)若利用500mL2mol/L的FeCl3溶液刻制印刷线路,并循环使用废液,当初次使用的FeCl3溶液恰好完全反应,可回收铜的质量为_______ 。
(1)在FeCl3溶液腐蚀铜的反应中离子方程式为
(2)从保护环境和节约资源的角度考虑,废液A不应作为废液排放。某化学兴趣小组的同学向废液A中加入某种足量的金属粉末,充分反应后,过滤,回收了铜,得到废液B,此过程中有关反应的离子方程式为
(3)若利用500mL2mol/L的FeCl3溶液刻制印刷线路,并循环使用废液,当初次使用的FeCl3溶液恰好完全反应,可回收铜的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】FeCl3是一种用途比较广泛的铁盐。
(1)印刷电路板是由高分子材料和铜箔复合而成的,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2,请写出该反应的离子方程式:___________________ 。
(2)FeCl3在天然水中可生成氢氧化铁胶体,其沉降水中悬浮物的速率高于铝盐,是城市污水和工业废水处理的高效絮凝剂.实验中制取氢氧化铁胶体的方法是_______ (填序号)。
①向FeCl3溶液中加入足量的NaOH溶液;
②将饱和的FeCl3溶液滴入沸水中,并继续煮沸至生成红褐色液体;
③将饱和的FeCl3溶液滴入沸水中,并继续煮沸至生成红褐色沉淀;
含有Fe3+的盐溶液遇到___________ 溶液时变成红色,我们可以利用这一反应检验Fe3+的存在。
(3)FeCl3可使湿润的淀粉碘化钾试纸变蓝,化学方程式为2FeCl3+2KI=2FeCl2+I2+2KCl,用双线桥法标出该反应中电子转移的方向和数目__________________________
将一定量的CCl4加入上述反应后的溶液中,振荡、静置后会发现下层液体为__________ 色,再将混合液倒入_________ (填仪器名称)中,可将两层液体分离。
(1)印刷电路板是由高分子材料和铜箔复合而成的,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2,请写出该反应的离子方程式:
(2)FeCl3在天然水中可生成氢氧化铁胶体,其沉降水中悬浮物的速率高于铝盐,是城市污水和工业废水处理的高效絮凝剂.实验中制取氢氧化铁胶体的方法是
①向FeCl3溶液中加入足量的NaOH溶液;
②将饱和的FeCl3溶液滴入沸水中,并继续煮沸至生成红褐色液体;
③将饱和的FeCl3溶液滴入沸水中,并继续煮沸至生成红褐色沉淀;
含有Fe3+的盐溶液遇到
(3)FeCl3可使湿润的淀粉碘化钾试纸变蓝,化学方程式为2FeCl3+2KI=2FeCl2+I2+2KCl,用双线桥法标出该反应中电子转移的方向和数目
将一定量的CCl4加入上述反应后的溶液中,振荡、静置后会发现下层液体为
您最近一年使用:0次



