在下列事实中,什么因素影响了化学反应的速率?
(1)集气瓶中有H2和Cl2的混合气体,在瓶外点燃镁条时发生爆炸________ ;
(2)黄铁矿煅烧时要粉碎成细小的矿粒________ ;
(3)KI晶体和HgCl2晶体混合后无明显现象,若一起投入水中,很快生成红色HgI2___________________________ ;
(4)熔化的KClO3放出气泡很慢,撒入少量MnO2后很快产生气体________ ;
(5)同浓度、同体积的盐酸中放入同样大小的锌粒和镁块,产生气体的速率有快有慢________ ;
(6)同样大小的石灰石分别在0.1 mol·L-1的盐酸和1 mol·L-1的盐酸中反应速率不同________ ;
(7)夏天的食品易变霉,冬天就不易发生该现象__________________________________
(8)葡萄糖在空气中燃烧时需要较高的温度,可是在人体里,在正常体温(37 ℃)时,就可以被氧化,这是因为______________________________________________
(1)集气瓶中有H2和Cl2的混合气体,在瓶外点燃镁条时发生爆炸
(2)黄铁矿煅烧时要粉碎成细小的矿粒
(3)KI晶体和HgCl2晶体混合后无明显现象,若一起投入水中,很快生成红色HgI2
(4)熔化的KClO3放出气泡很慢,撒入少量MnO2后很快产生气体
(5)同浓度、同体积的盐酸中放入同样大小的锌粒和镁块,产生气体的速率有快有慢
(6)同样大小的石灰石分别在0.1 mol·L-1的盐酸和1 mol·L-1的盐酸中反应速率不同
(7)夏天的食品易变霉,冬天就不易发生该现象
(8)葡萄糖在空气中燃烧时需要较高的温度,可是在人体里,在正常体温(37 ℃)时,就可以被氧化,这是因为
13-14高一·全国·课时练习 查看更多[3]
更新时间:2016-12-09 05:34:53
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】化学反应速率与生产、生活密切相关。
(1)A学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
①反应速率最大的时间段是______ (填“0~1”“1~2”“2~3”“3~4”“4~5”)min,原因是:_______ 。
②反应速率最小的时间段是___________ ,原因是:___________ 。
③2~3min内该反应的反应速率υ(HCl)=_________ mol∙L−1∙min−1(设溶液体积不变)。
(2)B学生也做同样的实验,但由于反应太快,测不准氢气体积,故想办法降低反应速率,请你帮他选择在盐酸中加入下列___________ (填字母)以减慢反应速率,同时不影响生成氢气的量。
A.蒸馏水 B.NaOH溶液 C.Na2CO3溶液 D.CuSO4溶液 E.NaCl溶液
(1)A学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标况) | 50 | 120 | 232 | 290 | 310 |
①反应速率最大的时间段是
②反应速率最小的时间段是
③2~3min内该反应的反应速率υ(HCl)=
(2)B学生也做同样的实验,但由于反应太快,测不准氢气体积,故想办法降低反应速率,请你帮他选择在盐酸中加入下列
A.蒸馏水 B.NaOH溶液 C.Na2CO3溶液 D.CuSO4溶液 E.NaCl溶液
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】一种新型催化剂用于NO和CO的反应:2NO+2CO⇌2CO2+N2。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在表中。

(1)请将表中数据补充完整:a___ ,b___ 。
(2)能验证温度对化学反应速率规律的是实验___ (填实验序号)。
(3)实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验Ⅱ的是曲线___ (填“甲”或“乙”)。
(4)在容积固定的容器中发生反应2NO+2CO 2CO2+N2,不能说明已达到平衡状态的是
2CO2+N2,不能说明已达到平衡状态的是___ (不定项选择);
A.容器内CO浓度不变
B.容器内NO的浓度等于CO2的浓度
C.v逆(NO)=2v正(N2)
D.容器内混合气体密度保持不变
| 实验编号 | t(℃) | NO初始浓度 (mol/L) | CO初始浓度(mol/L) | 催化剂的比表 面积(m2/g) |
| Ⅰ | 280 | 1.2×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 280 | 1.2×10-3 | b | 124 |
| Ⅲ | 350 | a | 5.80×10-3 | 82 |

(1)请将表中数据补充完整:a
(2)能验证温度对化学反应速率规律的是实验
(3)实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验Ⅱ的是曲线
(4)在容积固定的容器中发生反应2NO+2CO
 2CO2+N2,不能说明已达到平衡状态的是
2CO2+N2,不能说明已达到平衡状态的是A.容器内CO浓度不变
B.容器内NO的浓度等于CO2的浓度
C.v逆(NO)=2v正(N2)
D.容器内混合气体密度保持不变
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量。O3氧化烟气中SO2、NOx的主要反应的热化学方程式为:
NO(g)+O3(g)=NO2(g)+O2(g) △H=-200.9kJ·mol-1
NO(g)+ O2(g)=NO2(g) △H=-58.2kJ·mol-1
O2(g)=NO2(g) △H=-58.2kJ·mol-1
SO2(g)+O3(g)=SO3(g)+O2(g) △H=-241.6kJ·mol-1
室温下,固定进入反应器的NO、SO2的物质的量,改变加入O3的物质的量,反应一段时间后体系中n(NO)、n(NO2)和n(SO2)随反应前n(O3):n(NO)的变化见图。

①当n(O3):n(NO)>1时,反应后NO2的物质的量减少,其原因是__ 。
②增加n(O3),O3氧化SO2的反应几乎不受影响,其可能原因是__ 。
NO(g)+O3(g)=NO2(g)+O2(g) △H=-200.9kJ·mol-1
NO(g)+
 O2(g)=NO2(g) △H=-58.2kJ·mol-1
O2(g)=NO2(g) △H=-58.2kJ·mol-1SO2(g)+O3(g)=SO3(g)+O2(g) △H=-241.6kJ·mol-1
室温下,固定进入反应器的NO、SO2的物质的量,改变加入O3的物质的量,反应一段时间后体系中n(NO)、n(NO2)和n(SO2)随反应前n(O3):n(NO)的变化见图。

①当n(O3):n(NO)>1时,反应后NO2的物质的量减少,其原因是
②增加n(O3),O3氧化SO2的反应几乎不受影响,其可能原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】为达到下表中的实验目的,请选择合适的试剂及实验方法,将其标号填入对应的空格。
供选择的化学试剂及实验方法
A.取样,灼烧
B.取样,滴加酚酞试液
C.加水溶解、过滤、结晶
D.取样,滴加稀硫酸
| 实验目的 | 试剂及方法 |
| 证明炭粉中含有CuO | |
| 鉴别丝绸和棉布 | |
| 分离Na2SO4和CaCO3固体混合物 | |
| 证明Na2CO3溶液呈碱性 |
供选择的化学试剂及实验方法
A.取样,灼烧
B.取样,滴加酚酞试液
C.加水溶解、过滤、结晶
D.取样,滴加稀硫酸
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质。
(1)若将饱和FeCl3溶液分别滴入下列液体中,能形成胶体的是________。
(2)现有甲、乙、丙、丁四名同学进行Fe(OH)3胶体的制备
①甲同学的操作是:取一小烧杯,加入25 mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2 mL FeCl3饱和溶液,用玻璃棒搅拌,继续煮沸至溶液呈红褐色,停止加热。请评价该操作是否正确______________ 。
②乙向沸水中滴加饱和FeCl3溶液,为了使反应进行充分,煮沸10分钟,请评价是否正确____________ 。
(3)写出制备Fe(OH)3胶体的化学方程式:__________________________ 。
(4)怎样检验制备的物质是否为胶体?____________________________ 。
(5)取少量你制得的胶体加入试管中,加入(NH4)2SO4溶液,现象是______________ ,这种现象称为胶体的____________ 。
(6)氢氧化铁胶体稳定存在的主要原因是__________。
(1)若将饱和FeCl3溶液分别滴入下列液体中,能形成胶体的是________。
| A.冷水 | B.沸水 | C.NaOH浓溶液 | D.NaCl浓溶液 |
①甲同学的操作是:取一小烧杯,加入25 mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2 mL FeCl3饱和溶液,用玻璃棒搅拌,继续煮沸至溶液呈红褐色,停止加热。请评价该操作是否正确
②乙向沸水中滴加饱和FeCl3溶液,为了使反应进行充分,煮沸10分钟,请评价是否正确
(3)写出制备Fe(OH)3胶体的化学方程式:
(4)怎样检验制备的物质是否为胶体?
(5)取少量你制得的胶体加入试管中,加入(NH4)2SO4溶液,现象是
(6)氢氧化铁胶体稳定存在的主要原因是__________。
| A.胶粒直径小于1 nm | B.胶粒带正电荷 |
| C.胶粒作布朗运动 | D.胶粒能透过滤纸 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】已知稀溴水和氯化铁溶液都呈黄色,现在足量的稀氯化亚铁溶液中,加入1~2滴液溴,振荡后溶液呈黄色。
(1)甲同学认为这不是发生化学反应所致,则使溶液呈黄色的微粒是:______ (填粒子的化学式,下同);
乙同学认为这是发生化学反应所致,则使溶液呈黄色的微粒是_________ 。
(2)如果要验证乙同学判断的正确性,请根据下面所提供的可用试剂,用两种方法加以验证,请将选用的试剂代号及实验中观察到的现象填入下表。
实验可供选用试剂:
A.酸性高锰酸钾溶液 B.氢氧化钠溶液 C.四氯化碳
D.硫氰化钾溶液 E.硝酸银溶液 F.碘化钾淀粉溶液
(3)根据上述实验推测,若在稀溴化亚铁溶液中通入氯气,则首先被氧化的离子是________ ,相应的离子方程式为_______________________________________________ ;
(1)甲同学认为这不是发生化学反应所致,则使溶液呈黄色的微粒是:
乙同学认为这是发生化学反应所致,则使溶液呈黄色的微粒是
(2)如果要验证乙同学判断的正确性,请根据下面所提供的可用试剂,用两种方法加以验证,请将选用的试剂代号及实验中观察到的现象填入下表。
实验可供选用试剂:
A.酸性高锰酸钾溶液 B.氢氧化钠溶液 C.四氯化碳
D.硫氰化钾溶液 E.硝酸银溶液 F.碘化钾淀粉溶液
| 实验方案 | 所选用试剂(填代号) | 实验现象 |
| 方案一 | ||
| 方案二 |
(3)根据上述实验推测,若在稀溴化亚铁溶液中通入氯气,则首先被氧化的离子是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】在农业生产中常施用草木灰增加土壤中钾肥,草木灰的主要成分是K2CO3,请同学设计实验方案证明该物质的存在;(写出实验步骤、实验现象、实验结论)
(1)检验K+的方案:_______ ;
(2)检验CO 的方案:
的方案:_______ ;
(1)检验K+的方案:
(2)检验CO
 的方案:
的方案:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】钠是一种非常活泼的金属,它可以和冷水直接反应生成氢氧化钠和氢气,但是它与煤油不会发生反应。把一小块银白色的金属钠投入盛有蒸馏水的烧杯中(如图a所示),可以看到钠浮在水面上,与水发生剧烈反应,反应放出的热量使钠熔成小球,甚至会使钠和生成的氢气都发生燃烧。
如果在上述盛蒸馏水的烧杯中先注入一些煤油,再投入金属钠,可以看到金属钠悬浮在煤油和水的界面上(如图b所示),同样与水发生剧烈的反应,但是不发生燃烧。

(1)钠和水反应的文字表达式为_______________________________ 。
(2)氢氧化钠是一种碱,能让无色酚酞变为红色。如果预先在a烧杯中滴加几滴酚酞试液,实验中可以看到液体颜色由____ 色变为____ 色。
(3)在第二个实验中,钠也与水发生反应,但不发生燃烧,猜想这是因为___________________________________ 。
(4)在第一个实验中,钠浮在水面上;在第二个实验中,钠悬浮在煤油和水的界面上。这两个现象说明了_____________________________ 。
如果在上述盛蒸馏水的烧杯中先注入一些煤油,再投入金属钠,可以看到金属钠悬浮在煤油和水的界面上(如图b所示),同样与水发生剧烈的反应,但是不发生燃烧。

(1)钠和水反应的文字表达式为
(2)氢氧化钠是一种碱,能让无色酚酞变为红色。如果预先在a烧杯中滴加几滴酚酞试液,实验中可以看到液体颜色由
(3)在第二个实验中,钠也与水发生反应,但不发生燃烧,猜想这是因为
(4)在第一个实验中,钠浮在水面上;在第二个实验中,钠悬浮在煤油和水的界面上。这两个现象说明了
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
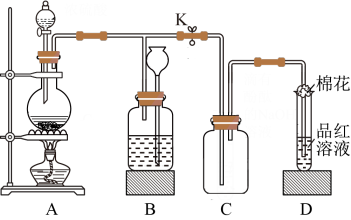
【推荐3】某化学课外兴趣小组用如图所示装置进行实验,制备某气体并验证其性质。请回答下列问题:
①装置A中发生反应的化学方程式为___________ 。
②实验中,取一定质量的铜片和一定体积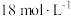 的浓硫酸在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
的浓硫酸在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
A.有一定量的余酸但未能使铜片完全溶解,你认为原因是___________ 。
B.下列药品中能用来证明反应结束后的烧瓶中确有余酸的是___________ (填标号)。
a.铁粉 b. 溶液 c.银粉 d.
溶液 c.银粉 d. 溶液
溶液
(2)若装置A中分液漏斗盛装浓硫酸,圆底烧瓶盛装木炭。
①装置A中发生反应的化学方程式为___________ 。
②设计实验证明装置C中含有 时,所需的试剂有
时,所需的试剂有___________ (填标号)。
a. 溶液 b.澄清石灰水 c.品红溶液 d.酸性
溶液 b.澄清石灰水 c.品红溶液 d.酸性 溶液
溶液
(3)若装置A中分液漏斗盛装浓盐酸,圆底烧瓶盛装 粉末。
粉末。
①装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭止水夹K并移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是___________ 。
②D中品红溶液褪色,加热试管里已褪色溶液时的现象为___________ 。
(4)装置D中试管口放置的棉花中浸了一种液体,可适用于(1)(2)(3)小题中实验,该液体是___________ 。
①装置A中发生反应的化学方程式为
②实验中,取一定质量的铜片和一定体积
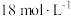 的浓硫酸在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
的浓硫酸在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。A.有一定量的余酸但未能使铜片完全溶解,你认为原因是
B.下列药品中能用来证明反应结束后的烧瓶中确有余酸的是
a.铁粉 b.
 溶液 c.银粉 d.
溶液 c.银粉 d. 溶液
溶液(2)若装置A中分液漏斗盛装浓硫酸,圆底烧瓶盛装木炭。
①装置A中发生反应的化学方程式为
②设计实验证明装置C中含有
 时,所需的试剂有
时,所需的试剂有a.
 溶液 b.澄清石灰水 c.品红溶液 d.酸性
溶液 b.澄清石灰水 c.品红溶液 d.酸性 溶液
溶液(3)若装置A中分液漏斗盛装浓盐酸,圆底烧瓶盛装
 粉末。
粉末。①装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭止水夹K并移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是
②D中品红溶液褪色,加热试管里已褪色溶液时的现象为
(4)装置D中试管口放置的棉花中浸了一种液体,可适用于(1)(2)(3)小题中实验,该液体是
您最近一年使用:0次



