电化学方法是化工生产及生活中常用的一种方法。回答下列问题:
I.闸门由钢质材料制作,长期浸于水中,通常采用如图装置对闸门进行保护。

(1)a、b间用导线连接时,X可以是___________ ,其保护方法的名称是___________ 。
(2)a、b间外接电源也可保护钢闸门,某员工因粗心把a错接到电源的正极,导致加快了钢闸门的腐蚀,检验阳极产物时加入___________ 溶液,现象为有蓝色沉淀生成。
Ⅱ.二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、快速、安全的杀菌消毒剂。目前已开发出用电解法制取ClO2的新工艺如图所示:
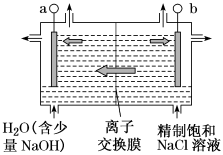
(3)图中用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。产生ClO2的电极发生___________ 反应(填“氧化”或“还原”),对应的电极反应式为___________ 。
(4)外电路每通过10NA电子时,生成的ClO2物质的量是___________ mol
(5)a极区溶液的pH___________ (填“增大”“减小”或“不变”),图中离子交换膜应使用___________ (填“阴”或“阳”)离子交换膜。
I.闸门由钢质材料制作,长期浸于水中,通常采用如图装置对闸门进行保护。

(1)a、b间用导线连接时,X可以是
(2)a、b间外接电源也可保护钢闸门,某员工因粗心把a错接到电源的正极,导致加快了钢闸门的腐蚀,检验阳极产物时加入
Ⅱ.二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、快速、安全的杀菌消毒剂。目前已开发出用电解法制取ClO2的新工艺如图所示:

(3)图中用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。产生ClO2的电极发生
(4)外电路每通过10NA电子时,生成的ClO2物质的量是
(5)a极区溶液的pH
更新时间:2023-07-14 22:42:34
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】电化学原理在能量转换、物质制备、防止金属腐蚀等方面应用广泛。
(1)下图是常见电化学装置图
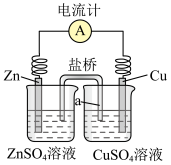
① 负极材料为Zn,其在此装置中的作用是___________ 。
② 若用一根铜丝代替盐桥插入两烧杯中,电流计指针也发生偏转,推测:其中一个为原电池,一个为电解池,写出a端发生的电极反应___________ 。
(2)下图探究金属Fe是否腐蚀的示意图
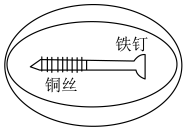
在培养皿中加入一定量的琼脂和饱和NaCl溶液混合,滴入5~6滴酚酞溶液,混合均匀,将缠有铜丝的铁钉放入培养皿中。溶液变红的部位为___________ 端(填“左”或“右”),结合化学用语解释变红的原因___________ 。
(3)下图是氯碱工业电解饱和NaCl溶液的示意图

①电解饱和NaCl溶液的化学方程式是___________ 。
② NaOH溶液从___________ (填b或c)口导出。结合化学用语解释NaOH在此区域生成的原因___________ 。
③电解时用盐酸控制阳极区溶液的pH在2~3,用化学平衡移动原理解释盐酸的作用___________ 。
(4)我国科学家通过电解,从海水中提取到锂单质,其工作原理如图所示。

①金属锂在电极___________ (填“A”或“B”)生成,发生的是___________ (填“氧化”或“还原”)反应。
②阳极产生两种气体单质,电极反应式分别是___________ ;___________ 。
(1)下图是常见电化学装置图

① 负极材料为Zn,其在此装置中的作用是
② 若用一根铜丝代替盐桥插入两烧杯中,电流计指针也发生偏转,推测:其中一个为原电池,一个为电解池,写出a端发生的电极反应
(2)下图探究金属Fe是否腐蚀的示意图

在培养皿中加入一定量的琼脂和饱和NaCl溶液混合,滴入5~6滴酚酞溶液,混合均匀,将缠有铜丝的铁钉放入培养皿中。溶液变红的部位为
(3)下图是氯碱工业电解饱和NaCl溶液的示意图

①电解饱和NaCl溶液的化学方程式是
② NaOH溶液从
③电解时用盐酸控制阳极区溶液的pH在2~3,用化学平衡移动原理解释盐酸的作用
(4)我国科学家通过电解,从海水中提取到锂单质,其工作原理如图所示。

①金属锂在电极
②阳极产生两种气体单质,电极反应式分别是
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐2】如图所示,水槽中试管内有一枚铁钉,放置数天观察:

(1)铁钉在逐渐生锈。
(2)若试管内液面上升,发生_______ 腐蚀,电极反应:负极:_______ ,正极:_______ 。
(3)若试管内液面下降,则原溶液呈_______ 性,发生的电极反应:正极:_______ 。

(1)铁钉在逐渐生锈。
(2)若试管内液面上升,发生
(3)若试管内液面下降,则原溶液呈
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】利用烧结的铁碳混合材料可除去废水中的污染物,在有、无溶解氧的情况下均可在溶液中生成絮凝剂,实现高效工作,其作用原理图示如下:
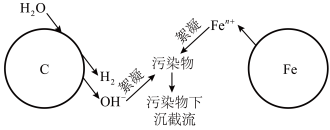
请回答:
(1)写出铁电极上电极方程式_________ 。
(2)下列叙述正确的是。
(3)有溶解氧时絮凝过程是利用了铁离子水解产物吸附污染物完成截流,写出相关的离子方程式_______ 。
(4)无溶解氧时,可以利用生成的絮凝剂处理含铬废水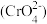 ,最终溶液中的金属离子均生成氢氧化物沉淀。已知国家标准中污染物排放浓度的单位为mg·L-1,若每处理10.0 m3污水,电极上共转移1.20 mol电子,则该污水在处理前的排放浓度为
,最终溶液中的金属离子均生成氢氧化物沉淀。已知国家标准中污染物排放浓度的单位为mg·L-1,若每处理10.0 m3污水,电极上共转移1.20 mol电子,则该污水在处理前的排放浓度为________ (以铬元素的量计算)。

请回答:
(1)写出铁电极上电极方程式
(2)下列叙述正确的是。
| A.铁电极为正极,碳电极为负极 |
| B.经过加热烧结的铁碳混合物表面空隙发达,吸附能力大幅提高,有利除污 |
| C.碳电极上的反应环境为无溶解氧环境 |
| D.铁碳混合材料工作过程中电子从铁电极流出,被絮凝剂运输至碳电极表面 |
(4)无溶解氧时,可以利用生成的絮凝剂处理含铬废水
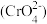 ,最终溶液中的金属离子均生成氢氧化物沉淀。已知国家标准中污染物排放浓度的单位为mg·L-1,若每处理10.0 m3污水,电极上共转移1.20 mol电子,则该污水在处理前的排放浓度为
,最终溶液中的金属离子均生成氢氧化物沉淀。已知国家标准中污染物排放浓度的单位为mg·L-1,若每处理10.0 m3污水,电极上共转移1.20 mol电子,则该污水在处理前的排放浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.如图所示,E为浸过含酚酞的Na2SO4溶液的滤纸。A、B分别为铂片,压在滤纸两端,R、S为电池的电极。M、N是用多微孔的Ni制成的电极,在碱溶液中可视为惰性电极。G为电流计,K为开关。C、D和电解池中都充满浓KOH溶液。若在滤纸中央滴一滴紫色的KMnO4溶液,将开关K打开,接通电源一段时间后,C、D中有气体产生。
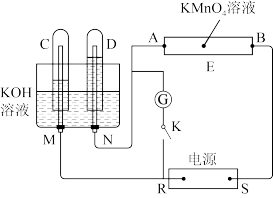
请回答下列问题:
(1)R为___________ (填“正”或“负”)极。
(2)通电一段时间后,M、N电极对应的电解质溶液的pH___________ (填“变大”、“变小”或“不变”);B附近发生的电极反应式为___________ 。
(3)滤纸上的紫色点向___________ (填“A”或“B”)方向移动。
(4)当C、D中的气体产生到一定量时,切断外电源并接通开关K,经过一段时间后,C、D中的气体逐渐减少,C中的电极为___________ (填“正”或“负”)极,电极反应式为___________ 。
Ⅱ.通过NOx传感器可监测NOx的含量,其工作原理示意图如下:
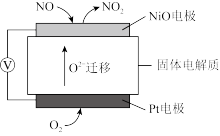
(5)Pt电极上发生的是___________ 反应(填“氧化”或“还原”)。
(6)写出NiO电极的电极反应式:___________ 。

请回答下列问题:
(1)R为
(2)通电一段时间后,M、N电极对应的电解质溶液的pH
(3)滤纸上的紫色点向
(4)当C、D中的气体产生到一定量时,切断外电源并接通开关K,经过一段时间后,C、D中的气体逐渐减少,C中的电极为
Ⅱ.通过NOx传感器可监测NOx的含量,其工作原理示意图如下:

(5)Pt电极上发生的是
(6)写出NiO电极的电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某科研机构用NaOH溶液吸收硫酸工业废气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到某种副产物,其原理如图所示(电极材料为石墨)。

(1)当有1molNa+通过阳离子交换膜时,a极生成气体_______ L(标准状况),阳极的电极反应式是_______ 。
(2)稀NaOH溶液的作用是_______ ,B处流出较浓的NaOH溶液,C处流出的是_______ 。
(3)在标准状况下,若用甲烷-空气燃料电池做电源,处理含SO2 20%(体积分数)的废气40m3,理论上需要消耗甲烷_______ m3

(1)当有1molNa+通过阳离子交换膜时,a极生成气体
(2)稀NaOH溶液的作用是
(3)在标准状况下,若用甲烷-空气燃料电池做电源,处理含SO2 20%(体积分数)的废气40m3,理论上需要消耗甲烷
您最近一年使用:0次
【推荐3】合成氨技术的发明使工业化人工固氮成为现实。请回答下列问题:
(1)合成氨的反应为:2NH3(g) N2(g)+3H2(g),有关化学键的键能如表所示。
N2(g)+3H2(g),有关化学键的键能如表所示。
①该反应的反应热ΔH=_______ 。
②已知该反应的ΔS=198.9 J·mol−1·K−1,在下列哪些温度下反应能自发进行?_______ (填标号)
A.25℃ B.125℃ C.225℃ D.325℃
(2)在一定温度下,将1 mol N2和3 mol H2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为3.0 mol。
①达平衡时,H2的转化率α=_______ 。
②已知平衡时,容器压强为8 MPa,则平衡常数Kp=_______ (用平衡分压代替浓度计算,分压=总压×物质的量分数)。
(3)利用电解原理,将氨转化为高纯氢气,其装置如图所示。
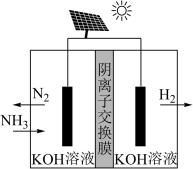
①阴极产生标准状况下112mL气体时,通过阴离子交换膜的离子的物质的量为_______ ;
②阳极的电极反应式为_______ 。
(1)合成氨的反应为:2NH3(g)
 N2(g)+3H2(g),有关化学键的键能如表所示。
N2(g)+3H2(g),有关化学键的键能如表所示。| 化学键 |  |  |  |
| 键能E/ kJ·mol−1 | 946 | 436.0 | 390.8 |
②已知该反应的ΔS=198.9 J·mol−1·K−1,在下列哪些温度下反应能自发进行?
A.25℃ B.125℃ C.225℃ D.325℃
(2)在一定温度下,将1 mol N2和3 mol H2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为3.0 mol。
①达平衡时,H2的转化率α=
②已知平衡时,容器压强为8 MPa,则平衡常数Kp=
(3)利用电解原理,将氨转化为高纯氢气,其装置如图所示。

①阴极产生标准状况下112mL气体时,通过阴离子交换膜的离子的物质的量为
②阳极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的三分之一。请回答钢铁在腐蚀、防护过程中的有关问题。
(1)在实际生产中,可在铁件的表面镀上锌保护层或锡保护层防止铁被腐蚀。镀层破损后,镀锡铁和镀锌铁更容易被腐蚀的是______ 。(填“镀锡铁”或“镀锌铁”)
(2)下列哪个装置可防止铁棒被腐蚀______ 。
(3)利用如图装置可以模拟铁的电化学防护。
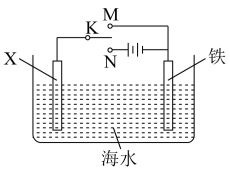
①若X为碳棒,为减缓铁的腐蚀,开关K应置于_____ 处。假设海水中只有NaCl溶质,写出此时总离子反应方程式:_____ 。
②若X为锌,开关K置于M处,该电化学防护法称为_____ ,写出铁电极处的电极反应式:_____ 。
(1)在实际生产中,可在铁件的表面镀上锌保护层或锡保护层防止铁被腐蚀。镀层破损后,镀锡铁和镀锌铁更容易被腐蚀的是
(2)下列哪个装置可防止铁棒被腐蚀
A.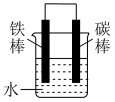 | B. | C.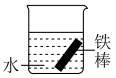 | D.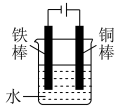 |

①若X为碳棒,为减缓铁的腐蚀,开关K应置于
②若X为锌,开关K置于M处,该电化学防护法称为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】钢铁工业是国家工业的基础。请回答钢铁腐蚀、防护过程中的有关问题:
(1)生产中可用盐酸来除铁锈。现将一生锈的铁片放入盐酸中,当铁锈被除尽后,溶液中发生的属于化合反应的化学方程式是______________ 。
(2)下列装置可防止铁棒被腐蚀的是___________ 。
A. B.
B.  C.
C.  D.
D. 
(3)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀,装置示意图如图所示。

①A电极对应的金属是______ (填元素名称),B电极的电极反应式是________ 。
②镀层破损后,镀铜铁比镀锌铁更易被腐蚀,原因是_________ 。
(1)生产中可用盐酸来除铁锈。现将一生锈的铁片放入盐酸中,当铁锈被除尽后,溶液中发生的属于化合反应的化学方程式是
(2)下列装置可防止铁棒被腐蚀的是
A.
 B.
B.  C.
C.  D.
D. 
(3)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀,装置示意图如图所示。

①A电极对应的金属是
②镀层破损后,镀铜铁比镀锌铁更易被腐蚀,原因是
您最近一年使用:0次
【推荐3】电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。
(1)图中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择__________ (填字母)。

a.碳棒 b.锌板 c.铜板 d.钠块
(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。

①E为该燃料电池的________ (填“正”或“负”)极。F电极上的电极反应式为__________
②镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因_________ 。
③0.4molCuSO4和0.4molNaCl溶于水,配成1L溶液,用该镁燃料电池用惰性电极进行电解,当一个电极得到0.3molCu时,另一个电极上生成的气体在标准状况下的体积为_______ L。
(3)如图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。

①b处应通入______ (填“CH4”或“O2”),a处电极上发生的电极反应式是_________________ ;
②电镀结束后,装置Ⅰ中溶液的pH_____________ ;(填写“变大”“变小”或“不变”)装置Ⅱ中Cu2+的物质的量浓度_______________ ;(填写“变大”“变小”或“不变”)
③在此过程中若完全反应,装置Ⅱ中阴极质量变化12.8g,则装置Ⅰ中理论上消耗甲烷________ L(标况)。
(1)图中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择

a.碳棒 b.锌板 c.铜板 d.钠块
(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。

①E为该燃料电池的
②镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因
③0.4molCuSO4和0.4molNaCl溶于水,配成1L溶液,用该镁燃料电池用惰性电极进行电解,当一个电极得到0.3molCu时,另一个电极上生成的气体在标准状况下的体积为
(3)如图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。

①b处应通入
②电镀结束后,装置Ⅰ中溶液的pH
③在此过程中若完全反应,装置Ⅱ中阴极质量变化12.8g,则装置Ⅰ中理论上消耗甲烷
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】碘酸钾在容量法分析中用作氧化剂。氢碘酸在化学分析中常用作还原剂,可用于测定硒、甲氧基、乙氧基。碘酸钾和氢碘酸均可用电解法制备。
(1)用电解法制备碘酸钾( )的装置如图1所示。
)的装置如图1所示。

①a极的电极反应式为_______ 。
②b极产生的气体的化学式为_______ 。
③电解一段时间后,若外电路转移10 mol电子,则阴极区生成的气体质量为_______ ,右室溶液的pH_______ (填“增大”、“减小”或“不变”)。
(2)用电解法制备氢碘酸(HI)的装置如图2所示。其中双极膜(BPM)是阴、阳复合膜,在直流电的作用下,阴、阳膜复合层间的 解离成
解离成 和
和 ,A、B膜为离子交换膜。
,A、B膜为离子交换膜。

①B膜最佳应选择_______ 。
a.阴离子交换膜 b. 交换膜 c.
交换膜 c. 交换膜
交换膜
②阳极的电极反应式是_______ 。
(1)用电解法制备碘酸钾(
 )的装置如图1所示。
)的装置如图1所示。
①a极的电极反应式为
②b极产生的气体的化学式为
③电解一段时间后,若外电路转移10 mol电子,则阴极区生成的气体质量为
(2)用电解法制备氢碘酸(HI)的装置如图2所示。其中双极膜(BPM)是阴、阳复合膜,在直流电的作用下,阴、阳膜复合层间的
 解离成
解离成 和
和 ,A、B膜为离子交换膜。
,A、B膜为离子交换膜。
①B膜最佳应选择
a.阴离子交换膜 b.
 交换膜 c.
交换膜 c. 交换膜
交换膜②阳极的电极反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某兴趣小组的同学用下图所示装里研究有关电化学的问题(甲、乙、丙三池中解质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。
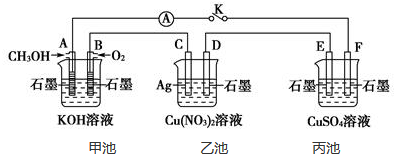
请回答下列问题:
(1)甲池_______ (填“原电池”、 “电解池”或“电镀”), B电极的电极反应式为_________ 。
(2)丙池中F电极为________ (填“正极”、“负极”、“阴极”或“阳极),该池的总反应方程式_______________ 。
(3)当乙池中C极质量减轻5.4g时,甲池中B电极理论上消耗O2的体积为______ mL(标准状况), 丙池中____ 极(填E或F)析出______ gCu。
(4)一段时间后,断开电键K,下列物质能使乙池恢复到反应前浓度的是____ (填选项字母)。
A. Cu B. CuO C. Cu(OH)2 D. Cu2(OH)2CO3
(5)若丙中电极不变,将其溶液换为NaCl溶液,电键闭合一段时间后,甲中溶液的pH将______ 。(填增大,减小或不变);丙中溶液的pH将_______ (填增大,减小或不变)。

请回答下列问题:
(1)甲池
(2)丙池中F电极为
(3)当乙池中C极质量减轻5.4g时,甲池中B电极理论上消耗O2的体积为
(4)一段时间后,断开电键K,下列物质能使乙池恢复到反应前浓度的是
A. Cu B. CuO C. Cu(OH)2 D. Cu2(OH)2CO3
(5)若丙中电极不变,将其溶液换为NaCl溶液,电键闭合一段时间后,甲中溶液的pH将
您最近一年使用:0次




