为探究钠的部分性质,设计实验操作如图:

①向如图所示的试管中加入苯(已知苯的密度为0.86 g·cm-3,苯不溶于水);
②拔出大头针,使Na(密度为0.97 g·cm-3)落入苯中(钠与苯不反应);
③从长颈漏斗中加入MgCl2溶液(密度约为1 g·cm-3)。
下列说法中正确的是

①向如图所示的试管中加入苯(已知苯的密度为0.86 g·cm-3,苯不溶于水);
②拔出大头针,使Na(密度为0.97 g·cm-3)落入苯中(钠与苯不反应);
③从长颈漏斗中加入MgCl2溶液(密度约为1 g·cm-3)。
下列说法中正确的是
| A.把MgCl2溶液加入苯中,MgCl2溶液在下层 |
| B.钠一直停留在苯层不发生反应 |
| C.Na在MgCl2溶液与苯的界面处反应,并上下跳动直至消失,下层有白色沉淀产生 |
| D.Na在MgCl2溶液底部四处游动,MgCl2溶液中有白色沉淀产生 |
23-24高一上·全国·课时练习 查看更多[1]
更新时间:2023-08-25 20:47:56
|
相似题推荐
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】一定质量的钠铝合金投入水中,充分反应后测得产生4 mol气体且固体有剩余,将相同质量的钠铝合金投入足量氢氧化钠溶液中,充分反应后产生5.5 mol气体,下列正确的是
| A.铝的质量为81 g | B.钠和铝的质量比为23:27 |
| C.剩余固体的物质的量为1.5 mol | D.两次实验中转移电子数之比为8:11 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】根据“反应规律”可以预测物质的性质,据有关“规律”下列结论合理的是
A.金属钠在纯氧中燃烧生成 ,推出金属 ,推出金属 在纯氧中燃烧生成 在纯氧中燃烧生成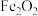 |
B.金属钠的活泼性比铜强,推出金属钠投入 溶液可以置换出单质 溶液可以置换出单质 |
C.根据较强酸可以制取较弱酸的规律,推出 通入次氯酸盐溶液中能生成 通入次氯酸盐溶液中能生成 |
D. 通入澄清的石灰水先变浑浊继续通又变澄清,推出 通入澄清的石灰水先变浑浊继续通又变澄清,推出 通入 通入 溶液能发生化学反应 溶液能发生化学反应 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】下列四组反应中既有沉淀产生又有气体放出的是
| A.金属钠投入到MgSO4溶液中 |
| B.BaCl2和NaHSO4溶液反应 |
| C.小苏打溶液和澄清石灰水反应 |
| D.Na2O2和CuSO4溶液反应 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】下列离子方程式正确的是
A.把金属Na投入CuSO4溶液中:2Na+Cu2++SO =Cu+2Na2++SO =Cu+2Na2++SO |
B.向AlCl3溶液中滴加浓氨水至过量:Al3++4NH3·H2O=AlO +4NH +4NH +2H2O +2H2O |
C.向NaHSO4溶液中加Ba(OH)2溶液至中性:Ba2++2OH-+2H++SO =BaSO4↓+2H2O =BaSO4↓+2H2O |
| D.向含0.1molFeBr2的溶液中通入0.1molCl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】下列反应没有氢气生成的是
| A.单质钠投入水中 | B.钠投入到氢氧化钠溶液中 |
| C.氧化钠投入水中 | D.往过氧化钠中滴加水 |
您最近一年使用:0次



