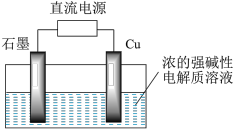
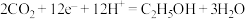Cu2O是一种半导体材料,基于绿色化学理论设计的制取Cu2O的电解池示意图如图,电解总反应为2Cu+H2O Cu2O+H2↑。下列说法正确的是
Cu2O+H2↑。下列说法正确的是
 Cu2O+H2↑。下列说法正确的是
Cu2O+H2↑。下列说法正确的是
| A.石墨电极上产生氢气 | B.铜电极发生还原反应 |
| C.铜电极接直流电源的负极 | D.当有0.1 mol电子转移时,有0.05 mol Cu2O生成 |
23-24高二上·全国·课时练习 查看更多[1]
更新时间:2023-08-27 12:58:12
|
相似题推荐
多选题
|
适中
(0.65)
解题方法
【推荐1】用如图所示装置回收金属钴。回收过程保持细菌所在环境pH相对稳定,借助其将乙酸盐转化为二氧化碳。使用废旧锂电池的正极材料LiCoO2转化为Co2+,工作时保持厌氧环境,并定时将乙室溶液转移到甲室。电极材料均为石墨材质,右侧为原电池。下列说法正确的是
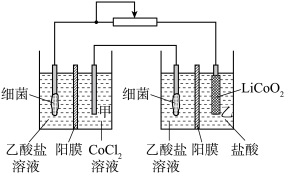

| A.细菌所处环境应为偏酸性环境 |
B.乙室电极反应式是: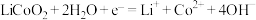 |
| C.若甲室Co2+减少1 mol,乙室Co2+增加2 mol,则此时已经进行过溶液转移 |
| D.将乙酸盐换为乙醇盐,可回收更多的Co |
您最近一年使用:0次
【推荐2】下列说法正确的是
| A.铜和铁与FeCl3溶液构成的原电池中:Cu +2 Fe3+= Cu2++ 2Fe2+ |
| B.铁上镀锌时阴极析出6.5g锌,溶液中减少Zn2+数为0.1mol |
| C.在反应:4CuS + 5O2= 2Cu2O + 4SO2中CuS既是氧化剂又是还原剂 |
| D.生铁与浓H2SO4加热反应可产生SO2和CO2气体 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】次磷酸(H3PO2)为一元弱酸,H3PO2可以通过电解的方法制备,其工作原理如下图所示。下列说法正确的是
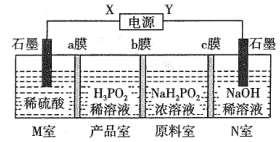

| A.X为电源正极,Y为电源负极 |
| B.电解一段时间后,N室的pH减小 |
| C.a、c为阳离子交换膜,b为阴离子交换膜 |
| D.当电路中通过3mol电子时,可生成1mol H3PO2 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】用电解法制备高纯金属铬和硫酸的原理如图所示。下列说法正确的是
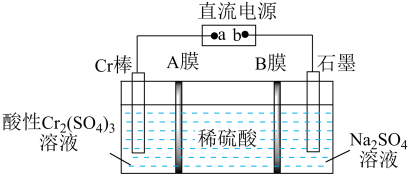

| A.b为直流电源的正极 |
| B.A膜是阳离子交换膜,B膜是阴离子交换膜 |
| C.阴极电极反应式为2H++2e-=H2↑ |
| D.若有1 mol离子通过A膜,理论上阳极生成0.5 mol气体 |
您最近一年使用:0次

 )的高效除去。原理如图所示,其中电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯。该装置工作时,下列叙述错误的是
)的高效除去。原理如图所示,其中电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯。该装置工作时,下列叙述错误的是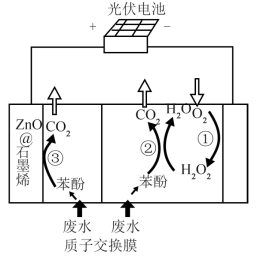
 +11H2O-28e-=6CO2+28H+
+11H2O-28e-=6CO2+28H+ 抑制酸性电解液中的析氢反应来提高多碳产物(乙烯、乙醇等)的生成率,装置如图所示。下列说法正确的是
抑制酸性电解液中的析氢反应来提高多碳产物(乙烯、乙醇等)的生成率,装置如图所示。下列说法正确的是