黄铜矿 是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。冶炼铜的反应为:
是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。冶炼铜的反应为:
(1)若 中
中 的化合价为
的化合价为 ,反应中被还原的元素是
,反应中被还原的元素是___________ (填元素符号)。
(2)过二硫酸钾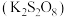 具有强氧化性,可将
具有强氧化性,可将 氧化为
氧化为 :
: 。通过改变反应途径,
。通过改变反应途径, 均可催化上述反应。试用离子方程式表示
均可催化上述反应。试用离子方程式表示 对上述反应催化的过程:
对上述反应催化的过程:___________ 、___________ 。
 是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。冶炼铜的反应为:
是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。冶炼铜的反应为:
(1)若
 中
中 的化合价为
的化合价为 ,反应中被还原的元素是
,反应中被还原的元素是(2)过二硫酸钾
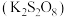 具有强氧化性,可将
具有强氧化性,可将 氧化为
氧化为 :
: 。通过改变反应途径,
。通过改变反应途径, 均可催化上述反应。试用离子方程式表示
均可催化上述反应。试用离子方程式表示 对上述反应催化的过程:
对上述反应催化的过程:
更新时间:2023-07-17 21:22:25
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】回答下列问题:
(1)粗盐的提纯和精制实验中用到水、碳酸钠、氢氧化钠、盐酸等试剂或溶剂,依据物质的分类标准,指出它们所属类别(答案从下面选项中选择,请填写字母):水___ ;碳酸钠___ ;氢氧化钠___ ;盐酸___ 。
A.氧化物B.碱C.酸D.盐E.有机物
(2)食盐水提纯过程中先后发生以下复分解反应:①BaCl2+Na2SO4─②BaCl2+Na2CO3─③CaCl2+Na2CO3─④MgCl2+NaOH─⑤Na2CO3+HCl─⑥NaOH+HCl─。
写出反应④的化学方程式___ 。写出反应①、③、⑤的离子方程式:①___ ;③____ ;⑤___ 。
(1)粗盐的提纯和精制实验中用到水、碳酸钠、氢氧化钠、盐酸等试剂或溶剂,依据物质的分类标准,指出它们所属类别(答案从下面选项中选择,请填写字母):水
A.氧化物B.碱C.酸D.盐E.有机物
(2)食盐水提纯过程中先后发生以下复分解反应:①BaCl2+Na2SO4─②BaCl2+Na2CO3─③CaCl2+Na2CO3─④MgCl2+NaOH─⑤Na2CO3+HCl─⑥NaOH+HCl─。
写出反应④的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】写出下列反应的离子方程式
(1)二氧化碳通入澄清石灰水_________________________________
(2)小苏打除胃酸___________________________________________
(3)硫酸和氢氧化钠反应_____________________________________
(4)金属铜和硝酸银溶液反应_________________________________
(1)二氧化碳通入澄清石灰水
(2)小苏打除胃酸
(3)硫酸和氢氧化钠反应
(4)金属铜和硝酸银溶液反应
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】 是高效、广谱、绿色的消毒剂,回答下列问题。
是高效、广谱、绿色的消毒剂,回答下列问题。
(1)氯在元素周期表中的位置是___________ ,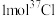 的中子数为
的中子数为___________ 。
(2)下列能判断Cl和O两种元素非金属性强弱的是___________ (填序号)。
a.原子得电子能力
b.与金属钠反应得电子的数目
c.最简单气态氢化物的稳定性
d.单质的沸点
(3)生产生活中含氯物质的排放会加快臭氧层的破坏。该过程的机理如图,总反应化学方程式为___________ 。

(4)化工、冶金行业的废水中存在 ,可用
,可用 气体将其转化为两种无毒气体
气体将其转化为两种无毒气体
① 的电子式为
的电子式为___________ 。
②该反应的离子方程式为___________ 。
(5)X、Y、Z、W四种短周期元素在周期表中的位置关系如图,Y和Z的核外电子数之和为22。将少量X的最高价氧化物通入到硅酸钠溶液中实现现象是___________ ,反应的离子方程式为___________ 。
 是高效、广谱、绿色的消毒剂,回答下列问题。
是高效、广谱、绿色的消毒剂,回答下列问题。(1)氯在元素周期表中的位置是
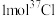 的中子数为
的中子数为(2)下列能判断Cl和O两种元素非金属性强弱的是
a.原子得电子能力
b.与金属钠反应得电子的数目
c.最简单气态氢化物的稳定性
d.单质的沸点
(3)生产生活中含氯物质的排放会加快臭氧层的破坏。该过程的机理如图,总反应化学方程式为

(4)化工、冶金行业的废水中存在
 ,可用
,可用 气体将其转化为两种无毒气体
气体将其转化为两种无毒气体①
 的电子式为
的电子式为②该反应的离子方程式为
(5)X、Y、Z、W四种短周期元素在周期表中的位置关系如图,Y和Z的核外电子数之和为22。将少量X的最高价氧化物通入到硅酸钠溶液中实现现象是
| X | Y | |
| Z | W |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】氧化还原反应原理在研究物质性质及物质转化方面具有重要的价值。
(1)化合价是学习氧化还原反应的基础。标出下列物质中划线元素的化合价。
NaI:___________ ;ClO :
:___________ ;K2MnO4:___________
(2)中国古代著作中有“银针验毒”的纪录,其原理为4Ag+2H2S+O2=2X+2H2O,则X的化学式是___________ ,其中H2S在该反应中___________ 。(填标号)。
A.作氧化剂 B.作还原剂 C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(3)已知铜在常温下能被浓硝酸溶解,其反应的化学方程式如下:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O。氧化产物是___________ ,还原产物是___________ 。用双线桥法表示反应电子得失的方向和数目___________
(1)化合价是学习氧化还原反应的基础。标出下列物质中划线元素的化合价。
NaI:
 :
:(2)中国古代著作中有“银针验毒”的纪录,其原理为4Ag+2H2S+O2=2X+2H2O,则X的化学式是
A.作氧化剂 B.作还原剂 C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(3)已知铜在常温下能被浓硝酸溶解,其反应的化学方程式如下:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O。氧化产物是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】阅读下列材料后,回答相应问题。
一个体重50 kg的健康人,含铁2 g,这2 g铁在人体中不是以单质金属的形式存在的,而是以Fe2+和Fe3+的形式存在。二价铁离子易被吸收,给贫血者补充铁时,应给予含二价铁离子的二价铁盐,如硫酸亚铁(FeSO4)。服用维生素C,可使食物中的三价铁离子还原成二价铁离子,有利于铁的吸收。
(1)人体中经常进行Fe2+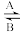 Fe3+的转化,A中Fe2+作
Fe3+的转化,A中Fe2+作___________ 剂。
(2)“服用维生素C,可使食物中的三价铁离子还原成二价铁离子”这句话指出维生素C在这一反应中作___________ 剂。
(3)检验硫酸亚铁溶液中含有Fe2+,使用的试剂正确的是___________ 。
①加入少量氯水 ②加入足量H2SO4溶液 ③加入少量KSCN溶液
A.①③ B.②③ C.①②
(4)鉴别Fe(OH)3胶体和FeCl3溶液的方法是___________ 。
一个体重50 kg的健康人,含铁2 g,这2 g铁在人体中不是以单质金属的形式存在的,而是以Fe2+和Fe3+的形式存在。二价铁离子易被吸收,给贫血者补充铁时,应给予含二价铁离子的二价铁盐,如硫酸亚铁(FeSO4)。服用维生素C,可使食物中的三价铁离子还原成二价铁离子,有利于铁的吸收。
(1)人体中经常进行Fe2+
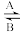 Fe3+的转化,A中Fe2+作
Fe3+的转化,A中Fe2+作(2)“服用维生素C,可使食物中的三价铁离子还原成二价铁离子”这句话指出维生素C在这一反应中作
(3)检验硫酸亚铁溶液中含有Fe2+,使用的试剂正确的是
①加入少量氯水 ②加入足量H2SO4溶液 ③加入少量KSCN溶液
A.①③ B.②③ C.①②
(4)鉴别Fe(OH)3胶体和FeCl3溶液的方法是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】“价一类”二维图是研究物质性质的重要工具,如图是硫元素的“价一类”二维图。
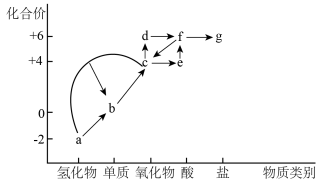
回答下列问题:
(1)c→d反应的化学方程式为________ 。
(2)反应a+c→b中,氧化产物与还原产物的物质的量之比为______ 。
(3)溶液e久置于空气中会生成f,该过程溶液的酸性______ (填“增强”或“减弱”)。
(4)可用铜与f的浓溶液反应制备c,反应的化学方程式为____________ 。
(5)将c通入到酸性KMnO₄溶液中,溶液颜色逐渐变浅,该反应中c表现出______ (填“还原”或“漂白”)性。
(6)实验室产生c排放到大气中会引起酸雨,应用_____ 溶液吸收,发生的反应方程式为__ 。

回答下列问题:
(1)c→d反应的化学方程式为
(2)反应a+c→b中,氧化产物与还原产物的物质的量之比为
(3)溶液e久置于空气中会生成f,该过程溶液的酸性
(4)可用铜与f的浓溶液反应制备c,反应的化学方程式为
(5)将c通入到酸性KMnO₄溶液中,溶液颜色逐渐变浅,该反应中c表现出
(6)实验室产生c排放到大气中会引起酸雨,应用
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】铁酸钠(Na2FeO4)是一种新型水处理剂,它有比高锰酸钾更强的氧化性,在水中反应被还原为Fe3+。
(1)铁酸钠中铁元素的化合价为________ 。铁酸钠能消毒杀菌,这是因为它具有________ 性。
(2)铁酸钠用于水处理时,除了能消毒杀菌外,还能沉降水中的悬浮杂质,起到净水作用,请说明其净水原理__________________________________________________ 。
(1)铁酸钠中铁元素的化合价为
(2)铁酸钠用于水处理时,除了能消毒杀菌外,还能沉降水中的悬浮杂质,起到净水作用,请说明其净水原理
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】Fe2+的性质:Fe2+具有较强的还原性,容易被一些氧化剂氧化为Fe3+。
(1)向FeCl2溶液中加入KSCN溶液,实验现象是_______ ,再加入氯水,实验现象是_______ ,Fe2+与Cl2反应的离子方程式为_______ 。
(2)Fe2+在酸性条件下与H2O2反应:_______ 。
(3)为除去废水中的Fe2+,常先将废水中的Fe2+_______ 为Fe3+(填“氧化”或“还原”),再调节溶液的pH使Fe3+转化为_______ 色的沉淀析出。
(1)向FeCl2溶液中加入KSCN溶液,实验现象是
(2)Fe2+在酸性条件下与H2O2反应:
(3)为除去废水中的Fe2+,常先将废水中的Fe2+
您最近一年使用:0次
【推荐1】(1)某同学写出以下三个化学方程式(未配平):
①
②
③
其中你认为不可能实现的是________ (填序号)。
(2)下列三个氧化还原反应中,氧化性最强的物质是________ (填化学式,下同)。
①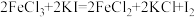
②
③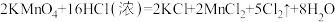
若溶质中 与
与 共存,为了氧化
共存,为了氧化 而
而 不被氧化,除
不被氧化,除 单质外,还可应用上述物质中的
单质外,还可应用上述物质中的________ 作氧化剂。
①

②

③

其中你认为不可能实现的是
(2)下列三个氧化还原反应中,氧化性最强的物质是
①
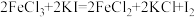
②

③
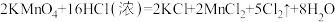
若溶质中
 与
与 共存,为了氧化
共存,为了氧化 而
而 不被氧化,除
不被氧化,除 单质外,还可应用上述物质中的
单质外,还可应用上述物质中的
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】(1)离子方程式是重要的化学用语。下列是有关离子方程式的一些错误观点,请在下列表格中用相应的“离子方程式”否定这些观点。【反应物请从下列物质中选取:Fe、HCl、NaOH、CuSO4、Ba(OH)2、CH3COOH】
(2)世界环保联盟即将全面禁止在自来水中加氯气(Cl2,黄绿色气体),推广采用光谱高效消毒剂二氧化氯,目前欧洲和我国主采用Kesting法[原料为氯酸钠(NaClO3)与盐酸]制取ClO2,该法的缺点是同时会产生Cl2.该法制ClO2的化学方程式为2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
①若生成1个 Cl2,转移的电子的个数为___________ ,该反应中氧化产物为___________ 。
②在题中化学方程式中标出电子的转移的方向和数目___________ 。
③盐酸在反应中显示出来的性质是:(填写编号)___________ 。两者的个数之比___________ 。
a。具有还原性和不稳定性 b。具有酸性和氧化性 c。有氧化性和不稳定性 d。具有酸性与还原性
| ① | 所有的离子方程式均可以表示一类反应 | |
| ② | 所有酸碱中和反应均可表示为:H++OH-=H2O |
①若生成1个 Cl2,转移的电子的个数为
②在题中化学方程式中标出电子的转移的方向和数目
③盐酸在反应中显示出来的性质是:(填写编号)
a。具有还原性和不稳定性 b。具有酸性和氧化性 c。有氧化性和不稳定性 d。具有酸性与还原性
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】根据要求完成下列问题
(1)单质铝和氢氧化钠溶液反应的化学方程式_________________ ,本反应中的氧化剂是______
(2)实验室用二氧化锰和浓盐酸制取氯气的离子方程式___________________________________ ,本反应中的氧化剂和还原剂的物质的量比为____________
(3)二氧化硫和氯气按等物质的量通入足量水中的化学方程式_______________ ,本反应中若有1mol氧化剂参加反应则转移电子数为_________
(4)硫氰化钾溶液检验三价铁离子的离子方程式:______________ ,本反应的现象__________
(1)单质铝和氢氧化钠溶液反应的化学方程式
(2)实验室用二氧化锰和浓盐酸制取氯气的离子方程式
(3)二氧化硫和氯气按等物质的量通入足量水中的化学方程式
(4)硫氰化钾溶液检验三价铁离子的离子方程式:
您最近一年使用:0次



