实验室利用下图装置用乙醇和浓硫酸在 反应制取乙烯,再用乙烯与溴的四氯化碳溶液反应制备1,2-二溴乙烷。
反应制取乙烯,再用乙烯与溴的四氯化碳溶液反应制备1,2-二溴乙烷。
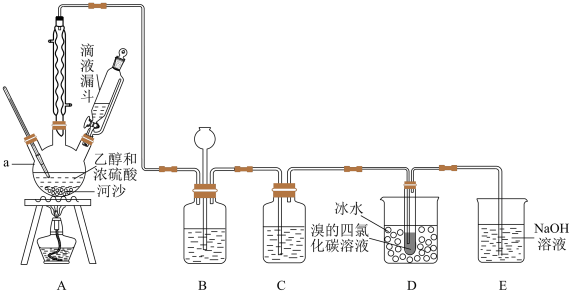
(1)在装置A中,生成的气体除乙烯外还有乙醚、 、
、 等,则生成乙烯的化学方程式为
等,则生成乙烯的化学方程式为___________ ,仪器a的名称为___________ 。
(2)装置B可起到安全瓶的作用,若气压过大,该装置中出现的现象为___________ 。
(3)装置C可除去 、
、 ,所盛放的溶液为
,所盛放的溶液为___________ 。
(4)装置D中进行的主要反应的化学方程式为___________ ,可观察到的实验现象是___________ 。把试管置于盛有冰水的小烧杯中的目的是___________ 。
 反应制取乙烯,再用乙烯与溴的四氯化碳溶液反应制备1,2-二溴乙烷。
反应制取乙烯,再用乙烯与溴的四氯化碳溶液反应制备1,2-二溴乙烷。
(1)在装置A中,生成的气体除乙烯外还有乙醚、
 、
、 等,则生成乙烯的化学方程式为
等,则生成乙烯的化学方程式为(2)装置B可起到安全瓶的作用,若气压过大,该装置中出现的现象为
(3)装置C可除去
 、
、 ,所盛放的溶液为
,所盛放的溶液为(4)装置D中进行的主要反应的化学方程式为
更新时间:2023-07-29 18:17:20
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D、四种有机物有如下转化关系(部分产物和转化条件已略去);
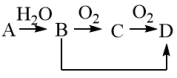
已知烯烃A可以作为水果的催熟剂,其产量可以用来衡量一个国家石油化学工业的发展水平,D是食醋的成分之一、请回答下列问题:
(1)写出A物质的结构简式___________ 。
(2)写出B物质中官能团的名称___________ 。
(3)写出B转化为C的反应类型___________ 。
(4)A在一定条件下与水反应能得到物质B,则该化学反应的反应类型是___________ 。
(5)写出在浓硫酸作用下B与D反应的化学方程式___________ 。

已知烯烃A可以作为水果的催熟剂,其产量可以用来衡量一个国家石油化学工业的发展水平,D是食醋的成分之一、请回答下列问题:
(1)写出A物质的结构简式
(2)写出B物质中官能团的名称
(3)写出B转化为C的反应类型
(4)A在一定条件下与水反应能得到物质B,则该化学反应的反应类型是
(5)写出在浓硫酸作用下B与D反应的化学方程式
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐2】以玉米淀粉为原料可以制备乙醇、乙二醇等多种物质,转化路线如下(部分反应条件已略去)。F的产量可以用来衡量一个国家石油化工的发展水平。
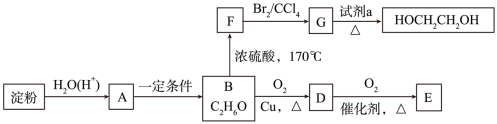
(1)A是不能再水解的糖,A的分子式是_______ 。
(2)B→F反应类型是_______ 。
(3)F→G的化学方程式是_______ 。
(4)试剂a是_______ 。
(5)检验D中的官能团可选用_______ 试剂(答出一种即可)
(6)F能与1,3-丁二烯以物质的量之比1∶1发生加成反应,生成六元环状化合物K,K的结构简式是_______ 。

(1)A是不能再水解的糖,A的分子式是
(2)B→F反应类型是
(3)F→G的化学方程式是
(4)试剂a是
(5)检验D中的官能团可选用
(6)F能与1,3-丁二烯以物质的量之比1∶1发生加成反应,生成六元环状化合物K,K的结构简式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】下图是先用浓硫酸与乙醇反应制取乙烯,再由乙烯与 反应制备1,2-二溴乙烷(熔点:9.5℃,沸点:131℃)的反应装置(加热和夹持装置略去)。回答下面问题。
反应制备1,2-二溴乙烷(熔点:9.5℃,沸点:131℃)的反应装置(加热和夹持装置略去)。回答下面问题。
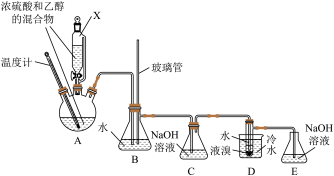
(1)混合浓硫酸和乙醇的方法是_______ ,
(2)为使液体顺利流下,仪器X使用前_______ (填“需”或“不需”)要先拔掉上口的玻璃塞。
(3)制得的乙烯气体中除含有挥发的乙醇杂质,还会混有_______ 杂质气体。
(4)装置B的作用是_______ 。
(5)装置C的作用是_______ ,若略去装置C,会使部分液溴损耗增多,可能的原因是_______ (用化学方程式表示)。
(6)装置D会生成1,2-二溴乙烷,写出对应的化学方程式_______ ,其反应类型是_______ 。
 反应制备1,2-二溴乙烷(熔点:9.5℃,沸点:131℃)的反应装置(加热和夹持装置略去)。回答下面问题。
反应制备1,2-二溴乙烷(熔点:9.5℃,沸点:131℃)的反应装置(加热和夹持装置略去)。回答下面问题。
(1)混合浓硫酸和乙醇的方法是
(2)为使液体顺利流下,仪器X使用前
(3)制得的乙烯气体中除含有挥发的乙醇杂质,还会混有
(4)装置B的作用是
(5)装置C的作用是
(6)装置D会生成1,2-二溴乙烷,写出对应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】在实验室制取乙烯时,其反应为CH3CH2OH CH2=CH2↑+H2O,该实验常因温度控制不当而发生副反应生成SO2、CO2、水蒸气等。实验室设计如图实验装置以验证上述反应生成的混合气体中含己烯、SO2和水蒸气。
CH2=CH2↑+H2O,该实验常因温度控制不当而发生副反应生成SO2、CO2、水蒸气等。实验室设计如图实验装置以验证上述反应生成的混合气体中含己烯、SO2和水蒸气。
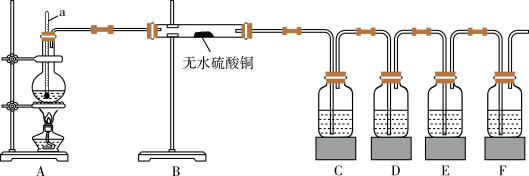
限用试剂(试剂均足量):乙醇、浓硫酸、品红溶液、氢氧化钠溶液、酸性高锰酸钾溶液、溴水。
(1)仪器a的名称为_________ 。
(2)请根据实验的要求完成下列填空:
①D中试剂的作用为_________ 。
②E中的试剂为_________ 。
③F中的试剂为_________ ,可能的实验现象为_________ 。
(3)简述装置B置于装置A、C之间的理由:_________ 。
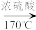 CH2=CH2↑+H2O,该实验常因温度控制不当而发生副反应生成SO2、CO2、水蒸气等。实验室设计如图实验装置以验证上述反应生成的混合气体中含己烯、SO2和水蒸气。
CH2=CH2↑+H2O,该实验常因温度控制不当而发生副反应生成SO2、CO2、水蒸气等。实验室设计如图实验装置以验证上述反应生成的混合气体中含己烯、SO2和水蒸气。
限用试剂(试剂均足量):乙醇、浓硫酸、品红溶液、氢氧化钠溶液、酸性高锰酸钾溶液、溴水。
(1)仪器a的名称为
(2)请根据实验的要求完成下列填空:
①D中试剂的作用为
②E中的试剂为
③F中的试剂为
(3)简述装置B置于装置A、C之间的理由:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】如图所示是实验室利用乙醇消去反应制取乙烯并检验产物的实验装置图。回答以下问题。___________ 。
(2)为避免发生副反应,烧瓶 中的温度需要迅速升至170C∘,副反应的化学方程式为
中的温度需要迅速升至170C∘,副反应的化学方程式为___________ 。
(3)反应中,观察到烧瓶 中混合液变为黑色,有气态副产物生成。
中混合液变为黑色,有气态副产物生成。
①装置 中所用试剂为滴加酚酞的
中所用试剂为滴加酚酞的 溶液,用于除去气体中的杂质,在虚线方框内将装置
溶液,用于除去气体中的杂质,在虚线方框内将装置 补充完整
补充完整___________ 。
②实验过程中,装置 中溶液颜色变浅,用化学方程式说明原因
中溶液颜色变浅,用化学方程式说明原因___________ 。
(4)装置C中所用试剂为溴水,用于检验乙烯的生成,实验中在该装置处观察到的实验现象为___________ ;反应一段时间后,装置C中溶液分层,有机物位于___________ (填“上”或“下”)层。
(5)有同学认为在装置C后应添加一个尾气处理装置,该装置中的试剂应选择___________ (填序号)。
 酸性
酸性 溶液
溶液  碱石灰
碱石灰  浓
浓

(2)为避免发生副反应,烧瓶
 中的温度需要迅速升至170C∘,副反应的化学方程式为
中的温度需要迅速升至170C∘,副反应的化学方程式为(3)反应中,观察到烧瓶
 中混合液变为黑色,有气态副产物生成。
中混合液变为黑色,有气态副产物生成。①装置
 中所用试剂为滴加酚酞的
中所用试剂为滴加酚酞的 溶液,用于除去气体中的杂质,在虚线方框内将装置
溶液,用于除去气体中的杂质,在虚线方框内将装置 补充完整
补充完整②实验过程中,装置
 中溶液颜色变浅,用化学方程式说明原因
中溶液颜色变浅,用化学方程式说明原因(4)装置C中所用试剂为溴水,用于检验乙烯的生成,实验中在该装置处观察到的实验现象为
(5)有同学认为在装置C后应添加一个尾气处理装置,该装置中的试剂应选择
 酸性
酸性 溶液
溶液  碱石灰
碱石灰  浓
浓
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】抗爆剂的添加剂常用1,2-二溴乙烷。如图为实验室制备1,2-二溴乙烷的装置图, 图中分液漏斗和烧瓶a中分别装有浓H2SO4和无水乙醇,d装置试管中装有液溴。
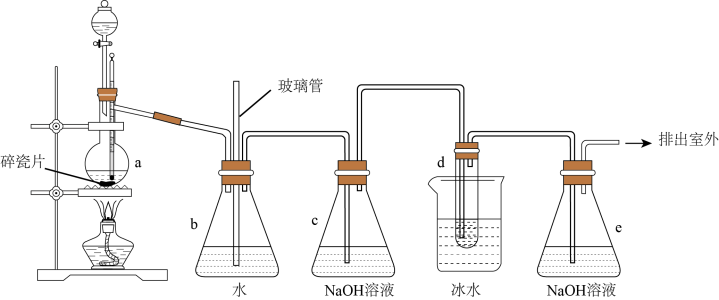
相关数据列表如下:
(1)安全瓶b在实验中有多重作用。其一可以检查实验进行中d装置中导管是否发生堵塞,请写出发生堵塞时瓶b中的现象:①_____________________________ ;如果实验时d装置中导管堵塞,你认为可能的原因是②___________________________________ ;安全瓶b还可以起到的作用是③_______________________________________ 。
(2)容器c、e中都盛有NaOH溶液,c中NaOH溶液的作用是_______________________ 。
(3)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正确情况下超过许多,如果装置的气密性没有问题,试分析可能的原因:________________________ 、_____________________________ (写出两条即可)。
(4)除去产物中少量未反应的Br2后,还含有的主要杂质为________________ ,要进一步提纯,下列操作中必需的是________________ (填字母)。
A.重结晶 B.过滤 C.萃取 D.蒸馏
(5)实验中也可以撤去d装置中盛冰水的烧杯,改为将冷水直接加入到d装置的试管中,则此时冷水除了能起到冷却1,2-二溴乙烷的作用外,还可以起到的作用是________________ 。

相关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | 溴 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 | 红棕色液体 |
| 密度/g·cm-3 | 0.79 | 2.18 | 0.71 | 3.10 |
| 沸点/℃ | 78.5 | 131.4 | 34.6 | 58.8 |
| 熔点/℃ | -114.3 | 9.79 | - 116.2 | -7.2 |
| 水溶性 | 混溶 | 难溶 | 微溶 | 可溶 |
(2)容器c、e中都盛有NaOH溶液,c中NaOH溶液的作用是
(3)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正确情况下超过许多,如果装置的气密性没有问题,试分析可能的原因:
(4)除去产物中少量未反应的Br2后,还含有的主要杂质为
A.重结晶 B.过滤 C.萃取 D.蒸馏
(5)实验中也可以撤去d装置中盛冰水的烧杯,改为将冷水直接加入到d装置的试管中,则此时冷水除了能起到冷却1,2-二溴乙烷的作用外,还可以起到的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】含氯消毒剂是指溶于水产生具有杀微生物活性的次氯酸的消毒剂,其杀微生物有效成分常以有效氯表示。这类消毒剂包括无机氯化合物(如次氯酸钠、次氯酸钙、氯化磷酸三钠)、有机氯化合物(如二氯异氰尿酸钠、三氯异氰尿酸、氯铵T等)。游泳池中的水通常为蓝色,是因为消毒和保证水质,加入了适量的胆矾和氯系消毒剂。然而,2016年里约奥运会跳水池中的水却由蓝色变成绿色,事后调查发现,是误加入的双氧水使前一天泳池中的含氯消毒剂失效,助长了藻类的滋生。
(1)写出加入双氧水后,发生反应的离子方程式为________ 。
(2)漂白粉的有效成分是___________ (填写化学式),该物质是由_________ 构成的(填“原子”、“分子”或“离子”),其生效原理的离子方程式为___________ 。
(3)在锥形瓶中盛有一定量研磨好的次氯酸钙固体(如下图):

用针筒向锥形瓶中注射一定浓度的盐酸2~3mL。选取以下药品:①刚开封的次氯酸钙固体,②在空气中久置的次氯酸钙固体,③2 mol/L盐酸,④0.2 mol/L盐酸,进行三次实验,观察到的现象如下:第一次:锥形瓶内产生黄绿色气体,有色纸片褪色;第二次:锥形瓶内无气泡产生,有色纸片褪色;第三次:锥形瓶内产生大量气泡,并有黄绿色气体,有色纸片褪色。
①分析三次实验现象,推测第一次选择的药品是_____ (填编号)。
②第三次实验过程中产生大量气泡,其中除了Cl2、水蒸气外,还有_______ 气体。
③第二次实验过程中发生反应的化学方程式为___________ , 解释产生与第一次的现象不同的原因:___________ 。
(1)写出加入双氧水后,发生反应的离子方程式为
(2)漂白粉的有效成分是
(3)在锥形瓶中盛有一定量研磨好的次氯酸钙固体(如下图):

用针筒向锥形瓶中注射一定浓度的盐酸2~3mL。选取以下药品:①刚开封的次氯酸钙固体,②在空气中久置的次氯酸钙固体,③2 mol/L盐酸,④0.2 mol/L盐酸,进行三次实验,观察到的现象如下:第一次:锥形瓶内产生黄绿色气体,有色纸片褪色;第二次:锥形瓶内无气泡产生,有色纸片褪色;第三次:锥形瓶内产生大量气泡,并有黄绿色气体,有色纸片褪色。
①分析三次实验现象,推测第一次选择的药品是
②第三次实验过程中产生大量气泡,其中除了Cl2、水蒸气外,还有
③第二次实验过程中发生反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】二氧化氯( )是一种高效消毒灭菌剂,可以有效杀灭新冠病毒。目前制备
)是一种高效消毒灭菌剂,可以有效杀灭新冠病毒。目前制备 常用氯酸钠还原法,其中一种方法是
常用氯酸钠还原法,其中一种方法是 与
与 在适当催化剂、温度为60
在适当催化剂、温度为60 时,发生反应得到,下图装置(夹持装置略)对其制备、吸收,释放进行了研究。已知:
时,发生反应得到,下图装置(夹持装置略)对其制备、吸收,释放进行了研究。已知:
① 的浓度较大时易分解爆炸,一般用
的浓度较大时易分解爆炸,一般用 或空气稀释到10%以下;实验室也常用稳定剂吸收,生成
或空气稀释到10%以下;实验室也常用稳定剂吸收,生成 ,使用时加酸释放出气体。
,使用时加酸释放出气体。
② 与KI在酸性溶液中反应的离子方程式为:
与KI在酸性溶液中反应的离子方程式为: 。
。
③

回答下列问题:
(1)仪器c的名称为___________ ,仪器b在装置中的作用是___________ 。
(2)根据反应条件判断制备装置甲中需改进的一项措施是___________ 。
(3)已知反应中甲醇被氧化为甲酸,写出制备 的化学反应方程式:
的化学反应方程式:___________ 。
(4)该制备法可选用不同的还原性物质作为还原剂,例如草酸(草酸的氧化产物为 ),相比甲醇法,草酸法的优点是
),相比甲醇法,草酸法的优点是___________ 。
(5)下列有关说法正确的是___________ 。
A.仪器a中NaOH溶液主要用于停止反应,并吸收多余的
B.装置e主要用于检验是否有 生成
生成
C.在 释放实验中,发生反应的离子方程式是:
释放实验中,发生反应的离子方程式是:
D. 和
和 都为强氧化剂,在相同条件下,等物质的量时,
都为强氧化剂,在相同条件下,等物质的量时, 的氧化能力是
的氧化能力是 的2.5倍
的2.5倍
(6) 常用于自来水的杀菌消毒。自来水厂用碘量法检测水中
常用于自来水的杀菌消毒。自来水厂用碘量法检测水中 的浓度,其实验操作如下:
的浓度,其实验操作如下:
Ⅰ.取100.0mL的水样,加入足量的碘化钾和少量稀硫酸
Ⅱ.待充分反应后,再加氢氧化钠溶液调至中性,并加入淀粉溶液
Ⅲ.用0.2000
 标准溶液进行滴定(已知
标准溶液进行滴定(已知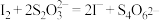 ),达到滴定终点时用去10.00mL
),达到滴定终点时用去10.00mL  标准溶液。滴定终点时溶液颜色的变化为
标准溶液。滴定终点时溶液颜色的变化为___________ ,该水样中 的含量为
的含量为___________  。
。
 )是一种高效消毒灭菌剂,可以有效杀灭新冠病毒。目前制备
)是一种高效消毒灭菌剂,可以有效杀灭新冠病毒。目前制备 常用氯酸钠还原法,其中一种方法是
常用氯酸钠还原法,其中一种方法是 与
与 在适当催化剂、温度为60
在适当催化剂、温度为60 时,发生反应得到,下图装置(夹持装置略)对其制备、吸收,释放进行了研究。已知:
时,发生反应得到,下图装置(夹持装置略)对其制备、吸收,释放进行了研究。已知:①
 的浓度较大时易分解爆炸,一般用
的浓度较大时易分解爆炸,一般用 或空气稀释到10%以下;实验室也常用稳定剂吸收,生成
或空气稀释到10%以下;实验室也常用稳定剂吸收,生成 ,使用时加酸释放出气体。
,使用时加酸释放出气体。②
 与KI在酸性溶液中反应的离子方程式为:
与KI在酸性溶液中反应的离子方程式为: 。
。③
| 物质 |  | HCOOH |  |
| 沸点 | 64.7 | 100.8 | 11 |

回答下列问题:
(1)仪器c的名称为
(2)根据反应条件判断制备装置甲中需改进的一项措施是
(3)已知反应中甲醇被氧化为甲酸,写出制备
 的化学反应方程式:
的化学反应方程式:(4)该制备法可选用不同的还原性物质作为还原剂,例如草酸(草酸的氧化产物为
 ),相比甲醇法,草酸法的优点是
),相比甲醇法,草酸法的优点是(5)下列有关说法正确的是
A.仪器a中NaOH溶液主要用于停止反应,并吸收多余的

B.装置e主要用于检验是否有
 生成
生成C.在
 释放实验中,发生反应的离子方程式是:
释放实验中,发生反应的离子方程式是:
D.
 和
和 都为强氧化剂,在相同条件下,等物质的量时,
都为强氧化剂,在相同条件下,等物质的量时, 的氧化能力是
的氧化能力是 的2.5倍
的2.5倍(6)
 常用于自来水的杀菌消毒。自来水厂用碘量法检测水中
常用于自来水的杀菌消毒。自来水厂用碘量法检测水中 的浓度,其实验操作如下:
的浓度,其实验操作如下:Ⅰ.取100.0mL的水样,加入足量的碘化钾和少量稀硫酸
Ⅱ.待充分反应后,再加氢氧化钠溶液调至中性,并加入淀粉溶液
Ⅲ.用0.2000

 标准溶液进行滴定(已知
标准溶液进行滴定(已知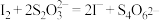 ),达到滴定终点时用去10.00mL
),达到滴定终点时用去10.00mL  标准溶液。滴定终点时溶液颜色的变化为
标准溶液。滴定终点时溶液颜色的变化为 的含量为
的含量为 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】叠氮化钾(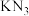 )能促使作物或难于萌发的种子发育。设计如下实验制备叠氮化钾并测定其纯度:
)能促使作物或难于萌发的种子发育。设计如下实验制备叠氮化钾并测定其纯度:
I.制备
步骤1:制备亚硝酸丁酯(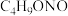 )
)

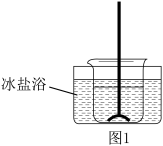
反应装置如图1(夹持装置略去),向烧杯中依次加入稀硫酸、丁醇、亚硝酸钠溶液,待反应完全后,分离出上层油状物,用 和
和 的混合溶液洗涤三次,经干燥后备用。
的混合溶液洗涤三次,经干燥后备用。
步骤2:制备叠氮化钾
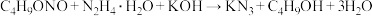
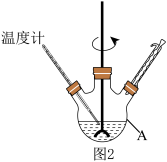
反应装置如图2(夹持及加热装置路去),向仪器A中加入 乙醇溶液、
乙醇溶液、 的联氨(
的联氨( )、亚硝酸丁酯,蒸汽浴加热,反应完全后,叠氮化钾即沉淀出来,冰浴冷却,过滤,先用无水乙醇洗涤,再用无水乙醚洗涤,在空气中于
)、亚硝酸丁酯,蒸汽浴加热,反应完全后,叠氮化钾即沉淀出来,冰浴冷却,过滤,先用无水乙醇洗涤,再用无水乙醚洗涤,在空气中于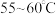 干燥。
干燥。
相关物质性质如下:
请回答:
(1)仪器A的名称为_____________ .
(2)步骤1中分离出亚硝酸丁酯的操作名称为_____________ ;步骤1中用NaCl和NaHCO3的混合溶液洗涤的目的是__________________________ .
(3)步骤2中冰浴冷却的目的是__________________________ ;步骤2中干燥产品的温度控制在55~60℃,原因是__________________________
(4)如需提高产品的纯度,可在_____________ (填编号)中进行重结晶。
A.无水乙醇 B.无水乙醚 C.水 D.乙醇的水溶液
Ⅱ.分光光度法测定产品的纯度
原理: 与
与 反应非常灵敏,生成红色络合物,在一定波长下测量红色溶液的吸光度,利用“
反应非常灵敏,生成红色络合物,在一定波长下测量红色溶液的吸光度,利用“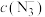 吸光度”曲线确定样品溶液中的
吸光度”曲线确定样品溶液中的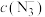 。测定步骤如下:
。测定步骤如下:
①用 晶体配制
晶体配制 标准溶液;
标准溶液;
②配制一组相同体积(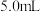 )不同浓度的
)不同浓度的 标准溶液,分别加入
标准溶液,分别加入 (足量)
(足量) 标准溶液,摇匀,测量吸光度,绘制标准溶液的
标准溶液,摇匀,测量吸光度,绘制标准溶液的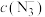 与吸光度的关系曲线,如图;
与吸光度的关系曲线,如图;
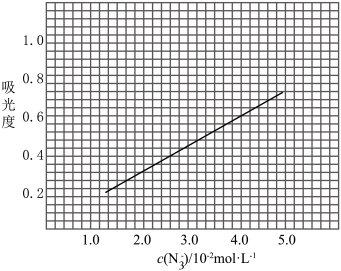
③产品测定:称取0.360g产品,配成 溶液,取出
溶液,取出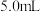 于标准管中,加入
于标准管中,加入 (足量)
(足量) 标准溶液,摇匀,测得吸光度为0.6。
标准溶液,摇匀,测得吸光度为0.6。
(5)实验室用 晶体配制
晶体配制 标准溶液的方法为
标准溶液的方法为_________________ .
(6)产品的纯度为_________________ ;若③中加入的 标准溶液不足以将产品完全反应,则测得的产品纯度
标准溶液不足以将产品完全反应,则测得的产品纯度________________ (填“偏高”“偏低”或“无影响”)。
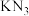 )能促使作物或难于萌发的种子发育。设计如下实验制备叠氮化钾并测定其纯度:
)能促使作物或难于萌发的种子发育。设计如下实验制备叠氮化钾并测定其纯度:I.制备
步骤1:制备亚硝酸丁酯(
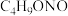 )
)
反应装置如图1(夹持装置略去),向烧杯中依次加入稀硫酸、丁醇、亚硝酸钠溶液,待反应完全后,分离出上层油状物,用
 和
和 的混合溶液洗涤三次,经干燥后备用。
的混合溶液洗涤三次,经干燥后备用。步骤2:制备叠氮化钾
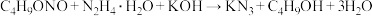
反应装置如图2(夹持及加热装置路去),向仪器A中加入
 乙醇溶液、
乙醇溶液、 的联氨(
的联氨( )、亚硝酸丁酯,蒸汽浴加热,反应完全后,叠氮化钾即沉淀出来,冰浴冷却,过滤,先用无水乙醇洗涤,再用无水乙醚洗涤,在空气中于
)、亚硝酸丁酯,蒸汽浴加热,反应完全后,叠氮化钾即沉淀出来,冰浴冷却,过滤,先用无水乙醇洗涤,再用无水乙醚洗涤,在空气中于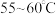 干燥。
干燥。

相关物质性质如下:
| 物质 | 颜色、状态 | 沸点(℃) | 溶解性 |
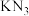 | 无色晶体 | 受热易分解 | 易溶于水,微溶于乙醇,不溶于乙醚 |
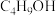 | 无色液体 | 118 | 微溶于水,与乙醇、乙醚混溶 |
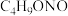 | 无色或淡黄色油状液体 | 78 | 不溶于水,与乙醇、乙醚混溶 |
 | 无色油状液体 | 118 | 与水、乙醇混溶,不溶于乙醚 |
请回答:
(1)仪器A的名称为
(2)步骤1中分离出亚硝酸丁酯的操作名称为
(3)步骤2中冰浴冷却的目的是
(4)如需提高产品的纯度,可在
A.无水乙醇 B.无水乙醚 C.水 D.乙醇的水溶液
Ⅱ.分光光度法测定产品的纯度
原理:
 与
与 反应非常灵敏,生成红色络合物,在一定波长下测量红色溶液的吸光度,利用“
反应非常灵敏,生成红色络合物,在一定波长下测量红色溶液的吸光度,利用“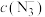 吸光度”曲线确定样品溶液中的
吸光度”曲线确定样品溶液中的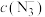 。测定步骤如下:
。测定步骤如下:①用
 晶体配制
晶体配制 标准溶液;
标准溶液;②配制一组相同体积(
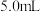 )不同浓度的
)不同浓度的 标准溶液,分别加入
标准溶液,分别加入 (足量)
(足量) 标准溶液,摇匀,测量吸光度,绘制标准溶液的
标准溶液,摇匀,测量吸光度,绘制标准溶液的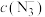 与吸光度的关系曲线,如图;
与吸光度的关系曲线,如图;
③产品测定:称取0.360g产品,配成
 溶液,取出
溶液,取出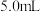 于标准管中,加入
于标准管中,加入 (足量)
(足量) 标准溶液,摇匀,测得吸光度为0.6。
标准溶液,摇匀,测得吸光度为0.6。(5)实验室用
 晶体配制
晶体配制 标准溶液的方法为
标准溶液的方法为(6)产品的纯度为
 标准溶液不足以将产品完全反应,则测得的产品纯度
标准溶液不足以将产品完全反应,则测得的产品纯度
您最近一年使用:0次



