请参考题中图表,根据要求回答问题:
(1)图I是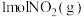 和
和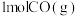 反应生成
反应生成 和
和 过程中的能量变化示意图,已知
过程中的能量变化示意图,已知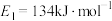 、
、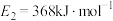 ,若在反应体系中加入催化剂,反应速率增大,
,若在反应体系中加入催化剂,反应速率增大, 的变化是
的变化是___________ (填“增大”、“减小”或“不变”,下同), 的变化是
的变化是___________ 。请写出 和
和 反应的热化学方程式:
反应的热化学方程式:___________ 。
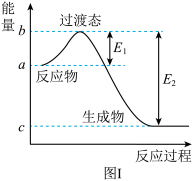
(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应的热化学方程式如下:
①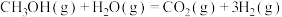
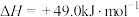
②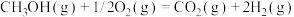
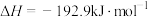
又知③
 ,则甲醇蒸汽燃烧为液态水的热化学方程式为
,则甲醇蒸汽燃烧为液态水的热化学方程式为___________ 。
(3)如表所示是部分化学键的键能参数:
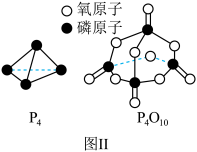
已知白磷的燃烧热为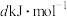 ,白磷及其完全燃烧的产物的结构如图II所示,
,白磷及其完全燃烧的产物的结构如图II所示,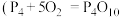 )则表中x=
)则表中x=___________  (用含a、b、c、d的代数式表示)。
(用含a、b、c、d的代数式表示)。
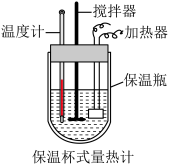
(4)某实验小组通过如图所示的量热计中,向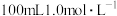 稀盐酸加
稀盐酸加 稀
稀 溶液(碱稍过量),测得中和热
溶液(碱稍过量),测得中和热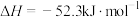 ,理论值为
,理论值为 ,造成这一结果的原因可能是
,造成这一结果的原因可能是___________ 。
a.用量筒量取盐酸时仰视读数
b.分多次将 溶液倒入量热计中
溶液倒入量热计中
c.温度计测量完盐酸的温度再次测量 溶液温度时,残留的酸液末用水冲洗干净
溶液温度时,残留的酸液末用水冲洗干净
d.错把同浓度的醋酸当成盐酸溶液与 溶液反应
溶液反应
(1)图I是
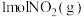 和
和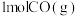 反应生成
反应生成 和
和 过程中的能量变化示意图,已知
过程中的能量变化示意图,已知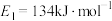 、
、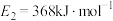 ,若在反应体系中加入催化剂,反应速率增大,
,若在反应体系中加入催化剂,反应速率增大, 的变化是
的变化是 的变化是
的变化是 和
和 反应的热化学方程式:
反应的热化学方程式:
(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应的热化学方程式如下:
①
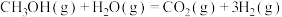
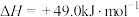
②
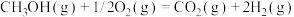
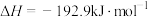
又知③

 ,则甲醇蒸汽燃烧为液态水的热化学方程式为
,则甲醇蒸汽燃烧为液态水的热化学方程式为(3)如表所示是部分化学键的键能参数:
| 化学键 |  |  |  | 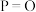 |
键能 |  |  |  |  |
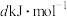 ,白磷及其完全燃烧的产物的结构如图II所示,
,白磷及其完全燃烧的产物的结构如图II所示,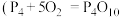 )则表中x=
)则表中x= (用含a、b、c、d的代数式表示)。
(用含a、b、c、d的代数式表示)。
(4)某实验小组通过如图所示的量热计中,向
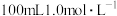 稀盐酸加
稀盐酸加 稀
稀 溶液(碱稍过量),测得中和热
溶液(碱稍过量),测得中和热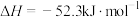 ,理论值为
,理论值为 ,造成这一结果的原因可能是
,造成这一结果的原因可能是
a.用量筒量取盐酸时仰视读数
b.分多次将
 溶液倒入量热计中
溶液倒入量热计中c.温度计测量完盐酸的温度再次测量
 溶液温度时,残留的酸液末用水冲洗干净
溶液温度时,残留的酸液末用水冲洗干净d.错把同浓度的醋酸当成盐酸溶液与
 溶液反应
溶液反应
更新时间:2023-07-30 21:03:06
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】50mL0.55mol·L-1盐酸与50mL0.50mol·L-1NaOH溶液在如下图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:
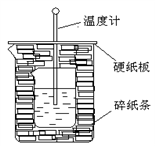
(1)从实验装置上看,尚缺少一种玻璃仪器,这玻璃仪器名称是_________ 。
(2)烧杯间填满碎纸条的作用是__________________ 。
(3)若大烧杯上不盖硬纸板,求得的反应热数值___________ (填“偏大”“偏小”或“无影响”)。
(4)实验中该用60mL0.50mol·L-1盐酸跟50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量_______ (填“相等”或“不相等”),所求中和热 ________ (填“相等”或“不相等”)。
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会_______ (填“偏大”、“偏小”或“无影响”)。
(6)若三次平行操作测得数据中起始时盐酸与烧碱溶液平均温度相同,而终止温度与起始温度差t2-t1分别为2.2℃ 3.5℃ 3.3℃,则最终代入计算式的温差均值为______ 。已知溶液的比热容4.18J /(g.℃),计算中和热ΔH=_____________ 。

(1)从实验装置上看,尚缺少一种玻璃仪器,这玻璃仪器名称是
(2)烧杯间填满碎纸条的作用是
(3)若大烧杯上不盖硬纸板,求得的反应热数值
(4)实验中该用60mL0.50mol·L-1盐酸跟50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会
(6)若三次平行操作测得数据中起始时盐酸与烧碱溶液平均温度相同,而终止温度与起始温度差t2-t1分别为2.2℃ 3.5℃ 3.3℃,则最终代入计算式的温差均值为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】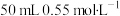 盐酸与
盐酸与 溶液在如图所示装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和反应反应热。回答下列问题:
溶液在如图所示装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和反应反应热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃仪器是_______ 。
(2)大烧杯上若不盖硬纸板,则求得的中和反应反应热( )
)_______ (填“偏大”、“偏小”或“无影响”),在操作正确的前提下,提高中和反应反应热( )的测定准确性的关键是
)的测定准确性的关键是_______ 。
(3)计算中和反应反应热时,至少需要的数据是_______ (填标号)。
a.盐酸的浓度b.NaOH溶液的浓度c.比热容d.反应后溶液的质量
e.生成水的物质的量f.反应前后溶液温度的变化g.操作所需的时间
(4)实验中改用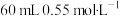 盐酸与
盐酸与 溶液进行反应,与上述实验相比,所放出的热量
溶液进行反应,与上述实验相比,所放出的热量_______ (填“相等”或“不相等”,下同),所求的生成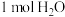 时中和反应反应热(
时中和反应反应热( )
)_______ ,简述理由:_______ 。
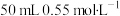 盐酸与
盐酸与 溶液在如图所示装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和反应反应热。回答下列问题:
溶液在如图所示装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和反应反应热。回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是
(2)大烧杯上若不盖硬纸板,则求得的中和反应反应热(
 )
) )的测定准确性的关键是
)的测定准确性的关键是(3)计算中和反应反应热时,至少需要的数据是
a.盐酸的浓度b.NaOH溶液的浓度c.比热容d.反应后溶液的质量
e.生成水的物质的量f.反应前后溶液温度的变化g.操作所需的时间
(4)实验中改用
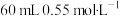 盐酸与
盐酸与 溶液进行反应,与上述实验相比,所放出的热量
溶液进行反应,与上述实验相比,所放出的热量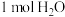 时中和反应反应热(
时中和反应反应热( )
)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
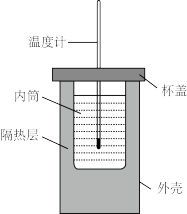
【推荐3】某实验小组用100mL0.50mol·L-1NaOH溶液与60mL0.50mol·L-1硫酸溶液进行中和热的测定,装置如图所示。回答下列问题:
(1)若实验共需要400mLNaOH溶液,实验室在配制该溶液时,则需要称量NaOH固体____ g。
(2)图中装置缺少的仪器是_____ 。
(3)硫酸稍过量的原因是_____ 。
(4)请填写表中的平均温度差:
(5)近似认为0.50mol·L-1NaOH溶液与0.50mol·L-1硫酸溶液的密度都是1g·cm-3,中和后生成溶液的比热容c=4.18J·g-1·℃-1,则上述实验测得的中和热ΔH(焓变)=____ (结果保留至小数点后一位)。
(6)上述实验测得中和热的数值小于57.3kJ·mol-1,产生偏差的原因可能是____ (填字母)。
(7)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1L1mol·L-1的稀盐酸恰好完全反应,其反应热分别为∆H1、∆H2、∆H3,则∆H1、∆H2、∆H3的大小关系为_____ 。

(1)若实验共需要400mLNaOH溶液,实验室在配制该溶液时,则需要称量NaOH固体
(2)图中装置缺少的仪器是
(3)硫酸稍过量的原因是
(4)请填写表中的平均温度差:
| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | 平均温度差(t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 31.2 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
(5)近似认为0.50mol·L-1NaOH溶液与0.50mol·L-1硫酸溶液的密度都是1g·cm-3,中和后生成溶液的比热容c=4.18J·g-1·℃-1,则上述实验测得的中和热ΔH(焓变)=
(6)上述实验测得中和热的数值小于57.3kJ·mol-1,产生偏差的原因可能是
| A.量取NaOH溶液时仰视读数 |
| B.为了使反应充分,向酸溶液中分次加入碱溶液 |
| C.实验装置保温隔热效果差 |
| D.用铜丝代替玻璃搅拌器搅拌 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】C、N、S的氧化物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的影响。
已知:2C(s)+O2(g)=2CO(g) ΔH1=-221 kJ·molˉ1
4Al(g)+3O2(g) =2Al2O3(s) ΔH2=-3351 kJ·molˉ1
2Al(g)+N2(g)=2AlN(s) ΔH3=-318 kJ·molˉ1
碳热还原Al2O3合成 AlN 的总热化学方程式是___________________ ;
已知:2C(s)+O2(g)=2CO(g) ΔH1=-221 kJ·molˉ1
4Al(g)+3O2(g) =2Al2O3(s) ΔH2=-3351 kJ·molˉ1
2Al(g)+N2(g)=2AlN(s) ΔH3=-318 kJ·molˉ1
碳热还原Al2O3合成 AlN 的总热化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烧, 电解质是熔融碳酸盐,电池总反应方程式为:C3H8+5O2 = 3CO2+4H2O。
(1)已知:2C3H8(g) + 7O2(g) = 6CO(g) + 8H2O(l) △H1
C(s) + O2(g) = CO2(g) △H2
2C(s) + O2(g) = 2CO(g) △H3
则 C3H8(g)+5O2((g) = 3CO2(g) + 4H2O(l) △H=________ (用△H1、△H2、△H3表示)
(2)写出该电池正极的电极反应式:_________ ,电池工作时CO32-移向_________ (填“正极”或“负极”);用该电池电解1000 mL lmol/L的AgNO3溶液(惰性电极),此电解池的反应方程式为_____________________________________ 。
(1)已知:2C3H8(g) + 7O2(g) = 6CO(g) + 8H2O(l) △H1
C(s) + O2(g) = CO2(g) △H2
2C(s) + O2(g) = 2CO(g) △H3
则 C3H8(g)+5O2((g) = 3CO2(g) + 4H2O(l) △H=
(2)写出该电池正极的电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】化学反应的焓变通常用实验进行测定,也可理论推算,回答下列问题。
(1)实验测得,1 g CH3OH(l)在氧气中充分燃烧生成二氧化碳和液态水释放出22.7kJ的热量,试写出甲醇燃烧的热化学方程式_______________________________________ 。
(2)已知某工业生产中甲烷与水蒸气存在如下反应:
i.CH4(g)+H2O(g)=CO(g)+3H2(g) △H1
ii.CO(g)+H2O(g)=CO2(g)+H2(g) △H2
iii.CH4(g)=C(s)+2H2(g) △H3
……
Iii为积炭反应,利用△H1和△H2计算△H3时,还需要利用_____________ 反应的△H。(写化学方程式)
(3)氯化氢转化为氯气的催化过程如下:
CuCl2(s)=CuCl(s)+ Cl2(g) △H1=+83 kJ·mol-1
Cl2(g) △H1=+83 kJ·mol-1
CuCl(s)+ O2(g)=CuO(s)+
O2(g)=CuO(s)+ Cl2(g) △H2=-20 kJ·mol-1
Cl2(g) △H2=-20 kJ·mol-1
CuO(s)+2HCl(g)= CuCl2(s)+H2O(g) △H3=-121 kJ·mol-1
则4HCl(g)+ O2(g)= 2Cl2(g)+2H2O(g)的△H=___________ kJ·mol-1
(1)实验测得,1 g CH3OH(l)在氧气中充分燃烧生成二氧化碳和液态水释放出22.7kJ的热量,试写出甲醇燃烧的热化学方程式
(2)已知某工业生产中甲烷与水蒸气存在如下反应:
i.CH4(g)+H2O(g)=CO(g)+3H2(g) △H1
ii.CO(g)+H2O(g)=CO2(g)+H2(g) △H2
iii.CH4(g)=C(s)+2H2(g) △H3
……
Iii为积炭反应,利用△H1和△H2计算△H3时,还需要利用
(3)氯化氢转化为氯气的催化过程如下:
CuCl2(s)=CuCl(s)+
 Cl2(g) △H1=+83 kJ·mol-1
Cl2(g) △H1=+83 kJ·mol-1 CuCl(s)+
 O2(g)=CuO(s)+
O2(g)=CuO(s)+ Cl2(g) △H2=-20 kJ·mol-1
Cl2(g) △H2=-20 kJ·mol-1CuO(s)+2HCl(g)= CuCl2(s)+H2O(g) △H3=-121 kJ·mol-1
则4HCl(g)+ O2(g)= 2Cl2(g)+2H2O(g)的△H=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氨气是生产化肥、硝酸等的重要原料,围绕合成氨人们进行了一系列的研究
(1)氢气既能与氮气又能与氧气发生反应,但是反应的条件却不相同。
已知:2H2(g)+O2(g)=2H2O(g) ∆H=-483.6 kJ/mol
N2(g)+3H2(g)⇌2NH3(g) ∆H=-92.4 kJ/mol
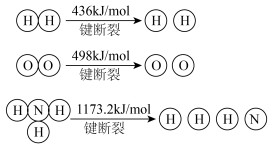
计算断裂1molN≡N键需要能量___________ kJ,氮气分子中化学键比氧气分子中的化学键键___________ (填“强”或“弱”),因此氢气与二者反应的条件不同。
(2)在恒温恒容密闭容器中按照甲、乙、丙三种方式分别投料,发生反应:
N2(g)+3H2(g)⇌2NH3(g) 测得甲容器中H2的转化率为40%。
①判断乙容器中反应进行的方向___________ 。(填“正向”或“逆向”)
②达平衡时,甲、乙、丙三容器中NH3的体积分数大小顺序为___________ 。
(1)氢气既能与氮气又能与氧气发生反应,但是反应的条件却不相同。
已知:2H2(g)+O2(g)=2H2O(g) ∆H=-483.6 kJ/mol
N2(g)+3H2(g)⇌2NH3(g) ∆H=-92.4 kJ/mol

计算断裂1molN≡N键需要能量
(2)在恒温恒容密闭容器中按照甲、乙、丙三种方式分别投料,发生反应:
N2(g)+3H2(g)⇌2NH3(g) 测得甲容器中H2的转化率为40%。
| N2(mol) | H2(mol) | NH3(mol) | |
| 甲 | 1 | 3 | 0 |
| 乙 | 0.5 | 1.5 | 1 |
| 丙 | 0 | 0 | 4 |
②达平衡时,甲、乙、丙三容器中NH3的体积分数大小顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】任何化学反应都伴随着能量的变化,化学能可转化为热能、电能等。回答下列有关问题:
(1) 的反应过程如图所示:
的反应过程如图所示:______ (填“放热”或“吸热”)反应,生成 吸收或放出的热量为
吸收或放出的热量为______ 。
(2)下列变化中属于吸热反应的是______ (填标号)。
①液态水汽化 ②生石灰与水反应生成熟石灰
③ ④
④ 与固体
与固体 混合
混合
(3)氢气燃料电池在北京冬奥会上得到广泛应用,下图是一种氢气燃料电池的工作原理示意图:______ ,发生了______ 反应(填“氧化”或“还原”):a电极是原电池的______ (填“正极”或“负极”),若该极改为通入 ,其电极反应式为
,其电极反应式为____________ 。
(4)为了验证Fe与Cu的还原性强弱,下图中能达到实验目的的装置是______ (填标号),其正极的电极反应式为______ ;若构建该原电池时两个电极的质量相等,当导线中通过0.2 mol电子时,理论上两个电极的质量差为______ g。
(1)
 的反应过程如图所示:
的反应过程如图所示:
 吸收或放出的热量为
吸收或放出的热量为(2)下列变化中属于吸热反应的是
①液态水汽化 ②生石灰与水反应生成熟石灰
③
 ④
④ 与固体
与固体 混合
混合(3)氢气燃料电池在北京冬奥会上得到广泛应用,下图是一种氢气燃料电池的工作原理示意图:
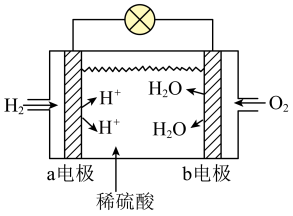
 ,其电极反应式为
,其电极反应式为(4)为了验证Fe与Cu的还原性强弱,下图中能达到实验目的的装置是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氨气是一种重要的物质,可用于制取化肥和硝酸等。已知H﹣H键、N﹣H键、N≡N键的键能分别是436 kJ·mol-1、391 kJ·mol-1、946 kJ·mol-1。
(1)写出合成氨的热反应方程式:____ 。生成1 mol NH3需要吸收或放出___ kJ。
(2)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图所示。图中t1时引起平衡移动的条件可能是______ 。其中表示平衡混合物中NH3的含量最高的一段时间是______ 。
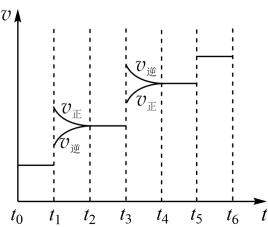
(1)写出合成氨的热反应方程式:
(2)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图所示。图中t1时引起平衡移动的条件可能是

您最近一年使用:0次



