现有下列物质:① 固体 ②
固体 ② 气体 ③
气体 ③ 固体 ④熔融
固体 ④熔融 ⑤铜 ⑥稀硫酸 ⑦
⑤铜 ⑥稀硫酸 ⑦ ⑧
⑧ ⑨氨水。
⑨氨水。
(1)上述物质中,属于电解质的是_______ (填序号)。
(2)写出②的水溶液和少量③反应的离子方程式_______ 。
(3)某同学用①配制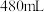
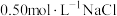 溶液。
溶液。
ⅰ.配制溶液时必需的仪器有:托盘天平、药匙、烧杯、玻璃棒、量筒、胶头滴管、_______ 以及等质量的几片滤纸。
ⅱ.下列操作会使所配溶液浓度偏低的是_______ (填字母)。
A.容量瓶洗涤干净后未干燥
B.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
C.定容时俯视刻度线
D.转移溶液后,未洗涤烧杯和玻璃棒
(4)在⑥中, 和
和 能发生氧化还原反应:
能发生氧化还原反应:
氧化反应:
还原反应:
写出该氧化还原反应的离子方程式_______ 。反应中若有
 参加反应,则转移电子的数目为
参加反应,则转移电子的数目为_______ 。
 固体 ②
固体 ② 气体 ③
气体 ③ 固体 ④熔融
固体 ④熔融 ⑤铜 ⑥稀硫酸 ⑦
⑤铜 ⑥稀硫酸 ⑦ ⑧
⑧ ⑨氨水。
⑨氨水。(1)上述物质中,属于电解质的是
(2)写出②的水溶液和少量③反应的离子方程式
(3)某同学用①配制
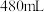
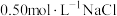 溶液。
溶液。ⅰ.配制溶液时必需的仪器有:托盘天平、药匙、烧杯、玻璃棒、量筒、胶头滴管、
ⅱ.下列操作会使所配溶液浓度偏低的是
A.容量瓶洗涤干净后未干燥
B.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
C.定容时俯视刻度线
D.转移溶液后,未洗涤烧杯和玻璃棒
(4)在⑥中,
 和
和 能发生氧化还原反应:
能发生氧化还原反应:氧化反应:

还原反应:

写出该氧化还原反应的离子方程式

 参加反应,则转移电子的数目为
参加反应,则转移电子的数目为
更新时间:2023-07-31 21:44:01
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】阅读资料回答下列问题:
Ⅰ.海洋的水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如 、
、 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和 用以生产
用以生产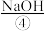 、
、 、
、 、
、 、
、 等,苦卤经过氯气氧化、热空气吹出、
等,苦卤经过氯气氧化、热空气吹出、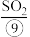 吸收等一系列操作可获得
吸收等一系列操作可获得 。电解熔融氯化钠可冶炼
。电解熔融氯化钠可冶炼 ,海底埋藏大量可燃冰资源,
,海底埋藏大量可燃冰资源, 是一种清洁能源。
是一种清洁能源。
(1)上述标有序号的物质中属于电解质的是_______ (填序号,下同);属于非电解质的是_______ 。
Ⅱ.钠的价类二维图如图所示:
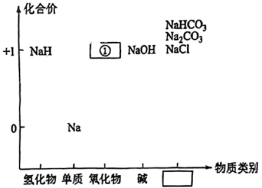
(2)钠是一种活泼性很强的金属,下列各项中属于保存金属钠的正确方法是_______。(填序号)
(3)若把金属钠放到硫酸铜溶液中,看不到红色固体生成,请写出发生反应的离子方程式:_______ 。
(4)二维图中缺失的①中有一种是具有强氧化性的固体物质,该固体中阳离子和阴离子的个数比为_______ 。写出其与水反应的化学方程式_______ 。
(5)氢化钠(NaH)能与水发生如下反应: ,该反应中氧化产物和还原产物的质量比为
,该反应中氧化产物和还原产物的质量比为_______ 。
Ⅰ.海洋的水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如
 、
、 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和 用以生产
用以生产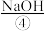 、
、 、
、 、
、 、
、 等,苦卤经过氯气氧化、热空气吹出、
等,苦卤经过氯气氧化、热空气吹出、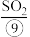 吸收等一系列操作可获得
吸收等一系列操作可获得 。电解熔融氯化钠可冶炼
。电解熔融氯化钠可冶炼 ,海底埋藏大量可燃冰资源,
,海底埋藏大量可燃冰资源, 是一种清洁能源。
是一种清洁能源。(1)上述标有序号的物质中属于电解质的是
Ⅱ.钠的价类二维图如图所示:

(2)钠是一种活泼性很强的金属,下列各项中属于保存金属钠的正确方法是_______。(填序号)
| A.放在细沙中 | B.放在水中 | C.放在煤油中 | D.放在细口瓶中 |
(4)二维图中缺失的①中有一种是具有强氧化性的固体物质,该固体中阳离子和阴离子的个数比为
(5)氢化钠(NaH)能与水发生如下反应:
 ,该反应中氧化产物和还原产物的质量比为
,该反应中氧化产物和还原产物的质量比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】现有下列10种物质:①铝,②纯醋酸,③CO2,④H2SO4,⑤Ba(OH)2,⑥红褐色的氢氧化铁胶体,⑦稀盐酸,⑧NaHSO4,⑨碳酸钙,⑩乙醇,请按要求书写离子方程式或化学方程式,
(1)上述物质中属于电解质的有_______ ,属于非电解质的有_______ ,既不属于电解质也不属于非电解质的有_______ (填序号)。
(2)写出⑧在水中的电离方程式为_______ 。
(3)向沸水中逐滴加入饱和FeCl3溶液,至液体呈透明的红褐色,写出化学方程式_______ 。
(4)已知酸性环境下,ClO-可将Mn2+氧化成MnO2,自身被还原成Cl-,该过程的离子反应方程式为_______ 。
(5)在酸性条件下,向含铬废水中加入FeSO4溶液,可将Cr2O 还原为Cr3+,该过程的离子方程式为
还原为Cr3+,该过程的离子方程式为_______ 。
(1)上述物质中属于电解质的有
(2)写出⑧在水中的电离方程式为
(3)向沸水中逐滴加入饱和FeCl3溶液,至液体呈透明的红褐色,写出化学方程式
(4)已知酸性环境下,ClO-可将Mn2+氧化成MnO2,自身被还原成Cl-,该过程的离子反应方程式为
(5)在酸性条件下,向含铬废水中加入FeSO4溶液,可将Cr2O
 还原为Cr3+,该过程的离子方程式为
还原为Cr3+,该过程的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】按要求书写下列反应的离子方程式:
(1)碳酸氢钠溶液和稀盐酸混合:________ 。
(2)少量二氧化碳通入澄清的石灰水:_________ 。
(3)氧化钠与稀盐酸反应:_________ 。
(4)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:________ 。
(1)碳酸氢钠溶液和稀盐酸混合:
(2)少量二氧化碳通入澄清的石灰水:
(3)氧化钠与稀盐酸反应:
(4)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】在工业上,次磷酸 常用于化学镀银,发生的反应如下:Ag++H3PO2+H2O→Ag↓+H3PO4+H+。请回答下列问题:
常用于化学镀银,发生的反应如下:Ag++H3PO2+H2O→Ag↓+H3PO4+H+。请回答下列问题:
(1)H3PO2中,P元素的化合价为_______ ;该反应中,H3PO2被_______ (填“氧化”或“还原”)。
(2)配平该离子方程式:_______ 。
(3)H3PO2是一元弱酸,写出其与足量NaOH溶液反应的化学方程式:_______ 。
(4)若该反应有0.1NA个电子转移,则镀件镀上银的质量为_______ g。
 常用于化学镀银,发生的反应如下:Ag++H3PO2+H2O→Ag↓+H3PO4+H+。请回答下列问题:
常用于化学镀银,发生的反应如下:Ag++H3PO2+H2O→Ag↓+H3PO4+H+。请回答下列问题:(1)H3PO2中,P元素的化合价为
(2)配平该离子方程式:
(3)H3PO2是一元弱酸,写出其与足量NaOH溶液反应的化学方程式:
(4)若该反应有0.1NA个电子转移,则镀件镀上银的质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】(1)写出下列反应的离子方程式:
①碳酸钙固体中加入盐酸____________ ;
②氢氧化钠溶液与硫酸铜溶液混合____________ ,
③氧化铁粉末中加入稀硫酸____________ ,
④氢氧化钡溶液与过量的硫酸氢钠溶液混合____________ 。
(2)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭按一定比例混合而成,爆炸时的反应为S+2KNO3+3C=K2S+N2↑+3CO2↑,反应中被还原的物质是________ .(填化学式)
(3)工业废水中的 有毒,常在酸性条件下用FeSO4·7H2O做处理剂,将
有毒,常在酸性条件下用FeSO4·7H2O做处理剂,将 转化为Cr3+反应的离子方程式为
转化为Cr3+反应的离子方程式为____________ 。
(4)NaH可在野外作生氢剂。反应原理为NaH+H2O=NaOH+H2↑,在该反应中,还原剂是_________ ,氧化产物和还原产物的质量比为________ 。
①碳酸钙固体中加入盐酸
②氢氧化钠溶液与硫酸铜溶液混合
③氧化铁粉末中加入稀硫酸
④氢氧化钡溶液与过量的硫酸氢钠溶液混合
(2)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭按一定比例混合而成,爆炸时的反应为S+2KNO3+3C=K2S+N2↑+3CO2↑,反应中被还原的物质是
(3)工业废水中的
 有毒,常在酸性条件下用FeSO4·7H2O做处理剂,将
有毒,常在酸性条件下用FeSO4·7H2O做处理剂,将 转化为Cr3+反应的离子方程式为
转化为Cr3+反应的离子方程式为(4)NaH可在野外作生氢剂。反应原理为NaH+H2O=NaOH+H2↑,在该反应中,还原剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】工厂烟气(主要污染物有SO2、NO)直接排放会造成空气污染,水溶性硝态氮(NO 、NO
、NO 等)是水体污染物,需要处理才能排放。
等)是水体污染物,需要处理才能排放。
(1)CO(NH2)2溶液脱硫的反应为:SO2+CO(NH2)2+2H2O=(NH4)2SO3+CO2(该反应为非氧化还原反应)。若吸收烟气时通入少量ClO2,可同时实现脱硫、脱硝。脱硝的反应分为两步。
第一步:5NO+2ClO2+H2O=5NO2+2HCl
第二步:NO2和CO(NH2)2反应生成N2、CO2和水。
请写出第二步反应的化学方程式为__ 。
(2)“纳米零价铁—H2O2”体系可将烟气中难溶的NO氧化为可溶的NO 。
。
在一定温度下,将H2O2溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
①NO与H2O2反应生成HNO3的化学方程式为__ 。
②Fe2+催化H2O2分解产生HO•,HO•将NO氧化为NO 的机理如图所示,Y的化学式为
的机理如图所示,Y的化学式为__ 。

③通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示。已知O2-可在固体电解质中自由移动。NiO电极上的电极反应式为__ 。

(3)纳米铁粉可用于去除废水中的硝态氮(以NO 表示)可大致分为2个过程,反应原理如图所示。
表示)可大致分为2个过程,反应原理如图所示。
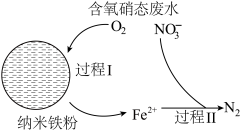
①有研究发现,在铁粉总量一定的条件下,水中的溶解氧过少或过多均不利于硝态氮去除。若水中的溶解氧过少,硝态氮去除率下降的原因是__ 。
②利用纳米铁粉与活性炭混合物可提升硝态废水中硝态氮的去除效率,可能原因是__ 。
 、NO
、NO 等)是水体污染物,需要处理才能排放。
等)是水体污染物,需要处理才能排放。(1)CO(NH2)2溶液脱硫的反应为:SO2+CO(NH2)2+2H2O=(NH4)2SO3+CO2(该反应为非氧化还原反应)。若吸收烟气时通入少量ClO2,可同时实现脱硫、脱硝。脱硝的反应分为两步。
第一步:5NO+2ClO2+H2O=5NO2+2HCl
第二步:NO2和CO(NH2)2反应生成N2、CO2和水。
请写出第二步反应的化学方程式为
(2)“纳米零价铁—H2O2”体系可将烟气中难溶的NO氧化为可溶的NO
 。
。在一定温度下,将H2O2溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
①NO与H2O2反应生成HNO3的化学方程式为
②Fe2+催化H2O2分解产生HO•,HO•将NO氧化为NO
 的机理如图所示,Y的化学式为
的机理如图所示,Y的化学式为
③通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示。已知O2-可在固体电解质中自由移动。NiO电极上的电极反应式为

(3)纳米铁粉可用于去除废水中的硝态氮(以NO
 表示)可大致分为2个过程,反应原理如图所示。
表示)可大致分为2个过程,反应原理如图所示。
①有研究发现,在铁粉总量一定的条件下,水中的溶解氧过少或过多均不利于硝态氮去除。若水中的溶解氧过少,硝态氮去除率下降的原因是
②利用纳米铁粉与活性炭混合物可提升硝态废水中硝态氮的去除效率,可能原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】反应2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O,Mn元素的化合价由________ 价变为__________ 价,被________ ;________ 元素的原子失去电子,被________ ;若参加反应的HCl是73 g,则被氧化的HCl是________ g.
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】(1)有标准状况下的四种气体:①6.72 L CH4,②3.01×1023个H2分子,③3.4 g H2S,④0.2 mol NH3,则其体积按从大到小的顺序为:_______ (填序号)。
(2)标准状况下,测得1.92克某气体的体积为672 mL,则此气体的相对分子质量为_______ 。
(3)实验室用Na2CO3•10H2O晶体配制0.5mol/L的Na2CO3溶液970mL,应称取Na2CO3•10H2O的质量是_______ 。
(4)某学生欲用12mol•L-1浓盐酸和蒸馏水配制500 mL 0.3 mol•L-1的稀盐酸。
①该学生需要量取_______ mL上述浓盐酸进行配制。
②下列实验操作会导致所配制的稀盐酸的物质的量浓度偏小的是_______ (填序号)。
a.用量筒量取浓盐酸时俯视观察凹液面
b.将量取浓盐酸的量筒进行洗涤,并将洗涤液转移到容量瓶中
c.稀释浓盐酸时,未冷却到室温即转移到容量瓶中
d.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
e.容量瓶洗涤干净后未干燥
(2)标准状况下,测得1.92克某气体的体积为672 mL,则此气体的相对分子质量为
(3)实验室用Na2CO3•10H2O晶体配制0.5mol/L的Na2CO3溶液970mL,应称取Na2CO3•10H2O的质量是
(4)某学生欲用12mol•L-1浓盐酸和蒸馏水配制500 mL 0.3 mol•L-1的稀盐酸。
①该学生需要量取
②下列实验操作会导致所配制的稀盐酸的物质的量浓度偏小的是
a.用量筒量取浓盐酸时俯视观察凹液面
b.将量取浓盐酸的量筒进行洗涤,并将洗涤液转移到容量瓶中
c.稀释浓盐酸时,未冷却到室温即转移到容量瓶中
d.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
e.容量瓶洗涤干净后未干燥
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】某实验小组用6%的氯化钠溶液(密度约为1.04g/cm3)配制50g质量分数为3%的氯化钠溶液,步骤如下:①计算;②量取;③混匀;④装瓶贴标签。回答下列问题:
(1)计算需要6%的氯化钠溶液的体积是_______ mL(结果取整数);
(2)实验中用到的仪器有25mL的量筒、细口瓶、烧杯、_______ ;
(3)下列实验操作会导致所配溶液中溶质的质量分数一定偏大的是_______。
(1)计算需要6%的氯化钠溶液的体积是
(2)实验中用到的仪器有25mL的量筒、细口瓶、烧杯、
(3)下列实验操作会导致所配溶液中溶质的质量分数一定偏大的是_______。
A.量取 的氯化钠溶液时仰视读数 的氯化钠溶液时仰视读数 |
| B.向烧杯内加入水时有液体溅出 |
| C.混匀过程中没有使用玻璃棒搅拌 |
| D.配制好的溶液装入未干燥的细口瓶 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】实验室用纯碱(Na2CO3)配制480mL 0.1mol/L Na2CO3溶液,操作步骤有:
(1)需称量纯碱的质量为_______ g。
(2)配制溶液时下列仪器中:A.锥形瓶 B.托盘天平 C.烧杯 D.胶头滴管 E.药匙。不需要用到的是_______ (填序号),尚缺的玻璃仪器有_______ (写名称)。
(3)人们常将配制过程简述为以下各步骤:A.冷却 B.称量 C.洗涤 D.定容 E.溶解 F.摇匀 G.转移 H.装瓶。其正确的操作顺序应是_______ (填序号)。
①BEAGCGDFH ②BEGACGFDH ③BEFGCGDHA ④BEAGCGDHF
(4)在此配制过程中,下列情况会使配制结果偏低的是_______ (填序号)。
①纯碱晶体有结晶水
②容量瓶使用时未干燥
③移液时未洗涤烧杯和玻璃棒
④定容时俯视刻度线观察液面
⑤定容时仰视刻度线观察液面
⑥摇匀后静置,发现液面低于刻度线,再加蒸馏水补至刻度线
(1)需称量纯碱的质量为
(2)配制溶液时下列仪器中:A.锥形瓶 B.托盘天平 C.烧杯 D.胶头滴管 E.药匙。不需要用到的是
(3)人们常将配制过程简述为以下各步骤:A.冷却 B.称量 C.洗涤 D.定容 E.溶解 F.摇匀 G.转移 H.装瓶。其正确的操作顺序应是
①BEAGCGDFH ②BEGACGFDH ③BEFGCGDHA ④BEAGCGDHF
(4)在此配制过程中,下列情况会使配制结果偏低的是
①纯碱晶体有结晶水
②容量瓶使用时未干燥
③移液时未洗涤烧杯和玻璃棒
④定容时俯视刻度线观察液面
⑤定容时仰视刻度线观察液面
⑥摇匀后静置,发现液面低于刻度线,再加蒸馏水补至刻度线
您最近一年使用:0次

 种物质:①
种物质:① ②稀硝酸;③固态醋酸;④
②稀硝酸;③固态醋酸;④ ⑤空气;⑥
⑤空气;⑥ ⑦Fe(OH)3胶体;⑧
⑦Fe(OH)3胶体;⑧ 晶体;⑨
晶体;⑨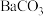
 胶体和
胶体和 溶液实验方法
溶液实验方法 N2+2CO2。
N2+2CO2。

