现有以下物质:①Ca(HCO3)2溶液;②CO2;③熔融Na2CO3;④NaOH;⑤SiO2;⑥Fe(OH)3胶体;⑦氨水;⑧Na2O2
(1)其中能导电的电解质:_________ (填编号,下同);属于非电解质的是:_________ 。
(2)请写出①和过量④的离子反应方程式__________________ 。
(3)利用 Fe(OH)3胶体进行下列实验:将其装入 形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明Fe(OH)3胶粒带
形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明Fe(OH)3胶粒带_________ 电荷(填“正”或“负”)。
(4)⑤为酸性氧化物,写出④与⑤反应的离子方程式__________________ 。
(5) Na2O2可作熔矿剂和氧化剂,则高温熔融条件下可将Cr2O3氧化为Na2CrO4,该反应的化学方程式为__________________ 。
(1)其中能导电的电解质:
(2)请写出①和过量④的离子反应方程式
(3)利用 Fe(OH)3胶体进行下列实验:将其装入
 形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明Fe(OH)3胶粒带
形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明Fe(OH)3胶粒带(4)⑤为酸性氧化物,写出④与⑤反应的离子方程式
(5) Na2O2可作熔矿剂和氧化剂,则高温熔融条件下可将Cr2O3氧化为Na2CrO4,该反应的化学方程式为
22-23高一上·山东淄博·期末 查看更多[2]
山东省淄博实验中学2022-2023学年高一上学期期末考试化学试题(已下线)专题01 物质的分类及转化-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)
更新时间:2023-08-22 14:33:30
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】Fe(OH)3 胶体是中学常见的胶体,某课外兴趣小组制备了 Fe(OH)3 胶体,并探究其性质。
(1)制备方法:将饱和 FeCl3 溶液滴入沸水中,继续煮沸至液体变为_____ 色,停止加热,可 得到 Fe(OH)3 胶体。制备胶体的离子反应方程式为_____ 。
(2)判断胶体制备是否成功,可利用胶体的_____ 。
(3)向 Fe(OH)3 胶体中逐滴加入了稀 H2SO4 溶液,结果出现了一系列变化。
a.先出现红褐色沉淀,原因是_____ 。
b. 随后沉淀溶解,此反应的离子方程式是_____ 。
(1)制备方法:将饱和 FeCl3 溶液滴入沸水中,继续煮沸至液体变为
(2)判断胶体制备是否成功,可利用胶体的
(3)向 Fe(OH)3 胶体中逐滴加入了稀 H2SO4 溶液,结果出现了一系列变化。
a.先出现红褐色沉淀,原因是
b. 随后沉淀溶解,此反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图为一“铁链”图案,小明在图案上分别写了H2、CO2、Na2O、NaCl、FeCl3五种物质,图中相连的两种物质均可归属为一类,相交部分A、B、C、D为其相应的分类依据代号。请回答下列问题:
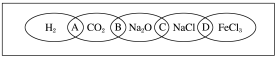
(1)请将分类依据代号填入相应的括号内。
( ) 两种物质都不是电解质 ( ) 两种物质都是钠的化合物
( ) 两种物质都是氧化物 ( ) 两种物质都是盐
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入饱和的上图中某种物质M的溶液,继续加热至呈红褐色。
①物质M的化学式为________ 。
②证明有红褐色胶体生成的实验操作是_________________________ 。

(1)请将分类依据代号填入相应的括号内。
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入饱和的上图中某种物质M的溶液,继续加热至呈红褐色。
①物质M的化学式为
②证明有红褐色胶体生成的实验操作是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求填空:
I.现有7种物质:① Na、② FeCl3溶液、③ CH3COOH、④ 熔融的KNO3、⑤ CO2、⑥ Fe(OH)3胶体、⑦ NH4Cl 固体。
(1)能导电的电解质有___________ (填序号)。
(2)属于盐的物质有___________ (填序号)。
(3)区分Fe(OH)3胶体和 FeCl3溶液的常用物理方法是___________ 。
(4)FeCl3在溶液中的电离方程式是___________ 。
II.依据信息书写下列反应的离子方程式。
(5)SO2是一种酸性氧化物,可用过量 NaOH溶液吸收含 SO2的尾气,该反应的离子方程式是___________
(6)市场上出售的抗酸药复方氢氧化铝片主要用于缓解人体胃酸(主要成分是盐酸)过多,相关反应的离子方程式为___________ 。
III.碳酸钠在轻工、建材、纺织、国防、医药等工业中有重要的应用。工业碳酸钠(纯度约为98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO 等杂质,提纯工艺线路如下:
等杂质,提纯工艺线路如下:

碳酸钠的饱和溶液在不同温度下析出的溶质如图所示:

请回答下列问题:
(7)试剂A是___________ ,“母液”中除了含有Na+、CO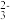 、OH-外,还含有
、OH-外,还含有___________ 等离子,过滤要“趁热”的目的是___________ 。
(8)检验试剂级Na2CO3中Cl-和SO 是否除尽,选用的试剂及加入的先后次序是___________(填字母)。
是否除尽,选用的试剂及加入的先后次序是___________(填字母)。
I.现有7种物质:① Na、② FeCl3溶液、③ CH3COOH、④ 熔融的KNO3、⑤ CO2、⑥ Fe(OH)3胶体、⑦ NH4Cl 固体。
(1)能导电的电解质有
(2)属于盐的物质有
(3)区分Fe(OH)3胶体和 FeCl3溶液的常用物理方法是
(4)FeCl3在溶液中的电离方程式是
II.依据信息书写下列反应的离子方程式。
(5)SO2是一种酸性氧化物,可用过量 NaOH溶液吸收含 SO2的尾气,该反应的离子方程式是
(6)市场上出售的抗酸药复方氢氧化铝片主要用于缓解人体胃酸(主要成分是盐酸)过多,相关反应的离子方程式为
III.碳酸钠在轻工、建材、纺织、国防、医药等工业中有重要的应用。工业碳酸钠(纯度约为98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO
 等杂质,提纯工艺线路如下:
等杂质,提纯工艺线路如下:
碳酸钠的饱和溶液在不同温度下析出的溶质如图所示:

请回答下列问题:
(7)试剂A是
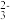 、OH-外,还含有
、OH-外,还含有(8)检验试剂级Na2CO3中Cl-和SO
 是否除尽,选用的试剂及加入的先后次序是___________(填字母)。
是否除尽,选用的试剂及加入的先后次序是___________(填字母)。| A.HCl、BaCl2、AgNO3 | B.AgNO3、HNO3、Ba(NO3)2 |
| C.HNO3、Ba(NO3)2、AgNO3 | D.AgNO3、HCl、BaCl2 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】完成下列问题
Ⅰ.现有下列十种物质:①蔗糖②熔融NaCl③盐酸④铜丝⑤NaOH固体⑥氧气⑦ 固体⑧乙醇⑨
固体⑧乙醇⑨ 溶液⑩液态
溶液⑩液态
(1)上述状态下物质中可导电的是______ (填序号,下同);
(2)上述状态下物质中不能导电,但属于电解质的是______ ;
(3)上述物质中属于非电解质的是______ ;
(4)上述物质中既不属于电解质也不属于非电解质的是______ ;
Ⅱ.写出下列除杂的离子方程式,括号内的物质为杂质。
(5) 溶液(
溶液( ):
):__________________
(6) 溶液(
溶液( ):
):__________________ ;
(7)______ ____ ______
______ ______
______ ______
______ ______
______ ______
______ ______
______
Ⅰ.现有下列十种物质:①蔗糖②熔融NaCl③盐酸④铜丝⑤NaOH固体⑥氧气⑦
 固体⑧乙醇⑨
固体⑧乙醇⑨ 溶液⑩液态
溶液⑩液态
(1)上述状态下物质中可导电的是
(2)上述状态下物质中不能导电,但属于电解质的是
(3)上述物质中属于非电解质的是
(4)上述物质中既不属于电解质也不属于非电解质的是
Ⅱ.写出下列除杂的离子方程式,括号内的物质为杂质。
(5)
 溶液(
溶液( ):
):(6)
 溶液(
溶液( ):
):(7)
 ______
______ ______
______ ______
______ ______
______ ______
______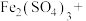 ______
______
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】利用“价类二维图”研究物质的性质是化学研究的重要手段。下图是氯元素的化合价与部分物质类别的对应关系。

(1)A、B、C三种物质中,属于电解质的是_______ (填化学式)。
(2)写出 的电离方程式
的电离方程式_______ 。
(3)C可与HCl反应生成A,写出该反应的化学方程式_______ 。
(4)已知D可用于实验室制 ,其焰色试验为紫色。D可以用A与某强碱溶液在加热下反应制得,除生成D外,还生成一种无氧酸盐和水,写出该反应的化学方程式
,其焰色试验为紫色。D可以用A与某强碱溶液在加热下反应制得,除生成D外,还生成一种无氧酸盐和水,写出该反应的化学方程式_______ 。

(1)A、B、C三种物质中,属于电解质的是
(2)写出
 的电离方程式
的电离方程式(3)C可与HCl反应生成A,写出该反应的化学方程式
(4)已知D可用于实验室制
 ,其焰色试验为紫色。D可以用A与某强碱溶液在加热下反应制得,除生成D外,还生成一种无氧酸盐和水,写出该反应的化学方程式
,其焰色试验为紫色。D可以用A与某强碱溶液在加热下反应制得,除生成D外,还生成一种无氧酸盐和水,写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】运用分类方法,可以发现物质及其变化的规律,预测物质的性质及可能发生的变化。科学的分类能够反映事物的本质特征,有利于人们分门别类地进行深入研究。利用所学过的知识回答下列问题:
有以下物质①石墨;②钠;③酒精;④氨气;⑤硫化氢;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氧化钠固体;⑩液态氯化氢。
(1)其中能导电的是_____ ;属于非电解质的是_____ 。
(2)等质量④和⑤中氢原子的数目之比为_____ ;若④和⑤中所含氢原子数相等,则④和⑤的质量之比为_____ 。
(3)写出⑥和⑩在水溶液中的离子方程式_____ 。
(4)室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2混合气体和1mol空气,此时活塞的位置如图所示。
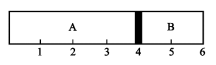
实验测得A室混合气体的质量为34g,若将A室H2、O2的混合气体点燃,恢复原温度后,(非气体体积忽略不计)最终活塞停留的位置在刻度_____ 处。
有以下物质①石墨;②钠;③酒精;④氨气;⑤硫化氢;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氧化钠固体;⑩液态氯化氢。
(1)其中能导电的是
(2)等质量④和⑤中氢原子的数目之比为
(3)写出⑥和⑩在水溶液中的离子方程式
(4)室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2混合气体和1mol空气,此时活塞的位置如图所示。

实验测得A室混合气体的质量为34g,若将A室H2、O2的混合气体点燃,恢复原温度后,(非气体体积忽略不计)最终活塞停留的位置在刻度
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在工业上次磷酸(H3PO2)常用于化学镀银,发生的反应如下:_______Ag++_______H3PO2_______H2O→_______Ag↓+_______H3PO4+_______H+
请回答下列问题:
(1)H3PO2中,P元素的化合价为_______ ;该反应中,还原产物是_______ 。若有lmolH3PO2参加该反应,则反应中转移电子的物质的量为_______ mol。
(2)该反应中,表现氧化性与表现还原性的微粒物质的量之比为_______ 。
(3)已知H3PO2是一元弱酸,写出其与足量NaOH溶液反应的离子方程:_______ 。
(4)若改用氯气将溶液中的H3PO2氧化为H3PO4,其反应的化学方程式为_______ 。
请回答下列问题:
(1)H3PO2中,P元素的化合价为
(2)该反应中,表现氧化性与表现还原性的微粒物质的量之比为
(3)已知H3PO2是一元弱酸,写出其与足量NaOH溶液反应的离子方程:
(4)若改用氯气将溶液中的H3PO2氧化为H3PO4,其反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铅酸蓄电池(图1)是一种电压稳定,使用方便、安全、可靠,又可以循环使用的化学电源,广泛应用于国防、交通、生产和生活中。

(1)铅蓄电池在放电时发生的总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O,负极电极反应式为_______ 。工作后,铅蓄电池里电解质溶液的pH_______ (填“变大”“变小”或“不变”)。
(2)图2是利用微生物将废水中的乙二胺[H2N(CH2)2NH2]氧化为环境友好物质而制作的化学电源,可给二次电池充电。

①用该微生物电池对铅酸蓄电池充电时,铅酸蓄电池的A极应该连接图2中的_______ 极(M或N),此时A处的电极反应方程式为_______ 。
②充电过程中如果B极质量减轻48g,理论上可处理乙二胺的物质的量为_______ mol。
(3)合理利用废旧铅蓄电池中的铅膏可缓解铅资源短缺,同时减少污染。一种从废旧电池的铅膏中回收铅的生产流程如下图(部分产物已略去)。

已知: PbSiF6和H2SiF6均为能溶于水的强电解质。
①为提高过程①的反应速率,你认为可采取的措施是_______ 。
②过程③发生反应的离子方程式为_______ 。
③过程④使用纯铅和粗铅作电极,H2SiF6和PbSiF6混合溶液作电解液,可进行粗铅精炼,则阳极的电极材料是_______ 。电解精炼时需要调控好电解液中H2SiF6的起始浓度,其他条件相同时,随起始时c(H2SiF6)的增大,铅产率先增大后减小,减小的原因可能是_______ 。

(1)铅蓄电池在放电时发生的总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O,负极电极反应式为
(2)图2是利用微生物将废水中的乙二胺[H2N(CH2)2NH2]氧化为环境友好物质而制作的化学电源,可给二次电池充电。

①用该微生物电池对铅酸蓄电池充电时,铅酸蓄电池的A极应该连接图2中的
②充电过程中如果B极质量减轻48g,理论上可处理乙二胺的物质的量为
(3)合理利用废旧铅蓄电池中的铅膏可缓解铅资源短缺,同时减少污染。一种从废旧电池的铅膏中回收铅的生产流程如下图(部分产物已略去)。

已知: PbSiF6和H2SiF6均为能溶于水的强电解质。
①为提高过程①的反应速率,你认为可采取的措施是
②过程③发生反应的离子方程式为
③过程④使用纯铅和粗铅作电极,H2SiF6和PbSiF6混合溶液作电解液,可进行粗铅精炼,则阳极的电极材料是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求填空。
(1)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体 ,请写出该过程的离子方程式:
,请写出该过程的离子方程式:_______ 。
(2)某无色溶液中的溶质可能由下列离子组成: 、
、 、
、 、
、 、
、 、
、 、
、 ,某同学为检验其成分,进行了如下实验:
,某同学为检验其成分,进行了如下实验:
①向适量原溶液中加入过量的稀盐酸,有无色气体a和无色溶液b生成;
②向无色溶液b中加入过量的 溶液,有白色沉淀c生成,过滤,得滤液d;
溶液,有白色沉淀c生成,过滤,得滤液d;
③取少量滤液d,加入过量的稀硝酸酸化,再滴加 溶液,有白色沉淀e生成。
溶液,有白色沉淀e生成。
依据以上实验可以推断,原溶液中一定含有大量的_______ (用离子符号表示,下同);可能含有_______ 。
(3) 常用作补铁剂,在酸性(常用稀硫酸酸化)条件下,
常用作补铁剂,在酸性(常用稀硫酸酸化)条件下, 能将
能将 中
中 价的Cr转化为
价的Cr转化为 价的Cr。则反应中氧化剂与还原剂的物质的量之比为
价的Cr。则反应中氧化剂与还原剂的物质的量之比为_______ 。
(4)某一反应体系中反应物和生成物共有六种物质: 、
、 、
、 、NaCl、NaOH、
、NaCl、NaOH、 ,已知该反应中
,已知该反应中 只发生如下过程:
只发生如下过程: ,则该反应的化学方程式为
,则该反应的化学方程式为_______ 。
(5)向 和
和 混合溶液中缓慢滴加一定浓度的盐酸,测得溶液中
混合溶液中缓慢滴加一定浓度的盐酸,测得溶液中 的物质的量与所加盐酸体积之间的关系如图所示。
的物质的量与所加盐酸体积之间的关系如图所示。

①盐酸的物质的量浓度为_______  。
。
②当滴入盐酸的体积为12.5mL时,溶液中 为
为_______ 。
(1)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体
 ,请写出该过程的离子方程式:
,请写出该过程的离子方程式:(2)某无色溶液中的溶质可能由下列离子组成:
 、
、 、
、 、
、 、
、 、
、 、
、 ,某同学为检验其成分,进行了如下实验:
,某同学为检验其成分,进行了如下实验:①向适量原溶液中加入过量的稀盐酸,有无色气体a和无色溶液b生成;
②向无色溶液b中加入过量的
 溶液,有白色沉淀c生成,过滤,得滤液d;
溶液,有白色沉淀c生成,过滤,得滤液d;③取少量滤液d,加入过量的稀硝酸酸化,再滴加
 溶液,有白色沉淀e生成。
溶液,有白色沉淀e生成。依据以上实验可以推断,原溶液中一定含有大量的
(3)
 常用作补铁剂,在酸性(常用稀硫酸酸化)条件下,
常用作补铁剂,在酸性(常用稀硫酸酸化)条件下, 能将
能将 中
中 价的Cr转化为
价的Cr转化为 价的Cr。则反应中氧化剂与还原剂的物质的量之比为
价的Cr。则反应中氧化剂与还原剂的物质的量之比为(4)某一反应体系中反应物和生成物共有六种物质:
 、
、 、
、 、NaCl、NaOH、
、NaCl、NaOH、 ,已知该反应中
,已知该反应中 只发生如下过程:
只发生如下过程: ,则该反应的化学方程式为
,则该反应的化学方程式为(5)向
 和
和 混合溶液中缓慢滴加一定浓度的盐酸,测得溶液中
混合溶液中缓慢滴加一定浓度的盐酸,测得溶液中 的物质的量与所加盐酸体积之间的关系如图所示。
的物质的量与所加盐酸体积之间的关系如图所示。
①盐酸的物质的量浓度为
 。
。②当滴入盐酸的体积为12.5mL时,溶液中
 为
为
您最近一年使用:0次
【推荐1】Ⅰ.已知铜在常温下能被HNO3溶解。反应方程式为: 3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(1)请将上述反应改成离子方程式,并用单线桥法表示电子得失的方向和数目_______ 。
(2)若生成0.2mol的NO,则该过程中转移的电子是___________ mol。
(3)被还原的硝酸占参加反应硝酸的比例为___________ 。
Ⅱ.某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2;已知该反应中H2O2只发生如下过程:H2O2→ O2,写出该化学方程式_________ 。
(1)请将上述反应改成离子方程式,并用单线桥法表示电子得失的方向和数目
(2)若生成0.2mol的NO,则该过程中转移的电子是
(3)被还原的硝酸占参加反应硝酸的比例为
Ⅱ.某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2;已知该反应中H2O2只发生如下过程:H2O2→ O2,写出该化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学可以为人类制备新物质,还可以提供能源。
(1)乳酸能与金属铁反应制备一种药物,配平下列化学方程式:____ 。

这个反应中的还原产物的化学式是____
(2)已知氢气完全燃烧生成1 mol的液态水放出286 kJ热量,某宇宙飞船上使用的氢氧燃料电池每产生1 kw h电能生成570 g液态水,该电池能量转化率为
h电能生成570 g液态水,该电池能量转化率为____
(1)乳酸能与金属铁反应制备一种药物,配平下列化学方程式:

这个反应中的还原产物的化学式是
(2)已知氢气完全燃烧生成1 mol的液态水放出286 kJ热量,某宇宙飞船上使用的氢氧燃料电池每产生1 kw
 h电能生成570 g液态水,该电池能量转化率为
h电能生成570 g液态水,该电池能量转化率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】运用所学知识,回答下列问题。
I、向硫酸铜溶液中逐滴加入KI溶液至恰好反应完全,观察到产生白色沉淀CuI,蓝色溶液变为棕色。该反应的离子方程式为__________ ;取一定量上述反应后的上层棕色清液于一支试管中,加入一定量的苯,振荡,此时观察到的现象是________ 。
II、工业上用铝土矿(主要成分为Al2O3,只含Fe2O3杂质)为原料冶炼铝的工艺流程如下:

回答下列问题:
(1)上述反应是否都是氧化还原反应_________ (填“是”或“否”);写出反应①的化学方程式_____ 。
(2)反应①后过滤的沉淀为_______ ,简述确定此物质中金属元素及其价态的操作过程_______ 。
I、向硫酸铜溶液中逐滴加入KI溶液至恰好反应完全,观察到产生白色沉淀CuI,蓝色溶液变为棕色。该反应的离子方程式为
II、工业上用铝土矿(主要成分为Al2O3,只含Fe2O3杂质)为原料冶炼铝的工艺流程如下:

回答下列问题:
(1)上述反应是否都是氧化还原反应
(2)反应①后过滤的沉淀为
您最近一年使用:0次



