某学生需要用烧碱固体配制2.0mol/L的NaOH溶液500mL。实验需要以下仪器:①100mL烧杯②玻璃棒 ③托盘天平(带砝码) ④量筒。
请回答下列问题:
(1)计算结果:需要称取NaOH固体___________ g。
(2)配制时,还需使用的玻璃仪器 为___________ 。
(3)如需配制100mL浓度为0.5mol/LNaOH溶液,需量取___________ mL 2.0mol/L的NaOH溶液稀释。
(4)在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度___________ (“偏大”或“偏小”)。
(5)实验中两次用到玻璃棒,其作用分别是:用于___________ 、用于___________ 。
(6)在容量瓶使用方法中,下列操作不正确的是___________(填序号)
请回答下列问题:
(1)计算结果:需要称取NaOH固体
(2)配制时,还需使用的
(3)如需配制100mL浓度为0.5mol/LNaOH溶液,需量取
(4)在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度
(5)实验中两次用到玻璃棒,其作用分别是:用于
(6)在容量瓶使用方法中,下列操作不正确的是___________(填序号)
| A.使用容量瓶前检查它是否漏水 |
| B.容量瓶用蒸馏水洗净后,未干燥 |
| C.将NaOH固体放在天平托盘的滤纸上,准确称量并放入烧杯中溶解后,立即注入容量瓶中 |
| D.定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀 |
更新时间:2023-08-28 14:41:40
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】用质量分数为375%的浓盐酸配制成250 mL 1 mol / L的稀盐酸。
(1)在量取浓盐酸后,进行了下列操作,在下列空格中填入仪器名称;
① 等稀释的盐酸其温度与室温一致后,沿玻璃棒注入___________ 中。
② 往容量瓶中小心加蒸馏水至液面接近环形标线2~3 cm处,改用___________ 加蒸馏水,使溶液的凹面最低处与刻度线相切。
③ 在盛浓盐酸的烧杯中注入蒸馏水几十毫升,并用___________ 搅动,使其混合均匀。
④ 用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
(2)上述操作中,正确的顺序是(填序号)___________ 。
(3)在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,其配制的稀盐酸浓度是_______ (填“偏高”、“偏低”、“无影响”)。
(4)vmL密度为 g/mL的某溶液中,含有相对分子质量为M的溶质m克,该溶液中溶质的质量分数为W%,物质的量浓度为c mol/L,那么下列关系式正确的是
g/mL的某溶液中,含有相对分子质量为M的溶质m克,该溶液中溶质的质量分数为W%,物质的量浓度为c mol/L,那么下列关系式正确的是
(1)在量取浓盐酸后,进行了下列操作,在下列空格中填入仪器名称;
① 等稀释的盐酸其温度与室温一致后,沿玻璃棒注入
② 往容量瓶中小心加蒸馏水至液面接近环形标线2~3 cm处,改用
③ 在盛浓盐酸的烧杯中注入蒸馏水几十毫升,并用
④ 用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
(2)上述操作中,正确的顺序是(填序号)
(3)在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,其配制的稀盐酸浓度是
(4)vmL密度为
 g/mL的某溶液中,含有相对分子质量为M的溶质m克,该溶液中溶质的质量分数为W%,物质的量浓度为c mol/L,那么下列关系式正确的是
g/mL的某溶液中,含有相对分子质量为M的溶质m克,该溶液中溶质的质量分数为W%,物质的量浓度为c mol/L,那么下列关系式正确的是A.c =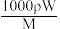 | B.c = | C.W%=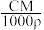 % % | D.m=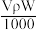 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
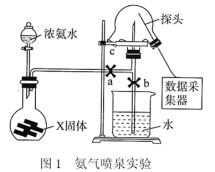
【推荐2】利用压强传感器测定氨气的喷泉实验中的压强变化。___________ 。
(2)可以用___________ 试纸置于三颈瓶口c处验满。
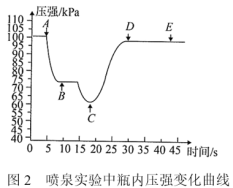
(3)关闭a,将单孔塞(插有吸入水的胶头滴管)塞紧瓶口c,挤压胶头滴管,打开b,完成喷泉实验,电脑绘制三颈瓶内压强变化曲线如图2,___________ 点时喷泉最剧烈(选填A、B、C、D、E)。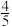 且混合均匀,实验开始前烧瓶中气体的平均分子量为
且混合均匀,实验开始前烧瓶中气体的平均分子量为___________ ,实验结束后烧瓶中溶液的物质的量浓度为___________ mol/L。
(2)可以用
(3)关闭a,将单孔塞(插有吸入水的胶头滴管)塞紧瓶口c,挤压胶头滴管,打开b,完成喷泉实验,电脑绘制三颈瓶内压强变化曲线如图2,
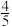 且混合均匀,实验开始前烧瓶中气体的平均分子量为
且混合均匀,实验开始前烧瓶中气体的平均分子量为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】某次实验需用80mL、3mol/L 的稀H2SO4溶液,某同学用98%的浓H2SO4(ρ=1.84g/cm3)进行配制,请回答下列问题:
(1)98%的浓H2SO4(ρ=1.84g/cm3)的物质的量浓度为________ 。
(2)配制80mL、3mol/L 的稀H2SO4溶液,则需取98%的浓H2SO4________ mL,量取浓硫酸所用的量筒的规格是________ (从下列中选用)A.10mL B.25mL C.50mL D.100mL
(3)将下列步骤中的空格补充填写完整
①用量筒量取所需的浓硫酸
②将烧杯中的溶液__________________________________________________
③将浓硫酸缓缓注入盛有适量蒸馏水的烧杯中,边加边搅拌
④将溶液冷却,恢复至室温
⑤向容量瓶中加入蒸馏水_____________________________________________
⑥盖好瓶塞,反复上下颠倒,摇匀
⑦洗涤烧杯2~3次,洗涤液也注入容量瓶中.轻轻摇动容量瓶,使溶液混合均匀.
(4)实验中上述步骤的正确排序为________ (填序号)
(5)下列各种情况使所配制溶液浓度偏高的__________________
A.未经冷却趁热将溶液注入容量瓶中
B将量筒中残留的浓硫酸洗涤后.转移入容量瓶中
C.定容时仰视液面读数
D量取浓硫酸时俯视读数
(6)取用任意体积的所配3mol/L硫酸溶液时,下列物理量中不随所取体积的多少而变化的是_______ (填字母)
A、溶液中H2SO4的物质的量 B、溶液的浓度 C、溶液中SO42¯的数目 D、溶液的密度
(1)98%的浓H2SO4(ρ=1.84g/cm3)的物质的量浓度为
(2)配制80mL、3mol/L 的稀H2SO4溶液,则需取98%的浓H2SO4
(3)将下列步骤中的空格补充填写完整
①用量筒量取所需的浓硫酸
②将烧杯中的溶液
③将浓硫酸缓缓注入盛有适量蒸馏水的烧杯中,边加边搅拌
④将溶液冷却,恢复至室温
⑤向容量瓶中加入蒸馏水
⑥盖好瓶塞,反复上下颠倒,摇匀
⑦洗涤烧杯2~3次,洗涤液也注入容量瓶中.轻轻摇动容量瓶,使溶液混合均匀.
(4)实验中上述步骤的正确排序为
(5)下列各种情况使所配制溶液浓度偏高的
A.未经冷却趁热将溶液注入容量瓶中
B将量筒中残留的浓硫酸洗涤后.转移入容量瓶中
C.定容时仰视液面读数
D量取浓硫酸时俯视读数
(6)取用任意体积的所配3mol/L硫酸溶液时,下列物理量中不随所取体积的多少而变化的是
A、溶液中H2SO4的物质的量 B、溶液的浓度 C、溶液中SO42¯的数目 D、溶液的密度
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】下面是用18mol/L的浓H2SO4稀释配制成500mL1mol/L的稀H2SO4的操作,请按要求填空:
(1)所需浓H2SO4的体积为_______ ;
(2)如果实验室有15mL、20mL、50mL的量筒,应选用_______ mL量筒最好。
(3)将量取的浓H2SO4慢慢注入盛有约100mL水的烧杯里,同时不断_______ 。
(4)将上述溶液沿玻璃棒转移到_______ 中,并用蒸馏水洗涤烧杯2~3次,并将洗涤液也转移到该仪器中,并摇匀。
(5)加水至距刻度1~2cm处时,改用_______ 加水,使溶液的凹液面正好跟刻度相平。
(6)试分析下列操作对所配溶液的浓度的影响(选填“偏高”、“偏低”、“无影响”)。
A.转移溶液时,不慎将少量溶液洒在桌面上。溶液浓度_______ ;
B.用量筒量取时,发现量筒不干净,用水洗净后直接量取浓硫酸。溶液浓度_______ 。
(1)所需浓H2SO4的体积为
(2)如果实验室有15mL、20mL、50mL的量筒,应选用
(3)将量取的浓H2SO4慢慢注入盛有约100mL水的烧杯里,同时不断
(4)将上述溶液沿玻璃棒转移到
(5)加水至距刻度1~2cm处时,改用
(6)试分析下列操作对所配溶液的浓度的影响(选填“偏高”、“偏低”、“无影响”)。
A.转移溶液时,不慎将少量溶液洒在桌面上。溶液浓度
B.用量筒量取时,发现量筒不干净,用水洗净后直接量取浓硫酸。溶液浓度
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】实验室需配制使用80mL 0.400mol·L-1的NaOH溶液,有如下操作步骤:
①把称量好的NaOH晶体放入小烧杯中,加适量蒸馏水溶液;
②把①所得溶液小心转入容量瓶中;
③继续向容量瓶中加蒸馏水至液面距刻度线1cm~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面底部与刻度线相切;
④洗涤完容量瓶后,将容量瓶烘干:
⑤用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤液体都小心转入容量瓶,并轻轻摇匀;
⑥定容摇匀后液面低于刻度线,又加水到刻度线;
⑦将容量瓶塞塞紧,上下颠倒摇匀;
⑧检查瓶塞处是否漏水。
完成下列各题:
(1)选择必要的操作步骤并进行排序(填序号)_______ 。
(2)其中第①步需要称取的NaOH为_______ g (结果保留三位有效数字)。
(3)本实验用到的基本玻璃仪器有胶头滴管,烧杯和_______ 。
(4)实验操作中,下列操作会使所配溶液浓度偏低的是_______ 。
a.没有进行操作步骤⑤
b.容量瓶底部中原残留少量蒸馏水
c.转移过程中有部分溶液洒落
d.NaOH溶解后未冷却立即转移
e.定容时,俯视刻度线
①把称量好的NaOH晶体放入小烧杯中,加适量蒸馏水溶液;
②把①所得溶液小心转入容量瓶中;
③继续向容量瓶中加蒸馏水至液面距刻度线1cm~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面底部与刻度线相切;
④洗涤完容量瓶后,将容量瓶烘干:
⑤用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤液体都小心转入容量瓶,并轻轻摇匀;
⑥定容摇匀后液面低于刻度线,又加水到刻度线;
⑦将容量瓶塞塞紧,上下颠倒摇匀;
⑧检查瓶塞处是否漏水。
完成下列各题:
(1)选择必要的操作步骤并进行排序(填序号)
(2)其中第①步需要称取的NaOH为
(3)本实验用到的基本玻璃仪器有胶头滴管,烧杯和
(4)实验操作中,下列操作会使所配溶液浓度偏低的是
a.没有进行操作步骤⑤
b.容量瓶底部中原残留少量蒸馏水
c.转移过程中有部分溶液洒落
d.NaOH溶解后未冷却立即转移
e.定容时,俯视刻度线
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】已知某浓盐酸试剂瓶标签上的有关数据为,相对分子质量:36.5,密度:1.19g.·m-3HCl的质量分数:36.5%。试根据有关数据回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为__ mol·L-1。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是_ 。
A.溶液中HCl的物质的量
B.溶液的物质的量浓度
C.溶液中Cl-的数目
D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制480mL物质的量浓度为0.2mol·L−1的稀盐酸。
①该学生需要量取__ mL上述浓盐酸进行配制。
②现有三种规格的量筒10mL、20mL、50mL应选用__ mL量筒。
(1)该浓盐酸中HCl的物质的量浓度为
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是
A.溶液中HCl的物质的量
B.溶液的物质的量浓度
C.溶液中Cl-的数目
D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制480mL物质的量浓度为0.2mol·L−1的稀盐酸。
①该学生需要量取
②现有三种规格的量筒10mL、20mL、50mL应选用
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】实验室用固体烧碱配制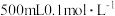 的NaOH溶液。
的NaOH溶液。
(1)计算并称量NaOH固体的质量为_______ g。
(2)配制过程中,不需要使用的仪器有(填写代号)_______ 。
a.烧杯 b.托盘天平 c.玻璃棒 d. 容量瓶 e.锥形瓶 f.胶头滴管 g.
容量瓶 e.锥形瓶 f.胶头滴管 g. 容量瓶
容量瓶
(3)配制溶液的实验步骤:
a.计算需要氢氧化钠固体的质量
b.称量氢氧化钠固体
c.用少量蒸馏水洗涤烧杯和玻璃棒2-3次,洗涤液也注入容量瓶
d.用适量的蒸馏水溶解称量好的氢氧化钠固体,冷却后将烧杯中的溶液注入容量瓶
e.盖好瓶塞,反复上下颠倒,摇匀。
f.继续向容量瓶中加蒸馏水至刻度线下1-2 时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切。将上述步骤正确操作顺序是
时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切。将上述步骤正确操作顺序是_______ 。
(4)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏大的是____ 。
a.转移溶液时不慎有少量洒到容量瓶外面
b.定容时俯视刻度线
c.未冷却到室温就将溶液转移到容量瓶并定容
d.定容后塞上瓶塞反复摇匀静置后,液面低于刻度线,再加水至刻度线
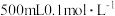 的NaOH溶液。
的NaOH溶液。(1)计算并称量NaOH固体的质量为
(2)配制过程中,不需要使用的仪器有(填写代号)
a.烧杯 b.托盘天平 c.玻璃棒 d.
 容量瓶 e.锥形瓶 f.胶头滴管 g.
容量瓶 e.锥形瓶 f.胶头滴管 g. 容量瓶
容量瓶(3)配制溶液的实验步骤:
a.计算需要氢氧化钠固体的质量
b.称量氢氧化钠固体
c.用少量蒸馏水洗涤烧杯和玻璃棒2-3次,洗涤液也注入容量瓶
d.用适量的蒸馏水溶解称量好的氢氧化钠固体,冷却后将烧杯中的溶液注入容量瓶
e.盖好瓶塞,反复上下颠倒,摇匀。
f.继续向容量瓶中加蒸馏水至刻度线下1-2
 时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切。将上述步骤正确操作顺序是
时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切。将上述步骤正确操作顺序是(4)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏大的是
a.转移溶液时不慎有少量洒到容量瓶外面
b.定容时俯视刻度线
c.未冷却到室温就将溶液转移到容量瓶并定容
d.定容后塞上瓶塞反复摇匀静置后,液面低于刻度线,再加水至刻度线
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】如图是硫酸试剂瓶标签上的内容:
(1)某化学兴趣小组进行硫酸性质的实验探究时,需要490mL 4.6 mol•L-1的稀硫酸,现要配制该浓度的溶液所需要的玻璃仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要_____ (填仪器名称);需要量取98%浓硫酸____ mL进行配制;
(2)配制溶液时有如下操作:a.稀释溶液b.摇匀c.洗涤d.冷却e.量取f.将溶液移至容量瓶g.定容,实验操作顺序正确的是____
A e→a→f→d→c→f→g→b B e→a→d→f→c→f→g→b
C e→a→f→d→c→f→b→g D e→a→d→f→c→f→b→g
(3)下列为配置过程中部分操作的示意图,其中有错误的是_____ (填序号);
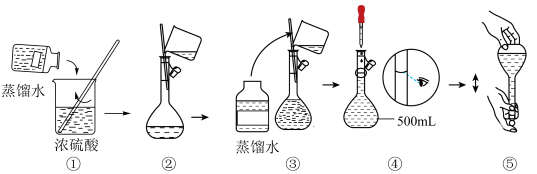
(4)在配制4.6 mol•L-1稀硫酸的过程中,下列情况会引起配制所得的硫酸溶液物质的量浓度偏高的是______ ;
A 未经冷却趁热将溶液注入容量瓶中 B 容量瓶洗涤后,未干燥处理
C 定容时仰视观察液面 D 未洗涤烧杯和玻璃棒
| 硫酸 化学纯(CP)(500mL) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84g/cm3 质量分数:98% |
(2)配制溶液时有如下操作:a.稀释溶液b.摇匀c.洗涤d.冷却e.量取f.将溶液移至容量瓶g.定容,实验操作顺序正确的是
A e→a→f→d→c→f→g→b B e→a→d→f→c→f→g→b
C e→a→f→d→c→f→b→g D e→a→d→f→c→f→b→g
(3)下列为配置过程中部分操作的示意图,其中有错误的是

(4)在配制4.6 mol•L-1稀硫酸的过程中,下列情况会引起配制所得的硫酸溶液物质的量浓度偏高的是
A 未经冷却趁热将溶液注入容量瓶中 B 容量瓶洗涤后,未干燥处理
C 定容时仰视观察液面 D 未洗涤烧杯和玻璃棒
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】实验室需要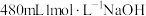 溶液,根据溶液配制情况回答下列问题:
溶液,根据溶液配制情况回答下列问题:
(1)实验中除需要托盘天平(带砝码)、药匙、量筒、烧杯、玻璃棒、试剂瓶外,还需要的玻璃仪器有_______________ 。
(2)如图所示是某同学在实验室配制该 溶液的过程示意图,其中有错误的是
溶液的过程示意图,其中有错误的是_____________ (填序号)。
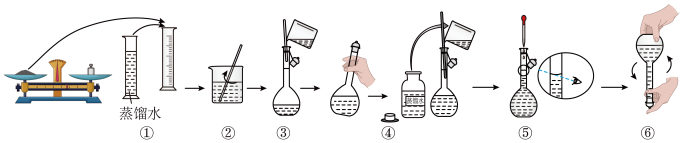
(3)配制溶液时,称取 固体的质量为
固体的质量为____________ 。
(4)下列操作会导致所配溶液的物质的量浓度偏高的是____________(填标号)。
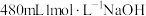 溶液,根据溶液配制情况回答下列问题:
溶液,根据溶液配制情况回答下列问题:(1)实验中除需要托盘天平(带砝码)、药匙、量筒、烧杯、玻璃棒、试剂瓶外,还需要的玻璃仪器有
(2)如图所示是某同学在实验室配制该
 溶液的过程示意图,其中有错误的是
溶液的过程示意图,其中有错误的是
(3)配制溶液时,称取
 固体的质量为
固体的质量为(4)下列操作会导致所配溶液的物质的量浓度偏高的是____________(填标号)。
A. 固体长期暴露在空气中 固体长期暴露在空气中 |
B.用蒸馏水溶解 固体后,立即转入容量瓶中 固体后,立即转入容量瓶中 |
| C.定容后发现溶液的凹液面最低点高于刻度线,用胶头滴管将多余的液体吸出 |
| D.定容时俯视刻度线 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某工厂废渣仅含有ZnCO3、CuCO3,以该废渣为原料生产硫酸锌和铜的工艺流程如图。回答下列问题:
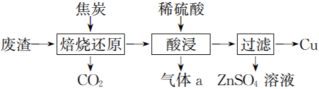
(1)“焙烧还原”时CuCO3被__ (填“氧化”“还原”),写出ZnCO3转化为Zn的化学方程式:__ 。
(2)气体a的化学式为__ 。
(3)酸浸时用到的4.5mol•L-1的H2SO4溶液需用18mol•L-1的H2SO4浓溶液配制。
①配制90.0mL4.5mol•L-1H2SO4溶液需要用到的玻璃仪器有量筒、烧杯、胶头滴管、玻璃棒、__ ,需量取__ mL18mol•L-1H2SO4浓溶液。
②下列操作使所配溶液浓度偏大的是__ (填字母)。
A.定容时,俯视刻度线
B.转移前容量瓶中含有少量蒸馏水
C.未洗涤稀释硫酸时用过的烧杯和玻璃棒
(4)已知ZnSO4的溶解度如表所示,则从ZnSO4溶液中获得ZnSO4•7H2O的方法是__ 、__ 、过滤。

(1)“焙烧还原”时CuCO3被
(2)气体a的化学式为
(3)酸浸时用到的4.5mol•L-1的H2SO4溶液需用18mol•L-1的H2SO4浓溶液配制。
①配制90.0mL4.5mol•L-1H2SO4溶液需要用到的玻璃仪器有量筒、烧杯、胶头滴管、玻璃棒、
②下列操作使所配溶液浓度偏大的是
A.定容时,俯视刻度线
B.转移前容量瓶中含有少量蒸馏水
C.未洗涤稀释硫酸时用过的烧杯和玻璃棒
(4)已知ZnSO4的溶解度如表所示,则从ZnSO4溶液中获得ZnSO4•7H2O的方法是
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 溶解度g/100mL | 41.6 | 47.2 | 53.8 | 61.3 | 70.5 | 73.2 | 75.4 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】Ⅰ.如图是某学校实验室从化学试剂商店买回来的NaOH试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
标签上的有关数据回答下列问题:
(1)该NaOH溶液的物质的量浓度为___________ (保留两位小数);现在要配制480mL该浓度的NaOH溶液,应用托盘天平称取NaOH的质量为___________ 。
(2)配制上述溶液的过程中需要用到的主要玻璃仪器除了量筒、烧杯、玻璃棒外,还缺少的必要玻璃仪器为___________ 、___________ (填仪器名称)。
(3)若取5mL该溶液用水稀释到100mL,所得溶液 的物质的量浓度为
的物质的量浓度为___________ 。
(4)下列操作能使NaOH溶液的物质的量浓度偏高的有___________ (填字母)。
a.摇匀后发现液面低于刻度线再加水
b.NaOH溶解后未恢复至室温就注入容量瓶中
c.转移时没有洗涤烧杯、玻璃棒
d.定容时俯视刻度线
e.容量瓶未烘干
Ⅱ.某同学发现上个月做实验用的NaOH溶液忘记盖瓶塞。对于该溶液是否变质,该同学对此进行了探究。请你一起完成下列实验报告。
【提出问题1】该溶液是否变质?
【实验探究1】
(5)完成下列表格
【提出问题2】该溶液变质程度怎样?
【提出猜想】
(6)猜想一:已完全变质,该溶液中溶质只含 。
。
猜想二:部分变质,该溶液中溶质含有___________ 。
该同学探究该溶液是否完全变质,准备了两种试剂:①酚酞试液,②足量的 溶液(
溶液( 溶液为中性溶液),若加入顺序为②①,当出现
溶液为中性溶液),若加入顺序为②①,当出现___________ 现象时,说明NaOH溶液已完全变质,其中加入②时发生反应的化学方程式为___________ 。
| 氢氧化钠溶液 化学式:NaOH 相对分子质量:40 密度: 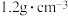 质量分数:20% |
(1)该NaOH溶液的物质的量浓度为
(2)配制上述溶液的过程中需要用到的主要玻璃仪器除了量筒、烧杯、玻璃棒外,还缺少的必要玻璃仪器为
(3)若取5mL该溶液用水稀释到100mL,所得溶液
 的物质的量浓度为
的物质的量浓度为(4)下列操作能使NaOH溶液的物质的量浓度偏高的有
a.摇匀后发现液面低于刻度线再加水
b.NaOH溶解后未恢复至室温就注入容量瓶中
c.转移时没有洗涤烧杯、玻璃棒
d.定容时俯视刻度线
e.容量瓶未烘干
Ⅱ.某同学发现上个月做实验用的NaOH溶液忘记盖瓶塞。对于该溶液是否变质,该同学对此进行了探究。请你一起完成下列实验报告。
【提出问题1】该溶液是否变质?
【实验探究1】
(5)完成下列表格
| 实验步骤 | 实验现象 | 解释与结论 |
| 取少量该溶液于试管中,滴加足量稀盐酸 | 有 | 说明该溶液已变质。变质的原因是 |
【提出问题2】该溶液变质程度怎样?
【提出猜想】
(6)猜想一:已完全变质,该溶液中溶质只含
 。
。猜想二:部分变质,该溶液中溶质含有
该同学探究该溶液是否完全变质,准备了两种试剂:①酚酞试液,②足量的
 溶液(
溶液( 溶液为中性溶液),若加入顺序为②①,当出现
溶液为中性溶液),若加入顺序为②①,当出现
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】回答下列问题:
(1)饮用水中NO 对人类健康会产生危害,为了降低饮用水中NO
对人类健康会产生危害,为了降低饮用水中NO 的浓度,某饮用水研究人员提出,可在碱性条件下用铝粉将NO
的浓度,某饮用水研究人员提出,可在碱性条件下用铝粉将NO 还原为N2。
还原为N2。
①配平方程式并用双线桥表示电子转移情况:_____ 。
_____Al+____NO +_____OH-+_____H2O=______[Al(OH)4]-+_____N2↑。
+_____OH-+_____H2O=______[Al(OH)4]-+_____N2↑。
②上述反应中,还原剂与还原产物的物质的量之比是_____ ,反应中转移电子0.3mol,生成_____ mL(标准状况下)N2。
II.如图是成外化学实验室浓盐酸试剂标签上的部分内容。乙同学现用该浓盐酸配制100mL1mol•L-1的稀盐酸。

可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;请回答下列问题:
(2)配制稀盐酸时,还缺少的仪器有_____ 。
(3)经计算,配制100mL1mol•L-1的稀盐酸需要用量筒量取上述浓盐酸的体积为_______ mL(保留小数点后一位)。
(4)对所配制的稀盐酸进行测定,发现其浓度小于1mol•L-1,引起误差的原因可能是_____ 。
(1)饮用水中NO
 对人类健康会产生危害,为了降低饮用水中NO
对人类健康会产生危害,为了降低饮用水中NO 的浓度,某饮用水研究人员提出,可在碱性条件下用铝粉将NO
的浓度,某饮用水研究人员提出,可在碱性条件下用铝粉将NO 还原为N2。
还原为N2。①配平方程式并用双线桥表示电子转移情况:
_____Al+____NO
 +_____OH-+_____H2O=______[Al(OH)4]-+_____N2↑。
+_____OH-+_____H2O=______[Al(OH)4]-+_____N2↑。②上述反应中,还原剂与还原产物的物质的量之比是
II.如图是成外化学实验室浓盐酸试剂标签上的部分内容。乙同学现用该浓盐酸配制100mL1mol•L-1的稀盐酸。

可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;请回答下列问题:
(2)配制稀盐酸时,还缺少的仪器有
(3)经计算,配制100mL1mol•L-1的稀盐酸需要用量筒量取上述浓盐酸的体积为
(4)对所配制的稀盐酸进行测定,发现其浓度小于1mol•L-1,引起误差的原因可能是
| A.定容时俯视容量瓶刻度线 |
| B.容量瓶在使用前未干燥,里面有少量蒸馏水 |
| C.转移溶液后,未洗涤烧杯和玻璃棒 |
| D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线 |
您最近一年使用:0次



