金属及金属材料广泛应用于生产、生活,其应用推动了社会的发展。
(1)下列金属应用的实例中,主要利用金属导电性的是_______(填标号)。
(2)钢铁是使用最多的金属材料。钢和生铁在性能上有较大差异的主要原因是_______ 。
(3)《天工开物》中记载“铁器淬于胆矾水中,即成铜色”,胆矾水即硫酸铜溶液,写出该反应的化学方程式_______ ,该反应的反应类型为_______ (填“氧化还原”或“非氧化还原”)反应。
(4)为了验证Fe、Cu、Ag三种金属的活动性顺序,下列选用的药品可行的是_______ (填标号)。
①Fe、Cu、Ag、稀盐酸 ②FeSO4溶液、Cu、AgNO3溶液 ③Fe、CuSO4溶液、Ag ④FeSO4溶液、CuSO4溶液、Ag ⑤FeSO4溶液、Cu、Ag
(5)将锌粉加入盛有一定量硝酸银和硝酸铜的混合溶液中,反应过程如图所示:

滤渣中一定含有_______ (填化学式)。
(1)下列金属应用的实例中,主要利用金属导电性的是_______(填标号)。
| A.铜导线 | B.银手镯 | C.铁锅 | D.金属乐器 |
(2)钢铁是使用最多的金属材料。钢和生铁在性能上有较大差异的主要原因是
(3)《天工开物》中记载“铁器淬于胆矾水中,即成铜色”,胆矾水即硫酸铜溶液,写出该反应的化学方程式
(4)为了验证Fe、Cu、Ag三种金属的活动性顺序,下列选用的药品可行的是
①Fe、Cu、Ag、稀盐酸 ②FeSO4溶液、Cu、AgNO3溶液 ③Fe、CuSO4溶液、Ag ④FeSO4溶液、CuSO4溶液、Ag ⑤FeSO4溶液、Cu、Ag
(5)将锌粉加入盛有一定量硝酸银和硝酸铜的混合溶液中,反应过程如图所示:

滤渣中一定含有
更新时间:2023-08-29 20:42:38
|
相似题推荐
【推荐1】已知铜在常温下能被稀硝酸溶解,其反应的化学方程式为3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(1)被还原的元素是__ ,还原剂是__ ,还原产物是__ 。
(2)该反应中的氧化剂与还原剂个数之比是__ 。
(3)完成NaClO3氧化FeCl2的离子方程式:________ ClO +
+________ Fe2++________ H+=________ Cl-+________ Fe3++________ H2O(化学计量数是 1 的也请填上)
(4)12个Na2SO3恰好与4个K2Cr2O7完全反应。已知Na2SO3可被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为___ 。
(5)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:KMnO4+HCl(浓)═KCl+MnCl2+Cl2↑+H2O(未配平)__ 。
配平该化学方程式:___KMnO4+___HCl═____KCl+__MnCl2+__Cl2↑+__H2O(化学计量数是 1 的也请填上) 并用单线桥 法标出电子转移情况。
(1)被还原的元素是
(2)该反应中的氧化剂与还原剂个数之比是
(3)完成NaClO3氧化FeCl2的离子方程式:
 +
+(4)12个Na2SO3恰好与4个K2Cr2O7完全反应。已知Na2SO3可被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为
(5)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:KMnO4+HCl(浓)═KCl+MnCl2+Cl2↑+H2O(未配平)
配平该化学方程式:___KMnO4+___HCl═____KCl+__MnCl2+__Cl2↑+__H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】I. 易溶于水,外观和食盐相似,有咸味,人误食会中毒。
易溶于水,外观和食盐相似,有咸味,人误食会中毒。
(1) 中氮元素的化合价为
中氮元素的化合价为___________ 价。
(2)已知 能发生反应:
能发生反应: 。
。
①用单线桥法表示该反应中电子转移情况___________ 。
②淀粉週碘单质会变蓝色,则鉴别 固体和
固体和 固体,选用的物质为
固体,选用的物质为___________ (填标号)。
a.水 b.淀粉一碘化钾溶液 c.白醋 d.白酒
II.
(3)工业废水中含有的重铬酸根离子(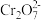 )有毒,必须处理达标后才能排放。工业上常用绿矾
)有毒,必须处理达标后才能排放。工业上常用绿矾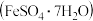 作处理剂,能将
作处理剂,能将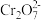 中
中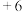 价
价 转化为
转化为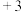 价
价 。则反应中氧化剂(氧化性离子)与还原剂(还原性离子)的个数之比为
。则反应中氧化剂(氧化性离子)与还原剂(还原性离子)的个数之比为___________ 。
(4)已知:①铁钉在氯气中被锈蚀成棕褐色含 的物质,而在稀硫酸中生成浅绿色溶液
的物质,而在稀硫酸中生成浅绿色溶液 含
含 ;②
;② 。则
。则 、
、 、
、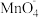 氧化性由强到弱排序为
氧化性由强到弱排序为___________ 。
 易溶于水,外观和食盐相似,有咸味,人误食会中毒。
易溶于水,外观和食盐相似,有咸味,人误食会中毒。(1)
 中氮元素的化合价为
中氮元素的化合价为(2)已知
 能发生反应:
能发生反应: 。
。①用单线桥法表示该反应中电子转移情况
②淀粉週碘单质会变蓝色,则鉴别
 固体和
固体和 固体,选用的物质为
固体,选用的物质为a.水 b.淀粉一碘化钾溶液 c.白醋 d.白酒
II.
(3)工业废水中含有的重铬酸根离子(
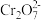 )有毒,必须处理达标后才能排放。工业上常用绿矾
)有毒,必须处理达标后才能排放。工业上常用绿矾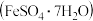 作处理剂,能将
作处理剂,能将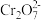 中
中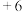 价
价 转化为
转化为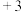 价
价 。则反应中氧化剂(氧化性离子)与还原剂(还原性离子)的个数之比为
。则反应中氧化剂(氧化性离子)与还原剂(还原性离子)的个数之比为(4)已知:①铁钉在氯气中被锈蚀成棕褐色含
 的物质,而在稀硫酸中生成浅绿色溶液
的物质,而在稀硫酸中生成浅绿色溶液 含
含 ;②
;② 。则
。则 、
、 、
、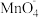 氧化性由强到弱排序为
氧化性由强到弱排序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)写出明矾[KAl(SO4)2•12H2O]在水中的电离方程式________________ ,明矾净水的原因是因为它与水反应产生的Al(OH)3胶体具有___________ 性。
(2)溶液的导电能力大小主要是由离子浓度大小决定的,利用“液体导电性的实验装置”(如图所示)作下列实验,灯泡能出现由亮—暗—熄灭—亮现象的是_______
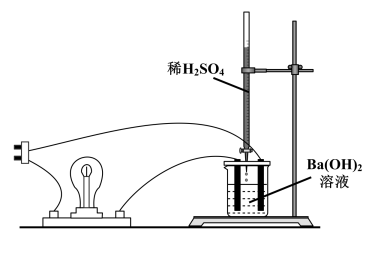
A.向BaCl2溶液中滴入稀H2SO4
B.向Ba(OH)2溶液中滴入稀H2SO4
C.向NaOH溶液中滴入盐酸
写出所选项的离子反应方程式_______________ (若上题选错,该项不得分)。
(3)Mn2+、Bi3+、BiO 、MnO
、MnO 、H+、H2O组成的一个氧化还原反应体系中,发生BiO
、H+、H2O组成的一个氧化还原反应体系中,发生BiO →Bi3+的反应过程。
→Bi3+的反应过程。
①该反应中,被氧化的元素是_______ ,氧化剂是______ 。
②将以上物质分别填入下面对应的横线上,组成一个未配平 的化学方程式_______ _____+ ______+ ________→ ______+ ________+ H2O
③反应中若产生0.2mol的还原产物,则有____ mol电子转移。
(1)写出明矾[KAl(SO4)2•12H2O]在水中的电离方程式
(2)溶液的导电能力大小主要是由离子浓度大小决定的,利用“液体导电性的实验装置”(如图所示)作下列实验,灯泡能出现由亮—暗—熄灭—亮现象的是

A.向BaCl2溶液中滴入稀H2SO4
B.向Ba(OH)2溶液中滴入稀H2SO4
C.向NaOH溶液中滴入盐酸
写出所选项的离子反应方程式
(3)Mn2+、Bi3+、BiO
 、MnO
、MnO 、H+、H2O组成的一个氧化还原反应体系中,发生BiO
、H+、H2O组成的一个氧化还原反应体系中,发生BiO →Bi3+的反应过程。
→Bi3+的反应过程。①该反应中,被氧化的元素是
②将以上物质分别填入下面对应的横线上,组成一个
③反应中若产生0.2mol的还原产物,则有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ、某校化学研究性学习小组欲设计实验验证Zn、Fe、Cu的金属活动性,他们提出了以下两种方案。请你帮助他们完成有关实验项目:
(1)用三种金属与盐酸反应的现象来判断,实验中除选择大小相同的金属片外,还需要控制_____________ 、_____________ 相同;若选用一种盐溶液验证三种金属的活泼性,该试剂为___________ 。
(2)某小组同学采用Zn、Fe作为电极,只用一个原电池证明三种金属的活动性,则电解质溶液最好选用___________ 。
A.0.5mol·L1氯化亚铁溶液
B.0.5mol·L1氯化铜溶液
C.0.5mol·L1盐酸
D.0.5mol·L1氯化亚铁和0.5mol·L1氯化铜混合溶液
Ⅱ、如图为甲烷燃料电池原理示意图。
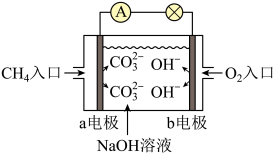
(3)甲烷通入的一极为电源的____________ 极,该电极反应式:____________
(4)当电路中累计有2mol电子通过时,消耗的氧气体积在标准状况下____________ L。
(1)用三种金属与盐酸反应的现象来判断,实验中除选择大小相同的金属片外,还需要控制
(2)某小组同学采用Zn、Fe作为电极,只用一个原电池证明三种金属的活动性,则电解质溶液最好选用
A.0.5mol·L1氯化亚铁溶液
B.0.5mol·L1氯化铜溶液
C.0.5mol·L1盐酸
D.0.5mol·L1氯化亚铁和0.5mol·L1氯化铜混合溶液
Ⅱ、如图为甲烷燃料电池原理示意图。

(3)甲烷通入的一极为电源的
(4)当电路中累计有2mol电子通过时,消耗的氧气体积在标准状况下
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平。下图表示了三种金属被人类开发利用的大致年限。

(1)上述图中的三种常用金属的开发利用之所以有先后,主要取决于____
(填选项序号)
A.金属的导电性强弱B.金属在地壳中的含量多少
C.金属的化合价高低D.金属的活动性大小
(2)早在西汉成书的《淮南万毕术》里,就有"曾青得铁则化为铜"的记载。曾青又有空青、白青、石胆、胆矾等名称其实都是天然的硫酸铜。
①写出"曾青得铁则化为铜"的离子方程式________________ 。
②若根据上述反应设计成原电池,请在方框中画出原电池的装置图,标出正、负极和电解质溶液,并写出电极反应式。

__________________
正极反应___________________________
负极反应___________________________
③设计一个实验方案,使如图装置中的铁棒上析出铜,而铁的质量不变。(可用文字叙述也可用图示意)。

______________________
(3)铁路工人常用铝热反应来焊接钢轨,写出有关的化学方程式_____________ 。教材中引发铝热反应的试剂是__________ 。

(1)上述图中的三种常用金属的开发利用之所以有先后,主要取决于
(填选项序号)
A.金属的导电性强弱B.金属在地壳中的含量多少
C.金属的化合价高低D.金属的活动性大小
(2)早在西汉成书的《淮南万毕术》里,就有"曾青得铁则化为铜"的记载。曾青又有空青、白青、石胆、胆矾等名称其实都是天然的硫酸铜。
①写出"曾青得铁则化为铜"的离子方程式
②若根据上述反应设计成原电池,请在方框中画出原电池的装置图,标出正、负极和电解质溶液,并写出电极反应式。

正极反应
负极反应
③设计一个实验方案,使如图装置中的铁棒上析出铜,而铁的质量不变。(可用文字叙述也可用图示意)。

(3)铁路工人常用铝热反应来焊接钢轨,写出有关的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】锌是人体的必需元素,可以促进人体的生长发育。但水体中如果含锌量超标,饮用后会导致急慢性锌中毒产生贫血等症状。纳米铝粉有很强的吸附性和还原性,常用于除去工业生产一水合甘氨酸锌的废水中过量的锌。
(1)写出Zn2+的核外电子排布式:________ 。
(2)一水合甘氨酸锌的结构简式如图所示,其中Zn2+的配位数为_________ 。

(3)相对于用纳米铁粉处理废水中Zn2+,使用纳米铝粉效率更高的原因是______ 。
(4)向含有甘氨酸锌的酸性废水中加入纳米铝粉,水中溶解的氧在纳米铝粉表面产生·OH,将甘氨酸锌中的有机基团(以甘氨酸根表示)降解,释放出的Zn2+被纳米铝粉去除。
①写出·OH氧化甘氨酸根(C2NH4O )生成NO
)生成NO 、CO2的离子方程式:
、CO2的离子方程式:_______ 。
②实验测得溶液中总氮含量[ ]随时间的变化如图所示,反应初期溶液中的总氮含量先迅速降低后随即上升的原因是
]随时间的变化如图所示,反应初期溶液中的总氮含量先迅速降低后随即上升的原因是________ 。

(1)写出Zn2+的核外电子排布式:
(2)一水合甘氨酸锌的结构简式如图所示,其中Zn2+的配位数为

(3)相对于用纳米铁粉处理废水中Zn2+,使用纳米铝粉效率更高的原因是
(4)向含有甘氨酸锌的酸性废水中加入纳米铝粉,水中溶解的氧在纳米铝粉表面产生·OH,将甘氨酸锌中的有机基团(以甘氨酸根表示)降解,释放出的Zn2+被纳米铝粉去除。
①写出·OH氧化甘氨酸根(C2NH4O
 )生成NO
)生成NO 、CO2的离子方程式:
、CO2的离子方程式:②实验测得溶液中总氮含量[
 ]随时间的变化如图所示,反应初期溶液中的总氮含量先迅速降低后随即上升的原因是
]随时间的变化如图所示,反应初期溶液中的总氮含量先迅速降低后随即上升的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】成都天府国际机场建设工程巨大,仅钢筋用量可修建11座法国埃菲尔铁塔。
(1)生铁和钢主要含铁和碳,生铁的含碳量比钢___________ 。(填“高”或“低”)
(2)铁制品锈蚀的实质是:铁与空气中的___________ 发生了化学反应。
(3)现代工业利用高炉炼铁,用赤铁矿石炼铁的原理是___________ 。(写化学方程式)
(4)某工厂利用铁与废硫酸反应制取硫酸亚铁。根据化学方程式计算,足量的铁与含 9.8t的废硫酸反应,可生产硫酸亚铁的质量是多少?
9.8t的废硫酸反应,可生产硫酸亚铁的质量是多少?________
(1)生铁和钢主要含铁和碳,生铁的含碳量比钢
(2)铁制品锈蚀的实质是:铁与空气中的
(3)现代工业利用高炉炼铁,用赤铁矿石炼铁的原理是
(4)某工厂利用铁与废硫酸反应制取硫酸亚铁。根据化学方程式计算,足量的铁与含
 9.8t的废硫酸反应,可生产硫酸亚铁的质量是多少?
9.8t的废硫酸反应,可生产硫酸亚铁的质量是多少?
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)随着生活水平的提高,人们越来越关注自身的健康。
①平时我们到药店能买到的药如阿司匹林属于___ (选填“R”或“OTC”)类;人体铁元素摄入量不足可能会导致___ 。
②“是药三分毒”说明药物在人体内可能产生不良反应,下列药物可能引起的不良反应叙述错误的是____ (填字母代号)。
A.青霉素一一过敏反应 B.阿司匹林——胃肠道反应 C.复方氢氧化铝——肠胃穿孔
③低血糖病症发作时,喝葡萄糖水可快速见效。葡萄糖作为营养剂供给人体能量,在体内发生的主要反应是___ (填字母代号)。
A.加成反应 B.取代反应 C.氧化反应 D.聚合反应
(2)材料是人类赖以生存的重要物质基础,而化学是材料科学发展的基础。
①在原子反应堆中广泛应用的钠钾合金在常温下呈液态。说明合金的熔点比其各成分金属的熔点___ (选填“高”或“低”)。
②炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会出现红褐色锈斑。我们将这种腐蚀方式称为___ 。
③人工合成的塑料有多种,其中聚丙烯是常见的食品级塑料,写出聚丙烯的结构简式___ 。
④世博会中国馆——“东方之冠”,它由钢筋混凝土、7000多块红色铝板和1200多块玻璃等建成。钢筋混凝土___ (选填“是”或“不是”)复合材料。
(3)可持续发展需要注意“环境保护”和“节约能源”。
①某污水处理厂处理含酸性物质、泥沙等的污水时,常先加入混凝剂,经曝气、沉砂后,再加入熟石灰处理,加入熟石灰的目的是___ 。
②汽车尾气的大量排放会引起环境污染,在机动车尾气系统中装置催化转化器,可将尾气中的NO、CO转化为无害的CO2和___ 。
(1)随着生活水平的提高,人们越来越关注自身的健康。
①平时我们到药店能买到的药如阿司匹林属于
②“是药三分毒”说明药物在人体内可能产生不良反应,下列药物可能引起的不良反应叙述错误的是_
A.青霉素一一过敏反应 B.阿司匹林——胃肠道反应 C.复方氢氧化铝——肠胃穿孔
③低血糖病症发作时,喝葡萄糖水可快速见效。葡萄糖作为营养剂供给人体能量,在体内发生的主要反应是
A.加成反应 B.取代反应 C.氧化反应 D.聚合反应
(2)材料是人类赖以生存的重要物质基础,而化学是材料科学发展的基础。
①在原子反应堆中广泛应用的钠钾合金在常温下呈液态。说明合金的熔点比其各成分金属的熔点
②炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会出现红褐色锈斑。我们将这种腐蚀方式称为
③人工合成的塑料有多种,其中聚丙烯是常见的食品级塑料,写出聚丙烯的结构简式
④世博会中国馆——“东方之冠”,它由钢筋混凝土、7000多块红色铝板和1200多块玻璃等建成。钢筋混凝土
(3)可持续发展需要注意“环境保护”和“节约能源”。
①某污水处理厂处理含酸性物质、泥沙等的污水时,常先加入混凝剂,经曝气、沉砂后,再加入熟石灰处理,加入熟石灰的目的是
②汽车尾气的大量排放会引起环境污染,在机动车尾气系统中装置催化转化器,可将尾气中的NO、CO转化为无害的CO2和
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】金属的用途和性质紧密相关。
(1)已知金属的物理性质有①导电性、②导热性、③延展性。请填表。
(2)铝是一种活泼金属,具有较强的还原性。
①金属铝在高温下与三氧化二铁反应,2Al+Fe2O3 Al2O3+2Fe,称为铝热反应。该反应中______是氧化剂,______是还原剂。
Al2O3+2Fe,称为铝热反应。该反应中______是氧化剂,______是还原剂。
②铝热反应不仅被用作焊接钢轨,还常用于冶炼熔点较高的金属,如钒、镉、锰等。用铝热反应原理从__________________。
(1)已知金属的物理性质有①导电性、②导热性、③延展性。请填表。
| 金属的用途 | 对应的金属物理性质 |
| 金可制成比纸还薄的金箔 | |
| 用铁、铝等做炊具 | |
| 用铜制作印刷电路 |
(2)铝是一种活泼金属,具有较强的还原性。
①金属铝在高温下与三氧化二铁反应,2Al+Fe2O3
 Al2O3+2Fe,称为铝热反应。该反应中______是氧化剂,______是还原剂。
Al2O3+2Fe,称为铝热反应。该反应中______是氧化剂,______是还原剂。②铝热反应不仅被用作焊接钢轨,还常用于冶炼熔点较高的金属,如钒、镉、锰等。用铝热反应原理从__________________。
您最近一年使用:0次



