根据要求,回答下列问题:
Ⅰ.有机物M经过太阳光光照可转化成有机物N,转化过程如下:

(1)两者中,较稳定的是:___________ (M或N)。
Ⅱ.已知: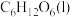 的燃烧热
的燃烧热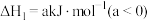 ;
; ,
,
(2)则
___________ a(填“>”“<”或“=”)。
Ⅲ.用如图所示的装置测定中和反应反应热。
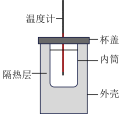
(3)从实验装置上看,还缺少___________ ,其能否用铁质材料替代?___________ (填“能”或“不能”)
(4)装置中隔热层的作用是___________
(5)实验中如果用相同体积、相同浓度的醋酸代替盐酸,测得的中和反应反应热的数值将___________ (填偏大、偏小或无影响)
Ⅰ.有机物M经过太阳光光照可转化成有机物N,转化过程如下:

(1)两者中,较稳定的是:
Ⅱ.已知:
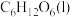 的燃烧热
的燃烧热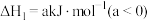 ;
; ,
,(2)则

Ⅲ.用如图所示的装置测定中和反应反应热。

(3)从实验装置上看,还缺少
(4)装置中隔热层的作用是
(5)实验中如果用相同体积、相同浓度的醋酸代替盐酸,测得的中和反应反应热的数值将
更新时间:2023-09-02 10:15:57
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如图:
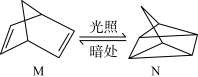 ΔH=+88.6 kJ/mol,
ΔH=+88.6 kJ/mol,
则M、N相比,较稳定的是_____ (用字母“M”或“N”表示)。
(2)已知CH3OH(l)的燃烧热ΔH=-238.6 kJ/mol,CH3OH(g)+O2(g)=CO2(g)+2H2O(l) ΔH=-a kJ/mol,则a_____ 238.6(填“>”“<”或“=”)。
(3)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+2N2(g) ⇌ Si3N4(s)+6CO(g),已知升高温度CO的浓度增大。
①该反应的焓变ΔH______ (填“>”“<”或“=”)0;
②降低温度,其平衡常数值将______ (填“增大”“减小”或“不变”);
③增大压强,N2的体积分数将_____ (填“增大”“减小”或“不变”)。
(1)有机物M经过太阳光光照可转化成N,转化过程如图:
 ΔH=+88.6 kJ/mol,
ΔH=+88.6 kJ/mol,则M、N相比,较稳定的是
(2)已知CH3OH(l)的燃烧热ΔH=-238.6 kJ/mol,CH3OH(g)+O2(g)=CO2(g)+2H2O(l) ΔH=-a kJ/mol,则a
(3)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+2N2(g) ⇌ Si3N4(s)+6CO(g),已知升高温度CO的浓度增大。
①该反应的焓变ΔH
②降低温度,其平衡常数值将
③增大压强,N2的体积分数将
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
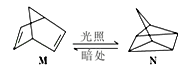 △H=+88.6kJ/mol
△H=+88.6kJ/mol
则M与N相比,较稳定的是____ 。
(2)已知CH3OH⑴的燃烧热为726.5kJ·mol-1,CH3OH(l) + l/2O2(g)=CO2(g)+2H2(g)
△H=-akJ·mol-1,则a_______ 726.5 (填“>”、“<”或 “=”)
(3)将Cl2和H2O(g)通过灼热的木炭层,生成HCl和CO2。当有1mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:______________________ 。
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料, 4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) △H=-1176kJ·mol-1,则27g铝粉完全反应放出的热量为_____________ 。
(5)已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) △H=+489.0 kJ • mol-1
CO(g)+l/2O2(g)=CO2(g) △H=-283. 0kJ • mol-1
C (石墨)+O2(g)=CO2(g) △H=-393.5kJ • mol-1
则4Fe (s)+3O2(g) =2Fe2O3 (s) △H=____________ 。
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
 △H=+88.6kJ/mol
△H=+88.6kJ/mol则M与N相比,较稳定的是
(2)已知CH3OH⑴的燃烧热为726.5kJ·mol-1,CH3OH(l) + l/2O2(g)=CO2(g)+2H2(g)
△H=-akJ·mol-1,则a
(3)将Cl2和H2O(g)通过灼热的木炭层,生成HCl和CO2。当有1mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料, 4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) △H=-1176kJ·mol-1,则27g铝粉完全反应放出的热量为
(5)已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) △H=+489.0 kJ • mol-1
CO(g)+l/2O2(g)=CO2(g) △H=-283. 0kJ • mol-1
C (石墨)+O2(g)=CO2(g) △H=-393.5kJ • mol-1
则4Fe (s)+3O2(g) =2Fe2O3 (s) △H=
您最近一年使用:0次
【推荐3】金刚石和石墨为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时完全燃烧生成二氧化碳,1mol金刚石和石墨分别与O2反应,放出的热量如图所示,回答下列问题:
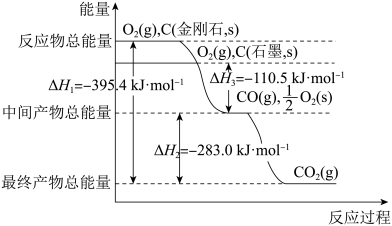
(1)金刚石、石墨与O2反应生成CO2均是_______ 反应(填“放热”或“吸热”),在通常状况下,金刚石和石墨的稳定性较大的是_______ (填“金刚石”或“石墨”);
(2)石墨的燃烧热△H=_______ kJ·mol-1,反应C(金刚石,s)=C(石墨,s)的反应热△H=_______ kJ·mol-1;
(3)12g石墨在一定量空气中燃烧,生成36g气体,该过程放出的热量为_______ kJ。

(1)金刚石、石墨与O2反应生成CO2均是
(2)石墨的燃烧热△H=
(3)12g石墨在一定量空气中燃烧,生成36g气体,该过程放出的热量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某实验小组用0.50mol/LNaOH溶液和0.50mol/L硫酸溶液进行中和热的测定。
I.配制0.50mol/LNaOH溶液
(1)若实验中大约要使用245mLNaOH溶液,则至少需要称量NaOH固体___________ g。
(2)从图1中选择称量NaOH固体所需要的仪器(填序号)___________ 。
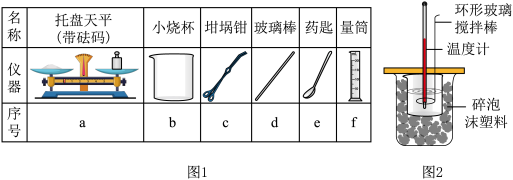
Ⅱ.测定中和热的实验装置如图2所示。取50mLNaOH溶液和30mL硫酸溶液进行实验,实验数据如下表。
(3)请填写下表中的空白:
(4)近似认为0.50mol/LNaOH溶液和0.50mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g·℃)。则中和热ΔH=___________ (取小数点后一位)。
(5)上述实验结果的数值与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)___________ 。
a.实验装置保温、隔热效果差
b.在量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
I.配制0.50mol/LNaOH溶液
(1)若实验中大约要使用245mLNaOH溶液,则至少需要称量NaOH固体
(2)从图1中选择称量NaOH固体所需要的仪器(填序号)

Ⅱ.测定中和热的实验装置如图2所示。取50mLNaOH溶液和30mL硫酸溶液进行实验,实验数据如下表。
(3)请填写下表中的空白:
| 温度 实验 次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
(5)上述实验结果的数值与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)
a.实验装置保温、隔热效果差
b.在量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据所学知识完成下列问题:
(1)某小组同学用量筒分别量取50mL的0.50mol∙L-1HC1溶液与50mL的0.55mol∙L-1NaOH溶液来测定中和热。
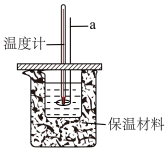
①仪器a是___________ (填名称)。
②近似认为0.55mol/L的NaOH溶液和0.50mol/L的HCl溶液的密度都是1g/mL,中和后生成溶液的比热容c=4.18J∙g-1∙℃-1,并忽略量热计的比热容;测得反应前、后体系的温度值(℃)分别为T0、T1,则所测中和热为△H=___________ kJ·mol-1(用含T0、T1的代数式表示)。
③若量取盐酸时候俯视刻度线,且其他操作无误,最终会使测得的中和热△H___________ (填“不变”、“变大”或“变小”)。
(2)研究氮和硫的氧化物的无害化处理对治理大气污染有着重要意义:
①已知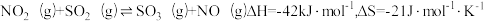 ,该反应能够自发进行的温度条件是
,该反应能够自发进行的温度条件是___________ K。
②将NO2和SO2以物质的量比1:2置于一体积不变的密闭容器中,在绝热条件下发生上述反应,下列不能说明该反应到达平衡状态的是:___________
a.每消耗1molNO2同时生成1molSO3 b.混合气体的颜色保持不变
c.体系的压强保持不变 d.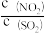 保持不变
保持不变
e.混合气体的平均摩尔质量保持不变
(3)HCN的电子式为___________ 。25℃时,HCN溶液与同浓度同体积的NaOH溶液充分反应后,最终pH为11.9,用离子方程式说明最终溶液虽碱性的原因:___________ 。
(4)阻燃剂Sb2O3(三氧化二铋)一般由SbCl3水解制备。实验室模拟制备过程如下:先将SbC13于一定条件下水解生成SbOC1白色沉淀,这一步的化学方程式为___________ ,再往其中加入少量氨水并搅拌,最终生成Sb2O3。
(1)某小组同学用量筒分别量取50mL的0.50mol∙L-1HC1溶液与50mL的0.55mol∙L-1NaOH溶液来测定中和热。

①仪器a是
②近似认为0.55mol/L的NaOH溶液和0.50mol/L的HCl溶液的密度都是1g/mL,中和后生成溶液的比热容c=4.18J∙g-1∙℃-1,并忽略量热计的比热容;测得反应前、后体系的温度值(℃)分别为T0、T1,则所测中和热为△H=
③若量取盐酸时候俯视刻度线,且其他操作无误,最终会使测得的中和热△H
(2)研究氮和硫的氧化物的无害化处理对治理大气污染有着重要意义:
①已知
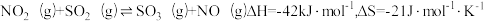 ,该反应能够自发进行的温度条件是
,该反应能够自发进行的温度条件是②将NO2和SO2以物质的量比1:2置于一体积不变的密闭容器中,在绝热条件下发生上述反应,下列不能说明该反应到达平衡状态的是:
a.每消耗1molNO2同时生成1molSO3 b.混合气体的颜色保持不变
c.体系的压强保持不变 d.
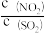 保持不变
保持不变e.混合气体的平均摩尔质量保持不变
(3)HCN的电子式为
(4)阻燃剂Sb2O3(三氧化二铋)一般由SbCl3水解制备。实验室模拟制备过程如下:先将SbC13于一定条件下水解生成SbOC1白色沉淀,这一步的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】化学是以实验为基础的学科,请回答以下问题:
I.利用如图所示装置测定中和热的实验步骤如下:
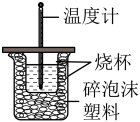
①用量筒量取50mL0.50mol·L-1盐酸倒入小烧杯中,测出盐酸温度;
②用另一量筒量取50mL 0.55mol·L-1 NaOH溶液,并用同一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。
回答下列问题:
(1)该图中有一处仪器未画出,它是_______ (填“仪器名称”)。
(2)倒入NaOH溶液时需一次性迅速倒入并立即盖上盖板,这样做的目的是_______ 。
(3)假设盐酸和氢氧化钠溶液的密度都是1 g·cm-3,又知中和反应后生成溶液的比热容c=4.2J·g-1·°C-1。
为了计算中和热,某学生实验记录数据如下:
该实验测得的中和热ΔH=_______ kJ·mol-1
II.现用0.1mol/LNa2S2O3溶液和0.1mol/LH2SO4溶液,研究不同条件对化学反应速率的影响。
【实验原理】 Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,反应过程中溶液出现乳白色浑浊和有刺激性气味的气体。
实验一:甲同学利用如图装置测定化学反应速率。

(4)除如图所示的实验用品外,还需要的实验仪器是_______ (填“名称”)。
实验二:乙同学得到各组实验数据如表。
(5)① V =_______
②实验I、III探究温度对化学反应速率的影响,实验测得t3<t1,则a_______ 20℃(填>、<或=)。
(6)已知50℃时c(S2O )与反应时间t的变化曲线如图。
)与反应时间t的变化曲线如图。
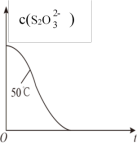
若保持其他条件不变,请在坐标图中画出25℃时c( S2O )~t的变化曲线示意图
)~t的变化曲线示意图_______ 。
I.利用如图所示装置测定中和热的实验步骤如下:

①用量筒量取50mL0.50mol·L-1盐酸倒入小烧杯中,测出盐酸温度;
②用另一量筒量取50mL 0.55mol·L-1 NaOH溶液,并用同一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。
回答下列问题:
(1)该图中有一处仪器未画出,它是
(2)倒入NaOH溶液时需一次性迅速倒入并立即盖上盖板,这样做的目的是
(3)假设盐酸和氢氧化钠溶液的密度都是1 g·cm-3,又知中和反应后生成溶液的比热容c=4.2J·g-1·°C-1。
为了计算中和热,某学生实验记录数据如下:
| 实验序号 | 起始温度t1/°C | 终止温度t2/°C | |
| 盐酸 | 氢氧化钠溶液 | 混合溶液 | |
| 1 | 20.0 | 20.2 | 23.2 |
| 2 | 20.2 | 20.4 | 23.2 |
| 3 | 20.5 | 20.6 | 25.6 |
II.现用0.1mol/LNa2S2O3溶液和0.1mol/LH2SO4溶液,研究不同条件对化学反应速率的影响。
【实验原理】 Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,反应过程中溶液出现乳白色浑浊和有刺激性气味的气体。
实验一:甲同学利用如图装置测定化学反应速率。

(4)除如图所示的实验用品外,还需要的实验仪器是
实验二:乙同学得到各组实验数据如表。
| 实验编号 | 加0.1mol/LNa2S2O3溶液的体积(mL) | 加水的体积(mL) | 加 0.1mol/LH2SO4溶液的体积(mL) | 水浴温度(℃) | 出现浑浊所用的时间(s) |
| I | 5 | 0 | 5 | 20 | t1 |
| II | 2 | V | 5 | 20 | t2 |
| III | 5 | 0 | 5 | a | t3 |
②实验I、III探究温度对化学反应速率的影响,实验测得t3<t1,则a
(6)已知50℃时c(S2O
 )与反应时间t的变化曲线如图。
)与反应时间t的变化曲线如图。
若保持其他条件不变,请在坐标图中画出25℃时c( S2O
 )~t的变化曲线示意图
)~t的变化曲线示意图
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】冬天常用煤炉燃煤取暖,夜里由于煤炉进气不足常导致煤气中毒事件发生。
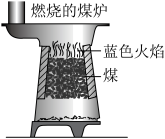
(1)等量的煤不充分燃烧放出的热量和完全燃烧相比有何变化_____ ?
(2)煤不完全燃烧放出的热量是不是标准燃烧热_____ ?

(1)等量的煤不充分燃烧放出的热量和完全燃烧相比有何变化
(2)煤不完全燃烧放出的热量是不是标准燃烧热
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知下列热化学方程式:
①2H2(g) +O2(g) = 2H2O(l) △H = -571.6 kJ/mol
②C(s) + O2(g) = CO2(g) △H = -393.5 kJ/mol
③C(s) + H2O(g) = CO(g) + H2(g) △H = +131.5 kJ/mol
请回答:
(1)上述反应中属于放热反应的是_______ (填序号),固体碳的燃烧热为_______ 。
(2)1molH2完全燃烧生成液态水,放出的热量为_______ 。
(3)依据事实,写出下列反应的热化学方程式。
①1molN2(g)与适量O2(g)反应生成NO(g),需吸收68 kJ的热量,该反应的热化学方程式为_______ 。
②已知HCl稀溶液与NaOH稀溶液反应生成1mol H2O时,放出57.3kJ热量,用离子方程式表示该反应的热化学方程为_______ 。
①2H2(g) +O2(g) = 2H2O(l) △H = -571.6 kJ/mol
②C(s) + O2(g) = CO2(g) △H = -393.5 kJ/mol
③C(s) + H2O(g) = CO(g) + H2(g) △H = +131.5 kJ/mol
请回答:
(1)上述反应中属于放热反应的是
(2)1molH2完全燃烧生成液态水,放出的热量为
(3)依据事实,写出下列反应的热化学方程式。
①1molN2(g)与适量O2(g)反应生成NO(g),需吸收68 kJ的热量,该反应的热化学方程式为
②已知HCl稀溶液与NaOH稀溶液反应生成1mol H2O时,放出57.3kJ热量,用离子方程式表示该反应的热化学方程为
您最近一年使用:0次
【推荐3】甲烷裂解法制取乙炔反应的化学方程式为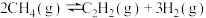 。
。
(1)已知断裂 下列化学键所吸收的能量数据:
下列化学键所吸收的能量数据:
则反应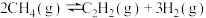 的
的
___________  。
。
(2)燃烧ag 生成二氧化碳气体和液态水,放出热量
生成二氧化碳气体和液态水,放出热量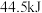 。经测定,生成的
。经测定,生成的 与足量澄清石灰水反应得到5g沉淀,则
与足量澄清石灰水反应得到5g沉淀,则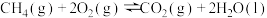

___________  ,其中a=
,其中a=___________ 。燃烧ag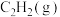 生成二氧化碳气体和液态水,放出热量
生成二氧化碳气体和液态水,放出热量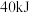 ,则
,则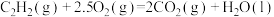

___________  。
。
(3)通氧气自热法生产 包含下列反应:
包含下列反应:
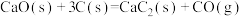
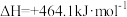
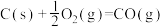
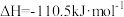
若不考虑热量耗散,物料转化率均为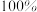 ,最终炉中出来的气体只有
,最终炉中出来的气体只有 。则为了维持热平衡,每生产
。则为了维持热平衡,每生产
 ,投料的量为
,投料的量为
 、
、___________ 
 及
及___________ 
 。
。
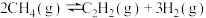 。
。(1)已知断裂
 下列化学键所吸收的能量数据:
下列化学键所吸收的能量数据:| 共价键 |  |  |  |
能量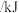 | 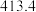 | 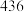 | 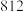 |
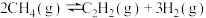 的
的
 。
。(2)燃烧ag
 生成二氧化碳气体和液态水,放出热量
生成二氧化碳气体和液态水,放出热量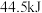 。经测定,生成的
。经测定,生成的 与足量澄清石灰水反应得到5g沉淀,则
与足量澄清石灰水反应得到5g沉淀,则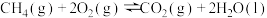

 ,其中a=
,其中a=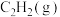 生成二氧化碳气体和液态水,放出热量
生成二氧化碳气体和液态水,放出热量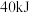 ,则
,则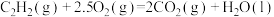

 。
。(3)通氧气自热法生产
 包含下列反应:
包含下列反应: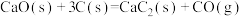
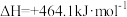
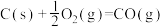
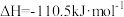
若不考虑热量耗散,物料转化率均为
 ,最终炉中出来的气体只有
,最终炉中出来的气体只有 。则为了维持热平衡,每生产
。则为了维持热平衡,每生产
 ,投料的量为
,投料的量为
 、
、
 及
及
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】已知:①CaCO3(s)=CaO+CO2(g) ΔH=+177.7 kJ·mol-1
②C(s)+H2O(g)=CO(g)+H2(g) ΔH=-131.3 kJ·mol-1
③C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
④CO(g)+ O2(g)=CO2(g) ΔH=-283 kJ·mol-1
O2(g)=CO2(g) ΔH=-283 kJ·mol-1
⑤ H2SO4(l)+NaOH(l)=
H2SO4(l)+NaOH(l)=  Na2SO4(l)+H2O(l) ΔH=-57.3 kJ·mol-1
Na2SO4(l)+H2O(l) ΔH=-57.3 kJ·mol-1
⑥HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) ΔH=-57.3 kJ·mol-1
⑦2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
(1)上述热化学方程式中,不正确的有___________ ,不正确的理由分别是:___________ 。
(2)根据上述信息,写出C转化为CO的热化学方程式___________ 。
(3)上述正确的热化学方程式中,表示燃烧热的热化学方程式有___________ ;表示中和热的热化学方程式有___________ 。
②C(s)+H2O(g)=CO(g)+H2(g) ΔH=-131.3 kJ·mol-1
③C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
④CO(g)+
 O2(g)=CO2(g) ΔH=-283 kJ·mol-1
O2(g)=CO2(g) ΔH=-283 kJ·mol-1⑤
 H2SO4(l)+NaOH(l)=
H2SO4(l)+NaOH(l)=  Na2SO4(l)+H2O(l) ΔH=-57.3 kJ·mol-1
Na2SO4(l)+H2O(l) ΔH=-57.3 kJ·mol-1⑥HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) ΔH=-57.3 kJ·mol-1
⑦2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
(1)上述热化学方程式中,不正确的有
(2)根据上述信息,写出C转化为CO的热化学方程式
(3)上述正确的热化学方程式中,表示燃烧热的热化学方程式有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】填空。
(1)1mol氢气完全燃烧生成液态水放热286kJ,则氢气燃烧的热化学方程式为:_______
(2)反应2H2+O2=2H2O的能量变化如图所示。已知拆开1molH2、1molO2和1molH-O中的化学键分别需要消耗436kJ、496kJ和463kJ能量,则反应过程(Ⅱ)_______ (填“吸收”或“放出”)_______ kJ能量。
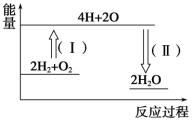
(1)1mol氢气完全燃烧生成液态水放热286kJ,则氢气燃烧的热化学方程式为:
(2)反应2H2+O2=2H2O的能量变化如图所示。已知拆开1molH2、1molO2和1molH-O中的化学键分别需要消耗436kJ、496kJ和463kJ能量,则反应过程(Ⅱ)

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知下列热化学方程式:
①2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ/mol
②C(s)+O2(g)=CO2(g) ΔH=-393.5kJ/mol
③C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131.5kJ/mol
请回答:
(1)上述反应中属于放热反应的是_____ (填序号,下同),属于吸热反应的是_______ 。
(2)2gH2完全燃烧生成液态水,放出的热量为_______ 。
(3)依据事实,写出下列反应的热化学方程式。
①1molN2(g)与适量O2(g)反应生成NO(g),需吸收68kJ的热量,该反应的热化学方程式为_____ 。
②在25℃、101kpa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为_______ 。
①2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ/mol
②C(s)+O2(g)=CO2(g) ΔH=-393.5kJ/mol
③C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131.5kJ/mol
请回答:
(1)上述反应中属于放热反应的是
(2)2gH2完全燃烧生成液态水,放出的热量为
(3)依据事实,写出下列反应的热化学方程式。
①1molN2(g)与适量O2(g)反应生成NO(g),需吸收68kJ的热量,该反应的热化学方程式为
②在25℃、101kpa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
您最近一年使用:0次



