碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
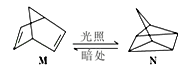 △H=+88.6kJ/mol
△H=+88.6kJ/mol
则M与N相比,较稳定的是____ 。
(2)已知CH3OH⑴的燃烧热为726.5kJ·mol-1,CH3OH(l) + l/2O2(g)=CO2(g)+2H2(g)
△H=-akJ·mol-1,则a_______ 726.5 (填“>”、“<”或 “=”)
(3)将Cl2和H2O(g)通过灼热的木炭层,生成HCl和CO2。当有1mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:______________________ 。
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料, 4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) △H=-1176kJ·mol-1,则27g铝粉完全反应放出的热量为_____________ 。
(5)已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) △H=+489.0 kJ • mol-1
CO(g)+l/2O2(g)=CO2(g) △H=-283. 0kJ • mol-1
C (石墨)+O2(g)=CO2(g) △H=-393.5kJ • mol-1
则4Fe (s)+3O2(g) =2Fe2O3 (s) △H=____________ 。
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
 △H=+88.6kJ/mol
△H=+88.6kJ/mol则M与N相比,较稳定的是
(2)已知CH3OH⑴的燃烧热为726.5kJ·mol-1,CH3OH(l) + l/2O2(g)=CO2(g)+2H2(g)
△H=-akJ·mol-1,则a
(3)将Cl2和H2O(g)通过灼热的木炭层,生成HCl和CO2。当有1mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料, 4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) △H=-1176kJ·mol-1,则27g铝粉完全反应放出的热量为
(5)已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) △H=+489.0 kJ • mol-1
CO(g)+l/2O2(g)=CO2(g) △H=-283. 0kJ • mol-1
C (石墨)+O2(g)=CO2(g) △H=-393.5kJ • mol-1
则4Fe (s)+3O2(g) =2Fe2O3 (s) △H=
更新时间:2017-10-16 23:59:06
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】已知一些烷烃的燃烧热如下表:
(1)热稳定性:正丁烷________ (填“>”或“<”)异丁烷。
(2)写出表示乙烷燃烧热的热化学方程式_____________________________________ 。
(3)相同物质的量的烷烃,碳原子数越多,燃烧放出的热量越_______ (填“多”或“少”)。
(4)有同学估计“正戊烷的燃烧热大约在3 540 kJ·mol−1左右”,你认为正确吗?______ 。理由是_______________________________________ 。
| 化合物 | 燃烧热/kJ·mol−1 | 化合物 | 燃烧热/kJ·mol−1 |
| 甲烷 | 891.0 | 正丁烷 | 2 878.0 |
| 乙烷 | 1 560.8 | 异丁烷 | 2 869.6 |
| 丙烷 | 2 221.5 | 异戊烷 | 3 531.3 |
(1)热稳定性:正丁烷
(2)写出表示乙烷燃烧热的热化学方程式
(3)相同物质的量的烷烃,碳原子数越多,燃烧放出的热量越
(4)有同学估计“正戊烷的燃烧热大约在3 540 kJ·mol−1左右”,你认为正确吗?
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某些以共价键结合的物质在气态时断裂每摩尔键吸收的能量数据如下表(单位:kJ∙mol-1):
(1)把1mol Cl2分解为气态原子时,需要______ (填“吸收”或“放出”)243kJ能量。
(2)由表中所列化学键形成的气体单质分子中,最稳定的是______ (填写化学式)。
(3)请写出氢气与碘气体反应的热化学方程式______ 。
共价键 |
|
|
|
|
|
|
|
|
|
能量数据 | 436 | 243 | 194 | 432 | 299 | 153 | 946 | 463 | 391 |
(2)由表中所列化学键形成的气体单质分子中,最稳定的是
(3)请写出氢气与碘气体反应的热化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知25℃、101kPa下,石墨、金刚石燃烧的热化学方程式分别为
C(石墨)+O2(g)=CO2(g)ΔH=-393.51kJ·mol-1
C(金刚石)+O2(g)=CO2(g)ΔH=-395.41kJ·mol-1
据此判断,下列说法中正确的是( )
A.由石墨制备金刚石是吸热反应;石墨的能量比金刚石的低
B.由石墨制备金刚石是吸热反应;石墨的能量比金刚石的高
C.由石墨制备金刚石是放热反应;石墨的能量比金刚石的低
D.由石墨制备金刚石是放热反应;石墨的能量比金刚石的高
相同温度时,下列两个反应的反应热分别用ΔH1和ΔH2表示,则( )
①H2(g)+ O2(g)=H2O(g)ΔH1=-Q1kJ·mol-1
O2(g)=H2O(g)ΔH1=-Q1kJ·mol-1
②2H2O(l)=2H2(g)+O2(g)ΔH2=+Q2kJ·mol-1
A.Q1>Q2 B.Q1=Q2 C.2Q1<Q2 D. Q2=Q1
Q2=Q1
C(石墨)+O2(g)=CO2(g)ΔH=-393.51kJ·mol-1
C(金刚石)+O2(g)=CO2(g)ΔH=-395.41kJ·mol-1
据此判断,下列说法中正确的是
A.由石墨制备金刚石是吸热反应;石墨的能量比金刚石的低
B.由石墨制备金刚石是吸热反应;石墨的能量比金刚石的高
C.由石墨制备金刚石是放热反应;石墨的能量比金刚石的低
D.由石墨制备金刚石是放热反应;石墨的能量比金刚石的高
相同温度时,下列两个反应的反应热分别用ΔH1和ΔH2表示,则
①H2(g)+
 O2(g)=H2O(g)ΔH1=-Q1kJ·mol-1
O2(g)=H2O(g)ΔH1=-Q1kJ·mol-1②2H2O(l)=2H2(g)+O2(g)ΔH2=+Q2kJ·mol-1
A.Q1>Q2 B.Q1=Q2 C.2Q1<Q2 D.
 Q2=Q1
Q2=Q1
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据已知信息,完成下列问题
(1)汽车尾气中的NOx是大气污染物之一。压缩天然气(CNG)汽车的优点之一是利用催化技术能够将NOx转变成无毒的CO2和N2。
已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1,
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2。
则2CH4(g)+4NO2(g)=2N2(g)+2CO2(g)+4H2O(g) ΔH3=____ (用ΔH1和ΔH2表示)。
(2)工业上用水煤气法制氢气,
已知:①C(s)+ O2(g)=CO(g) ΔH1=-110.5 kJ·mol-1,
O2(g)=CO(g) ΔH1=-110.5 kJ·mol-1,
②2H2(g)+O2(g)=2H2O(g) ΔH2=-483.6 kJ·mol-1。
则水煤气法制氢气C(s)+H2O(g)=CO(g)+H2(g) ΔH3=____ kJ·mol-1。
(3)Cu2O是一种半导体材料,
已知:①Cu2O(s)+1/2O2(g)=2CuO(s) ΔH1=-145 kJ·mol-1,
②CuO(s)+H2(g)=Cu(s)+H2O(l) ΔH2=-129 kJ·mol-1,
③H2(g)+1/2O2(g)=H2O(l) ΔH3=-285.8 kJ·mol-1。
则反应2Cu(s)+H2O(l)=Cu2O(s)+H2(g) ΔH4=____ kJ·mol-1。
(4)工业上由金红石(TiO2)制取单质Ti,
已知:①C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ·mol-1,
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566.0 kJ·mol-1,
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) ΔH3=+141.0 kJ·mol-1。
则反应TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g) ΔH4=____ kJ·mol-1。
(5)工业上用天然气制备CH3OH。
已知:①CH4(g)+O2(g)=CO(g)+H2(g)+H2O(g) ΔH1=-321.5 kJ·mol-1,
②CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH2=+250.3 kJ·mol-1,
③CO(g)+2H2(g)=CH3OH(g) ΔH3=-90.0 kJ·mol-1。
则CH4(g)与O2(g)反应生成CH3OH(g)的热化学方程式为____ 。
(6)已知1mol N2H4(l)在O2(g)中燃烧,生成N2(g)和H2O(l),放出622 kJ热量,则N2H4(l)燃烧的热化学方程式为____ 。
(7)已知0.5mol CH4(g)完全燃烧,生成CO2(g)和H2O(l)时,放出445 kJ热量,则CH4(g)燃烧的热化学方程式为____ 。
(8)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。已知在300℃、Fe做催化剂时,在氨气足量的情况下,烟气中c(NO2):c(NO)=1:1时脱氮效果最佳,且生成1mol N2(g)反应放出的热量为Q kJ(Q>0),此时对应的脱氮反应的热化学方程式为____ 。
(1)汽车尾气中的NOx是大气污染物之一。压缩天然气(CNG)汽车的优点之一是利用催化技术能够将NOx转变成无毒的CO2和N2。
已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1,
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2。
则2CH4(g)+4NO2(g)=2N2(g)+2CO2(g)+4H2O(g) ΔH3=
(2)工业上用水煤气法制氢气,
已知:①C(s)+
 O2(g)=CO(g) ΔH1=-110.5 kJ·mol-1,
O2(g)=CO(g) ΔH1=-110.5 kJ·mol-1,②2H2(g)+O2(g)=2H2O(g) ΔH2=-483.6 kJ·mol-1。
则水煤气法制氢气C(s)+H2O(g)=CO(g)+H2(g) ΔH3=
(3)Cu2O是一种半导体材料,
已知:①Cu2O(s)+1/2O2(g)=2CuO(s) ΔH1=-145 kJ·mol-1,
②CuO(s)+H2(g)=Cu(s)+H2O(l) ΔH2=-129 kJ·mol-1,
③H2(g)+1/2O2(g)=H2O(l) ΔH3=-285.8 kJ·mol-1。
则反应2Cu(s)+H2O(l)=Cu2O(s)+H2(g) ΔH4=
(4)工业上由金红石(TiO2)制取单质Ti,
已知:①C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ·mol-1,
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566.0 kJ·mol-1,
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) ΔH3=+141.0 kJ·mol-1。
则反应TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g) ΔH4=
(5)工业上用天然气制备CH3OH。
已知:①CH4(g)+O2(g)=CO(g)+H2(g)+H2O(g) ΔH1=-321.5 kJ·mol-1,
②CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH2=+250.3 kJ·mol-1,
③CO(g)+2H2(g)=CH3OH(g) ΔH3=-90.0 kJ·mol-1。
则CH4(g)与O2(g)反应生成CH3OH(g)的热化学方程式为
(6)已知1mol N2H4(l)在O2(g)中燃烧,生成N2(g)和H2O(l),放出622 kJ热量,则N2H4(l)燃烧的热化学方程式为
(7)已知0.5mol CH4(g)完全燃烧,生成CO2(g)和H2O(l)时,放出445 kJ热量,则CH4(g)燃烧的热化学方程式为
(8)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。已知在300℃、Fe做催化剂时,在氨气足量的情况下,烟气中c(NO2):c(NO)=1:1时脱氮效果最佳,且生成1mol N2(g)反应放出的热量为Q kJ(Q>0),此时对应的脱氮反应的热化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图中:E1=134kJ·mol-1,E2=368kJ·mol-1,根据要求回答问题:

(1)如图是1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是_____ (填“增大”“减小”或“不变”,下同),ΔH的变化是_____ 。请写出NO2(g)和CO(g)反应生成CO2(g)和NO(g)的热化学方程式:_____ 。
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应的热化学方程式如下:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0kJ·mol-1
②CH3OH(g)+ O2(g)=CO2(g)+2H2(g) ΔH=-192.9kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9kJ·mol-1
又知③H2O(g)=H2O(l) ΔH=-44kJ·mol-1,则甲醇蒸气燃烧为液态水的热化学方程式为_____ 。
(3)已知在常温常压下:
④2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=-1275.6kJ·mol-1
⑤2CO(g)+O2(g)=2CO2(g) ΔH=-566.0kJ·mol-1
⑥H2O(g)=H2O(l) ΔH=-44.0kJ·mol-1
请写出1mol甲醇不完全燃烧生成1mol一氧化碳和液态水的热化学方程式:_____ 。

(1)如图是1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应的热化学方程式如下:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0kJ·mol-1
②CH3OH(g)+
 O2(g)=CO2(g)+2H2(g) ΔH=-192.9kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9kJ·mol-1又知③H2O(g)=H2O(l) ΔH=-44kJ·mol-1,则甲醇蒸气燃烧为液态水的热化学方程式为
(3)已知在常温常压下:
④2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=-1275.6kJ·mol-1
⑤2CO(g)+O2(g)=2CO2(g) ΔH=-566.0kJ·mol-1
⑥H2O(g)=H2O(l) ΔH=-44.0kJ·mol-1
请写出1mol甲醇不完全燃烧生成1mol一氧化碳和液态水的热化学方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2 )在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g) CH 3OH(g)+H2O(g) △H2
CH 3OH(g)+H2O(g) △H2
③CO2(g)+H2(g) CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3
已知反应①中相关的化学键键能数据如下:
回答下列问题:
(1)CH3OH中氧在周期表中位于___ ,属于___ 区元素,与其同周期相邻两种元素原子的第一电离能由大到小的顺序为___ (用元素符号表示),其原因是___ 。
(2)写出CH3OH的结构式___ ;反应①的热化学方程式(热量用具体数值表示)___ 。
(3)当△H2=-58kJ mol-1,则△H3=__ kJ mol-1。
(4)CO和H2的混合气体又称水煤气,可由水和煤在一定条件下产生,写出该反应的化学方程式___ 。
①CO(g)+2H2(g)
 CH3OH(g) △H1
CH3OH(g) △H1②CO2(g)+3H2(g)
 CH 3OH(g)+H2O(g) △H2
CH 3OH(g)+H2O(g) △H2③CO2(g)+H2(g)
 CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3已知反应①中相关的化学键键能数据如下:
| 化学键 | H—H | C—O |  | H—O | C—H |
| E/(kJ mol-1) | 436 | 343 | 1076 | 465 | 413 |
回答下列问题:
(1)CH3OH中氧在周期表中位于
(2)写出CH3OH的结构式
(3)当△H2=-58kJ mol-1,则△H3=
(4)CO和H2的混合气体又称水煤气,可由水和煤在一定条件下产生,写出该反应的化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】Ⅰ.已知下列反应的反应热:
(1)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l);;△H1=-870.3kJ/mol
(2)C(s)+O2(g)=CO2(g);ΔH2=-393.5 kJ/mol
(3)H2(g)+1/2O2(g)=H2O(l);△H3=-285.8kJ/mol
试计算下列反应的反应热:2C(s)+2H2(g)+O2(g) = CH3COOH(l);ΔH=___________ ;CH3COOH(l)的燃烧热是________ ;在(3)式中,当有71.45KJ的热量放出时需要燃烧标准状况下的H2___________ 升。
Ⅱ.已知下列两个热化学方程式;
2H2(g)+O2(g)===2H2O(1); △H=-570.kJ/mol
C3H8(g)+5O2(g)===3CO2(g)+4H2O(1); △H=-2220.0kJ/mol
(1)实验测得H2和C3H8的混合气体共1mol,完全燃烧生成液态水时放热1252.5kJ,则混合气体中H2和C3H8的体积比是________________ 。
(2)已知:H2O(1)=H2O(g);△H=+44.0kJ/mol,写出丙烷燃烧生成CO2和气态水的热化学方程式____________
Ⅲ.8 g硫磺在 O2中完全燃烧生成SO2气体,放出的热量是74.2KJ,则生成标准状况下的二氧化硫体积是_____________ L,热化学方程式为______________________________________ 。产生的SO2用NaOH溶液吸收,最少需要NaOH____________________ mol
(1)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l);;△H1=-870.3kJ/mol
(2)C(s)+O2(g)=CO2(g);ΔH2=-393.5 kJ/mol
(3)H2(g)+1/2O2(g)=H2O(l);△H3=-285.8kJ/mol
试计算下列反应的反应热:2C(s)+2H2(g)+O2(g) = CH3COOH(l);ΔH=
Ⅱ.已知下列两个热化学方程式;
2H2(g)+O2(g)===2H2O(1); △H=-570.kJ/mol
C3H8(g)+5O2(g)===3CO2(g)+4H2O(1); △H=-2220.0kJ/mol
(1)实验测得H2和C3H8的混合气体共1mol,完全燃烧生成液态水时放热1252.5kJ,则混合气体中H2和C3H8的体积比是
(2)已知:H2O(1)=H2O(g);△H=+44.0kJ/mol,写出丙烷燃烧生成CO2和气态水的热化学方程式
Ⅲ.8 g硫磺在 O2中完全燃烧生成SO2气体,放出的热量是74.2KJ,则生成标准状况下的二氧化硫体积是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知:
①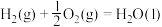

②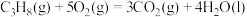
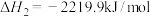
(1)在25℃和101kPa下, 和
和 的混合气体5mol完全燃烧生成
的混合气体5mol完全燃烧生成 和液态水,放出6264.2kJ的热量。计算混合气体中
和液态水,放出6264.2kJ的热量。计算混合气体中 和
和 的体积比
的体积比___________ 。
(2)已知:
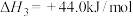 。写出
。写出 燃烧生成
燃烧生成 和水蒸气的热化学方程式
和水蒸气的热化学方程式___________ 。
①
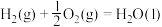

②
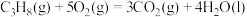
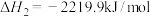
(1)在25℃和101kPa下,
 和
和 的混合气体5mol完全燃烧生成
的混合气体5mol完全燃烧生成 和液态水,放出6264.2kJ的热量。计算混合气体中
和液态水,放出6264.2kJ的热量。计算混合气体中 和
和 的体积比
的体积比(2)已知:

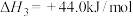 。写出
。写出 燃烧生成
燃烧生成 和水蒸气的热化学方程式
和水蒸气的热化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.摩托罗拉公司开发了一种以甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可以连续使用一个月。已知该电池的总反应式为:2CH3OH+3O2+4KOH 2K2CO3+6H2O,请填空:
2K2CO3+6H2O,请填空:
(1)放电时,负极的电极反应式为____ 。
(2)通入甲醇一端的电极是__ 极,电池在放电过程中溶液的pH将__ (填“上升”“下降”或“不变”)。
(3)若在常温、常压下,1gCH3CH2OH燃烧生成CO2和液态水时放出29.7kJ的热量,表示该反应的热化学方程式为__
II.(4)CO无色无味有毒,世界各国每年均有不少人因CO中毒而失去生命。一种CO分析仪的工作原理如图所示,该装置中电解质为氧化钇—氧化钠,其中O2—可以在固体介质NASICON中自由移动。传感器中通过的电流越大,尾气中CO的含量越高,请回答:a极电极反应式为___ 。

III.(5)如图为某实验小组依据氧化还原反应:(用离子方程式表示)____ 设计的原电池装置,反应前,电极质量相等,一段时间后,两电极质量相差12g,导线中通过____ mol电子。

 2K2CO3+6H2O,请填空:
2K2CO3+6H2O,请填空:(1)放电时,负极的电极反应式为
(2)通入甲醇一端的电极是
(3)若在常温、常压下,1gCH3CH2OH燃烧生成CO2和液态水时放出29.7kJ的热量,表示该反应的热化学方程式为
II.(4)CO无色无味有毒,世界各国每年均有不少人因CO中毒而失去生命。一种CO分析仪的工作原理如图所示,该装置中电解质为氧化钇—氧化钠,其中O2—可以在固体介质NASICON中自由移动。传感器中通过的电流越大,尾气中CO的含量越高,请回答:a极电极反应式为

III.(5)如图为某实验小组依据氧化还原反应:(用离子方程式表示)

您最近半年使用:0次












