Ⅰ.已知下列反应的反应热:
(1)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l);;△H1=-870.3kJ/mol
(2)C(s)+O2(g)=CO2(g);ΔH2=-393.5 kJ/mol
(3)H2(g)+1/2O2(g)=H2O(l);△H3=-285.8kJ/mol
试计算下列反应的反应热:2C(s)+2H2(g)+O2(g) = CH3COOH(l);ΔH=___________ ;CH3COOH(l)的燃烧热是________ ;在(3)式中,当有71.45KJ的热量放出时需要燃烧标准状况下的H2___________ 升。
Ⅱ.已知下列两个热化学方程式;
2H2(g)+O2(g)===2H2O(1); △H=-570.kJ/mol
C3H8(g)+5O2(g)===3CO2(g)+4H2O(1); △H=-2220.0kJ/mol
(1)实验测得H2和C3H8的混合气体共1mol,完全燃烧生成液态水时放热1252.5kJ,则混合气体中H2和C3H8的体积比是________________ 。
(2)已知:H2O(1)=H2O(g);△H=+44.0kJ/mol,写出丙烷燃烧生成CO2和气态水的热化学方程式____________
Ⅲ.8 g硫磺在 O2中完全燃烧生成SO2气体,放出的热量是74.2KJ,则生成标准状况下的二氧化硫体积是_____________ L,热化学方程式为______________________________________ 。产生的SO2用NaOH溶液吸收,最少需要NaOH____________________ mol
(1)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l);;△H1=-870.3kJ/mol
(2)C(s)+O2(g)=CO2(g);ΔH2=-393.5 kJ/mol
(3)H2(g)+1/2O2(g)=H2O(l);△H3=-285.8kJ/mol
试计算下列反应的反应热:2C(s)+2H2(g)+O2(g) = CH3COOH(l);ΔH=
Ⅱ.已知下列两个热化学方程式;
2H2(g)+O2(g)===2H2O(1); △H=-570.kJ/mol
C3H8(g)+5O2(g)===3CO2(g)+4H2O(1); △H=-2220.0kJ/mol
(1)实验测得H2和C3H8的混合气体共1mol,完全燃烧生成液态水时放热1252.5kJ,则混合气体中H2和C3H8的体积比是
(2)已知:H2O(1)=H2O(g);△H=+44.0kJ/mol,写出丙烷燃烧生成CO2和气态水的热化学方程式
Ⅲ.8 g硫磺在 O2中完全燃烧生成SO2气体,放出的热量是74.2KJ,则生成标准状况下的二氧化硫体积是
更新时间:2019-01-01 16:34:54
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】在日常生活和工农业生产中经常涉及到吸热反应和放热反应,回答下面问题:
(1)下列反应一定属于吸热反应的是____ 。
(2)在101kPa时,H2在1.0molO2中完全燃烧,生成2.0mol液态水,放出571.6k的热量,表示氢气燃烧的热化学方程式为____ ,氢气的燃烧热为____ kJ•mol-1。
(3)我国科学家利用计算机模拟了甲醇(CH3OH)与水在铜基催化剂上的反应机理和能量图如图:
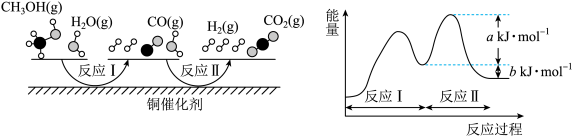
①反应I的△H____ 0(填“<”“>”或“=”),反应II的活化能是____ kJ•mol-1。
②在相同条件下反应I的反应速率____ (填“<”“>”或“=”)反应II的反应速率。
③写出反应II的热化学方程式____ 。
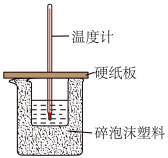
(4)取30mL0.5mol•L-1H2SO4溶液与50mL0.5mol•L-1NaOH溶液于小烧杯中,用如图所示装置进行中和反应反应热的测定实验。
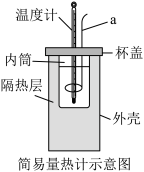
①仪器a的名称是____ 。
②利用温度计记录某一次实验,最少需要测量____ 次温度。
③若实验中测得中和热数值总是偏小,可能的原因是____ (答出一条即可)。
(1)下列反应一定属于吸热反应的是
| A.酸碱中和反应 | B.燃烧反应 |
| C.铝热反应 | D.C(s)+CO2(g)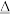 2CO(g) 2CO(g) |
(3)我国科学家利用计算机模拟了甲醇(CH3OH)与水在铜基催化剂上的反应机理和能量图如图:

①反应I的△H
②在相同条件下反应I的反应速率
③写出反应II的热化学方程式
(4)取30mL0.5mol•L-1H2SO4溶液与50mL0.5mol•L-1NaOH溶液于小烧杯中,用如图所示装置进行中和反应反应热的测定实验。

①仪器a的名称是
②利用温度计记录某一次实验,最少需要测量
③若实验中测得中和热数值总是偏小,可能的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】请回答:
(1)氨遇氯化氢时会产生白烟,写出白烟化学成分的电子式:___________ 。
(2)氨的催化氧化是工业制硝酸的基础,写出化学方程式___________ 。
(3)写出铝和NaOH溶液反应的离子方程式___________ 。
(4)工业上可用氨水吸收燃煤烟气中少量的SO2,写出离子方程式___________ 。
(5)氯气与二氧化硫混合后通入某有色溶液,漂白能力减弱的原因___________ (用离子方程式说明) 。
(6)肼( )的结构式为
)的结构式为___________
(7)已知298K时,正丁烷、异丁烷完全燃烧的热化学方程式分别为:
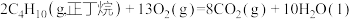
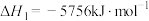
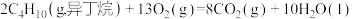

则该温度下,正丁烷转化为异丁烷的热化学方程式为___________ 。
(8)稀溶液中,1molH2SO4与NaOH完全反应时,放出114.6kJ热量,写出表示中和热的热化学方程式___________ 。
(9)Ti基态的电子排布式为___________ 。
(10)l配合物[TiCl(H2O)5]Cl2·H2O。1mol该配合物中含有δ键的数目为___________ 。
(1)氨遇氯化氢时会产生白烟,写出白烟化学成分的电子式:
(2)氨的催化氧化是工业制硝酸的基础,写出化学方程式
(3)写出铝和NaOH溶液反应的离子方程式
(4)工业上可用氨水吸收燃煤烟气中少量的SO2,写出离子方程式
(5)氯气与二氧化硫混合后通入某有色溶液,漂白能力减弱的原因
(6)肼(
 )的结构式为
)的结构式为(7)已知298K时,正丁烷、异丁烷完全燃烧的热化学方程式分别为:
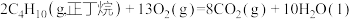
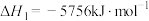
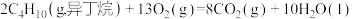

则该温度下,正丁烷转化为异丁烷的热化学方程式为
(8)稀溶液中,1molH2SO4与NaOH完全反应时,放出114.6kJ热量,写出表示中和热的热化学方程式
(9)Ti基态的电子排布式为
(10)l配合物[TiCl(H2O)5]Cl2·H2O。1mol该配合物中含有δ键的数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】饮用水中的N主要来自于NH4+。已知在微生物的作用下, NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下:
1molNH4+全部被氧化成NO3-的热化学方程式为________________________________ 。
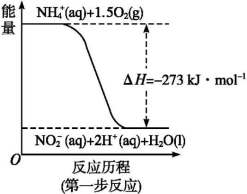
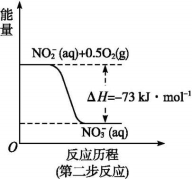
1molNH4+全部被氧化成NO3-的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】当前能源危机是一个全球性问题,开源节流是应对能源危机的重要举措。
(1)下列做法不利于能源“开源节流”的是________ (填字母)。
A.开发太阳能、水能、风能等新能源,减少使用煤、石油等化石燃料
B.研究采煤、采油新技术,提高产量以满足工业生产的快速发展
C.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
D.减少资源消耗、增加资源的重复使用和资源的循环再生

(2)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。则在通常状况下,金刚石和石墨相比较,_________ (填 “金刚石”或“石墨”)更稳定,石墨的燃烧热ΔH=______________ 。
(3)N2、O2分子中化学键的键能分别是946 kJ/mol、497kJ/mol。已知:N2(g)+O2(g)=2NO(g) ΔH=+180.0 kJ/mol。NO分子中化学键的键能为_____ 。
(4)综合上述有关信息,请写出用CO除去NO生成无污染气体的热化学方程式:_______________ 。
(1)下列做法不利于能源“开源节流”的是
A.开发太阳能、水能、风能等新能源,减少使用煤、石油等化石燃料
B.研究采煤、采油新技术,提高产量以满足工业生产的快速发展
C.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
D.减少资源消耗、增加资源的重复使用和资源的循环再生

(2)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。则在通常状况下,金刚石和石墨相比较,
(3)N2、O2分子中化学键的键能分别是946 kJ/mol、497kJ/mol。已知:N2(g)+O2(g)=2NO(g) ΔH=+180.0 kJ/mol。NO分子中化学键的键能为
(4)综合上述有关信息,请写出用CO除去NO生成无污染气体的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)N2H4和H2O2混合可作火箭推进剂,已知:16g液态N2H4和足量氧气反应生成N2(g)和H2O(l),放出310.6kJ的热量;2H2O2(l)=O2(g)+2H2O(l) ΔH=-196.4kJ·mol-1。反应N2H4(g)+O2(g)=N2(g)+2H2O(l)的ΔH=__ kJ·mol-1。N2H4和H2O2反应生成N2(g)和H2O(l)的热化学方程式为__ 。
(2)已知拆开1mol氢气中的化学键需要消耗436kJ能量,拆开1mol氧气中的化学键需要消耗498kJ能量,根据下面的能量图,回答下列问题::
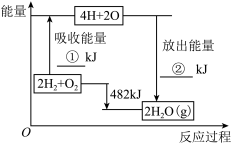
分别写出①、②的数值:①__ kJ;②__ kJ。
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=-1275.6kJ·mol-1
②H2O(l)=H2O(g) ΔH=+44.0kJ·mol-1
写出表示甲醇燃烧热的热化学方程式__ 。
(4)实验室用50mL0.50mol·L-1盐酸与50mL某浓度的NaOH溶液在如图所示装置中反应,通过测定反应过程中所放出的热量可计算中和热。该装置有两处明显的错误,其中一处是缺少一种玻璃仪器,该仪器的名称为__ ;实验室提供了0.50mol·L-1和0.55mol·L-1两种浓度的NaOH溶液,应选择__ mol·L-1的NaOH溶液进行实验。
(2)已知拆开1mol氢气中的化学键需要消耗436kJ能量,拆开1mol氧气中的化学键需要消耗498kJ能量,根据下面的能量图,回答下列问题::

分别写出①、②的数值:①
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=-1275.6kJ·mol-1
②H2O(l)=H2O(g) ΔH=+44.0kJ·mol-1
写出表示甲醇燃烧热的热化学方程式
(4)实验室用50mL0.50mol·L-1盐酸与50mL某浓度的NaOH溶液在如图所示装置中反应,通过测定反应过程中所放出的热量可计算中和热。该装置有两处明显的错误,其中一处是缺少一种玻璃仪器,该仪器的名称为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】Ⅰ.(1)当1 g氨气完全分解为N2和H2时,吸收2.7kJ的热量,写出其热化学方程式:___________________________________________________________ 。
(2)HCl和NaOH反应的中和热ΔH=-57.3kJ·mol-1,则H2SO4和NaOH反应的中和热的热化学方程式为____________________________________________ 。
Ⅱ.已知下列反应,回答下列问题:
2CO(g)+O2(g)=2CO2(g) △H=﹣566kJ/mol ①
Na2O2(s)+CO2(g)=Na2CO3(s)+ O2(g) △H=﹣266kJ/mol ②
O2(g) △H=﹣266kJ/mol ②
(1)CO的燃烧热为______________ 。
(2)在催化剂作用下,一氧化碳可与过氧化钠反应生成固体碳酸钠,该反应的热化学方程式为:______________________________________________________________ 。
(3)已知反应①中的相关的化学键键能数据如下:则a=____________ kJ/mol
(2)HCl和NaOH反应的中和热ΔH=-57.3kJ·mol-1,则H2SO4和NaOH反应的中和热的热化学方程式为
Ⅱ.已知下列反应,回答下列问题:
2CO(g)+O2(g)=2CO2(g) △H=﹣566kJ/mol ①
Na2O2(s)+CO2(g)=Na2CO3(s)+
 O2(g) △H=﹣266kJ/mol ②
O2(g) △H=﹣266kJ/mol ②(1)CO的燃烧热为
(2)在催化剂作用下,一氧化碳可与过氧化钠反应生成固体碳酸钠,该反应的热化学方程式为:
(3)已知反应①中的相关的化学键键能数据如下:则a=
| 化学键 | C=O(CO2) | C  O(CO) O(CO) | O=O |
| E/(kJ.mol-1) | 803.5 | 1076 | a |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】为流少大气污染。科学家采取多种措施处理工业废气中排放的氮氧化物( )、
)、 、
、 等。回答下列问题:
等。回答下列问题:
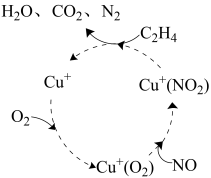
(1)某脱硝反应机理如图所示, 的作用为
的作用为_______ ,此过程总反应的方程式为_______ 。
(2)选择性催化还原技术(SCR)是目前较为成熟脱硝技术,其反应原理主要为: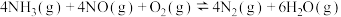
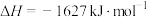 。
。
①若反应过程放出热量为32.54 kJ,则除去的NO物质的量为_______ 。
②不考虑催化剂因素,催化还原时应控制反应温度在315~400℃之间,反应温度不宜过高的原因是_______ 。
(3) 是性能优良的脱硫脱硝试剂,常温下,
是性能优良的脱硫脱硝试剂,常温下, 的含
的含 的盐溶液中,
的盐溶液中, 能把
能把 氧化生成硫酸盐,自身被还原成
氧化生成硫酸盐,自身被还原成 ,该反应的离子方程式为
,该反应的离子方程式为_______ ,反应一段时间后溶液pH_______ (填“增大”或“减小”)
 )、
)、 、
、 等。回答下列问题:
等。回答下列问题:
(1)某脱硝反应机理如图所示,
 的作用为
的作用为(2)选择性催化还原技术(SCR)是目前较为成熟脱硝技术,其反应原理主要为:
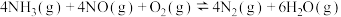
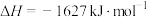 。
。①若反应过程放出热量为32.54 kJ,则除去的NO物质的量为
②不考虑催化剂因素,催化还原时应控制反应温度在315~400℃之间,反应温度不宜过高的原因是
(3)
 是性能优良的脱硫脱硝试剂,常温下,
是性能优良的脱硫脱硝试剂,常温下, 的含
的含 的盐溶液中,
的盐溶液中, 能把
能把 氧化生成硫酸盐,自身被还原成
氧化生成硫酸盐,自身被还原成 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.摩托罗拉公司开发了一种以甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可以连续使用一个月。已知该电池的总反应式为:2CH3OH+3O2+4KOH 2K2CO3+6H2O,请填空:
2K2CO3+6H2O,请填空:
(1)放电时,负极的电极反应式为____ 。
(2)通入甲醇一端的电极是__ 极,电池在放电过程中溶液的pH将__ (填“上升”“下降”或“不变”)。
(3)若在常温、常压下,1gCH3CH2OH燃烧生成CO2和液态水时放出29.7kJ的热量,表示该反应的热化学方程式为__
II.(4)CO无色无味有毒,世界各国每年均有不少人因CO中毒而失去生命。一种CO分析仪的工作原理如图所示,该装置中电解质为氧化钇—氧化钠,其中O2—可以在固体介质NASICON中自由移动。传感器中通过的电流越大,尾气中CO的含量越高,请回答:a极电极反应式为___ 。

III.(5)如图为某实验小组依据氧化还原反应:(用离子方程式表示)____ 设计的原电池装置,反应前,电极质量相等,一段时间后,两电极质量相差12g,导线中通过____ mol电子。

 2K2CO3+6H2O,请填空:
2K2CO3+6H2O,请填空:(1)放电时,负极的电极反应式为
(2)通入甲醇一端的电极是
(3)若在常温、常压下,1gCH3CH2OH燃烧生成CO2和液态水时放出29.7kJ的热量,表示该反应的热化学方程式为
II.(4)CO无色无味有毒,世界各国每年均有不少人因CO中毒而失去生命。一种CO分析仪的工作原理如图所示,该装置中电解质为氧化钇—氧化钠,其中O2—可以在固体介质NASICON中自由移动。传感器中通过的电流越大,尾气中CO的含量越高,请回答:a极电极反应式为

III.(5)如图为某实验小组依据氧化还原反应:(用离子方程式表示)

您最近一年使用:0次



