饮用水中的N主要来自于NH4+。已知在微生物的作用下, NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下:
1molNH4+全部被氧化成NO3-的热化学方程式为________________________________ 。
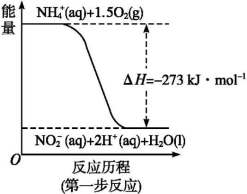
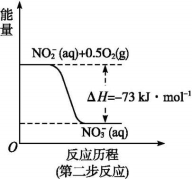
1molNH4+全部被氧化成NO3-的热化学方程式为
2019高三·全国·专题练习 查看更多[1]
(已下线)2019高考备考一轮复习精品资料 第二章 化学物质及其变化第4讲 守恒思想在化学中的应用——守恒法解题技巧【教学案】
更新时间:2018-09-13 22:35:24
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】依据事实,写出下列反应的热化学方程式
(1)适量的N2和O2完全反应,每生成23 g NO2吸收16.95 kJ热量。N2与O2反应的热化学方程式为_______________________________________ 。
(2)18 g葡萄糖与适量O2反应,生成CO2和液态水,放出280.4 kJ热量。葡萄糖燃烧的热化学方程式为__________________________________________ 。
(3)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O。已知室温下2 g SiH4自燃放出热量89.2 kJ。SiH4自燃的热化学方程式为____________________________________ 。
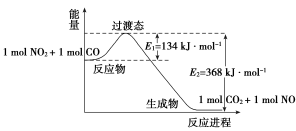
(4)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:____________________________________ 。
(5)直接排放煤燃烧产生的烟气会引起严重的环境问题。煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2Og)ΔH1=-867 kJ·mol-1①
2NO2(g) N2O4(g) ΔH2=-56.9 kJ·mol-1②
N2O4(g) ΔH2=-56.9 kJ·mol-1②
写出CH4(g)催化还原N2O4(g)生成N2(g)和H2O(g)的热化学方程式________________________ 。
(1)适量的N2和O2完全反应,每生成23 g NO2吸收16.95 kJ热量。N2与O2反应的热化学方程式为
(2)18 g葡萄糖与适量O2反应,生成CO2和液态水,放出280.4 kJ热量。葡萄糖燃烧的热化学方程式为
(3)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O。已知室温下2 g SiH4自燃放出热量89.2 kJ。SiH4自燃的热化学方程式为
(4)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:

(5)直接排放煤燃烧产生的烟气会引起严重的环境问题。煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2Og)ΔH1=-867 kJ·mol-1①
2NO2(g)
 N2O4(g) ΔH2=-56.9 kJ·mol-1②
N2O4(g) ΔH2=-56.9 kJ·mol-1②写出CH4(g)催化还原N2O4(g)生成N2(g)和H2O(g)的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求回答下列问题:
(1)已知在200℃,101kPa时,H2与碘蒸气作用生成1mol HI放出7.45kJ热量,则该反应的热化学方程式为_______________________________________ 。
(2)太阳能的开发和利用是21世纪一个重要课题。利用储能介质储存太阳能的原理是:白天在太阳照射下使某种盐熔化,吸收热量,晚间熔盐固化释放出相应能量。已知下列数据:
其中最适宜作为储能介质的是________ 。(选填物质序号)
(3)离子晶体晶格能的定义是气态离子形成1mol离子晶体释放的能量,通常取正值。现已知: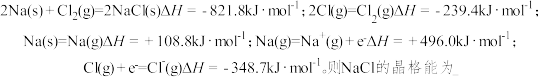
______________ 。
(1)已知在200℃,101kPa时,H2与碘蒸气作用生成1mol HI放出7.45kJ热量,则该反应的热化学方程式为
(2)太阳能的开发和利用是21世纪一个重要课题。利用储能介质储存太阳能的原理是:白天在太阳照射下使某种盐熔化,吸收热量,晚间熔盐固化释放出相应能量。已知下列数据:
| 序号 | 盐 | 熔点/℃ | 熔化热/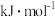 | 参考价格/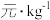 |
| ① | CaCl2·6H2O | 29.0 | 37.3 | 780~850 |
| ② | Na2SO4·10H2O | 32.4 | 77.0 | 800~900 |
| ③ | Na2HPO4·12H2O | 36.1 | 100.1 | 1800~2400 |
| ④ | Na2SiO3·5H2O | 52.5 | 49.7 | 1400~1800 |
其中最适宜作为储能介质的是
(3)离子晶体晶格能的定义是气态离子形成1mol离子晶体释放的能量,通常取正值。现已知:
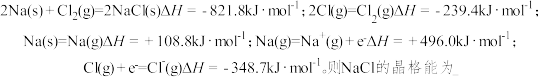
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求写热化学方程式:
(1)已知稀溶液中,1 mol H2SO4与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式__________ 。
(2)已知在25℃、101kPa下,1 g乙醇在氧气中充分燃烧生成二氧化碳和液态水释放出29.7 kJ的热量,试写出乙醇燃烧热的热化学方程式_______________ 。
(3)标准状况下,4.48L H2在足量O2中完全燃烧放出热量Q kJ,写出H2燃烧的热化学方程式_________________________________ 。
(1)已知稀溶液中,1 mol H2SO4与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式
(2)已知在25℃、101kPa下,1 g乙醇在氧气中充分燃烧生成二氧化碳和液态水释放出29.7 kJ的热量,试写出乙醇燃烧热的热化学方程式
(3)标准状况下,4.48L H2在足量O2中完全燃烧放出热量Q kJ,写出H2燃烧的热化学方程式
您最近一年使用:0次
【推荐1】物质的摩尔燃烧焓是指在一定温度和压强条件下,1mol物质完全氧化为同温下的指定产物时的焓变,其中物质中所含的N元素氧化为N2(g)、H元素氧化为H2O(l)、C元素氧化为CO2(g)。
已知:①几种物质的摩尔燃烧焓:
②298k,101kPa时,部分化学键键能:
③H2O(l)=H2O(g) △H=+44.0kJ/mol
回答下列问题:
(1)计算反应2CO(g)+O2(g)=2CO2(g)的焓变△H1=___________ kJ·mol-1,由此可求CO的化学键C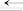 O键能a=
O键能a=___________ kJ·mol-1。
(2)已知相同条件下,石墨比金刚石稳定,则1mol金刚石的燃烧放热___________ 393.5kJ(填“>”、“<”、“=”)。
(3)写出常温下氢气燃烧的热化学方程式___________ ,则反应CO(g)+H2O(g)=CO2(g)+H2(g)的焓变△H2=___________ kJ·mol-1。
已知:①几种物质的摩尔燃烧焓:
| 物质 | 石墨(s) | H2(g) | CO(g) |
| △H/(kJ·mol—1) | -393.5 | -285.8 | -283.0 |
②298k,101kPa时,部分化学键键能:
| 化学键 | C O O | O=O | C=O | C-O |
| E/(kJ·mol-1) | a | 498 | 745 | 351 |
③H2O(l)=H2O(g) △H=+44.0kJ/mol
回答下列问题:
(1)计算反应2CO(g)+O2(g)=2CO2(g)的焓变△H1=
 O键能a=
O键能a=(2)已知相同条件下,石墨比金刚石稳定,则1mol金刚石的燃烧放热
(3)写出常温下氢气燃烧的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知下列热化学方程式:
① H2(g)+ O2(g)=H2O(l) ΔH =―285kJ/mol
O2(g)=H2O(l) ΔH =―285kJ/mol
② H2(g)+ O2(g)=H2O(g) ΔH =―241.8kJ/mol
O2(g)=H2O(g) ΔH =―241.8kJ/mol
③ C(s)+ O2(g)=CO(g) ΔH =―110.4 kJ/mol
O2(g)=CO(g) ΔH =―110.4 kJ/mol
④ C(s)+ O2(g)=CO2(g) ΔH =―393.5 kJ/mol
回答下列各问:
(1)上述反应中属于放热反应的是___________ 。
(2)C的燃烧热为_________________ 。
(3)燃烧10g H2生成液态水,放出的热量为_____________________ 。
(4)CO燃烧的热化学方程式为______________________ 。
(5)为了控制温室效应,各国科学家提出了不少设想。有人根据液态CO2密度大于海水密度的事实,设想将CO2液化后,送入深海海底,以减少大气中的CO2。为使CO2液化,可采取的措施________ 。
a 减压、升温 b 增压、降温
c 减压、降温 d 增压、升温
① H2(g)+
 O2(g)=H2O(l) ΔH =―285kJ/mol
O2(g)=H2O(l) ΔH =―285kJ/mol② H2(g)+
 O2(g)=H2O(g) ΔH =―241.8kJ/mol
O2(g)=H2O(g) ΔH =―241.8kJ/mol③ C(s)+
 O2(g)=CO(g) ΔH =―110.4 kJ/mol
O2(g)=CO(g) ΔH =―110.4 kJ/mol④ C(s)+ O2(g)=CO2(g) ΔH =―393.5 kJ/mol
回答下列各问:
(1)上述反应中属于放热反应的是
(2)C的燃烧热为
(3)燃烧10g H2生成液态水,放出的热量为
(4)CO燃烧的热化学方程式为
(5)为了控制温室效应,各国科学家提出了不少设想。有人根据液态CO2密度大于海水密度的事实,设想将CO2液化后,送入深海海底,以减少大气中的CO2。为使CO2液化,可采取的措施
a 减压、升温 b 增压、降温
c 减压、降温 d 增压、升温
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】空气污染问题日益引起全民关注。
(1)汽车尾气中存在大量的CO、NO、NO2和碳氢化合物,可采用铂等贵金属作为催化剂,使CO和NO转化为无毒的气体,请写出其化学方程式____________________________
(2)科研工作者研究出利用石灰乳除工业燃煤尾气中的硫 (SO2、SO3)和氮 (NO、NO2)的新工艺,既能净化尾气,又能获得应用广泛的CaSO4 和Ca(NO3)2 。

①硫酸型酸雨的形成过程是大气中的SO2 溶于雨水生成某种弱酸,在空气中经催化氧化生成硫酸,该过程中反应的化学方程式为____________________________ 、 ______________________________
②CaSO4 可以调节水泥的硬化时间。尾气中 SO2 与石灰乳反应生成CaSO4 的化学方程式为___________________________
③ Ca(NO3)2可制成混凝土防冻剂、钢筋阻锈剂等.尾气中NO、NO2与石灰乳反应生成Ca(NO3)2的化学方程式___________________________
(3)还可用NaClO2溶液(溶液呈碱性)作为吸收剂,对含有SO2和NOX的燃煤烟气进行脱硫、脱硝。(已知:酸性条件下,ClO2-会转化成ClO2和Cl-。ClO2是黄绿色、易溶于水的气体,具有强氧化性,能氧化SO2或NOX)在鼓泡反应期中通入含SO2和NO的烟气,反应温度为323K,NaClO2溶液的浓度为5×10-3mol·L-1。反应一段时间后溶液中离子浓度的分析结果如下表。
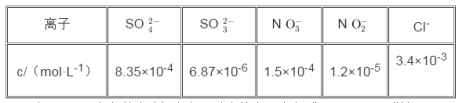
①写出NaClO2溶液脱硝过程中主要反应的离子方程式_____________________________ 。增加压强,NO的转化率_______ (填“提高”、“不变”或“降低”)。
②随着吸收反应的进行,吸收剂溶液的pH逐渐__________ (填“提高”、“不变”或“减小”)。
(1)汽车尾气中存在大量的CO、NO、NO2和碳氢化合物,可采用铂等贵金属作为催化剂,使CO和NO转化为无毒的气体,请写出其化学方程式
(2)科研工作者研究出利用石灰乳除工业燃煤尾气中的硫 (SO2、SO3)和氮 (NO、NO2)的新工艺,既能净化尾气,又能获得应用广泛的CaSO4 和Ca(NO3)2 。

①硫酸型酸雨的形成过程是大气中的SO2 溶于雨水生成某种弱酸,在空气中经催化氧化生成硫酸,该过程中反应的化学方程式为
②CaSO4 可以调节水泥的硬化时间。尾气中 SO2 与石灰乳反应生成CaSO4 的化学方程式为
③ Ca(NO3)2可制成混凝土防冻剂、钢筋阻锈剂等.尾气中NO、NO2与石灰乳反应生成Ca(NO3)2的化学方程式
(3)还可用NaClO2溶液(溶液呈碱性)作为吸收剂,对含有SO2和NOX的燃煤烟气进行脱硫、脱硝。(已知:酸性条件下,ClO2-会转化成ClO2和Cl-。ClO2是黄绿色、易溶于水的气体,具有强氧化性,能氧化SO2或NOX)在鼓泡反应期中通入含SO2和NO的烟气,反应温度为323K,NaClO2溶液的浓度为5×10-3mol·L-1。反应一段时间后溶液中离子浓度的分析结果如下表。

①写出NaClO2溶液脱硝过程中主要反应的离子方程式
②随着吸收反应的进行,吸收剂溶液的pH逐渐
您最近一年使用:0次



