物质的摩尔燃烧焓是指在一定温度和压强条件下,1mol物质完全氧化为同温下的指定产物时的焓变,其中物质中所含的N元素氧化为N2(g)、H元素氧化为H2O(l)、C元素氧化为CO2(g)。
已知:①几种物质的摩尔燃烧焓:
②298k,101kPa时,部分化学键键能:
③H2O(l)=H2O(g) △H=+44.0kJ/mol
回答下列问题:
(1)计算反应2CO(g)+O2(g)=2CO2(g)的焓变△H1=___________ kJ·mol-1,由此可求CO的化学键C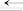 O键能a=
O键能a=___________ kJ·mol-1。
(2)已知相同条件下,石墨比金刚石稳定,则1mol金刚石的燃烧放热___________ 393.5kJ(填“>”、“<”、“=”)。
(3)写出常温下氢气燃烧的热化学方程式___________ ,则反应CO(g)+H2O(g)=CO2(g)+H2(g)的焓变△H2=___________ kJ·mol-1。
已知:①几种物质的摩尔燃烧焓:
| 物质 | 石墨(s) | H2(g) | CO(g) |
| △H/(kJ·mol—1) | -393.5 | -285.8 | -283.0 |
②298k,101kPa时,部分化学键键能:
| 化学键 | C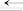 O O | O=O | C=O | C-O |
| E/(kJ·mol-1) | a | 498 | 745 | 351 |
③H2O(l)=H2O(g) △H=+44.0kJ/mol
回答下列问题:
(1)计算反应2CO(g)+O2(g)=2CO2(g)的焓变△H1=
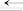 O键能a=
O键能a=(2)已知相同条件下,石墨比金刚石稳定,则1mol金刚石的燃烧放热
(3)写出常温下氢气燃烧的热化学方程式
更新时间:2021-05-11 08:15:05
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】回答下列问题
(1)丙烷热值较高,污染较小,是一种优良的燃料。试回答下列问题:
①如图是一定量丙烷完全燃烧生成 和
和 过程中的能量变化叫反应物图,在图中的括号内填入的是
过程中的能量变化叫反应物图,在图中的括号内填入的是___________ (填“+”或“-”)。
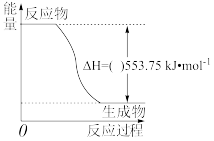
②写出表示丙烷燃烧热的热化学方程式:___________ 。
③二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1mol二甲醚完全燃烧生成 和液态水放出1455kJ热量。若1mol丙烷和二甲醚的混合气体完全燃烧生成
和液态水放出1455kJ热量。若1mol丙烷和二甲醚的混合气体完全燃烧生成 液态水共放出1645kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为
液态水共放出1645kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为___________ 。
(2)回答下列问题:
①已知:Ⅰ.
Ⅱ.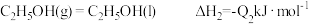
Ⅲ.
若使46g液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为___________ kJ。
②碳(s)在氧气供应不充足时,生成CO同时还部分生成CO2,因此无法通过实验直接测得反应: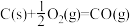 的
的 ,但可设计实验利用盖斯定律计算出该反应的
,但可设计实验利用盖斯定律计算出该反应的 ,计算时需要测得的实验数据有
,计算时需要测得的实验数据有___________ 。
(1)丙烷热值较高,污染较小,是一种优良的燃料。试回答下列问题:
①如图是一定量丙烷完全燃烧生成
 和
和 过程中的能量变化叫反应物图,在图中的括号内填入的是
过程中的能量变化叫反应物图,在图中的括号内填入的是
②写出表示丙烷燃烧热的热化学方程式:
③二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1mol二甲醚完全燃烧生成
 和液态水放出1455kJ热量。若1mol丙烷和二甲醚的混合气体完全燃烧生成
和液态水放出1455kJ热量。若1mol丙烷和二甲醚的混合气体完全燃烧生成 液态水共放出1645kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为
液态水共放出1645kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为(2)回答下列问题:
①已知:Ⅰ.

Ⅱ.
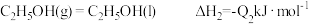
Ⅲ.

若使46g液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为
②碳(s)在氧气供应不充足时,生成CO同时还部分生成CO2,因此无法通过实验直接测得反应:
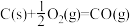 的
的 ,但可设计实验利用盖斯定律计算出该反应的
,但可设计实验利用盖斯定律计算出该反应的 ,计算时需要测得的实验数据有
,计算时需要测得的实验数据有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)已知下列数据:
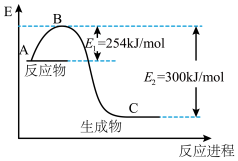
如图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量变化示意图,试根据表中及图中数据计算N-H的键能______________ 。
(2)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)=N2O4(l) ΔH1=-19.5 kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534.2 kJ·mol-1
写出肼和N2O4反应的热化学方程式______________________________ 。
(3)若用标准状况下4.48LO2氧化N2H4至N2,整个过程中转移的电子总数为___________ (阿伏加 德罗常数用NA表示)。
| 化学键 | H-H | N≡N |
| 键能/kJ·mol-1 | 435 | 943 |
如图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量变化示意图,试根据表中及图中数据计算N-H的键能

(2)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)=N2O4(l) ΔH1=-19.5 kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534.2 kJ·mol-1
写出肼和N2O4反应的热化学方程式
(3)若用标准状况下4.48LO2氧化N2H4至N2,整个过程中转移的电子总数为
您最近一年使用:0次
【推荐1】氧化还原反应在人类生活中应用非常广泛。
(Ⅰ)钢铁“发蓝”是在钢铁的表面形成一层Fe3O4的技术过程。经过“发蓝”处理的钢铁制品不易生锈,经久耐用。某厂对钢铁制品进行“发蓝”处理时发生反应的化学方程式如下(其中反应②未配平):
①3Fe+NaNO2+5NaOH=3Na2FeO2+H2O+NH3↑
②___ Na2FeO2+___ NaNO2+____ H2O →____ Na2Fe2O4+____ NH3↑+ _____ NaOH
③ Na2FeO2+ Na2Fe2O4+2H2O = Fe3O4+4NaOH
(1)请把反应②的系数填入上述相应位置的横线上。其中__________ 元素被氧化。
(2)上述3个反应中氧化剂共有_______ 种,氧化剂的化学式是___________________ 。
(3)如果有3.36L NH3(标准状况下)生成,则上述反应中还原剂总共失去电子________ 个。
(Ⅱ)发射火箭时常用肼(N2H4)为燃料,二氧化氮作氧化剂,两者反应生成氮气和水蒸气。已知4g N2H4(g)在上述反应中放出71kJ的热量,热化学方程式为_________________ 。
(Ⅰ)钢铁“发蓝”是在钢铁的表面形成一层Fe3O4的技术过程。经过“发蓝”处理的钢铁制品不易生锈,经久耐用。某厂对钢铁制品进行“发蓝”处理时发生反应的化学方程式如下(其中反应②未配平):
①3Fe+NaNO2+5NaOH=3Na2FeO2+H2O+NH3↑
②
③ Na2FeO2+ Na2Fe2O4+2H2O = Fe3O4+4NaOH
(1)请把反应②的系数填入上述相应位置的横线上。其中
(2)上述3个反应中氧化剂共有
(3)如果有3.36L NH3(标准状况下)生成,则上述反应中还原剂总共失去电子
(Ⅱ)发射火箭时常用肼(N2H4)为燃料,二氧化氮作氧化剂,两者反应生成氮气和水蒸气。已知4g N2H4(g)在上述反应中放出71kJ的热量,热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氢气既能与氮气又能与氧气发生反应,但是反应的条件却不相同。已知:
2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ·mol-1
3H2(g)+N2(g)=2NH3(g) ΔH=-92.4kJ·mol-1

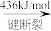
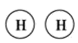
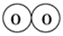
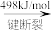

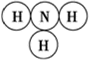
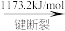

计算断裂1 molN≡N键需要消耗能量________ kJ,氮气分子中化学键比氧气分子中的化学键________ (填“强”或“弱”),因此氢气与二者反应的条件不同。
2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ·mol-1
3H2(g)+N2(g)=2NH3(g) ΔH=-92.4kJ·mol-1

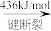
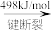


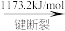

计算断裂1 molN≡N键需要消耗能量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求填空
(1)某反应A(g)+B(g)= C(g)+D(g)过程中的能量变化如图所示,回答问题。
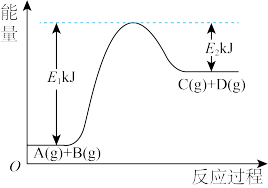
该反应是_______ (填“吸热”或“放热”)反应,该反应过程中,断裂旧化学键吸收的总能量_______ (填“>”“ <”或“=”)形成新化学键释放的总能量。
(2)由金红石(TiO2)制取单质Ti的步骤为:

已知:Ⅰ.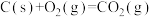

Ⅱ.
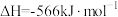
Ⅲ.
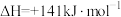
①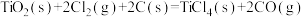 的
的
_______ kJ/mol。
②若已知2H2(g)+O2(g)=2H2O(g) ΔH1=-Q1
2H2(g)+O2(g)=2H2O(l) ΔH2=-Q2
则Q1_______ Q2(填“>”、“<”或“=”)。
(3)在2 L密闭容器中,800 ℃时反应2NO(g)+O2(g) 2NO2(g) ΔH<0体系中,各成分浓度随时间的变化如图所示。
2NO2(g) ΔH<0体系中,各成分浓度随时间的变化如图所示。
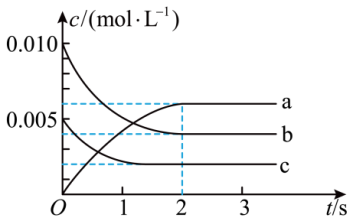
①用O2表示0~2 s内该反应的平均速率v =_______ mol/(L·s)。
②能使该反应的反应速率增大,且平衡向正反应方向移动的是_______ 。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效的催化剂
③达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a时改变的条件可能是_______ 。
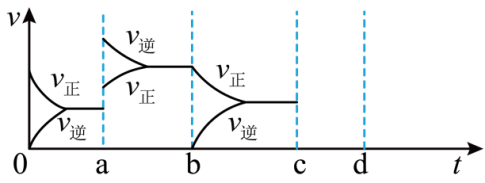
A.升温 B.增大压强 C.加入生成物 D.加入催化剂
(4)已知:①C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
②2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
现有0.2 mol木炭粉和氢气组成的悬浮气,在氧气中完全燃烧,共放出67.93 kJ的热量,则混合物中C与H2的物质的量之比为
A.1∶2 B.1∶1 C.2∶3 D.3∶2
(1)某反应A(g)+B(g)= C(g)+D(g)过程中的能量变化如图所示,回答问题。

该反应是
(2)由金红石(TiO2)制取单质Ti的步骤为:

已知:Ⅰ.
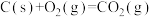

Ⅱ.

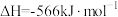
Ⅲ.

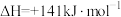
①
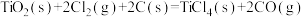 的
的
②若已知2H2(g)+O2(g)=2H2O(g) ΔH1=-Q1
2H2(g)+O2(g)=2H2O(l) ΔH2=-Q2
则Q1
(3)在2 L密闭容器中,800 ℃时反应2NO(g)+O2(g)
 2NO2(g) ΔH<0体系中,各成分浓度随时间的变化如图所示。
2NO2(g) ΔH<0体系中,各成分浓度随时间的变化如图所示。
①用O2表示0~2 s内该反应的平均速率v =
②能使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效的催化剂
③达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a时改变的条件可能是

A.升温 B.增大压强 C.加入生成物 D.加入催化剂
(4)已知:①C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
②2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
现有0.2 mol木炭粉和氢气组成的悬浮气,在氧气中完全燃烧,共放出67.93 kJ的热量,则混合物中C与H2的物质的量之比为
A.1∶2 B.1∶1 C.2∶3 D.3∶2
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】已知拆开1 mol氢气中的化学键需要消耗436 kJ能量,拆开1 mol氧气中的化学键需要消耗498 kJ能量,根据如图中的能量图,回答下列问题:

(1)分别写出①②的数值:
①__________ ;②__________ 。
(2)生成H2(Xg)中的1 mol H—O键放出__________ kJ的能量。
(3)已知:H2O(l)二H2O(g)△H=+44 kJ • mol−1,试写出氢气在氧气中完全燃烧生成液态水的热化学方程式:___________________________________ 。

(1)分别写出①②的数值:
①
(2)生成H2(Xg)中的1 mol H—O键放出
(3)已知:H2O(l)二H2O(g)△H=+44 kJ • mol−1,试写出氢气在氧气中完全燃烧生成液态水的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】人们常常利用化学反应中的能量变化为人类服务。
(1)氢能是一种具有发展前景的理想清洁能源,氢气燃烧时放出大量的热。氢气燃烧生成水蒸气的能量变化如下图所示:
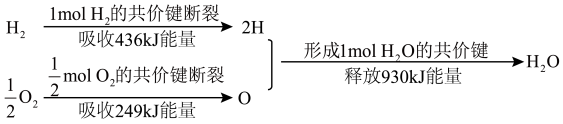
根据上图可知,1molH2完全燃烧生成1molH2O(气态)时,释放的能量是___________ kJ。
(2)下列化学反应在理论上可以设计成原电池的是___________ 。
A.Fe+2FeCl3=3FeCl2 B.SO3+H2O=H2SO4
C.CH4+2O2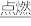 CO2+2H2O D.Ba(OH)2+H2SO4=BaSO4+2H2O
CO2+2H2O D.Ba(OH)2+H2SO4=BaSO4+2H2O
(3)下图是某兴趣小组设计的原电池示意图,实验结束后,在实验报告上记录信息如下:
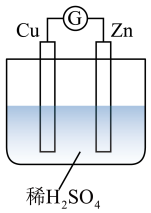
①实验报告中记录合理的是___________ (填序号)。
②请写出该电池的负极反应式___________ 。
③若有1mol电子流过导线,则理论上产生H2的质量为___________ g。
④将稀H2SO4换成CuSO4溶液电极质量增加的是___________ (填“锌极”或“铜极”,下同),溶液中SO 移向
移向___________ 。
(1)氢能是一种具有发展前景的理想清洁能源,氢气燃烧时放出大量的热。氢气燃烧生成水蒸气的能量变化如下图所示:

根据上图可知,1molH2完全燃烧生成1molH2O(气态)时,释放的能量是
(2)下列化学反应在理论上可以设计成原电池的是
A.Fe+2FeCl3=3FeCl2 B.SO3+H2O=H2SO4
C.CH4+2O2
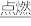 CO2+2H2O D.Ba(OH)2+H2SO4=BaSO4+2H2O
CO2+2H2O D.Ba(OH)2+H2SO4=BaSO4+2H2O(3)下图是某兴趣小组设计的原电池示意图,实验结束后,在实验报告上记录信息如下:

| a.电流计指针偏转 |
| b.Cu极有H2产生 |
| c.H+向负极移动 |
| d.电流由Zn经导线流向Cu |
①实验报告中记录合理的是
②请写出该电池的负极反应式
③若有1mol电子流过导线,则理论上产生H2的质量为
④将稀H2SO4换成CuSO4溶液电极质量增加的是
 移向
移向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】化学反应的变化通常表现为热量的变化,反应热的研究对于化学学科的发展具有重要意义。
(1)“即热饭盒”为生活带来便利,它可利用_____ (填序号)反应放出的热量来加热食物。
(2)1-甲基萘(1-MN)可制备四氢萘类物质(MTLs,包括1-MTL和5-MTL)。反应过程中伴有生成1-MD的副反应,涉及反应如图。

已知一定条件下反应R1、R2、R3的焓变分别为ΔH1、ΔH2、ΔH3,则反应R4的焓变为______ (用含ΔH1、ΔH2、ΔH3的代数式表示)。
(3)研究和深度开发CO2的综合利用,实现碳循环是解决温室问题的有效途径,对构建生态文明社会具有重要意义。CO2可实现以下转化:
①2CO2(g)+2H2O(l) C2H4(g)+3O2(g) ΔH=akJ•mol-1
C2H4(g)+3O2(g) ΔH=akJ•mol-1
②C2H4(g)+H2O(l) C2H5OH(l) ΔH=bkJ•mol-1
C2H5OH(l) ΔH=bkJ•mol-1
2CO2(g)+3H2O(l) C2H5OH(l)+3O2(g)正反应的活化能为ckJ•mol-1,则逆反应的活化能为
C2H5OH(l)+3O2(g)正反应的活化能为ckJ•mol-1,则逆反应的活化能为______ kJ•mol-1(用含a、b、c的代数式表示)。
(4)已知,在25℃和101kPa下,部分化学键的键能(kJ·mol-1)数据如表所示。
①在25℃和101kPa下,工业合成氨每生成1molNH3(g)放出46kJ热量,在该条件下,向某容器中加入2molN2(g)、6molH2(g)及合适的催化剂,充分反应后测得其放出的热量小于92kJ,原因可能是_____ ,表中的x=_____ 。
②科学家发现一种新的气态分子N4( )。在25℃和101kPa下N4(g)转化为N2(g)的热化学方程式为
)。在25℃和101kPa下N4(g)转化为N2(g)的热化学方程式为______ 。由此可知,N4(g)与N2(g)中更稳定的是_____ (填化学式)。
(1)“即热饭盒”为生活带来便利,它可利用
| A.浓硫酸和水 | B.生石灰和水 | C.纯碱和水 | D.食盐和白醋 |

已知一定条件下反应R1、R2、R3的焓变分别为ΔH1、ΔH2、ΔH3,则反应R4的焓变为
(3)研究和深度开发CO2的综合利用,实现碳循环是解决温室问题的有效途径,对构建生态文明社会具有重要意义。CO2可实现以下转化:
①2CO2(g)+2H2O(l)
 C2H4(g)+3O2(g) ΔH=akJ•mol-1
C2H4(g)+3O2(g) ΔH=akJ•mol-1②C2H4(g)+H2O(l)
 C2H5OH(l) ΔH=bkJ•mol-1
C2H5OH(l) ΔH=bkJ•mol-12CO2(g)+3H2O(l)
 C2H5OH(l)+3O2(g)正反应的活化能为ckJ•mol-1,则逆反应的活化能为
C2H5OH(l)+3O2(g)正反应的活化能为ckJ•mol-1,则逆反应的活化能为(4)已知,在25℃和101kPa下,部分化学键的键能(kJ·mol-1)数据如表所示。
| 化学键 | H-H | H-N | N≡N | O=O | C-H | C=O | H-O | N-N |
| 键能 | 436 | 391 | x | 498 | 413 | 745 | 462 | 193 |
②科学家发现一种新的气态分子N4(
 )。在25℃和101kPa下N4(g)转化为N2(g)的热化学方程式为
)。在25℃和101kPa下N4(g)转化为N2(g)的热化学方程式为
您最近一年使用:0次



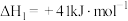


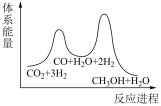
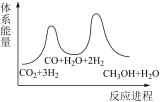
 ;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是
;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是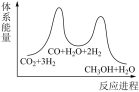 B.
B. C.
C.