(1)已知下列数据:
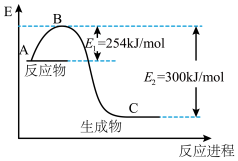
如图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量变化示意图,试根据表中及图中数据计算N-H的键能______________ 。
(2)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)=N2O4(l) ΔH1=-19.5 kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534.2 kJ·mol-1
写出肼和N2O4反应的热化学方程式______________________________ 。
(3)若用标准状况下4.48LO2氧化N2H4至N2,整个过程中转移的电子总数为___________ (阿伏加 德罗常数用NA表示)。
| 化学键 | H-H | N≡N |
| 键能/kJ·mol-1 | 435 | 943 |
如图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量变化示意图,试根据表中及图中数据计算N-H的键能

(2)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)=N2O4(l) ΔH1=-19.5 kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534.2 kJ·mol-1
写出肼和N2O4反应的热化学方程式
(3)若用标准状况下4.48LO2氧化N2H4至N2,整个过程中转移的电子总数为
更新时间:2020-01-01 12:45:11
|
相似题推荐
填空题
|
适中
(0.64)
【推荐1】(1)有下列八种晶体:①晶体硅 ②汞 ③氯化钾 ④二氧化硅 ⑤晶体碘 ⑥溴化钠 ⑦镁 ⑧二氧化碳。其中属于金属晶体的是__________ (填序号,下同),属于原子晶体的是_________ ,属于离子晶体的是________ ,属于分子晶体的是_______ 。
(2)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式:_________ 。若1g水蒸气转化为液态水放热2.444kJ,则反应H2(g)+ O2(g) = H2O(l)的△H=
O2(g) = H2O(l)的△H=___________ kJ∙mol-1。
(2)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式:
 O2(g) = H2O(l)的△H=
O2(g) = H2O(l)的△H=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】能源是人类赖以生存和发展的重要物质基础,常规能源的合理利用和新能源的合理开发是当今社会面临的严峻课题,回答下列问题:
(1)乙醇(C2H5OH)是未来内燃机的首选环保型液体燃料。1 g乙醇完全燃烧生成液态水放出a kJ的热量,则乙醇燃烧的热化学方程式为__________ 。
(2)由于C3H8(g)= C3H6(g)+H2(g) H=+bkJmol(b>0)的反应中,反应物具有的总能量________ (填“大于”“等于”或“小于”)生成物具有的总能量,那么在化学反应时,反应物就需要________ (填“放出”或“吸收”)能量才能转化为生成物。
(3)关于用水制取二次能源氢气,以下研究方向不正确的是________ 。
A 组成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下,使氢成为二次能源
B 设法将太阳光聚焦,产生高温,使水分解产生氢气
C 寻找高效催化剂,使水分解产生氢气,同时释放能量
D 寻找特殊催化剂,用于开发廉价能源,以分解水制取氢气
(4)已知下列两个热化学方程式,
A 2H2(g)+O2(g)=2H2O(l) H = -571.6kJ∙mol-1
B C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) H= -2220kJ∙mol-1
能表示燃烧热的热化学方程式为________ (填A或B)。将标况下22.4L的C3H8和H2混合气体(其中H2的体积分数为1/2),在上述条件下完全燃烧,则放出的热量为________ kJ。
(1)乙醇(C2H5OH)是未来内燃机的首选环保型液体燃料。1 g乙醇完全燃烧生成液态水放出a kJ的热量,则乙醇燃烧的热化学方程式为
(2)由于C3H8(g)= C3H6(g)+H2(g) H=+bkJmol(b>0)的反应中,反应物具有的总能量
(3)关于用水制取二次能源氢气,以下研究方向不正确的是
A 组成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下,使氢成为二次能源
B 设法将太阳光聚焦,产生高温,使水分解产生氢气
C 寻找高效催化剂,使水分解产生氢气,同时释放能量
D 寻找特殊催化剂,用于开发廉价能源,以分解水制取氢气
(4)已知下列两个热化学方程式,
A 2H2(g)+O2(g)=2H2O(l) H = -571.6kJ∙mol-1
B C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) H= -2220kJ∙mol-1
能表示燃烧热的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ. (1)下列条件的改变能增大活化分子百分数的是_____________ 。
A.增大压强 B.增大反应物的浓度
C.升高温度 D.使用催化剂
(2)破坏(或形成)1 mol化学键所吸收(或放出)的能量称为键能。已知白磷和PCl3的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P-P 198、Cl-Cl 243、P-Cl 331。

则反应P4(s,白磷)+6Cl2(g)=4PCl3(s)的反应热△H=__________ kJ·mol-1。
Ⅱ.2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。
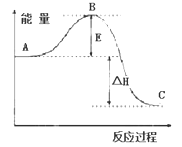
已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99 kJ·mol-1。请回答下列问题:
(1)图中C表示___________ ,E表示______________ ;该反应通常用V2O5作催化剂,加V2O5会使图中B点降低,理由是____________ ;
(2)图中△H=_________ kJ·mol-1。
A.增大压强 B.增大反应物的浓度
C.升高温度 D.使用催化剂
(2)破坏(或形成)1 mol化学键所吸收(或放出)的能量称为键能。已知白磷和PCl3的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P-P 198、Cl-Cl 243、P-Cl 331。

则反应P4(s,白磷)+6Cl2(g)=4PCl3(s)的反应热△H=
Ⅱ.2SO2(g)+O2(g)
 2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。
已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99 kJ·mol-1。请回答下列问题:
(1)图中C表示
(2)图中△H=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)请你写出298K,101kPa时,下列反应的热化学方程式。
①在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为___ 。
②1molC与1mol水蒸气反应生成1molCO和1molH2,吸热131.5kJ:___ 。
(2)硝酸厂的尾气直接排放将污染空气,目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160kJ·mol-1
则甲烷直接将NO2还原为N2的热化学方程式为___ 。
(3)CO、H2可用于合成甲醇和甲醚,其反应为(m、n均大于0):
反应①:CO(g)+2H2(g) CH3OH(g)ΔH=-mkJ·mol-1
CH3OH(g)ΔH=-mkJ·mol-1
反应②:2CO(g)+4H2(g) CH3OCH3(g)+H2O(g)ΔH=-nkJ·mol-1
CH3OCH3(g)+H2O(g)ΔH=-nkJ·mol-1
反应③:2CH3OH(g) CH3OCH3(g)+H2O(g)ΔH<0
CH3OCH3(g)+H2O(g)ΔH<0
则m与n的关系为__ 。
①在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
②1molC与1mol水蒸气反应生成1molCO和1molH2,吸热131.5kJ:
(2)硝酸厂的尾气直接排放将污染空气,目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160kJ·mol-1
则甲烷直接将NO2还原为N2的热化学方程式为
(3)CO、H2可用于合成甲醇和甲醚,其反应为(m、n均大于0):
反应①:CO(g)+2H2(g)
 CH3OH(g)ΔH=-mkJ·mol-1
CH3OH(g)ΔH=-mkJ·mol-1反应②:2CO(g)+4H2(g)
 CH3OCH3(g)+H2O(g)ΔH=-nkJ·mol-1
CH3OCH3(g)+H2O(g)ΔH=-nkJ·mol-1反应③:2CH3OH(g)
 CH3OCH3(g)+H2O(g)ΔH<0
CH3OCH3(g)+H2O(g)ΔH<0则m与n的关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】科学研究表明: 存储能量的能力是
存储能量的能力是 的12000倍左右,在大气中的寿命可达740年,如表所示是几种化学键的键能(断裂或形成1mol化学键时吸收或释放的热量)
的12000倍左右,在大气中的寿命可达740年,如表所示是几种化学键的键能(断裂或形成1mol化学键时吸收或释放的热量)
回答下列问题:
(1)①过程
___________ (填“吸收”或“放出”)能量。
②反应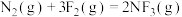
 =
=___________ 。
(2)已知:
①
 ;
;
②
 。
。
现有2mol由炭粉和氢气组成的悬浮气,在足量氧气中完全燃烧生成 (g)和
(g)和 (l),共放出679.0kJ的热量,则2mol悬浮气中C与
(l),共放出679.0kJ的热量,则2mol悬浮气中C与 的物质的量之比为
的物质的量之比为___________ 。
(3)电石( )可通过下列反应制备:
)可通过下列反应制备:
①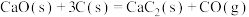
 ;
;
②
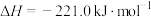 。
。
若不考虑热量损耗,物料转化率均为100%,最终炉中出来的气体只有CO。则为了维持热量平衡,每生产64g ,投料的量为56g CaO及
,投料的量为56g CaO及___________ mol C、___________ mol  。
。
 存储能量的能力是
存储能量的能力是 的12000倍左右,在大气中的寿命可达740年,如表所示是几种化学键的键能(断裂或形成1mol化学键时吸收或释放的热量)
的12000倍左右,在大气中的寿命可达740年,如表所示是几种化学键的键能(断裂或形成1mol化学键时吸收或释放的热量)| 化学键 | N≡N | F—F | N—F |
键能( ) ) | 946 | 154 | 283 |
(1)①过程

②反应
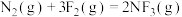
 =
=(2)已知:
①

 ;
;②

 。
。现有2mol由炭粉和氢气组成的悬浮气,在足量氧气中完全燃烧生成
 (g)和
(g)和 (l),共放出679.0kJ的热量,则2mol悬浮气中C与
(l),共放出679.0kJ的热量,则2mol悬浮气中C与 的物质的量之比为
的物质的量之比为(3)电石(
 )可通过下列反应制备:
)可通过下列反应制备:①
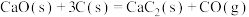
 ;
;②

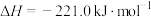 。
。若不考虑热量损耗,物料转化率均为100%,最终炉中出来的气体只有CO。则为了维持热量平衡,每生产64g
 ,投料的量为56g CaO及
,投料的量为56g CaO及 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】金刚石和石墨燃烧,氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如图所示。
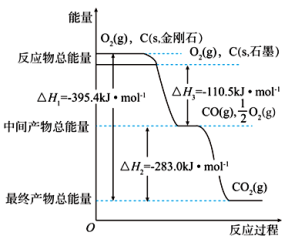
(1)在通常状况下,金刚石和石墨中___________ (填“金刚石”或“石墨”)更稳定,石墨的燃烧热ΔH为___________ 。
(2)当10g丁烷完全燃烧生成CO2和液态水时,放出热量为500kJ,写出表示丁烷燃烧热的热化学方程式:___________ 。
(3)已知:N2、O2分子中化学键的键能分别是946kJ·mol-1、497kJ·mol-1;N2(g)+O2(g)=2NO(g) ΔH=+180.0kJ·mol-1。NO分子中化学键的键能为___________ kJ·mol-1。
(4)由盖斯定律结合下述反应方程式,回答问题:
已知:①C(s)+O2(g)=CO2(g) ΔH1; ②2CO(g)+O2(g)=2CO2(g) ΔH2;③TiO2(g)+2Cl2(g)=TiCl4(s)+O2(g) ΔH3;则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=___________ 。(列出关于ΔH1、ΔH2、ΔH3的表达式)

(1)在通常状况下,金刚石和石墨中
(2)当10g丁烷完全燃烧生成CO2和液态水时,放出热量为500kJ,写出表示丁烷燃烧热的热化学方程式:
(3)已知:N2、O2分子中化学键的键能分别是946kJ·mol-1、497kJ·mol-1;N2(g)+O2(g)=2NO(g) ΔH=+180.0kJ·mol-1。NO分子中化学键的键能为
(4)由盖斯定律结合下述反应方程式,回答问题:
已知:①C(s)+O2(g)=CO2(g) ΔH1; ②2CO(g)+O2(g)=2CO2(g) ΔH2;③TiO2(g)+2Cl2(g)=TiCl4(s)+O2(g) ΔH3;则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=
您最近一年使用:0次
【推荐1】已知25℃、101kpa时,一些物质的燃烧热为:
请回答下列问题:
(1)写出该条件下CH3OH(l)完全燃烧的热化学方程式:______________________ 。
(2)根据盖斯定律完成下列反应的热化学方程式:CO(g)+2H2(g)=CH3OH(l);△H=_________________ 。
(3)现有H2和CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2(g)和H2O(l),共放出热量3242.5 kJ,则原混合气体中H2和CH4的物质的量之比是:___________ 。
A.1∶1 B.1∶3 C.1∶4 D.2∶3
| 化学式 | CO(g) | H2(g) | CH3OH(l) | CH4(g) |
| △H/(kJ/mol) | -283.0 | -285.8 | -726.5 | -890.3 |
请回答下列问题:
(1)写出该条件下CH3OH(l)完全燃烧的热化学方程式:
(2)根据盖斯定律完成下列反应的热化学方程式:CO(g)+2H2(g)=CH3OH(l);△H=
(3)现有H2和CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2(g)和H2O(l),共放出热量3242.5 kJ,则原混合气体中H2和CH4的物质的量之比是:
A.1∶1 B.1∶3 C.1∶4 D.2∶3
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)肼 和
和 两种物质混合发生反应生成
两种物质混合发生反应生成 和
和 ,已知4g气体肼反应放出71kJ热量,其热化学方程式为
,已知4g气体肼反应放出71kJ热量,其热化学方程式为______
(2)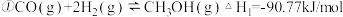
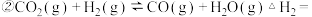
______
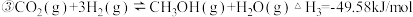 则
则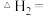
______
 和
和 两种物质混合发生反应生成
两种物质混合发生反应生成 和
和 ,已知4g气体肼反应放出71kJ热量,其热化学方程式为
,已知4g气体肼反应放出71kJ热量,其热化学方程式为(2)
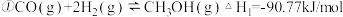
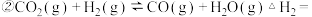
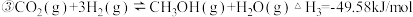 则
则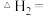
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)实验测得,5 g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5 kJ的热量,试写出甲醇燃烧的热化学方程式:_________________________________________ 。
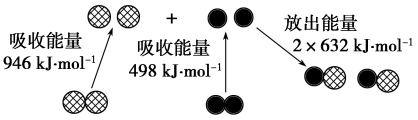
(2)下图为N2(g)和O2(g)生成NO (g)过程中的能量变化:
则N≡N键的键能为________ kJ·mol-1。根据上图写出N2(g)和O2(g)生成NO(g)的热化学方程式:_____________________________________________________________
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知: C(石墨,s)+O2(g)===CO2(g) ΔH1=-393.5 kJ·mol-1①
2H2(g)+O2(g)===2H2O(l) ΔH2=-571.6 kJ·mol-1②
2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH3=-2599 kJ·mol-1③
根据盖斯定律,计算298 K时由C(石墨,s)和H2(g)生成1 mol C2H2(g)反应的焓变:________________________________________________________________________ 。
(4)接触法制硫酸工艺中,其主反应在450 ℃并有催化剂存在下进行:2SO2(g)+O2(g) 2SO3(g) ΔH=-190 kJ·mol-1。
2SO3(g) ΔH=-190 kJ·mol-1。
①该热化学反应方程式的意义是___________________________________________________
②已知单质硫16 g燃烧放热为149 kJ,写出硫燃烧热的热化学方程式:_________________
(2)下图为N2(g)和O2(g)生成NO (g)过程中的能量变化:

则N≡N键的键能为
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知: C(石墨,s)+O2(g)===CO2(g) ΔH1=-393.5 kJ·mol-1①
2H2(g)+O2(g)===2H2O(l) ΔH2=-571.6 kJ·mol-1②
2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH3=-2599 kJ·mol-1③
根据盖斯定律,计算298 K时由C(石墨,s)和H2(g)生成1 mol C2H2(g)反应的焓变:
(4)接触法制硫酸工艺中,其主反应在450 ℃并有催化剂存在下进行:2SO2(g)+O2(g)
 2SO3(g) ΔH=-190 kJ·mol-1。
2SO3(g) ΔH=-190 kJ·mol-1。①该热化学反应方程式的意义是
②已知单质硫16 g燃烧放热为149 kJ,写出硫燃烧热的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
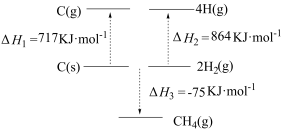
【推荐2】(1)根据下图中的能量关系,可求得C-H的键能为______________ 。
(2)X(s)+3Y(g) Z(g)+3W(g) ΔH=-akJ/mol,一定条件下,将2molX和2molY通入2L的恒容密闭容器中,反应10s后达到平衡,测得生成0.5molZ。
Z(g)+3W(g) ΔH=-akJ/mol,一定条件下,将2molX和2molY通入2L的恒容密闭容器中,反应10s后达到平衡,测得生成0.5molZ。
①则10s内,Y的平均反应速率为_____________ ,第10s时,X的物质的量为__________ ,Y的浓度为_______ ,10s内,X和Y反应放出的热量Q为______ 。
②判断该反应是否达到平衡的依据是__________ (填字母)。
A.压强不随时间改变 B.气体的密度不随时间改变
C.c(Y)不随时间改变 D.单位时间里生成Z和W的物质的量之比为1∶2

(2)X(s)+3Y(g)
 Z(g)+3W(g) ΔH=-akJ/mol,一定条件下,将2molX和2molY通入2L的恒容密闭容器中,反应10s后达到平衡,测得生成0.5molZ。
Z(g)+3W(g) ΔH=-akJ/mol,一定条件下,将2molX和2molY通入2L的恒容密闭容器中,反应10s后达到平衡,测得生成0.5molZ。①则10s内,Y的平均反应速率为
②判断该反应是否达到平衡的依据是
A.压强不随时间改变 B.气体的密度不随时间改变
C.c(Y)不随时间改变 D.单位时间里生成Z和W的物质的量之比为1∶2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】完成下列问题
(1)用CH4催化还原NOx可以消除氮氧化物的污染,例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1= - 574kJ/mol
CH4(g)+4NO(g)=2N2(g)+ CO2(g)+2H2O(g) △H2
若1molCH4还原NO2制N2,整个过程中放出的热量为867kJ,则△H2=_______ 。
(2)根据盖斯提出的“不管化学过程是一步完成或几步完成这个总过程的热效应是相等的”观点来计算反应热。已知:
C(石墨,s)+O2(g)=CO2(g) △H1= -393.5kJ/mol
C(金刚石,s)+O2(g)=CO2(g) △H2= -395.0kJ/mol
则石墨的稳定性比金刚石_______ (填“高”或“低”)
(3)利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1;
CH3OH(g)+H2O(g) △H1;
②CO(g)+2H2(g) CH3OH(g) △H2;
CH3OH(g) △H2;
③CO2(g)+H2(g) CO(g)+H2O(g) △H3;
CO(g)+H2O(g) △H3;
回答下列问题:
已知反应①中的相关的化学键键能(“C O”表示CO的化学键)数据见表:由此计算△H2=
O”表示CO的化学键)数据见表:由此计算△H2=_______ kJ·mol-1,已知△H1=-58kJ·mol-1,则△H3=_______ kJ·mol-1。
(1)用CH4催化还原NOx可以消除氮氧化物的污染,例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1= - 574kJ/mol
CH4(g)+4NO(g)=2N2(g)+ CO2(g)+2H2O(g) △H2
若1molCH4还原NO2制N2,整个过程中放出的热量为867kJ,则△H2=
(2)根据盖斯提出的“不管化学过程是一步完成或几步完成这个总过程的热效应是相等的”观点来计算反应热。已知:
C(石墨,s)+O2(g)=CO2(g) △H1= -393.5kJ/mol
C(金刚石,s)+O2(g)=CO2(g) △H2= -395.0kJ/mol
则石墨的稳定性比金刚石
(3)利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1;
CH3OH(g)+H2O(g) △H1;②CO(g)+2H2(g)
 CH3OH(g) △H2;
CH3OH(g) △H2;③CO2(g)+H2(g)
 CO(g)+H2O(g) △H3;
CO(g)+H2O(g) △H3;回答下列问题:
| 化学键 | H-H | C-O | C O O | H-O | C-H |
| E/(kJ·mol-1) | 436 | 343 | 1076 | 465 | 413 |
 O”表示CO的化学键)数据见表:由此计算△H2=
O”表示CO的化学键)数据见表:由此计算△H2=
您最近一年使用:0次



