氧化还原反应在人类生活中应用非常广泛。
(Ⅰ)钢铁“发蓝”是在钢铁的表面形成一层Fe3O4的技术过程。经过“发蓝”处理的钢铁制品不易生锈,经久耐用。某厂对钢铁制品进行“发蓝”处理时发生反应的化学方程式如下(其中反应②未配平):
①3Fe+NaNO2+5NaOH=3Na2FeO2+H2O+NH3↑
②___ Na2FeO2+___ NaNO2+____ H2O →____ Na2Fe2O4+____ NH3↑+ _____ NaOH
③ Na2FeO2+ Na2Fe2O4+2H2O = Fe3O4+4NaOH
(1)请把反应②的系数填入上述相应位置的横线上。其中__________ 元素被氧化。
(2)上述3个反应中氧化剂共有_______ 种,氧化剂的化学式是___________________ 。
(3)如果有3.36L NH3(标准状况下)生成,则上述反应中还原剂总共失去电子________ 个。
(Ⅱ)发射火箭时常用肼(N2H4)为燃料,二氧化氮作氧化剂,两者反应生成氮气和水蒸气。已知4g N2H4(g)在上述反应中放出71kJ的热量,热化学方程式为_________________ 。
(Ⅰ)钢铁“发蓝”是在钢铁的表面形成一层Fe3O4的技术过程。经过“发蓝”处理的钢铁制品不易生锈,经久耐用。某厂对钢铁制品进行“发蓝”处理时发生反应的化学方程式如下(其中反应②未配平):
①3Fe+NaNO2+5NaOH=3Na2FeO2+H2O+NH3↑
②
③ Na2FeO2+ Na2Fe2O4+2H2O = Fe3O4+4NaOH
(1)请把反应②的系数填入上述相应位置的横线上。其中
(2)上述3个反应中氧化剂共有
(3)如果有3.36L NH3(标准状况下)生成,则上述反应中还原剂总共失去电子
(Ⅱ)发射火箭时常用肼(N2H4)为燃料,二氧化氮作氧化剂,两者反应生成氮气和水蒸气。已知4g N2H4(g)在上述反应中放出71kJ的热量,热化学方程式为
2011·上海普陀·零模 查看更多[1]
(已下线)上海市普陀区2011届高三下学期质量调研化学试题
更新时间:2020-03-31 14:10:14
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】 是高效、绿色的水处理剂,其原理如图所示。请回答下列问题:
是高效、绿色的水处理剂,其原理如图所示。请回答下列问题:

(1)高铁酸钾( )属于
)属于_______ (“酸”、“碱”、“盐”或“氧化物”),其中铁的化合价为_______ 价。
(2)过程 中、
中、 体现
体现_______ (填“氧化“或“还原”)性,氧化产物是_______ ,反应过程中转移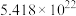 电子,需要
电子,需要_______  。
。
(3)过程 反应的离子方程式为
反应的离子方程式为_______ 。
(4)过程 属于
属于_______ (填“物理”或“化学”)变化。
(5)碱性条件下用 和
和 反应制备
反应制备 。配平其反应的化学方程式:
。配平其反应的化学方程式:_______ 。
_______ _______
_______ _______
_______ _______
_______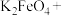 _______
_______ _______
_______
 是高效、绿色的水处理剂,其原理如图所示。请回答下列问题:
是高效、绿色的水处理剂,其原理如图所示。请回答下列问题:
(1)高铁酸钾(
 )属于
)属于(2)过程
 中、
中、 体现
体现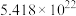 电子,需要
电子,需要 。
。(3)过程
 反应的离子方程式为
反应的离子方程式为(4)过程
 属于
属于(5)碱性条件下用
 和
和 反应制备
反应制备 。配平其反应的化学方程式:
。配平其反应的化学方程式:_______
 _______
_______ _______
_______ _______
_______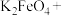 _______
_______ _______
_______
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】元素及其化合物的应用广泛,回答下列问题:
(1)碘盐中含有KIO3,KIO3中碘元素的化合价是____________ 。
(2)84消毒液的有效成分是____________ (填“NaCl”或“NaClO”)。
(3)高温下Fe2O3与CO反应是工业上炼铁的原理,该原理的化学反应方程式为____________ ,反应中Fe2O3做________ (填“氧化剂”或“还原剂”)。
(4)实验室用NaOH溶液吸收含SO2的尾气,该反应的离子方程式为____________ ,SO2属于____________ (填“酸性氧化物”或“碱性氧化物”),SO2能使品红溶液褪色,说明SO2具有的性质是____________ 。
(1)碘盐中含有KIO3,KIO3中碘元素的化合价是
(2)84消毒液的有效成分是
(3)高温下Fe2O3与CO反应是工业上炼铁的原理,该原理的化学反应方程式为
(4)实验室用NaOH溶液吸收含SO2的尾气,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】二氧化氯(ClO2)是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
(1)若以单位质量的氧化剂所得到的电子数来表示消毒效率,则ClO2、Cl2两种消毒剂的消毒效率较大的是哪种_____ 。(填化学式)
(2)某小组设计了如图所示的实验装置用于制备ClO2。

①装置A三颈烧瓶中,通入氮气的主要作用有两个,其一是可以起到搅拌作用,其二是_____ 。
②装置B的作用是_____ 。
③装置A用于生成ClO2气体,该反应的离子方程式为_____ 。
④当看到装置C中导管液面上升时应进行的操作是_____ 。
(1)若以单位质量的氧化剂所得到的电子数来表示消毒效率,则ClO2、Cl2两种消毒剂的消毒效率较大的是哪种
(2)某小组设计了如图所示的实验装置用于制备ClO2。

①装置A三颈烧瓶中,通入氮气的主要作用有两个,其一是可以起到搅拌作用,其二是
②装置B的作用是
③装置A用于生成ClO2气体,该反应的离子方程式为
④当看到装置C中导管液面上升时应进行的操作是
您最近一年使用:0次
【推荐1】按要求填空。
(1)高铁酸钠(Na2FeO4)是一种新型净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH +3NaClO=2Na2FeO4+3NaCl+5H2O。
①Na2FeO4中Fe元素的化合价是___________ ,该反应中被还原的物质是___________ (用化学式表示,下同),氧化产物是___________ 。
②用双线桥法表示反应中电子转移的方向和数目:___________ 。
(2)饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以用化学方法处理
的浓度,可以用化学方法处理 ,其化学方程式为10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。
,其化学方程式为10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。
①上述反应中,被氧化的元素是________ (用元素符号表示)。
②在上述反应中,每生成1个N2分子,转移电子数目为________ 个。
③配平方程式:_____ 。
___KMnO4+____HCl(浓)=____ KCl+___MnCl2+__Cl2↑+___H2O
(1)高铁酸钠(Na2FeO4)是一种新型净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH +3NaClO=2Na2FeO4+3NaCl+5H2O。
①Na2FeO4中Fe元素的化合价是
②用双线桥法表示反应中电子转移的方向和数目:
(2)饮用水中的
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以用化学方法处理
的浓度,可以用化学方法处理 ,其化学方程式为10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。
,其化学方程式为10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。①上述反应中,被氧化的元素是
②在上述反应中,每生成1个N2分子,转移电子数目为
③配平方程式:
___KMnO4+____HCl(浓)=____ KCl+___MnCl2+__Cl2↑+___H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】废水中氨氮(NH3、NH )的处理技术有生物脱氮法、化学沉淀法、折点加氯法和电催化氧化法等。
)的处理技术有生物脱氮法、化学沉淀法、折点加氯法和电催化氧化法等。
(1)氨氮污水直接排放入河流、湖泊导致的环境问题是_____ 。
(2)生物脱氮法:利用微生物脱氮,原理如下:



 N2
N2
反应①的离子方程式为_____ 。
(3)化学沉淀法:向废水中加入含MgCl2、Na3PO4的溶液, 转化为MgNH4PO4·6H2O沉淀。若pH过大,氨氮去除率和磷利用率均降低,其原因是
转化为MgNH4PO4·6H2O沉淀。若pH过大,氨氮去除率和磷利用率均降低,其原因是_____ (用离子方程式表示)。
(4)折点加氯法:向废水中加入NaClO溶液,使氨氮氧化成N2,相关反应如下:
NaClO+H2O=HClO+NaOH(Ⅰ);
NH3+HClO=NH2Cl+H2O(Ⅱ);
NH2Cl+HClO=NHCl2+H2O(Ⅲ);
NHCl2+H2O=NOH+2HCl(Ⅳ);
NHCl2+NOH=N2↑+HClO+HCl(Ⅴ)。
探究NaClO的投加量[以m(Cl2)表示]对氨氮去除率的影响,实验结果如图所示。

①当m(Cl2)∶m(NH3)≥7.7时,污水中总氮去除率缓慢下降,其原因是_____ 。
②当m(Cl2)∶m(NH3)<7.7时,随着m(Cl2)∶m(NH3)的减小,污水中余氯(除Cl-外的氯元素存在形式)浓度升高,其原因是_____ 。
 )的处理技术有生物脱氮法、化学沉淀法、折点加氯法和电催化氧化法等。
)的处理技术有生物脱氮法、化学沉淀法、折点加氯法和电催化氧化法等。(1)氨氮污水直接排放入河流、湖泊导致的环境问题是
(2)生物脱氮法:利用微生物脱氮,原理如下:



 N2
N2反应①的离子方程式为
(3)化学沉淀法:向废水中加入含MgCl2、Na3PO4的溶液,
 转化为MgNH4PO4·6H2O沉淀。若pH过大,氨氮去除率和磷利用率均降低,其原因是
转化为MgNH4PO4·6H2O沉淀。若pH过大,氨氮去除率和磷利用率均降低,其原因是(4)折点加氯法:向废水中加入NaClO溶液,使氨氮氧化成N2,相关反应如下:
NaClO+H2O=HClO+NaOH(Ⅰ);
NH3+HClO=NH2Cl+H2O(Ⅱ);
NH2Cl+HClO=NHCl2+H2O(Ⅲ);
NHCl2+H2O=NOH+2HCl(Ⅳ);
NHCl2+NOH=N2↑+HClO+HCl(Ⅴ)。
探究NaClO的投加量[以m(Cl2)表示]对氨氮去除率的影响,实验结果如图所示。

①当m(Cl2)∶m(NH3)≥7.7时,污水中总氮去除率缓慢下降,其原因是
②当m(Cl2)∶m(NH3)<7.7时,随着m(Cl2)∶m(NH3)的减小,污水中余氯(除Cl-外的氯元素存在形式)浓度升高,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某一反应体系中有反应物和生成物共八种物质:KMnO4、SO2、CuS、H2SO4、CuSO4、K2SO4、MnSO4、H2O。反应中氧化过程如下:CuS→SO2。
(1)该反应中被还原的元素是___________ ,CuS发生氧化反应的实质是__________ 。
(2)若反应过程中转移了3 mol电子,则参加反应的CuS的物质的量为________ mol。
(3)写出并配平该反应的化学方程式________________________________________ 。
(4)当KMnO4过量时,KMnO4会继续与SO2发生如下反应:
2KMnO4+5SO2+2H2O=2H2SO4+K2SO4+2MnSO4
该反应中氧化产物与还原产物的物质的量之比为_______ 。
(1)该反应中被还原的元素是
(2)若反应过程中转移了3 mol电子,则参加反应的CuS的物质的量为
(3)写出并配平该反应的化学方程式
(4)当KMnO4过量时,KMnO4会继续与SO2发生如下反应:
2KMnO4+5SO2+2H2O=2H2SO4+K2SO4+2MnSO4
该反应中氧化产物与还原产物的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】写出下列反应的热化学方程式:
(1)1mol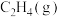 与适量
与适量 反应,生成
反应,生成 和
和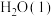 ,放出1411kJ的热量
,放出1411kJ的热量_______ 。
(2)1mol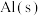 与适量
与适量 发生反应,生成
发生反应,生成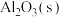 ,放出834.9kJ的热量
,放出834.9kJ的热量_______ 。
(3)23g某液态有机物和一定量的氧气混合点燃,恰好完全反应,生成27g液态水和22.4L(标准状况下)CO2并放出683.5kJ的热量_______ 。
(1)1mol
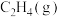 与适量
与适量 反应,生成
反应,生成 和
和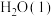 ,放出1411kJ的热量
,放出1411kJ的热量(2)1mol
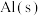 与适量
与适量 发生反应,生成
发生反应,生成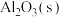 ,放出834.9kJ的热量
,放出834.9kJ的热量(3)23g某液态有机物和一定量的氧气混合点燃,恰好完全反应,生成27g液态水和22.4L(标准状况下)CO2并放出683.5kJ的热量
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知:
①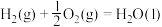

②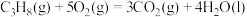
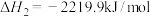
(1)在25℃和101kPa下, 和
和 的混合气体5mol完全燃烧生成
的混合气体5mol完全燃烧生成 和液态水,放出6264.2kJ的热量。计算混合气体中
和液态水,放出6264.2kJ的热量。计算混合气体中 和
和 的体积比
的体积比___________ 。
(2)已知:
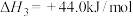 。写出
。写出 燃烧生成
燃烧生成 和水蒸气的热化学方程式
和水蒸气的热化学方程式___________ 。
①
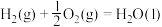

②
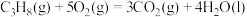
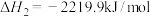
(1)在25℃和101kPa下,
 和
和 的混合气体5mol完全燃烧生成
的混合气体5mol完全燃烧生成 和液态水,放出6264.2kJ的热量。计算混合气体中
和液态水,放出6264.2kJ的热量。计算混合气体中 和
和 的体积比
的体积比(2)已知:

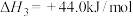 。写出
。写出 燃烧生成
燃烧生成 和水蒸气的热化学方程式
和水蒸气的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量的热。已知0.4mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256KJ的热量。
(1)反应的热化学方程式为______ 。
(2)又已知H2O(l)=H2O(g);ΔH=+44kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是______ KJ。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是______ 。
(4)已知N2(g) + 2O2(g) = 2NO2(g) ΔH=+67.7kJ/mol
N2H4(g) + O2(g) = N2(g) + 2H2O(g) ΔH=-534kJ/mol
则肼与NO2完全反应生成氮气和液态水的热化学方程式______ 。
(1)反应的热化学方程式为
(2)又已知H2O(l)=H2O(g);ΔH=+44kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是
(4)已知N2(g) + 2O2(g) = 2NO2(g) ΔH=+67.7kJ/mol
N2H4(g) + O2(g) = N2(g) + 2H2O(g) ΔH=-534kJ/mol
则肼与NO2完全反应生成氮气和液态水的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】反应3MoS2+18HNO3+12HCl=3H2[MoO2Cl4]+18NO↑+6H2SO4+6H2O中,每溶解1molMoS2,转移电子的物质的量为_______ 。
您最近一年使用:0次
【推荐2】饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为N2,其化学方程式为:
还原为N2,其化学方程式为: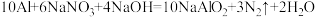 。请回答下列问题:
。请回答下列问题:
(1)上述反应中,被氧化的元素___________ ,还原产物是___________ 。
(2)用“双线桥法”表示反应中电子转移的方向和数目:___________ 。
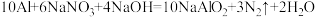
(3)反应中每生成1个N2,转移___________ 个电子。
(4)请配平下列离子方程式___________ 。

(5)已知I-、Fe2+、SO2、Cl-、H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为: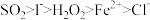 ,则下列反应不能发生的是___________。
,则下列反应不能发生的是___________。
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为N2,其化学方程式为:
还原为N2,其化学方程式为: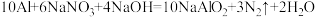 。请回答下列问题:
。请回答下列问题:(1)上述反应中,被氧化的元素
(2)用“双线桥法”表示反应中电子转移的方向和数目:
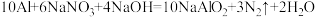
(3)反应中每生成1个N2,转移
(4)请配平下列离子方程式

(5)已知I-、Fe2+、SO2、Cl-、H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为:
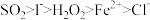 ,则下列反应不能发生的是___________。
,则下列反应不能发生的是___________。A.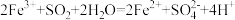 | B.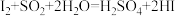 |
C.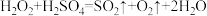 | D.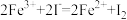 |
您最近一年使用:0次
【推荐3】储氢纳米碳管研究成功体现了科技的进步。但用电弧法合成的碳纳米管常伴有大量的杂质——碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应方程式为3C+2K2Cr2O7+8H2SO4=3CO2↑ +2K2SO4+2Cr2(SO4)3 +8H2O。请回答下列问题:
(1)用双线桥法标明上述反应方程式中电子转移的方向和数目_______ 。
(2)上述反应中氧化剂是__ , 每生成 lmolCO2,转移电子数目为_______ 。
(3)请配平下列离子方程式__ 。 Fe 2+ +_______ H++_______ =_______Fe3++_______N2O↑+_______H2O
=_______Fe3++_______N2O↑+_______H2O
(1)用双线桥法标明上述反应方程式中电子转移的方向和数目
(2)上述反应中氧化剂是
(3)请配平下列离子方程式
 =_______Fe3++_______N2O↑+_______H2O
=_______Fe3++_______N2O↑+_______H2O
您最近一年使用:0次



