写出下列反应的热化学方程式:
(1)1mol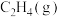 与适量
与适量 反应,生成
反应,生成 和
和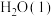 ,放出1411kJ的热量
,放出1411kJ的热量_______ 。
(2)1mol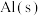 与适量
与适量 发生反应,生成
发生反应,生成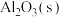 ,放出834.9kJ的热量
,放出834.9kJ的热量_______ 。
(3)23g某液态有机物和一定量的氧气混合点燃,恰好完全反应,生成27g液态水和22.4L(标准状况下)CO2并放出683.5kJ的热量_______ 。
(1)1mol
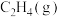 与适量
与适量 反应,生成
反应,生成 和
和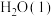 ,放出1411kJ的热量
,放出1411kJ的热量(2)1mol
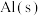 与适量
与适量 发生反应,生成
发生反应,生成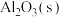 ,放出834.9kJ的热量
,放出834.9kJ的热量(3)23g某液态有机物和一定量的氧气混合点燃,恰好完全反应,生成27g液态水和22.4L(标准状况下)CO2并放出683.5kJ的热量
更新时间:2021-01-08 11:07:38
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表的一部分,其中甲~戊共五种元素,回答下列问题:
(1)五种元素最高价氧化物对应的水化物中酸性最强的是______ 填化学式,下同),显两性的是_____ 。
(2)乙与丙按原子数 1:1 形成的一种化合物,其电子式为_____ ,该化合物固态时所属晶体类型为_____ ,所含化学键类型有_________ 。
(3)乙、丙、丁三种元素分别形成简单离子,按离子半径从大到小的顺序排列为_____ (用离子符号表示)。
(4)有人认为,元素甲还可以排在第ⅦA族,理由是它们的负化合价都是_____ ;也有人认为,根据元素甲的正、负化合价代数和为零,也可以将元素甲排在第_________ 族。
(5)甲与丙两种元素形成的化合物与水反应,生成—种可燃性气体单质,该反应的化学方程式为_____ 。
(6)通常状况下,1g甲的单质在戊的单质中燃烧放热92kJ,写出该反应的热化学方程式_____
周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | 甲 | ||||||
| 2 | 乙 | ||||||
| 3 | 丙 | 丁 | 戊 |
(1)五种元素最高价氧化物对应的水化物中酸性最强的是
(2)乙与丙按原子数 1:1 形成的一种化合物,其电子式为
(3)乙、丙、丁三种元素分别形成简单离子,按离子半径从大到小的顺序排列为
(4)有人认为,元素甲还可以排在第ⅦA族,理由是它们的负化合价都是
(5)甲与丙两种元素形成的化合物与水反应,生成—种可燃性气体单质,该反应的化学方程式为
(6)通常状况下,1g甲的单质在戊的单质中燃烧放热92kJ,写出该反应的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)乙醇是未来内燃机的首选环保型液体燃料。2.0g乙醇完全燃烧生成液态水放出59.43kJ的热量,则乙醇燃烧的热化学方程式__ 。
(2)已知下列热化学方程式:
①C(s,石墨)+O2(g)═CO2(g) △H=-393.5kJ•mol-1
②2H2(g)+O2(g)═2H2O(l) △H=-571.6kJ•mol-1
③2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l) △H=-2599kJ•mol-1
请写出C(s,石墨)和H2(g)生成1mol C2H2(g)的热化学方程式_____ 。
(3)已知几种共价键的键能数据如下表:
写出合成氨反应的热化学方程式:____ 。
(2)已知下列热化学方程式:
①C(s,石墨)+O2(g)═CO2(g) △H=-393.5kJ•mol-1
②2H2(g)+O2(g)═2H2O(l) △H=-571.6kJ•mol-1
③2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l) △H=-2599kJ•mol-1
请写出C(s,石墨)和H2(g)生成1mol C2H2(g)的热化学方程式
(3)已知几种共价键的键能数据如下表:
| 共价键 | N≡N | H—H | N—H |
| 键能(kJ/mol) | 946 | 436 | 390.8 |
写出合成氨反应的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】2SO2(g)+O2(g) 2SO3(g) ΔH=akJ•mol-1,反应过程的能量变化如图所示。已知1molSO2(g)完全转化为1molSO3(g)放热99kJ。请回答:
2SO3(g) ΔH=akJ•mol-1,反应过程的能量变化如图所示。已知1molSO2(g)完全转化为1molSO3(g)放热99kJ。请回答:

(1)a=_____ kJ•mol-1.
(2)该反应常用V2O5作催化剂使图中ΔH_____ (填“升高”“降低”或“不变”)。
(3)已知单质硫的燃烧热为296kJ•mol-1,写出反应的热化学方程式:_____ 。
(4)工业上用H2和Cl2反应制HCl,各键能数据为:H—H:436kJ/mol,Cl—Cl:243kJ/mol,H—Cl:431kJ/mol。该反应的热化学方程式是_____ 。
(5)已知:①C(s)+O2(g)=CO2(g) ΔH=ΔH1;②2CO(g)+O2(g)=2CO2(g) ΔH=ΔH2;③TiO2(g)+2Cl2(g)=TiCl4(s)+O2(g) ΔH=ΔH3;则TiO2(g)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=_____ 。(列出关于ΔH1、ΔH2、ΔH3的表达式)
 2SO3(g) ΔH=akJ•mol-1,反应过程的能量变化如图所示。已知1molSO2(g)完全转化为1molSO3(g)放热99kJ。请回答:
2SO3(g) ΔH=akJ•mol-1,反应过程的能量变化如图所示。已知1molSO2(g)完全转化为1molSO3(g)放热99kJ。请回答:
(1)a=
(2)该反应常用V2O5作催化剂使图中ΔH
(3)已知单质硫的燃烧热为296kJ•mol-1,写出反应的热化学方程式:
(4)工业上用H2和Cl2反应制HCl,各键能数据为:H—H:436kJ/mol,Cl—Cl:243kJ/mol,H—Cl:431kJ/mol。该反应的热化学方程式是
(5)已知:①C(s)+O2(g)=CO2(g) ΔH=ΔH1;②2CO(g)+O2(g)=2CO2(g) ΔH=ΔH2;③TiO2(g)+2Cl2(g)=TiCl4(s)+O2(g) ΔH=ΔH3;则TiO2(g)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求书写热化学方程式

(1)一定条件下,由SO2和CO反应生成S和CO2的能量变化如图所示,写出该反应的热化学方程式_________
(2)CO(g)和CH3OH(l)的燃烧热ΔH分别为- 283.0 kJ·mol -1和-726.5 kJ·mol-1。则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为__________
(3)已知H2O(g)=H2O(l) ΔH = - 44 kJ·mol-1
则表示氢气燃烧热的热化学方程式为_____________________________

(1)一定条件下,由SO2和CO反应生成S和CO2的能量变化如图所示,写出该反应的热化学方程式
(2)CO(g)和CH3OH(l)的燃烧热ΔH分别为- 283.0 kJ·mol -1和-726.5 kJ·mol-1。则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为
(3)已知H2O(g)=H2O(l) ΔH = - 44 kJ·mol-1
| 化学键 | O=O(g) | H—H | H—O |
| 键能/(kJ·mol-1) | 496 | 436 | 463 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】依据事实,写出下列反应的热化学方程式
(1)适量的N2和O2完全反应,每生成23 g NO2吸收16.95 kJ热量。N2与O2反应的热化学方程式为_______________________________________ 。
(2)18 g葡萄糖与适量O2反应,生成CO2和液态水,放出280.4 kJ热量。葡萄糖燃烧的热化学方程式为__________________________________________ 。
(3)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O。已知室温下2 g SiH4自燃放出热量89.2 kJ。SiH4自燃的热化学方程式为____________________________________ 。
(4)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:____________________________________ 。
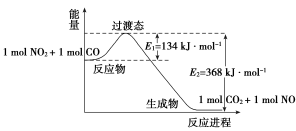
(5)直接排放煤燃烧产生的烟气会引起严重的环境问题。煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2Og)ΔH1=-867 kJ·mol-1①
2NO2(g) N2O4(g) ΔH2=-56.9 kJ·mol-1②
N2O4(g) ΔH2=-56.9 kJ·mol-1②
写出CH4(g)催化还原N2O4(g)生成N2(g)和H2O(g)的热化学方程式________________________ 。
(1)适量的N2和O2完全反应,每生成23 g NO2吸收16.95 kJ热量。N2与O2反应的热化学方程式为
(2)18 g葡萄糖与适量O2反应,生成CO2和液态水,放出280.4 kJ热量。葡萄糖燃烧的热化学方程式为
(3)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O。已知室温下2 g SiH4自燃放出热量89.2 kJ。SiH4自燃的热化学方程式为
(4)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:

(5)直接排放煤燃烧产生的烟气会引起严重的环境问题。煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2Og)ΔH1=-867 kJ·mol-1①
2NO2(g)
 N2O4(g) ΔH2=-56.9 kJ·mol-1②
N2O4(g) ΔH2=-56.9 kJ·mol-1②写出CH4(g)催化还原N2O4(g)生成N2(g)和H2O(g)的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】能源是人类赖以生存和发展的重要物质基础,常规能源的合理利用和新能源的合理开发是当今社会面临的严峻课题,回答下列问题:
(1)乙醇(C2H5OH)是未来内燃机的首选环保型液体燃料。1 g乙醇完全燃烧生成液态水放出a kJ的热量,则乙醇燃烧的热化学方程式为__________ 。
(2)由于C3H8(g)= C3H6(g)+H2(g) H=+bkJmol(b>0)的反应中,反应物具有的总能量________ (填“大于”“等于”或“小于”)生成物具有的总能量,那么在化学反应时,反应物就需要________ (填“放出”或“吸收”)能量才能转化为生成物。
(3)关于用水制取二次能源氢气,以下研究方向不正确的是________ 。
A 组成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下,使氢成为二次能源
B 设法将太阳光聚焦,产生高温,使水分解产生氢气
C 寻找高效催化剂,使水分解产生氢气,同时释放能量
D 寻找特殊催化剂,用于开发廉价能源,以分解水制取氢气
(4)已知下列两个热化学方程式,
A 2H2(g)+O2(g)=2H2O(l) H = -571.6kJ∙mol-1
B C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) H= -2220kJ∙mol-1
能表示燃烧热的热化学方程式为________ (填A或B)。将标况下22.4L的C3H8和H2混合气体(其中H2的体积分数为1/2),在上述条件下完全燃烧,则放出的热量为________ kJ。
(1)乙醇(C2H5OH)是未来内燃机的首选环保型液体燃料。1 g乙醇完全燃烧生成液态水放出a kJ的热量,则乙醇燃烧的热化学方程式为
(2)由于C3H8(g)= C3H6(g)+H2(g) H=+bkJmol(b>0)的反应中,反应物具有的总能量
(3)关于用水制取二次能源氢气,以下研究方向不正确的是
A 组成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下,使氢成为二次能源
B 设法将太阳光聚焦,产生高温,使水分解产生氢气
C 寻找高效催化剂,使水分解产生氢气,同时释放能量
D 寻找特殊催化剂,用于开发廉价能源,以分解水制取氢气
(4)已知下列两个热化学方程式,
A 2H2(g)+O2(g)=2H2O(l) H = -571.6kJ∙mol-1
B C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) H= -2220kJ∙mol-1
能表示燃烧热的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】碳的单质及化合物在人类生产生活中起着非常重要的作用。请回答下列问题:
(1)已知CH3OH(l)的燃烧热 ,
,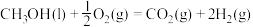
 ,则
,则
______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(2)Cl2(g)和H2O(g)通过灼热的炭层,生成HCl(g)和CO2(g),当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式:___________ 。
(3)火箭和导弹表面的薄层是耐高温物质。下列反应可制得耐高温材料,热化学方程式为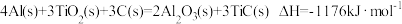 。该反应过程中每转移1mol电子放出的热量为
。该反应过程中每转移1mol电子放出的热量为_________ kJ。
(4)工业上乙烯催化氧化制乙醛的反应原理为: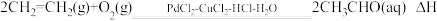 ,该反应原理可以拆解为如下三步反应:
,该反应原理可以拆解为如下三步反应:
I.
II.……
III.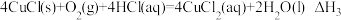
若第II步反应的反应热为 ,且
,且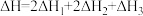 ,则第II步反应的热化学方程式为
,则第II步反应的热化学方程式为__ 。
(5)山西是全国最大的炼焦用煤资源基地,炼焦过程的副产品之一焦炉煤气富含H2、CH4和CO,因此可通过甲烷化反应来提高热值,使绝大部分CO、CO2转化成CH4.甲烷化反应的主要化学原理为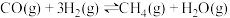 ,已知CO分子中的C与O之间为共价三键。下表所列为常见化学键的键能数据(键能指气态分子中1mol化学键解离成气态原子所吸收的能量):
,已知CO分子中的C与O之间为共价三键。下表所列为常见化学键的键能数据(键能指气态分子中1mol化学键解离成气态原子所吸收的能量):
该反应的
__________  。
。
(1)已知CH3OH(l)的燃烧热
 ,
,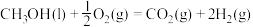
 ,则
,则
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(2)Cl2(g)和H2O(g)通过灼热的炭层,生成HCl(g)和CO2(g),当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式:
(3)火箭和导弹表面的薄层是耐高温物质。下列反应可制得耐高温材料,热化学方程式为
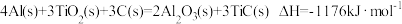 。该反应过程中每转移1mol电子放出的热量为
。该反应过程中每转移1mol电子放出的热量为(4)工业上乙烯催化氧化制乙醛的反应原理为:
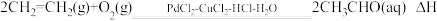 ,该反应原理可以拆解为如下三步反应:
,该反应原理可以拆解为如下三步反应:I.

II.……
III.
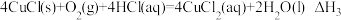
若第II步反应的反应热为
 ,且
,且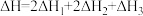 ,则第II步反应的热化学方程式为
,则第II步反应的热化学方程式为(5)山西是全国最大的炼焦用煤资源基地,炼焦过程的副产品之一焦炉煤气富含H2、CH4和CO,因此可通过甲烷化反应来提高热值,使绝大部分CO、CO2转化成CH4.甲烷化反应的主要化学原理为
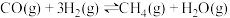 ,已知CO分子中的C与O之间为共价三键。下表所列为常见化学键的键能数据(键能指气态分子中1mol化学键解离成气态原子所吸收的能量):
,已知CO分子中的C与O之间为共价三键。下表所列为常见化学键的键能数据(键能指气态分子中1mol化学键解离成气态原子所吸收的能量):| 化学键 |  |  |  |  |  |  |
键能/( ) ) | 347.7 | 413.4 | 436 | 351 | 1065 | 462.8 |

 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】硒(Se)是第四周期VIA族元素,是人体内不可或缺的微量元素,其氢化物H2Se是制备新型光伏太阳能电池、半导体材料和金属硒化物的基础原料。
(1)T°C时,向一恒容密闭容器中加入3molH2和1molSe,发生反应H2(g)+Se(s)⇌H2Se(g)。以5小时内得到的H2Se为产量指标,且温度、压强对H2Se产率的影响如图1、图2所示:
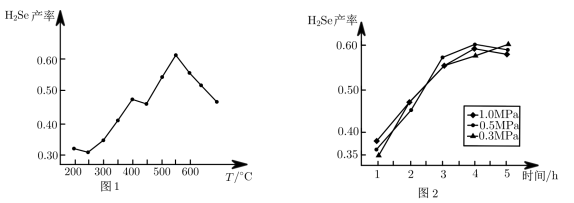
则制备H2Se的最佳温度和压强为_____ 。
(2)由H2Se在一定条件下制备CuSe,已知25℃时CuSe的Ksp=7.9×10-49,CuS的Ksp=l.3×10-36,则反应CuS(s)+Se2-(aq)⇌CuSe(s)+S2-(aq)的化学平衡常数K=____ (保留2位有效数字)。
(1)T°C时,向一恒容密闭容器中加入3molH2和1molSe,发生反应H2(g)+Se(s)⇌H2Se(g)。以5小时内得到的H2Se为产量指标,且温度、压强对H2Se产率的影响如图1、图2所示:

则制备H2Se的最佳温度和压强为
(2)由H2Se在一定条件下制备CuSe,已知25℃时CuSe的Ksp=7.9×10-49,CuS的Ksp=l.3×10-36,则反应CuS(s)+Se2-(aq)⇌CuSe(s)+S2-(aq)的化学平衡常数K=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
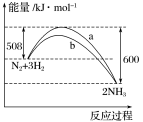
【推荐3】N2与H2反应生成NH3的过程中能量变化曲线如图所示。若在一个固定容积的密闭容器中充入1 mol N2和3 mol H2,使反应N2+3H2 2NH3达到平衡,测得反应放出热量为Q1。
2NH3达到平衡,测得反应放出热量为Q1。
填写下列空白:
(1)Q1________ 92 kJ(填“>”“<”或“=”)。
(2)b曲线是________ 时的能量变化曲线。
(3)上述条件下达到平衡时H2的转化率为________ 。
(4)在温度体积一定的条件下,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则2Q1与Q2的关系为______________ 。
 2NH3达到平衡,测得反应放出热量为Q1。
2NH3达到平衡,测得反应放出热量为Q1。
填写下列空白:
(1)Q1
(2)b曲线是
(3)上述条件下达到平衡时H2的转化率为
(4)在温度体积一定的条件下,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则2Q1与Q2的关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】完成下列问题。
(1)研究化学物质的方法有很多,常用的有①核磁共振氢谱②蒸馏③重结晶④萃取⑤过滤⑥红外光谱,其中用于分子结构确定的有______ (填序号)
(2)下列物质中,其核磁共振氢谱中只有一个吸收峰的是______(填字母)。
(3)7.4 g某有机物甲在足量的氧气中完成燃烧,生成17.6 g  和9 g
和9 g  。
。______ ,分子式为______ 。
②确定甲的官能团:通过实验可知甲中一定含有羟基,甲可能的结构有______ 种。
③确定甲的结构简式:
a.经测定有机物甲的核磁共振氢谱如图b所示,则甲的结构简式为____________ 。
b.若甲的红外光谱如图c所示,则该有机物的结构简式为____________ 。
(1)研究化学物质的方法有很多,常用的有①核磁共振氢谱②蒸馏③重结晶④萃取⑤过滤⑥红外光谱,其中用于分子结构确定的有
(2)下列物质中,其核磁共振氢谱中只有一个吸收峰的是______(填字母)。
A. | B. | C. | D. |
 和9 g
和9 g  。
。
②确定甲的官能团:通过实验可知甲中一定含有羟基,甲可能的结构有
③确定甲的结构简式:
a.经测定有机物甲的核磁共振氢谱如图b所示,则甲的结构简式为
b.若甲的红外光谱如图c所示,则该有机物的结构简式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】称取某有机物(含C、H、O元素)2.3g样品,经充分燃烧后,产生CO24.4g、H2O2.7g。计算:
(1)该有机物中C、H、O原子个数比_______ 。
(2)若该有机物的相对分子质量为46,且能与金属钠反应放出氢气,请写出该有机物的结构简式_______ 。
(1)该有机物中C、H、O原子个数比
(2)若该有机物的相对分子质量为46,且能与金属钠反应放出氢气,请写出该有机物的结构简式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】根据所学,回答下列问题并按要求填空:
(1)①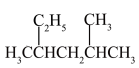 给此有机物予以命名
给此有机物予以命名________
② 的系统命名为:
的系统命名为:_____ 。
③写出有机化合物的结构简式:3-乙基-2-戊醇_____
(2)按要求完成下列反应化学方程式:
①CH3-CH2-Br 与氢氧化钠溶液在加热条件下的反应:____ 。
②乙醛与银氨溶液水浴加热条件下的反应:____ 。
③甲苯和硝酸合成炸药 TNT 的化学方程式:____ ;
④氯乙烯为单体合成塑料聚氯乙烯(PVC)的化学方程式:____ ;
⑤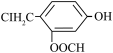 与 NaOH溶液在加热条件下的化学反应方程式
与 NaOH溶液在加热条件下的化学反应方程式________________ 。
(3)下列括号内的物质为杂质,将除去下列各组混合物中杂质所需的试剂填写在横线上:
①乙酸乙酯(乙醇)_____ ;②甲苯(溴)_____ ;
(4)某有机化合物 A 的相对分子质量为 60,分子中含碳 40%,含氢 6.6%,其余为氧。
①通过计算确定该有机物的分子式_____ ;
②按中学常见官能团,写出两个其链状结构的有机物可能的结构简式:_____ 、_____ 。
(5)某有机物的结构简式为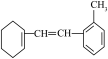 据此填写下列空格。
据此填写下列空格。
①该物质苯环上一氯代物有_____ 种;
②1mol 该物质和溴水混合,消耗 Br2的物质的量为_____ mol;
(1)①
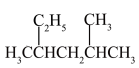 给此有机物予以命名
给此有机物予以命名②
 的系统命名为:
的系统命名为:③写出有机化合物的结构简式:3-乙基-2-戊醇
(2)按要求完成下列反应化学方程式:
①CH3-CH2-Br 与氢氧化钠溶液在加热条件下的反应:
②乙醛与银氨溶液水浴加热条件下的反应:
③甲苯和硝酸合成炸药 TNT 的化学方程式:
④氯乙烯为单体合成塑料聚氯乙烯(PVC)的化学方程式:
⑤
 与 NaOH溶液在加热条件下的化学反应方程式
与 NaOH溶液在加热条件下的化学反应方程式(3)下列括号内的物质为杂质,将除去下列各组混合物中杂质所需的试剂填写在横线上:
①乙酸乙酯(乙醇)
(4)某有机化合物 A 的相对分子质量为 60,分子中含碳 40%,含氢 6.6%,其余为氧。
①通过计算确定该有机物的分子式
②按中学常见官能团,写出两个其链状结构的有机物可能的结构简式:
(5)某有机物的结构简式为
 据此填写下列空格。
据此填写下列空格。①该物质苯环上一氯代物有
②1mol 该物质和溴水混合,消耗 Br2的物质的量为
您最近一年使用:0次



