已知25℃、101kPa下,石墨、金刚石燃烧的热化学方程式分别为
C(石墨)+O2(g)=CO2(g)ΔH=-393.51kJ·mol-1
C(金刚石)+O2(g)=CO2(g)ΔH=-395.41kJ·mol-1
据此判断,下列说法中正确的是( )
A.由石墨制备金刚石是吸热反应;石墨的能量比金刚石的低
B.由石墨制备金刚石是吸热反应;石墨的能量比金刚石的高
C.由石墨制备金刚石是放热反应;石墨的能量比金刚石的低
D.由石墨制备金刚石是放热反应;石墨的能量比金刚石的高
相同温度时,下列两个反应的反应热分别用ΔH1和ΔH2表示,则( )
①H2(g)+ O2(g)=H2O(g)ΔH1=-Q1kJ·mol-1
O2(g)=H2O(g)ΔH1=-Q1kJ·mol-1
②2H2O(l)=2H2(g)+O2(g)ΔH2=+Q2kJ·mol-1
A.Q1>Q2 B.Q1=Q2 C.2Q1<Q2 D. Q2=Q1
Q2=Q1
C(石墨)+O2(g)=CO2(g)ΔH=-393.51kJ·mol-1
C(金刚石)+O2(g)=CO2(g)ΔH=-395.41kJ·mol-1
据此判断,下列说法中正确的是
A.由石墨制备金刚石是吸热反应;石墨的能量比金刚石的低
B.由石墨制备金刚石是吸热反应;石墨的能量比金刚石的高
C.由石墨制备金刚石是放热反应;石墨的能量比金刚石的低
D.由石墨制备金刚石是放热反应;石墨的能量比金刚石的高
相同温度时,下列两个反应的反应热分别用ΔH1和ΔH2表示,则
①H2(g)+
 O2(g)=H2O(g)ΔH1=-Q1kJ·mol-1
O2(g)=H2O(g)ΔH1=-Q1kJ·mol-1②2H2O(l)=2H2(g)+O2(g)ΔH2=+Q2kJ·mol-1
A.Q1>Q2 B.Q1=Q2 C.2Q1<Q2 D.
 Q2=Q1
Q2=Q1
更新时间:2020-12-14 20:41:45
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】实验是化学学习的基础,请完成以下实验填空:
(1)某实验小组用0.50mol/LNaOH溶液和0.55mol/L硫酸溶液进行中和热的测定,取50mLNaOH溶液和25mL硫酸溶液进行实验,实验数据如表。
近似认为0.50mol/LNaOH溶液和0.55mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃),则该中和反应生成1molH2O反应热△H=____ (取小数点后两位)。
(2)已知:P(s,白磷)=P(s,黑磷) ΔH=-39.3kJ•mol-1;
P(s,白磷)=P(s,红磷) ΔH=-17.6kJ•mol-1;
由此推知,其中最稳定的磷单质是____ 。
(3)在298K、100kPa时,已知:C(s,石墨)的燃烧热为393.5kJ•mol-1;
H2(g)的燃烧热为285.8kJ•mol-1;C2H2(g)的燃烧热为1299.5kJ•mol-1。
则2C(s,石墨)+H2(g) C2H2(g) △H=
C2H2(g) △H=____ kJ•mol-1。
(4)在2L的恒温容器中加入240g石墨和足量氢气发生反应:2C(s,石墨)+H2(g) C2H2(g)。能判断该反应达到化学平衡状态的依据是
C2H2(g)。能判断该反应达到化学平衡状态的依据是____ 。
A.v(H2)=v(C2H2)
B.容器中的气体压强不再改变
C.容器中的气体密度不再改变
D.石墨的质量不再改变
E.断开1molH-H键时,同时生成2molC-H键
(5)在绝热恒容密闭容器中加入1molX和3molY发生反应:X(g)+3Y(g) 4Z(g) △H<0。
4Z(g) △H<0。
①相同时间内生成Z的量比恒温恒容时多,原因是___ 。
②当气体压强不再变化时,该反应____ (填“是”或“否”)达到平衡状态。
(1)某实验小组用0.50mol/LNaOH溶液和0.55mol/L硫酸溶液进行中和热的测定,取50mLNaOH溶液和25mL硫酸溶液进行实验,实验数据如表。
| 温度 实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.6 | a |
| 2 | 27.0 | 27.4 | 27.2 | 31.8 | |
| 3 | 25.9 | 25.9 | 25.9 | 30.3 | |
| 4 | 26.4 | 26.2 | 26.3 | 31.9 | |
近似认为0.50mol/LNaOH溶液和0.55mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃),则该中和反应生成1molH2O反应热△H=
(2)已知:P(s,白磷)=P(s,黑磷) ΔH=-39.3kJ•mol-1;
P(s,白磷)=P(s,红磷) ΔH=-17.6kJ•mol-1;
由此推知,其中最稳定的磷单质是
(3)在298K、100kPa时,已知:C(s,石墨)的燃烧热为393.5kJ•mol-1;
H2(g)的燃烧热为285.8kJ•mol-1;C2H2(g)的燃烧热为1299.5kJ•mol-1。
则2C(s,石墨)+H2(g)
 C2H2(g) △H=
C2H2(g) △H=(4)在2L的恒温容器中加入240g石墨和足量氢气发生反应:2C(s,石墨)+H2(g)
 C2H2(g)。能判断该反应达到化学平衡状态的依据是
C2H2(g)。能判断该反应达到化学平衡状态的依据是A.v(H2)=v(C2H2)
B.容器中的气体压强不再改变
C.容器中的气体密度不再改变
D.石墨的质量不再改变
E.断开1molH-H键时,同时生成2molC-H键
(5)在绝热恒容密闭容器中加入1molX和3molY发生反应:X(g)+3Y(g)
 4Z(g) △H<0。
4Z(g) △H<0。①相同时间内生成Z的量比恒温恒容时多,原因是
②当气体压强不再变化时,该反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据要求,回答下列问题:
Ⅰ.有机物M经过太阳光光照可转化成有机物N,转化过程如下:

(1)两者中,较稳定的是:___________ (M或N)。
Ⅱ.已知: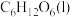 的燃烧热
的燃烧热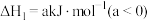 ;
; ,
,
(2)则
___________ a(填“>”“<”或“=”)。
Ⅲ.用如图所示的装置测定中和反应反应热。
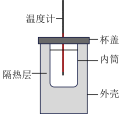
(3)从实验装置上看,还缺少___________ ,其能否用铁质材料替代?___________ (填“能”或“不能”)
(4)装置中隔热层的作用是___________
(5)实验中如果用相同体积、相同浓度的醋酸代替盐酸,测得的中和反应反应热的数值将___________ (填偏大、偏小或无影响)
Ⅰ.有机物M经过太阳光光照可转化成有机物N,转化过程如下:

(1)两者中,较稳定的是:
Ⅱ.已知:
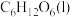 的燃烧热
的燃烧热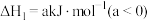 ;
; ,
,(2)则

Ⅲ.用如图所示的装置测定中和反应反应热。

(3)从实验装置上看,还缺少
(4)装置中隔热层的作用是
(5)实验中如果用相同体积、相同浓度的醋酸代替盐酸,测得的中和反应反应热的数值将
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化学反应过程中释放或吸收的热量在生活、生产、科技及科学研究中具有广泛的应用。
(1)“神舟”系列火箭用偏二甲肼 作燃料,
作燃料, 作氧化剂,反应后产物无污染。
作氧化剂,反应后产物无污染。
已知:
反应1: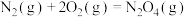
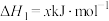 ;
;
反应2: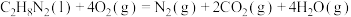
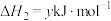 。
。
写出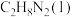 和
和 反应生成
反应生成 、
、 、
、 的热化学方程式:
的热化学方程式:_______ 。
(2)已知某金属氧化物催化丙烷脱氢过程中,部分反应进程如图,则能 过程中的焓变为
过程中的焓变为_______ (列式表示)。
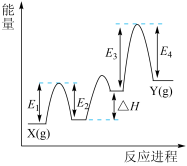
(3)已知,在25℃和101kPa下,部分化学键的键能数据如表所示。
①在25℃和101kPa下,工业合成氨的反应中每生成1mol 就会放出46kJ热量,在该条件下,向某容器中加入2mol
就会放出46kJ热量,在该条件下,向某容器中加入2mol 、6mol
、6mol 及合适的催化剂,充分反应后测得其放出的热量小于92kJ,原因可能是
及合适的催化剂,充分反应后测得其放出的热量小于92kJ,原因可能是_______ ,表中的a=_______ 。
②科学家发现了一种新的气态分子 (
(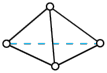 ),在25℃和101kPa下,
),在25℃和101kPa下, 转化为
转化为 的热化学方程式为
的热化学方程式为_______ ,此可知1mol 与1mol
与1mol 中能量更低的是
中能量更低的是_______ (填化学式)。
③已知:
 。甲烷是一种常用燃料,则表示甲烷的燃烧热的热化学方程式为
。甲烷是一种常用燃料,则表示甲烷的燃烧热的热化学方程式为_______ 。
(1)“神舟”系列火箭用偏二甲肼
 作燃料,
作燃料, 作氧化剂,反应后产物无污染。
作氧化剂,反应后产物无污染。已知:
反应1:
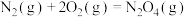
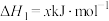 ;
;反应2:
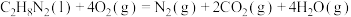
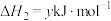 。
。写出
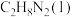 和
和 反应生成
反应生成 、
、 、
、 的热化学方程式:
的热化学方程式:(2)已知某金属氧化物催化丙烷脱氢过程中,部分反应进程如图,则能
 过程中的焓变为
过程中的焓变为
(3)已知,在25℃和101kPa下,部分化学键的键能数据如表所示。
| 化学键 | H—H | H—N | N≡N | O=O | C—H | C=O | H—O | N—N |
键能/( ) ) | 436 | 391 | a | 498 | 414 | 803 | 462 | 193 |
①在25℃和101kPa下,工业合成氨的反应中每生成1mol
 就会放出46kJ热量,在该条件下,向某容器中加入2mol
就会放出46kJ热量,在该条件下,向某容器中加入2mol 、6mol
、6mol 及合适的催化剂,充分反应后测得其放出的热量小于92kJ,原因可能是
及合适的催化剂,充分反应后测得其放出的热量小于92kJ,原因可能是②科学家发现了一种新的气态分子
 (
( ),在25℃和101kPa下,
),在25℃和101kPa下, 转化为
转化为 的热化学方程式为
的热化学方程式为 与1mol
与1mol 中能量更低的是
中能量更低的是③已知:

 。甲烷是一种常用燃料,则表示甲烷的燃烧热的热化学方程式为
。甲烷是一种常用燃料,则表示甲烷的燃烧热的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】请根据所学知识回答下列问题:
(1)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2,ΔH1__ ΔH2(填“>”、“<”或“=”,下同)。
(2)相同条件下,2 mol氢原子所具有的能量__ 1 mol氢分子所具有的能量。
(3)已知常温时红磷比白磷稳定,比较下列反应中ΔH的大小:ΔH1__ ΔH2。
①P4(白磷,s)+5O2(g)= 2P2O5(s)ΔH1
②4P(红磷,s)+5O2(g)= 2P2O5(s)ΔH2
(4)已知:稀溶液中,H+(aq)+OH﹣(aq)= H2O(l)ΔH=﹣57.3 kJ/mol,则浓硫酸与稀氢氧化钠溶液反应生成1 mol水,放出的热量__ 57.3 kJ.
(5)已知:0.5 mol CH4(g)与0.5 mol水蒸气在t℃、pkPa时,完全反应生成CO和H2的混合气体,吸收了akJ热量,该反应的热化学方程式是____________ 。
(1)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2,ΔH1
(2)相同条件下,2 mol氢原子所具有的能量
(3)已知常温时红磷比白磷稳定,比较下列反应中ΔH的大小:ΔH1
①P4(白磷,s)+5O2(g)= 2P2O5(s)ΔH1
②4P(红磷,s)+5O2(g)= 2P2O5(s)ΔH2
(4)已知:稀溶液中,H+(aq)+OH﹣(aq)= H2O(l)ΔH=﹣57.3 kJ/mol,则浓硫酸与稀氢氧化钠溶液反应生成1 mol水,放出的热量
(5)已知:0.5 mol CH4(g)与0.5 mol水蒸气在t℃、pkPa时,完全反应生成CO和H2的混合气体,吸收了akJ热量,该反应的热化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】中和热是一类重要的反应热,也是化学研究的重要课题。已知强酸稀溶液与强碱稀溶液发生反应生成1 mol H2O(l)的焓变为:ΔH1=-57.3 kJ/mol。
(1)下列各组试剂混合发生反应的离子方程式为H++OH-=H2O的是_______ (填字母)。
A.稀硫酸与氢氧化钡溶液
B.盐酸与氢氧化钠溶液
C.浓硫酸与氢氧化钠固体
D.硫酸氢钠溶液与氢氧化钾溶液
E.氢氧化镁溶于稀盐酸
(2)若稀硫酸与氢氧化钡稀溶液反应生成1 mol H2O(l),则反应放出的热量_______ (填“大于”“等于”或“小于”)57.3 kJ,原因是_______ (从化学键的角度简单解释即可)。
(3)若稀硫酸与氢氧化钠固体反应生成1 mol H2O(l),则反应放出的热量_______ (填“大于”“等于”或“小于”)57.3 kJ,原因是_______ 。
(4)醋酸(CH3COOH)是一种常见弱酸,醋酸与氢氧化钠稀溶液反应生成1 mol H2O(l) 的焓变为: ΔH2=a kJ/mol,则ΔH1和ΔH2的大小关系为ΔH1_______ ΔH2(填“>”“=”或“<”)。
(1)下列各组试剂混合发生反应的离子方程式为H++OH-=H2O的是
A.稀硫酸与氢氧化钡溶液
B.盐酸与氢氧化钠溶液
C.浓硫酸与氢氧化钠固体
D.硫酸氢钠溶液与氢氧化钾溶液
E.氢氧化镁溶于稀盐酸
(2)若稀硫酸与氢氧化钡稀溶液反应生成1 mol H2O(l),则反应放出的热量
(3)若稀硫酸与氢氧化钠固体反应生成1 mol H2O(l),则反应放出的热量
(4)醋酸(CH3COOH)是一种常见弱酸,醋酸与氢氧化钠稀溶液反应生成1 mol H2O(l) 的焓变为: ΔH2=a kJ/mol,则ΔH1和ΔH2的大小关系为ΔH1
您最近一年使用:0次
【推荐3】完成下列问题。
(1)第十四届运动会于2021年9月15日在西安奥体中心体育场隆重开幕,00”后体坛新秀杨倩,带着我们共同的希望和梦想,点燃主火炬。火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料。试回答下列问题:
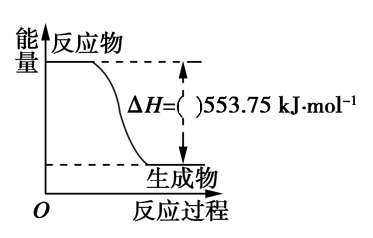
①如图是一定量丙烷完全燃烧生成CO2和1molH2O(l)过程中的能量变化图,图中的括号内应该填入___________ 。(“+”或“−”)
②写出表示丙烷燃烧热的热化学方程式:___________ 。
③二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1mol二甲醚完全燃烧生成CO2和液态水放出1455kJ热量。若1mol丙烷和二甲醚的混合气体完全燃烧生成CO2和液态水共放出1645kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为___________ 。
(2)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160kJ/mol
若用标准状况下4.48LCH4还原NO2生成N2,反应中转移的电子总数为___________ (用阿伏加德罗常数NA表示),放出的热量为___________ kJ。
(3)反应热大小比较(填“>”“<”或“=”)
A(g)+B(g)=C(g) ΔH1<0;A(g)+B(g)=C(l) ΔH2<0,则ΔH1___________ ΔH2
S(g)+O2(g)=SO2(g) ΔH1<0;S(s)+O2(g)=SO2(g) ΔH2<0,则ΔH1___________ ΔH2
C(s)+O2(g)=CO2(g) ΔH1<0;C(s)+ O2(g)=CO(g) ΔH2<0,则ΔH1
O2(g)=CO(g) ΔH2<0,则ΔH1___________ ΔH2
(1)第十四届运动会于2021年9月15日在西安奥体中心体育场隆重开幕,00”后体坛新秀杨倩,带着我们共同的希望和梦想,点燃主火炬。火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料。试回答下列问题:
①如图是一定量丙烷完全燃烧生成CO2和1molH2O(l)过程中的能量变化图,图中的括号内应该填入

②写出表示丙烷燃烧热的热化学方程式:
③二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1mol二甲醚完全燃烧生成CO2和液态水放出1455kJ热量。若1mol丙烷和二甲醚的混合气体完全燃烧生成CO2和液态水共放出1645kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为
(2)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160kJ/mol
若用标准状况下4.48LCH4还原NO2生成N2,反应中转移的电子总数为
(3)反应热大小比较(填“>”“<”或“=”)
A(g)+B(g)=C(g) ΔH1<0;A(g)+B(g)=C(l) ΔH2<0,则ΔH1
S(g)+O2(g)=SO2(g) ΔH1<0;S(s)+O2(g)=SO2(g) ΔH2<0,则ΔH1
C(s)+O2(g)=CO2(g) ΔH1<0;C(s)+
 O2(g)=CO(g) ΔH2<0,则ΔH1
O2(g)=CO(g) ΔH2<0,则ΔH1
您最近一年使用:0次



