实验是化学学习的基础,请完成以下实验填空:
(1)某实验小组用0.50mol/LNaOH溶液和0.55mol/L硫酸溶液进行中和热的测定,取50mLNaOH溶液和25mL硫酸溶液进行实验,实验数据如表。
近似认为0.50mol/LNaOH溶液和0.55mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃),则该中和反应生成1molH2O反应热△H=____ (取小数点后两位)。
(2)已知:P(s,白磷)=P(s,黑磷) ΔH=-39.3kJ•mol-1;
P(s,白磷)=P(s,红磷) ΔH=-17.6kJ•mol-1;
由此推知,其中最稳定的磷单质是____ 。
(3)在298K、100kPa时,已知:C(s,石墨)的燃烧热为393.5kJ•mol-1;
H2(g)的燃烧热为285.8kJ•mol-1;C2H2(g)的燃烧热为1299.5kJ•mol-1。
则2C(s,石墨)+H2(g) C2H2(g) △H=
C2H2(g) △H=____ kJ•mol-1。
(4)在2L的恒温容器中加入240g石墨和足量氢气发生反应:2C(s,石墨)+H2(g) C2H2(g)。能判断该反应达到化学平衡状态的依据是
C2H2(g)。能判断该反应达到化学平衡状态的依据是____ 。
A.v(H2)=v(C2H2)
B.容器中的气体压强不再改变
C.容器中的气体密度不再改变
D.石墨的质量不再改变
E.断开1molH-H键时,同时生成2molC-H键
(5)在绝热恒容密闭容器中加入1molX和3molY发生反应:X(g)+3Y(g) 4Z(g) △H<0。
4Z(g) △H<0。
①相同时间内生成Z的量比恒温恒容时多,原因是___ 。
②当气体压强不再变化时,该反应____ (填“是”或“否”)达到平衡状态。
(1)某实验小组用0.50mol/LNaOH溶液和0.55mol/L硫酸溶液进行中和热的测定,取50mLNaOH溶液和25mL硫酸溶液进行实验,实验数据如表。
| 温度 实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.6 | a |
| 2 | 27.0 | 27.4 | 27.2 | 31.8 | |
| 3 | 25.9 | 25.9 | 25.9 | 30.3 | |
| 4 | 26.4 | 26.2 | 26.3 | 31.9 | |
近似认为0.50mol/LNaOH溶液和0.55mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃),则该中和反应生成1molH2O反应热△H=
(2)已知:P(s,白磷)=P(s,黑磷) ΔH=-39.3kJ•mol-1;
P(s,白磷)=P(s,红磷) ΔH=-17.6kJ•mol-1;
由此推知,其中最稳定的磷单质是
(3)在298K、100kPa时,已知:C(s,石墨)的燃烧热为393.5kJ•mol-1;
H2(g)的燃烧热为285.8kJ•mol-1;C2H2(g)的燃烧热为1299.5kJ•mol-1。
则2C(s,石墨)+H2(g)
 C2H2(g) △H=
C2H2(g) △H=(4)在2L的恒温容器中加入240g石墨和足量氢气发生反应:2C(s,石墨)+H2(g)
 C2H2(g)。能判断该反应达到化学平衡状态的依据是
C2H2(g)。能判断该反应达到化学平衡状态的依据是A.v(H2)=v(C2H2)
B.容器中的气体压强不再改变
C.容器中的气体密度不再改变
D.石墨的质量不再改变
E.断开1molH-H键时,同时生成2molC-H键
(5)在绝热恒容密闭容器中加入1molX和3molY发生反应:X(g)+3Y(g)
 4Z(g) △H<0。
4Z(g) △H<0。①相同时间内生成Z的量比恒温恒容时多,原因是
②当气体压强不再变化时,该反应
更新时间:2022-10-27 11:56:47
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】按题意要求填空:
(1)已知 己烷完全燃烧生成液态水放出
己烷完全燃烧生成液态水放出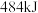 的热量,写出表示己烷燃烧热的热化学方程
的热量,写出表示己烷燃烧热的热化学方程_______ 。
(2)已知在微生物作用的条件下, 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
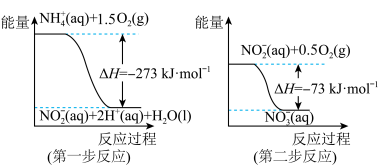
则 全部被氧化成
全部被氧化成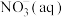 的热化学方程式为:
的热化学方程式为:_______ 。
(3)化学键的键能是原子间形成(或断裂) 化学键时释放(或吸收)的能量。以下是部分共价键键能数据:H-S:
化学键时释放(或吸收)的能量。以下是部分共价键键能数据:H-S: ;S-S:
;S-S: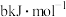 ;S=O:
;S=O: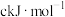 ;H-O:
;H-O: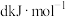 。
。
已知反应:
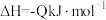 ,其反应产物中的固体
,其反应产物中的固体 实为
实为 ,实际分子是一个8元环状分子(即
,实际分子是一个8元环状分子(即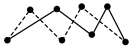 ),试根据这些数据计算已知反应的反应热:则
),试根据这些数据计算已知反应的反应热:则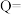
_______ (用a、b、c、d表示)。若已知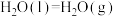
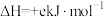 ,试写出
,试写出 和
和 反应生成
反应生成 的热化学方程式为:
的热化学方程式为:_______ 。
(4)已知 (金刚石,s)
(金刚石,s)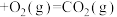
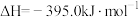
 (石墨,s)
(石墨,s)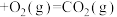
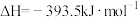
①石墨和金刚石相比,石墨的稳定性_______ 金刚石的稳定性。(填“大于”“小于”或“等于”,下同)
②石墨中 键键能
键键能_______ 金刚石中 键键能。
键键能。
(5)把煤作为燃料有下列两种途径:
途径I:
 ①
①
途径II:先制成水煤气:
 ②
②
再燃烧水煤气:
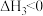 ③
③

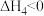 ④
④
则途径I放出的热量_______ (填“大于”“等于”或“小于”)途径II放出的热量; 、
、 、
、 、
、 的数学关系式是
的数学关系式是_______ 。
(6)某学生在测定稀盐酸和氢氧化钠稀溶液发生中和反应的反应热的实验前,先配制 的
的 溶液:若实验中大约要使用
溶液:若实验中大约要使用 溶液需要用托盘天平称量
溶液需要用托盘天平称量 固体
固体_______  ,溶液配制过程中所需用到的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和
,溶液配制过程中所需用到的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和_______ 。
(1)已知
 己烷完全燃烧生成液态水放出
己烷完全燃烧生成液态水放出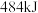 的热量,写出表示己烷燃烧热的热化学方程
的热量,写出表示己烷燃烧热的热化学方程(2)已知在微生物作用的条件下,
 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
则
 全部被氧化成
全部被氧化成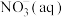 的热化学方程式为:
的热化学方程式为:(3)化学键的键能是原子间形成(或断裂)
 化学键时释放(或吸收)的能量。以下是部分共价键键能数据:H-S:
化学键时释放(或吸收)的能量。以下是部分共价键键能数据:H-S: ;S-S:
;S-S: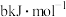 ;S=O:
;S=O: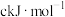 ;H-O:
;H-O: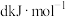 。
。已知反应:

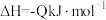 ,其反应产物中的固体
,其反应产物中的固体 实为
实为 ,实际分子是一个8元环状分子(即
,实际分子是一个8元环状分子(即 ),试根据这些数据计算已知反应的反应热:则
),试根据这些数据计算已知反应的反应热:则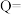
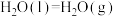
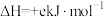 ,试写出
,试写出 和
和 反应生成
反应生成 的热化学方程式为:
的热化学方程式为:(4)已知
 (金刚石,s)
(金刚石,s)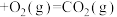
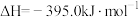
 (石墨,s)
(石墨,s)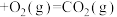
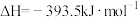
①石墨和金刚石相比,石墨的稳定性
②石墨中
 键键能
键键能 键键能。
键键能。(5)把煤作为燃料有下列两种途径:
途径I:

 ①
①途径II:先制成水煤气:

 ②
②再燃烧水煤气:

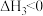 ③
③
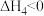 ④
④则途径I放出的热量
 、
、 、
、 、
、 的数学关系式是
的数学关系式是(6)某学生在测定稀盐酸和氢氧化钠稀溶液发生中和反应的反应热的实验前,先配制
 的
的 溶液:若实验中大约要使用
溶液:若实验中大约要使用 溶液需要用托盘天平称量
溶液需要用托盘天平称量 固体
固体 ,溶液配制过程中所需用到的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和
,溶液配制过程中所需用到的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据要求,回答下列问题:
Ⅰ.有机物M经过太阳光光照可转化成有机物N,转化过程如下:

(1)两者中,较稳定的是:___________ (M或N)。
Ⅱ.已知: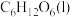 的燃烧热
的燃烧热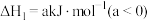 ;
; ,
,
(2)则
___________ a(填“>”“<”或“=”)。
Ⅲ.用如图所示的装置测定中和反应反应热。
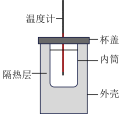
(3)从实验装置上看,还缺少___________ ,其能否用铁质材料替代?___________ (填“能”或“不能”)
(4)装置中隔热层的作用是___________
(5)实验中如果用相同体积、相同浓度的醋酸代替盐酸,测得的中和反应反应热的数值将___________ (填偏大、偏小或无影响)
Ⅰ.有机物M经过太阳光光照可转化成有机物N,转化过程如下:

(1)两者中,较稳定的是:
Ⅱ.已知:
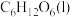 的燃烧热
的燃烧热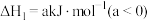 ;
; ,
,(2)则

Ⅲ.用如图所示的装置测定中和反应反应热。

(3)从实验装置上看,还缺少
(4)装置中隔热层的作用是
(5)实验中如果用相同体积、相同浓度的醋酸代替盐酸,测得的中和反应反应热的数值将
您最近一年使用:0次
【推荐3】金刚石和石墨为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时完全燃烧生成二氧化碳,1mol金刚石和石墨分别与O2反应,放出的热量如图所示,回答下列问题:
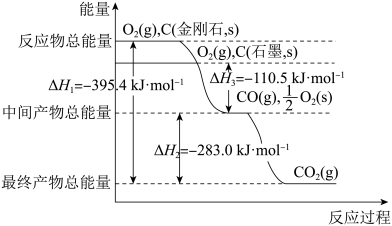
(1)金刚石、石墨与O2反应生成CO2均是_______ 反应(填“放热”或“吸热”),在通常状况下,金刚石和石墨的稳定性较大的是_______ (填“金刚石”或“石墨”);
(2)石墨的燃烧热△H=_______ kJ·mol-1,反应C(金刚石,s)=C(石墨,s)的反应热△H=_______ kJ·mol-1;
(3)12g石墨在一定量空气中燃烧,生成36g气体,该过程放出的热量为_______ kJ。

(1)金刚石、石墨与O2反应生成CO2均是
(2)石墨的燃烧热△H=
(3)12g石墨在一定量空气中燃烧,生成36g气体,该过程放出的热量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】将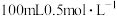 盐酸与
盐酸与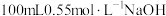 溶液在量热计中进行中和反应(可将稀酸、稀碱的密度近似与水的密度相等,生成溶液的比热容
溶液在量热计中进行中和反应(可将稀酸、稀碱的密度近似与水的密度相等,生成溶液的比热容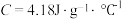 )。
)。
i.若温度计示数从 升高到
升高到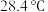 ,则中和反应的反应热
,则中和反应的反应热
______  。
。
ii.若分多次将NaOH溶液倒入内筒中,则测得中和热 的绝对值将
的绝对值将______ (选填“A:偏大”“B:偏小”或“C:不变”,下同);若配制 溶液时俯视容量瓶的刻度线,则测得中和热
溶液时俯视容量瓶的刻度线,则测得中和热 的绝对值将
的绝对值将______ 。
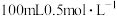 盐酸与
盐酸与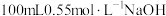 溶液在量热计中进行中和反应(可将稀酸、稀碱的密度近似与水的密度相等,生成溶液的比热容
溶液在量热计中进行中和反应(可将稀酸、稀碱的密度近似与水的密度相等,生成溶液的比热容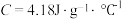 )。
)。i.若温度计示数从
 升高到
升高到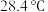 ,则中和反应的反应热
,则中和反应的反应热
 。
。ii.若分多次将NaOH溶液倒入内筒中,则测得中和热
 的绝对值将
的绝对值将 溶液时俯视容量瓶的刻度线,则测得中和热
溶液时俯视容量瓶的刻度线,则测得中和热 的绝对值将
的绝对值将
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据要求回答问题:
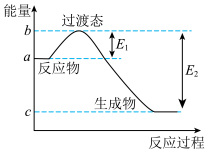
(1)如图是1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,活化能E1的变化是_____ (填“增大”“减小”或“不变”,下同),ΔH的变化是_____ 。图中最稳定的是_____ (填“反应物”“过渡态”或“生成物”)。
(2)50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应反应热(设溶液的密度均为1g•cm-3,反应后溶液的比热容c=4.18J•g-1•℃-1)。回答下列问题:
从实验装置上看,图中仪器A的名称是_____ ,隔热层的作用是_____ 。根据表中数据,结合题干信息,请写出生成1molH2O的热化学方程式_____ (保留3位有效数字)。
(3)生产液晶显示器的过程中使用的化学清洗剂NF3是一种温室气体,其存储能量的能力是CO2的1.2~2.0万倍,在大气中的寿命可长达740年之久,表中是几种化学键的键能:
写出N2(g)与F2(g)反应合成NF3(g)的热化学方程式_____ 。
(4)在微生物作用的条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。这两步反应的能量变化如图:
。这两步反应的能量变化如图:
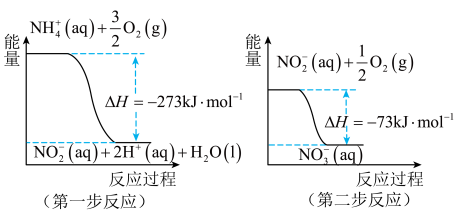
第二步反应是_____ (填“放热”或“吸热”)反应。1molNH (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是_____ 。
(1)如图是1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,活化能E1的变化是

(2)50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应反应热(设溶液的密度均为1g•cm-3,反应后溶液的比热容c=4.18J•g-1•℃-1)。回答下列问题:
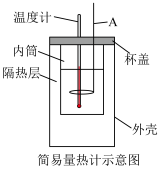 | 实验次数 | 反应物的温度/℃ | 反应前体系的温度 | 反应后体系的温度 | 温度差 | |
| 盐酸 | NaOH溶液 | t1/℃ | t2/℃ | (t2-t1)/℃ | ||
| 1 | 25.0 | 25.2 | 25.1 | 28.5 | 3.4 | |
| 2 | 24.9 | 25.1 | 25.0 | 28.3 | 3.3 | |
| 3 | 25.6 | 25.4 | 25.5 | 29.0 | 3.5 | |
(3)生产液晶显示器的过程中使用的化学清洗剂NF3是一种温室气体,其存储能量的能力是CO2的1.2~2.0万倍,在大气中的寿命可长达740年之久,表中是几种化学键的键能:
| 化学键 | N≡N | F-F | N-F |
| 键能/kJ•mol-1 | 941.7 | 154.8 | 283.0 |
(4)在微生物作用的条件下,NH
 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。这两步反应的能量变化如图:
。这两步反应的能量变化如图:
第二步反应是
 (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】结合已学化学反应原理知识回答下列问题。
(1)某同学欲进行中和反应反应热的测定,现进行以下实验。
①取 溶液和
溶液和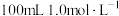 盐酸进行实验,测得反应前后温度差的平均值
盐酸进行实验,测得反应前后温度差的平均值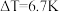 。若近似认为
。若近似认为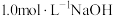 溶液和
溶液和 盐酸的密度都是
盐酸的密度都是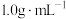 ,反应后生成溶液的比热容
,反应后生成溶液的比热容 ,则生成
,则生成 时的反应热
时的反应热
_______ (结果保留到小数点后一位)。
②强酸与强碱的稀溶液发生中和反应生成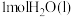 时的反应热
时的反应热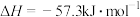 。若用一定浓度的稀硫酸与含
。若用一定浓度的稀硫酸与含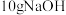 的稀碱溶液完全反应,则反应放出的热量为
的稀碱溶液完全反应,则反应放出的热量为_______ (结果保留到小数点后一位)。
(2)为比较 对
对 分解的催化效果,某实验小组同学设计了如图所示的实验。
分解的催化效果,某实验小组同学设计了如图所示的实验。
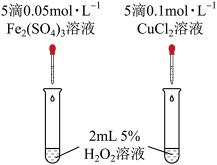
某同学认为通过观察_______ (填实验现象),可得出 的催化效果的差异。有同学提出将
的催化效果的差异。有同学提出将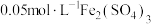 ,溶液改为
,溶液改为 溶液更合理,其理由是
溶液更合理,其理由是_______ 。
(3) 溶液中存在平衡:
溶液中存在平衡: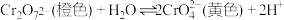 ,若向
,若向 溶液中加入硫酸,上述平衡向
溶液中加入硫酸,上述平衡向_______ (填“左”或“右”)移动:若向橙色 溶液中逐滴加入
溶液中逐滴加入 溶液,除生成
溶液,除生成 黄色沉淀外,溶液的颜色变化是
黄色沉淀外,溶液的颜色变化是_______ 。
(1)某同学欲进行中和反应反应热的测定,现进行以下实验。
①取
 溶液和
溶液和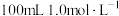 盐酸进行实验,测得反应前后温度差的平均值
盐酸进行实验,测得反应前后温度差的平均值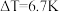 。若近似认为
。若近似认为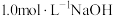 溶液和
溶液和 盐酸的密度都是
盐酸的密度都是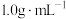 ,反应后生成溶液的比热容
,反应后生成溶液的比热容 ,则生成
,则生成 时的反应热
时的反应热
②强酸与强碱的稀溶液发生中和反应生成
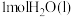 时的反应热
时的反应热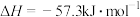 。若用一定浓度的稀硫酸与含
。若用一定浓度的稀硫酸与含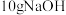 的稀碱溶液完全反应,则反应放出的热量为
的稀碱溶液完全反应,则反应放出的热量为(2)为比较
 对
对 分解的催化效果,某实验小组同学设计了如图所示的实验。
分解的催化效果,某实验小组同学设计了如图所示的实验。
某同学认为通过观察
 的催化效果的差异。有同学提出将
的催化效果的差异。有同学提出将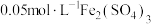 ,溶液改为
,溶液改为 溶液更合理,其理由是
溶液更合理,其理由是(3)
 溶液中存在平衡:
溶液中存在平衡: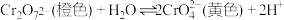 ,若向
,若向 溶液中加入硫酸,上述平衡向
溶液中加入硫酸,上述平衡向 溶液中逐滴加入
溶液中逐滴加入 溶液,除生成
溶液,除生成 黄色沉淀外,溶液的颜色变化是
黄色沉淀外,溶液的颜色变化是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】在 101kPa时, H 2在 1molO2中完全燃烧生成 2mol液态 H2O,放出 571.6kJ的热量。
(1)H2的燃烧热为_______ ,表示 H2燃烧热的热化学方程式为 _______ 。
(2)1L 1mol/L H2SO4溶液与 2L 1mol/L NaOH溶液完全反应,放出 114.6kJ的热量,该反应的中和热为_______ ,表示其中和热的热化学方程式为 _______ 。
(1)H2的燃烧热为
(2)1L 1mol/L H2SO4溶液与 2L 1mol/L NaOH溶液完全反应,放出 114.6kJ的热量,该反应的中和热为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示。
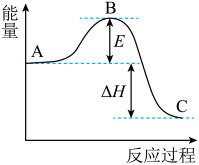
(已知1molSO2(g)氧化为1molSO3(g)的△H=-99kJ·mol-1。)请回答下列问题:
(1)图中A、C分别表示____ 、____ ,E的大小对该反应的反应热____ (填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点____ (填“变大”、“变小”或“不变”)。
(2)图中ΔH=____ kJ·mol-1。
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化为V2O5。写也该催化循环机理的化学方程式____ 。
(4)已知单质硫的燃烧热为296kJ·mol-1,计算由S(s)生成3molSO3(g)的ΔH=____ 。

(已知1molSO2(g)氧化为1molSO3(g)的△H=-99kJ·mol-1。)请回答下列问题:
(1)图中A、C分别表示
(2)图中ΔH=
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化为V2O5。写也该催化循环机理的化学方程式
(4)已知单质硫的燃烧热为296kJ·mol-1,计算由S(s)生成3molSO3(g)的ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
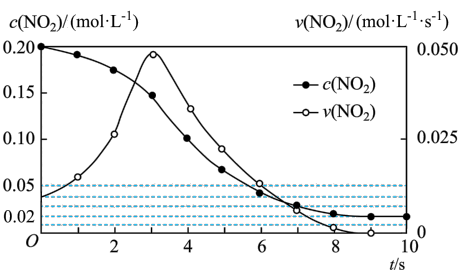
【推荐1】容积均为1 L的甲、乙两个容器,其中甲为绝热容器,乙为恒温容器。相同温度下,分别充入0.2 mol的NO2,发生反应:2NO2(g)  N2O4(g) ΔH<0,甲中NO2的相关量随时间变化如下图所示。0~3 s内,甲容器中NO2的反应速率增大的原因是
N2O4(g) ΔH<0,甲中NO2的相关量随时间变化如下图所示。0~3 s内,甲容器中NO2的反应速率增大的原因是___________
 N2O4(g) ΔH<0,甲中NO2的相关量随时间变化如下图所示。0~3 s内,甲容器中NO2的反应速率增大的原因是
N2O4(g) ΔH<0,甲中NO2的相关量随时间变化如下图所示。0~3 s内,甲容器中NO2的反应速率增大的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在密闭容器中发生3X(g)+Y(g)  Z (g)+2W(g)反应,现在控制下列三种不同的条件:
Z (g)+2W(g)反应,现在控制下列三种不同的条件:
那么,反应开始时,正反应速率最大的是(填序号,下同)__________ ,正反应速率最小的是___________ 。
 Z (g)+2W(g)反应,现在控制下列三种不同的条件:
Z (g)+2W(g)反应,现在控制下列三种不同的条件:①在400℃时,9molX与3molY反应
②在400℃时,15 molX与5molY反应
③在300℃时,9molX与3molY反应
那么,反应开始时,正反应速率最大的是(填序号,下同)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知放热反应: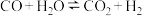 ,起始温度为600℃,在甲、乙、丙三个容积均为4L的恒容绝热(与外界没有热量交换)的密闭容器中分别充入不同物质的量的起始气体(如图所示),开始发生反应,甲容器达到平衡时用时10s,平衡时
,起始温度为600℃,在甲、乙、丙三个容积均为4L的恒容绝热(与外界没有热量交换)的密闭容器中分别充入不同物质的量的起始气体(如图所示),开始发生反应,甲容器达到平衡时用时10s,平衡时 的物质的量为0.6mol。回答下列问题:
的物质的量为0.6mol。回答下列问题:
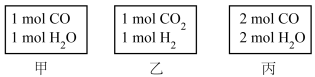
(1)甲容器0~10s内用CO表示的平均反应速率为__________ ,CO的转化率为__________ 。
(2)甲容器达到平衡时体系温度__________ (填“>”“<”或“=”)600℃,乙容器达到平衡时,容器内的温度低于甲容器,可能的原因为__________ 。
(3)下列说法能说明乙容器达到平衡状态的是__________(填序号)。
(4)丙容器达到平衡所需的时间__________ 10s(填“>”“<”或“=”),原因是__________ 。
(5)达到平衡后保持温度不变,向丙容器中通入2molNe,此时反应的速率将__________ (填“增大”“减小”或“不变”)。
 ,起始温度为600℃,在甲、乙、丙三个容积均为4L的恒容绝热(与外界没有热量交换)的密闭容器中分别充入不同物质的量的起始气体(如图所示),开始发生反应,甲容器达到平衡时用时10s,平衡时
,起始温度为600℃,在甲、乙、丙三个容积均为4L的恒容绝热(与外界没有热量交换)的密闭容器中分别充入不同物质的量的起始气体(如图所示),开始发生反应,甲容器达到平衡时用时10s,平衡时 的物质的量为0.6mol。回答下列问题:
的物质的量为0.6mol。回答下列问题: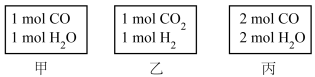
(1)甲容器0~10s内用CO表示的平均反应速率为
(2)甲容器达到平衡时体系温度
(3)下列说法能说明乙容器达到平衡状态的是__________(填序号)。
A.每消耗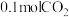 ,同时生成 ,同时生成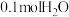 |
| B.容器内CO的体积分数不再改变 |
C.CO、 、 、 和 和 的物质的量之比为1:1:1:1 的物质的量之比为1:1:1:1 |
| D.容器内温度不再变化 |
(5)达到平衡后保持温度不变,向丙容器中通入2molNe,此时反应的速率将
您最近一年使用:0次

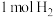 完全燃烧时放热约
完全燃烧时放热约 ,而
,而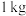 汽油完全燃烧时放热约
汽油完全燃烧时放热约 。请回答:
。请回答:

