根据要求回答问题:
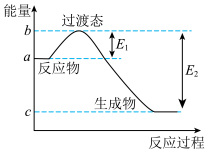
(1)如图是1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,活化能E1的变化是_____ (填“增大”“减小”或“不变”,下同),ΔH的变化是_____ 。图中最稳定的是_____ (填“反应物”“过渡态”或“生成物”)。
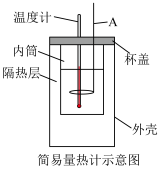
(2)50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应反应热(设溶液的密度均为1g•cm-3,反应后溶液的比热容c=4.18J•g-1•℃-1)。回答下列问题:
从实验装置上看,图中仪器A的名称是_____ ,隔热层的作用是_____ 。根据表中数据,结合题干信息,请写出生成1molH2O的热化学方程式_____ (保留3位有效数字)。
(3)生产液晶显示器的过程中使用的化学清洗剂NF3是一种温室气体,其存储能量的能力是CO2的1.2~2.0万倍,在大气中的寿命可长达740年之久,表中是几种化学键的键能:
写出N2(g)与F2(g)反应合成NF3(g)的热化学方程式_____ 。
(4)在微生物作用的条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。这两步反应的能量变化如图:
。这两步反应的能量变化如图:
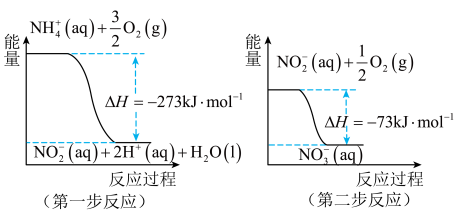
第二步反应是_____ (填“放热”或“吸热”)反应。1molNH (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是_____ 。
(1)如图是1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,活化能E1的变化是

(2)50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应反应热(设溶液的密度均为1g•cm-3,反应后溶液的比热容c=4.18J•g-1•℃-1)。回答下列问题:
 | 实验次数 | 反应物的温度/℃ | 反应前体系的温度 | 反应后体系的温度 | 温度差 | |
| 盐酸 | NaOH溶液 | t1/℃ | t2/℃ | (t2-t1)/℃ | ||
| 1 | 25.0 | 25.2 | 25.1 | 28.5 | 3.4 | |
| 2 | 24.9 | 25.1 | 25.0 | 28.3 | 3.3 | |
| 3 | 25.6 | 25.4 | 25.5 | 29.0 | 3.5 | |
(3)生产液晶显示器的过程中使用的化学清洗剂NF3是一种温室气体,其存储能量的能力是CO2的1.2~2.0万倍,在大气中的寿命可长达740年之久,表中是几种化学键的键能:
| 化学键 | N≡N | F-F | N-F |
| 键能/kJ•mol-1 | 941.7 | 154.8 | 283.0 |
(4)在微生物作用的条件下,NH
 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。这两步反应的能量变化如图:
。这两步反应的能量变化如图:
第二步反应是
 (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是
更新时间:2023-05-06 14:05:36
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)配平下列方程式
①___ FeCl3 +___ KI===____ FeCl2+____ KCl+_____ I2
②____ ClO-+_____ Fe(OH)3+_____ OH-===_____ Cl-+____ FeO +
+____ H2O
(2)用浓硫酸配制稀硫酸的过程中,下列操作会使配制的稀硫酸溶液浓度偏高的是___ (填序号)。
①量取浓硫酸的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③溶解后未经冷却就移液并定容
④定容时不小心有少量蒸馏水滴到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
①
②
 +
+(2)用浓硫酸配制稀硫酸的过程中,下列操作会使配制的稀硫酸溶液浓度偏高的是
①量取浓硫酸的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③溶解后未经冷却就移液并定容
④定容时不小心有少量蒸馏水滴到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知亚磷酸 是具有强还原性的二元弱酸,可被银离子氧化为磷酸。
是具有强还原性的二元弱酸,可被银离子氧化为磷酸。
 亚磷酸与银离子反应的离子方程式为
亚磷酸与银离子反应的离子方程式为______ 。
 向亚磷酸溶液中滴加氢氧化钠溶液至中性,写出所得溶液中电荷守恒方程式
向亚磷酸溶液中滴加氢氧化钠溶液至中性,写出所得溶液中电荷守恒方程式______ 。
 某温度下,
某温度下, 的亚磷酸溶液的pH为
的亚磷酸溶液的pH为 ,即c(H+)=3.9×10-2,则该温度下亚磷酸的一级电离平衡常数
,即c(H+)=3.9×10-2,则该温度下亚磷酸的一级电离平衡常数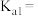
______ 。 亚磷酸第二级电离忽略不计,结果保留两位有效数字
亚磷酸第二级电离忽略不计,结果保留两位有效数字
 是具有强还原性的二元弱酸,可被银离子氧化为磷酸。
是具有强还原性的二元弱酸,可被银离子氧化为磷酸。 亚磷酸与银离子反应的离子方程式为
亚磷酸与银离子反应的离子方程式为 向亚磷酸溶液中滴加氢氧化钠溶液至中性,写出所得溶液中电荷守恒方程式
向亚磷酸溶液中滴加氢氧化钠溶液至中性,写出所得溶液中电荷守恒方程式 某温度下,
某温度下, 的亚磷酸溶液的pH为
的亚磷酸溶液的pH为 ,即c(H+)=3.9×10-2,则该温度下亚磷酸的一级电离平衡常数
,即c(H+)=3.9×10-2,则该温度下亚磷酸的一级电离平衡常数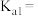
 亚磷酸第二级电离忽略不计,结果保留两位有效数字
亚磷酸第二级电离忽略不计,结果保留两位有效数字
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】三氟化氮是一种无色、无味、无毒且不可燃的气体,可在铜的催化作用下由F2和过量NH3反应得到,在半导体加工,太阳能电池和液晶显示器的制造中得到广泛应用。它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO 和 HNO3,请根据要求回答下列问题:
(1)写出制备NF3的化学反应方程式:______________________________ 。反应过程中,氧化剂与还原剂的物质的量之比为________ 。
(2)写出三氟化氮与水蒸气反应的化学方程式:______________________________________ 。
(3)NF3是一种无色、无臭的气体,但一旦NF3在空气中泄漏,还是易于发现。你判断该气体泄漏时的现象是_____________________________________ 。
(4)一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少污染。其产物除H2O外,还有另三种钠盐:_________________________________ (填化学式)。
(1)写出制备NF3的化学反应方程式:
(2)写出三氟化氮与水蒸气反应的化学方程式:
(3)NF3是一种无色、无臭的气体,但一旦NF3在空气中泄漏,还是易于发现。你判断该气体泄漏时的现象是
(4)一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少污染。其产物除H2O外,还有另三种钠盐:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】完成下列问题。
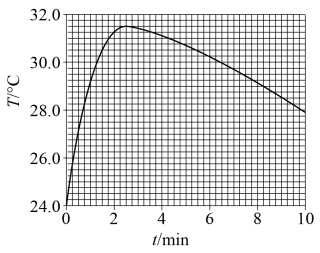
(1)①体积和浓度均为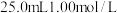 的硝酸和NaOH溶液(起始温度相同)混合时,测得混合溶液的温度与时间的关系如图所示,已知硝酸和NaOH溶液的密度均为
的硝酸和NaOH溶液(起始温度相同)混合时,测得混合溶液的温度与时间的关系如图所示,已知硝酸和NaOH溶液的密度均为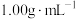 ,混合溶液的比热容为
,混合溶液的比热容为 。由实验数据可计算出该反应的中和热
。由实验数据可计算出该反应的中和热 为
为___________  (结果保留1位小数)。
(结果保留1位小数)。
②在一定条件下,将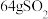 气体和32g氧气通入密闭容器中反应生成
气体和32g氧气通入密闭容器中反应生成 气体,达到平衡时,共放出热量78.64kJ,已知
气体,达到平衡时,共放出热量78.64kJ,已知 在此条件下转化率为80%,则该反应的热化学方程式为:
在此条件下转化率为80%,则该反应的热化学方程式为:___________ 。
(2)某氢氧燃料电池以熔融态的碳酸盐为电解质,其中 参与电极反应。工作时负极的电极反应为
参与电极反应。工作时负极的电极反应为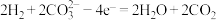 。如图所示,根据相关信息回答下列问题:
。如图所示,根据相关信息回答下列问题:
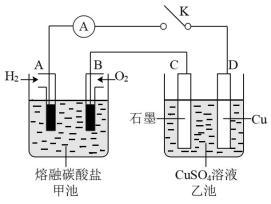
①正极的电极反应为___________ 。
②当甲池中A电极理论上消耗 的体积为448mL(标准状况)时,乙池中C、D两电极质量变化量之差为
的体积为448mL(标准状况)时,乙池中C、D两电极质量变化量之差为___________ g。
(3)如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。

①写出甲装置中通入氧气一极的电极反应方程式___________ 。
②乙装置中Fe电极为___________ 极,写出该装置中的总反应化学方程式___________ 。
(4)以Fe为阳极,Pt为阴极,对足量的 溶液进行电解,一段时间后得到
溶液进行电解,一段时间后得到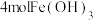 沉淀,此间共消耗水的质量为
沉淀,此间共消耗水的质量为___________ 。
(1)①体积和浓度均为
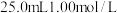 的硝酸和NaOH溶液(起始温度相同)混合时,测得混合溶液的温度与时间的关系如图所示,已知硝酸和NaOH溶液的密度均为
的硝酸和NaOH溶液(起始温度相同)混合时,测得混合溶液的温度与时间的关系如图所示,已知硝酸和NaOH溶液的密度均为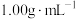 ,混合溶液的比热容为
,混合溶液的比热容为 。由实验数据可计算出该反应的中和热
。由实验数据可计算出该反应的中和热 为
为 (结果保留1位小数)。
(结果保留1位小数)。
②在一定条件下,将
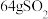 气体和32g氧气通入密闭容器中反应生成
气体和32g氧气通入密闭容器中反应生成 气体,达到平衡时,共放出热量78.64kJ,已知
气体,达到平衡时,共放出热量78.64kJ,已知 在此条件下转化率为80%,则该反应的热化学方程式为:
在此条件下转化率为80%,则该反应的热化学方程式为:(2)某氢氧燃料电池以熔融态的碳酸盐为电解质,其中
 参与电极反应。工作时负极的电极反应为
参与电极反应。工作时负极的电极反应为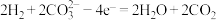 。如图所示,根据相关信息回答下列问题:
。如图所示,根据相关信息回答下列问题:
①正极的电极反应为
②当甲池中A电极理论上消耗
 的体积为448mL(标准状况)时,乙池中C、D两电极质量变化量之差为
的体积为448mL(标准状况)时,乙池中C、D两电极质量变化量之差为(3)如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。

①写出甲装置中通入氧气一极的电极反应方程式
②乙装置中Fe电极为
(4)以Fe为阳极,Pt为阴极,对足量的
 溶液进行电解,一段时间后得到
溶液进行电解,一段时间后得到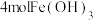 沉淀,此间共消耗水的质量为
沉淀,此间共消耗水的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列问题
(1)中和热测定的实验中,用到玻璃仪器有:烧杯、温度计、___________ 。
(2)量取反应物时,取50mL 0.50mol/L的盐酸,还需加入的试剂是___________ (填序号)。
A.50mL 0.50mol/L NaOH溶液 B.50mL 0.55mol/L NaOH溶液 C.1.0g NaOH固体
(3)由甲、乙两人组成的实验小组,在同样的实验条件下,用同样的实验仪器和方法进行两组测定中和热的实验,实验试剂及其用量如下表所示。
①甲在实验之前预计 。他的根据是
。他的根据是___________ ;乙在实验之前预计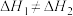 ,他的根据是
,他的根据是___________ 。
②实验测得的温度是:A的起始温度为13.0℃、终止温度为19.8℃;B的起始温度为13.0℃、终止温度为19.3℃。设充分反应后溶液的比热容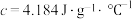 ,忽略实验仪器的比热容及溶液体积的变化,则
,忽略实验仪器的比热容及溶液体积的变化,则
___________ ,写出B发生中和热的热化学方程式___________ 。
③做一次完整的中和热测定实验,温度计需使用___________ 次。
(1)中和热测定的实验中,用到玻璃仪器有:烧杯、温度计、
(2)量取反应物时,取50mL 0.50mol/L的盐酸,还需加入的试剂是
A.50mL 0.50mol/L NaOH溶液 B.50mL 0.55mol/L NaOH溶液 C.1.0g NaOH固体
(3)由甲、乙两人组成的实验小组,在同样的实验条件下,用同样的实验仪器和方法进行两组测定中和热的实验,实验试剂及其用量如下表所示。
| 反应物 | 起始温度 /℃ /℃ | 终止温度 /℃ /℃ | 中和热/ |
A.1.0 HCl溶液50mL、1.1 HCl溶液50mL、1.1 NaOH溶液50mL NaOH溶液50mL | 13.0 |  | |
B.1.0 HCl溶液50mL、1.1 HCl溶液50mL、1.1  溶液50mL 溶液50mL | 13.0 |  |
 。他的根据是
。他的根据是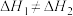 ,他的根据是
,他的根据是②实验测得的温度是:A的起始温度为13.0℃、终止温度为19.8℃;B的起始温度为13.0℃、终止温度为19.3℃。设充分反应后溶液的比热容
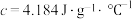 ,忽略实验仪器的比热容及溶液体积的变化,则
,忽略实验仪器的比热容及溶液体积的变化,则
③做一次完整的中和热测定实验,温度计需使用
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
(1) 焙烧产生的
焙烧产生的 可用于制硫酸。
可用于制硫酸。
已知:25℃、101kPa时,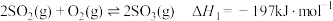 ;
;
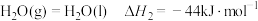 ;
;
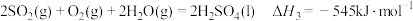 ;
;
则 与
与 反应生成
反应生成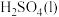 的热化学方程式是
的热化学方程式是___________ 。
(2)某实验小组用 的NaOH溶液和
的NaOH溶液和 的
的 溶液进行中和反应的反应热测定。
溶液进行中和反应的反应热测定。
①测定稀硫酸和氢氧化钠稀溶液反应的反应热的实验装置如图所示。则仪器A的名称为___________ 。

②碎泡沫塑料的作用是___________ 。
(3)取 溶液和
溶液和 溶液进行实验,实验数据如下表。
溶液进行实验,实验数据如下表。
①温度差的平均值为___________ ℃。(保留两位有效数字)
②近似认为 的NaOH溶液和
的NaOH溶液和 的
的 溶液的密度都是
溶液的密度都是 ,中和后生成的溶液的比热容
,中和后生成的溶液的比热容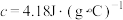 。则测得生成
。则测得生成 时中和反应的反应热
时中和反应的反应热
___________ (取小数点后一位)。
(1)
 焙烧产生的
焙烧产生的 可用于制硫酸。
可用于制硫酸。已知:25℃、101kPa时,
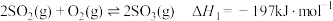 ;
;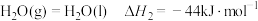 ;
;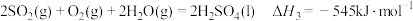 ;
;则
 与
与 反应生成
反应生成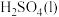 的热化学方程式是
的热化学方程式是(2)某实验小组用
 的NaOH溶液和
的NaOH溶液和 的
的 溶液进行中和反应的反应热测定。
溶液进行中和反应的反应热测定。①测定稀硫酸和氢氧化钠稀溶液反应的反应热的实验装置如图所示。则仪器A的名称为

②碎泡沫塑料的作用是
(3)取
 溶液和
溶液和 溶液进行实验,实验数据如下表。
溶液进行实验,实验数据如下表。| 实验次数 | 反应物温度/℃ | 反应前体系的温度 /℃ /℃ | 反应后体系的温度 /℃ /℃ | |
 | NaOH | |||
| 1 | 26.6 | 26.6 | 26.6 | 29.1 |
| 2 | 27.0 | 27.0 | 27.0 | 31.0 |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 |
②近似认为
 的NaOH溶液和
的NaOH溶液和 的
的 溶液的密度都是
溶液的密度都是 ,中和后生成的溶液的比热容
,中和后生成的溶液的比热容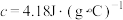 。则测得生成
。则测得生成 时中和反应的反应热
时中和反应的反应热
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I.已知:键能指在标准状况下,将 1mol 气态分子 AB(g)解离为气态原子 A(g),B(g)所需的能量,用符号 E 表示,单位为 kJ/mol。N≡N的键能为 946 kJ/mol,H-H 的键能为 436 kJ/mol,N-H 的键能为 391 kJ/mol,则生成 2 mol NH3 过程中______ (填“吸收”或“放出”)的能量为______ 。
II.(1)下列装置属于原电池的是______ ;
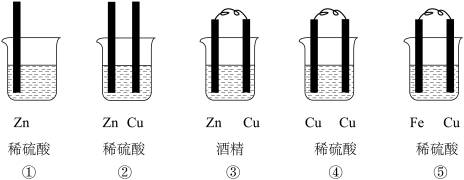
(2)在选出的原电池中,______ 是负极,发生______ 反应,正极的现象______ ;
(3)此原电池反应的化学方程式为______ 。
(4)将 CH4设计成燃料电池, 其利用率更高, 装置如图所示( A、B 为多孔碳棒), 电池总反应为:CH4+2O2+2KOH=K2CO3+3H2O。
①实验测得 OH-定向移向 B 电极,则_______ 处电极入口通甲烷(填 A 或 B)。
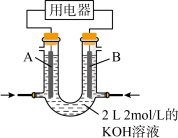
②当消耗甲烷的体积为 33.6L(标准状况下)时,假设电池的能量转化率为 80%,则导线中转移电子的物质的量为_______ 。
II.(1)下列装置属于原电池的是

(2)在选出的原电池中,
(3)此原电池反应的化学方程式为
(4)将 CH4设计成燃料电池, 其利用率更高, 装置如图所示( A、B 为多孔碳棒), 电池总反应为:CH4+2O2+2KOH=K2CO3+3H2O。
①实验测得 OH-定向移向 B 电极,则

②当消耗甲烷的体积为 33.6L(标准状况下)时,假设电池的能量转化率为 80%,则导线中转移电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据要求回答:
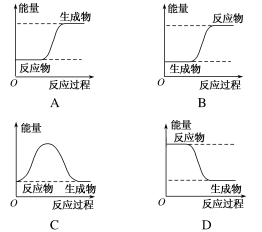
(1)下列各图中,表示反应是吸热反应的是_______
(2)到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源。在25 ℃、101 kPa下,16 g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352 kJ的热量,则表示甲醇燃烧的热化学方程式为_____________________________ 。
(3)化学反应中放出的热能(焓变,ΔH)与反应物和生成物的键能(E)有关。
已知:H2(g)+Cl2(g)===2HCl(g) ΔH=-185 kJ·mol-1
E(H—H)=436 kJ·mol-1
E(Cl—Cl)=243 kJ·mol-1
则E(H—Cl)=________________________________ 。
(4)已知:
甲醇脱水反应 2CH3OH(g)=CH3OCH3(g)+H2O(g)△H1=-23.9KJ·mol-1
甲醇制烯烃反应 2CH3OH(g)=C2H4(g)+2H2O(g)△H2=-29.1KJ·mol-1
乙醇异构化反应 CH3CH2OH(g)=CH3OCH3(g)△H3=+50.7KJ·mol-1
则乙烯气相直接水合反应C2H4(g)+H2O(g)=C2H5OH(g)的△H=____________ kJ·mol-1
(1)下列各图中,表示反应是吸热反应的是

(2)到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源。在25 ℃、101 kPa下,16 g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352 kJ的热量,则表示甲醇燃烧的热化学方程式为
(3)化学反应中放出的热能(焓变,ΔH)与反应物和生成物的键能(E)有关。
已知:H2(g)+Cl2(g)===2HCl(g) ΔH=-185 kJ·mol-1
E(H—H)=436 kJ·mol-1
E(Cl—Cl)=243 kJ·mol-1
则E(H—Cl)=
(4)已知:
甲醇脱水反应 2CH3OH(g)=CH3OCH3(g)+H2O(g)△H1=-23.9KJ·mol-1
甲醇制烯烃反应 2CH3OH(g)=C2H4(g)+2H2O(g)△H2=-29.1KJ·mol-1
乙醇异构化反应 CH3CH2OH(g)=CH3OCH3(g)△H3=+50.7KJ·mol-1
则乙烯气相直接水合反应C2H4(g)+H2O(g)=C2H5OH(g)的△H=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)化学反应中的能量变化,是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同所致。下图为N2(g)和O2(g)生成NO(g)过程中的能量变化:

N2(g)和O2(g)生成NO(g)过程中的能量变化
①人们通常把拆开1mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,则N≡N的键能为________ kJ/mol。
②由上图写出N2(g)和O2(g)生成NO(g)的热化学方程式:___________________________
(2)①已知:C(石墨,s)+O2(g)===CO2(g) ΔH1=-393.5kJ/mol
2H2(g)+O2(g)===2H2O(l) ΔH2=-571.6kJ/mol
2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH3=-2599.2kJ/mol,
则由C(石墨,s)和H2(g)反应生成1mol C2H2(g)时ΔH=________ kJ/mol。
②火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101 kPa下测得的热量)。反应的热化学方程式为__________________________ 。

N2(g)和O2(g)生成NO(g)过程中的能量变化
①人们通常把拆开1mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,则N≡N的键能为
②由上图写出N2(g)和O2(g)生成NO(g)的热化学方程式:
(2)①已知:C(石墨,s)+O2(g)===CO2(g) ΔH1=-393.5kJ/mol
2H2(g)+O2(g)===2H2O(l) ΔH2=-571.6kJ/mol
2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH3=-2599.2kJ/mol,
则由C(石墨,s)和H2(g)反应生成1mol C2H2(g)时ΔH=
②火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101 kPa下测得的热量)。反应的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
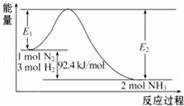
【推荐1】科学家一直致力于“人工固氮”的方法研究.用N2和H2合成NH3的能量变化如图所示。
(1)合成氨反应的热化学方程式_________________________ ,已知E2=212.4kJ/mol,则该反应正反应的活化能是______ 。
(2)反应体系中加入催化剂,反应速率______ ,E2的变化是______ 。(填“增大”、“减小”或“不变”)
(3)工业上常采用高温高压,使用催化剂的方法改变该反应的反应速率,在甲乙两个体积均为2L固定容积的密闭容器中,分别充入1molN2、3molH2和1molN2、3molH2、1molHe,反应速率甲__ 乙(填大于、小于或等于)。
(4)该反应的△S______ 0,(填大于、小于或等于),理论上在______ 条件下可以自发。
(1)合成氨反应的热化学方程式
(2)反应体系中加入催化剂,反应速率
(3)工业上常采用高温高压,使用催化剂的方法改变该反应的反应速率,在甲乙两个体积均为2L固定容积的密闭容器中,分别充入1molN2、3molH2和1molN2、3molH2、1molHe,反应速率甲
(4)该反应的△S
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请认真观察下图,然后回答问题:

(1)图中所示反应是_____ (填“吸热”或“放热”)反应,该反应的ΔH=______ (用含E1、E2的代数式表示)。
(2)对于同一反应,图中虚线(Ⅱ)与实线(Ⅰ)相比,活化能大大降低,活化分子的百分数增多, 反应速率明显加快,你认为最可能的原因是_________________________________________________________ 。
(3)甲醇(CH3OH)广泛用作燃料电池的燃料,可由天然气来合成,已知:①2CH4(g)+O2(g)===2CO(g)+4H2(g)ΔH=-71 kJ·mol-1②CO(g)+2H2(g)===CH3OH(l)ΔH=-90.5 kJ·mol-1③CH4(g)+2O2(g)===CO2(g)+2H2O(l)ΔH=-890 kJ·mol-1,则甲醇的燃烧热为________ 。

(1)图中所示反应是
(2)对于同一反应,图中虚线(Ⅱ)与实线(Ⅰ)相比,活化能大大降低,活化分子的百分数增多, 反应速率明显加快,你认为最可能的原因是
(3)甲醇(CH3OH)广泛用作燃料电池的燃料,可由天然气来合成,已知:①2CH4(g)+O2(g)===2CO(g)+4H2(g)ΔH=-71 kJ·mol-1②CO(g)+2H2(g)===CH3OH(l)ΔH=-90.5 kJ·mol-1③CH4(g)+2O2(g)===CO2(g)+2H2O(l)ΔH=-890 kJ·mol-1,则甲醇的燃烧热为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。
甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式 A:CH3OH* →CH3O* +H* Ea= +103.1kJ·mol-1
方式 B:CH3OH* →CH3* +OH* Eb= +249.3kJ·mol-1
由活化能E值推测,甲醇裂解过程主要历经的方式应为___________ (填A、B)。
下图为计算机模拟的各步反应的能量变化示意图。

该历程中,放热最多的步骤的化学方程式为___________ 。
Ⅱ.TiCl4是由钛精矿(主要成分为TiO2)制备钛(Ti)的重要中间产物,制备纯TiCl4的流程示意图如下:

氯化过程:TiO2与Cl2难以直接反应,加碳生成CO和CO2可使反应得以进行。
已知:TiO2(s)+2 Cl2(g)= TiCl4(g)+ O2(g) ΔH1=+175.4 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH2=-220.9 kJ·mol-1
(1)沸腾炉中加碳氯化生成TiCl4(g)和CO(g)的热化学方程式_____ 。
(2)工业上处理尾气中NO的方法为:将NO与H2的混合气体通入Ce(SO4)2与Ce2(SO4)3的混合溶液中,其物质转化如图所示。写出图示转化的总反应的化学方程式_____ 。

Ⅲ.甲醇可作为燃料电池的原料。CO2和CO可作为工业合成甲醇(CH3OH)的直接碳源,
(1)已知在常温常压下:①CH3OH(l)+ O2(g)=CO(g) + 2H2O(g); ΔH=﹣355.0 kJ∕mol
②2CO(g)+ O2(g)= 2CO2(g) ΔH=-566.0 kJ/mol ③H2O(l)=H2O(g) ΔH=+44.0 kJ/mol
写出表示甲醇燃烧热的热化学方程式:___________
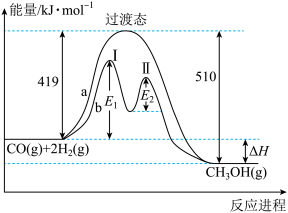
(2)利用CO和H2在一定条件下可合成甲醇,发生如下反应:CO(g)+2H2(g)=CH3OH(g),其两种反应过程中能量的变化曲线如下图a、b所示,下列说法正确的是___________ 。
A.上述反应的ΔH=-91kJ·mol-1
B.a反应正反应的活化能为510kJ·mol-1
C.b过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应
D.b过程使用催化剂后降低了反应的活化能和ΔH
E.b过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式 A:CH3OH* →CH3O* +H* Ea= +103.1kJ·mol-1
方式 B:CH3OH* →CH3* +OH* Eb= +249.3kJ·mol-1
由活化能E值推测,甲醇裂解过程主要历经的方式应为
下图为计算机模拟的各步反应的能量变化示意图。

该历程中,放热最多的步骤的化学方程式为
Ⅱ.TiCl4是由钛精矿(主要成分为TiO2)制备钛(Ti)的重要中间产物,制备纯TiCl4的流程示意图如下:

氯化过程:TiO2与Cl2难以直接反应,加碳生成CO和CO2可使反应得以进行。
已知:TiO2(s)+2 Cl2(g)= TiCl4(g)+ O2(g) ΔH1=+175.4 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH2=-220.9 kJ·mol-1
(1)沸腾炉中加碳氯化生成TiCl4(g)和CO(g)的热化学方程式
(2)工业上处理尾气中NO的方法为:将NO与H2的混合气体通入Ce(SO4)2与Ce2(SO4)3的混合溶液中,其物质转化如图所示。写出图示转化的总反应的化学方程式

Ⅲ.甲醇可作为燃料电池的原料。CO2和CO可作为工业合成甲醇(CH3OH)的直接碳源,
(1)已知在常温常压下:①CH3OH(l)+ O2(g)=CO(g) + 2H2O(g); ΔH=﹣355.0 kJ∕mol
②2CO(g)+ O2(g)= 2CO2(g) ΔH=-566.0 kJ/mol ③H2O(l)=H2O(g) ΔH=+44.0 kJ/mol
写出表示甲醇燃烧热的热化学方程式:
(2)利用CO和H2在一定条件下可合成甲醇,发生如下反应:CO(g)+2H2(g)=CH3OH(g),其两种反应过程中能量的变化曲线如下图a、b所示,下列说法正确的是

A.上述反应的ΔH=-91kJ·mol-1
B.a反应正反应的活化能为510kJ·mol-1
C.b过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应
D.b过程使用催化剂后降低了反应的活化能和ΔH
E.b过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
您最近一年使用:0次



