根据要求回答:
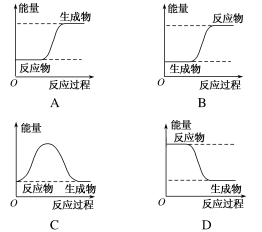
(1)下列各图中,表示反应是吸热反应的是_______
(2)到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源。在25 ℃、101 kPa下,16 g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352 kJ的热量,则表示甲醇燃烧的热化学方程式为_____________________________ 。
(3)化学反应中放出的热能(焓变,ΔH)与反应物和生成物的键能(E)有关。
已知:H2(g)+Cl2(g)===2HCl(g) ΔH=-185 kJ·mol-1
E(H—H)=436 kJ·mol-1
E(Cl—Cl)=243 kJ·mol-1
则E(H—Cl)=________________________________ 。
(4)已知:
甲醇脱水反应 2CH3OH(g)=CH3OCH3(g)+H2O(g)△H1=-23.9KJ·mol-1
甲醇制烯烃反应 2CH3OH(g)=C2H4(g)+2H2O(g)△H2=-29.1KJ·mol-1
乙醇异构化反应 CH3CH2OH(g)=CH3OCH3(g)△H3=+50.7KJ·mol-1
则乙烯气相直接水合反应C2H4(g)+H2O(g)=C2H5OH(g)的△H=____________ kJ·mol-1
(1)下列各图中,表示反应是吸热反应的是

(2)到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源。在25 ℃、101 kPa下,16 g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352 kJ的热量,则表示甲醇燃烧的热化学方程式为
(3)化学反应中放出的热能(焓变,ΔH)与反应物和生成物的键能(E)有关。
已知:H2(g)+Cl2(g)===2HCl(g) ΔH=-185 kJ·mol-1
E(H—H)=436 kJ·mol-1
E(Cl—Cl)=243 kJ·mol-1
则E(H—Cl)=
(4)已知:
甲醇脱水反应 2CH3OH(g)=CH3OCH3(g)+H2O(g)△H1=-23.9KJ·mol-1
甲醇制烯烃反应 2CH3OH(g)=C2H4(g)+2H2O(g)△H2=-29.1KJ·mol-1
乙醇异构化反应 CH3CH2OH(g)=CH3OCH3(g)△H3=+50.7KJ·mol-1
则乙烯气相直接水合反应C2H4(g)+H2O(g)=C2H5OH(g)的△H=
17-18高二下·河南省直辖县级单位·阶段练习 查看更多[3]
(已下线)《2018-2019学年同步单元双基双测AB卷》第一单元 化学反应与能量单元测试(B卷)黑龙江省绥化市第二中学2019届高三上学期第一次月考化学试题河南省济源第一中学2017-2018学年高二下期6月月考化学试题
更新时间:2018-06-29 11:50:49
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)已知下列数据:
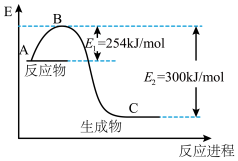
如图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量变化示意图,试根据表中及图中数据计算N-H的键能______________ 。
(2)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)=N2O4(l) ΔH1=-19.5 kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534.2 kJ·mol-1
写出肼和N2O4反应的热化学方程式______________________________ 。
(3)若用标准状况下4.48LO2氧化N2H4至N2,整个过程中转移的电子总数为___________ (阿伏加 德罗常数用NA表示)。
| 化学键 | H-H | N≡N |
| 键能/kJ·mol-1 | 435 | 943 |
如图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量变化示意图,试根据表中及图中数据计算N-H的键能

(2)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)=N2O4(l) ΔH1=-19.5 kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534.2 kJ·mol-1
写出肼和N2O4反应的热化学方程式
(3)若用标准状况下4.48LO2氧化N2H4至N2,整个过程中转移的电子总数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.在发射“神舟”七号的火箭推进器中装有肼(N2H4)和过氧化氢,当两者混合时即产生气体,并放出大量的热。已知:N2H4(l)+2H2O2(l)===N2(g)+4H2O(g)ΔH=-641.6 kJ·mol-1
H2O(l)===H2O(g) ΔH=+44 kJ·mol-1若用3.2 g液态肼与足量过氧化氢反应生成氮气和液态水,则整个过程中转移的电子的物质的量为_______ 。该反应的热化学方程式为_________________________ 。
Ⅱ.(1)已知H2(g)+Br2(l)===2HBr(g) ΔH=-72 kJ·mol-1。蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其它相关数据如下表:
则表中a为_________________ 。
A.404 B.260 C.230 D.200
(2)为减少SO2的排放,常采取的措施有:①将煤转化为清洁气体燃料。
已知:H2(g)+ O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1 C(s)+
O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1 C(s)+ O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
写出焦炭与水蒸气反应的热化学方程式:_____________________________________ 。
H2O(l)===H2O(g) ΔH=+44 kJ·mol-1若用3.2 g液态肼与足量过氧化氢反应生成氮气和液态水,则整个过程中转移的电子的物质的量为
Ⅱ.(1)已知H2(g)+Br2(l)===2HBr(g) ΔH=-72 kJ·mol-1。蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其它相关数据如下表:
| H2(g) | Br2(g) | HBr(g) | |
| 1 mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | a | 369 |
则表中a为
A.404 B.260 C.230 D.200
(2)为减少SO2的排放,常采取的措施有:①将煤转化为清洁气体燃料。
已知:H2(g)+
 O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1 C(s)+
O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1 C(s)+ O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
O2(g)===CO(g) ΔH=-110.5 kJ·mol-1写出焦炭与水蒸气反应的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请回答下列问题:
(1)已知1molSi固体中有2molSi—Si键,1molO2中有1molO=O键,1molSiO2固体中有4molSi—O键。某些化学键键能数据如下:
根据化学键数据写出Si(s)在O2中完全燃烧生成SiO2的热化学方程式:___ 。
(2)肼(N2H4)通常作为火箭的燃料。已知3.2g液态肼在O2(g)中完全燃烧,生成N2(g)和H2O(l),放出62.2kJ热量,写出上述反应的热化学方程式:___ 。
(1)已知1molSi固体中有2molSi—Si键,1molO2中有1molO=O键,1molSiO2固体中有4molSi—O键。某些化学键键能数据如下:
| 化学键 | Si—O | Si—Si | O=O |
| 键能(kJ·mol-1) | 460 | 176 | 498 |
根据化学键数据写出Si(s)在O2中完全燃烧生成SiO2的热化学方程式:
(2)肼(N2H4)通常作为火箭的燃料。已知3.2g液态肼在O2(g)中完全燃烧,生成N2(g)和H2O(l),放出62.2kJ热量,写出上述反应的热化学方程式:
您最近一年使用:0次
【推荐1】工业废气、汽车尾气排放出的 SO2、NOx等,是形成雾霾的重要因素.霾是由空气中的灰尘、硫酸、硝酸、有机碳氢化合物等粒子形成的烟雾.
(1)NOx和 SO2在空气中存在下列平衡:
2NO(g) + O2(g) 2NO2(g) △ H =− 113.0kJ
2NO2(g) △ H =− 113.0kJ mol−1
mol−1
2SO2(g) + O2(g) 2SO3(g) △ H =− 196.6kJ
2SO3(g) △ H =− 196.6kJ mol−1
mol−1
SO2通常在二氧化氮的存在下,进一步被氧化,生成 SO3.
①写出 NO2和 SO2反应的热化学方程式为_____ .
②随温度升高,该反应化学平衡常数变化趋势是_____ .
(2)提高2SO2(g) + O2(g) 2SO3(g)反应中 SO2的转化率,是减少 SO2排放的有效措施:①T 温度时,在 1L 的密闭容器中加入 2.0mol SO2和 1.0mol O2,5min 后反应达到平衡,二氧化硫的转化率为 50%,该反应的平衡常数是
2SO3(g)反应中 SO2的转化率,是减少 SO2排放的有效措施:①T 温度时,在 1L 的密闭容器中加入 2.0mol SO2和 1.0mol O2,5min 后反应达到平衡,二氧化硫的转化率为 50%,该反应的平衡常数是_____ .②在①中条件下,反应达到平衡后,改变下列条件,能使 SO2的转化率提高的是_____ (填字母).
a.温度和容器体积不变,充入 1.0mol He
b.温度和容器体积不变,充入 1.0mol O2
c.在其他条件不变时,减少容器的体积
d.在其他条件不变时,改用高效催化剂
e.在其他条件不变时,升高体系温度

(3)工业上利用氯碱工业产品治理含二氧化硫的废气.如图是氯碱工业中电解饱和食盐水的原理示意图
①用溶液A吸收含二氧化硫的废气,其反应的离子方程式是_____ .
②用含气体B的阳极区溶液吸收含二氧化硫的废气,其反应的离子方程式是_____ .
(1)NOx和 SO2在空气中存在下列平衡:
2NO(g) + O2(g)
 2NO2(g) △ H =− 113.0kJ
2NO2(g) △ H =− 113.0kJ mol−1
mol−12SO2(g) + O2(g)
 2SO3(g) △ H =− 196.6kJ
2SO3(g) △ H =− 196.6kJ mol−1
mol−1SO2通常在二氧化氮的存在下,进一步被氧化,生成 SO3.
①写出 NO2和 SO2反应的热化学方程式为
②随温度升高,该反应化学平衡常数变化趋势是
(2)提高2SO2(g) + O2(g)
 2SO3(g)反应中 SO2的转化率,是减少 SO2排放的有效措施:①T 温度时,在 1L 的密闭容器中加入 2.0mol SO2和 1.0mol O2,5min 后反应达到平衡,二氧化硫的转化率为 50%,该反应的平衡常数是
2SO3(g)反应中 SO2的转化率,是减少 SO2排放的有效措施:①T 温度时,在 1L 的密闭容器中加入 2.0mol SO2和 1.0mol O2,5min 后反应达到平衡,二氧化硫的转化率为 50%,该反应的平衡常数是a.温度和容器体积不变,充入 1.0mol He
b.温度和容器体积不变,充入 1.0mol O2
c.在其他条件不变时,减少容器的体积
d.在其他条件不变时,改用高效催化剂
e.在其他条件不变时,升高体系温度

(3)工业上利用氯碱工业产品治理含二氧化硫的废气.如图是氯碱工业中电解饱和食盐水的原理示意图
①用溶液A吸收含二氧化硫的废气,其反应的离子方程式是
②用含气体B的阳极区溶液吸收含二氧化硫的废气,其反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知下列热化学方程式:
CuSO4·5H2O(s)=CuSO4(s)+5H2O(g) ΔH1=akJ·mol−1
CuSO4·xH2O(s)=CuSO4(s)+xH2O(g) ΔH2=bkJ·mol−1
CuSO4·yH2O(s)=CuSO4(s)+yH2O(g) ΔH3=ckJ·mol−1
则CuSO4·5H2O(s)+CuSO4·yH2O(s)=2[CuSO4·xH2O(s)]的△H=_____ kJ/mol。
CuSO4·5H2O(s)=CuSO4(s)+5H2O(g) ΔH1=akJ·mol−1
CuSO4·xH2O(s)=CuSO4(s)+xH2O(g) ΔH2=bkJ·mol−1
CuSO4·yH2O(s)=CuSO4(s)+yH2O(g) ΔH3=ckJ·mol−1
则CuSO4·5H2O(s)+CuSO4·yH2O(s)=2[CuSO4·xH2O(s)]的△H=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请运用反应热的知识填写下列空白:
(1)已知: (s,白磷)=
(s,白磷)= (s,黑磷)
(s,黑磷) 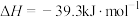 ;
;
 (s,白磷)=
(s,白磷)= (s,红磷)
(s,红磷) 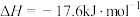 ;
;
由此推知,其中最稳定的磷单质是___________ 。
(2)①硅粉与HCl在300℃时反应生成1 mol SiHCl3气体和H2,放出225 kJ热量,该反应的热化学方程式为___________ 。
②在 25℃ 和 101kPa时,4 g硫粉在O2中完全燃烧生成SO2气体,放出37 kJ的热量,写出表示S燃烧热的热化学方程式:___________ 。
(3)已知上述反应中相关的化学键键能数据如下:
则该反应的 ΔH = ___________ 。
(4)将 氢化为
氢化为 有三种方法,对应的反应依次为:
有三种方法,对应的反应依次为:
①

②

③

反应③的 ΔH3 =___________ (用ΔH1,ΔH2表示)
(5)①2Cu2O(s) + O2(g) =4CuO(s) ΔH1=-277kJ·mol-1
②8CuO(s) + CH4(g)=4Cu2O(s) + CO2(g)+2H2O(g) ΔH2=-348kJ·mol-1
反应CH4(g) +2O2(g)=CO2(g)+2H2O(g) ΔH=___________ kJ·mol-1
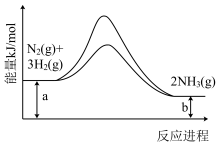
(6)合成氨反应常使用铁触媒提高反应速率。如图为有、无铁触媒时,反应的能量变化示意图。写出该反应的热化学方程式___________ 。
(1)已知:
 (s,白磷)=
(s,白磷)= (s,黑磷)
(s,黑磷) 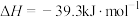 ;
; (s,白磷)=
(s,白磷)= (s,红磷)
(s,红磷) 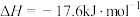 ;
;由此推知,其中最稳定的磷单质是
(2)①硅粉与HCl在300℃时反应生成1 mol SiHCl3气体和H2,放出225 kJ热量,该反应的热化学方程式为
②在 25℃ 和 101kPa时,4 g硫粉在O2中完全燃烧生成SO2气体,放出37 kJ的热量,写出表示S燃烧热的热化学方程式:
(3)已知上述反应中相关的化学键键能数据如下:
| 化学键 | C-H | C=O | H-H | C O(CO) O(CO) |
| 键能/kJ·mol−1 | 413 | 745 | 436 | 1075 |
(4)将
 氢化为
氢化为 有三种方法,对应的反应依次为:
有三种方法,对应的反应依次为:①


②


③


反应③的 ΔH3 =
(5)①2Cu2O(s) + O2(g) =4CuO(s) ΔH1=-277kJ·mol-1
②8CuO(s) + CH4(g)=4Cu2O(s) + CO2(g)+2H2O(g) ΔH2=-348kJ·mol-1
反应CH4(g) +2O2(g)=CO2(g)+2H2O(g) ΔH=
(6)合成氨反应常使用铁触媒提高反应速率。如图为有、无铁触媒时,反应的能量变化示意图。写出该反应的热化学方程式

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。反应A:4HCl+O2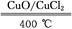 2Cl2+2H2O
2Cl2+2H2O
已知:ⅰ.反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
ⅱ.

(1)反应A的热化学方程式是____ 。
(2)断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为____ kJ,H2O中H—O键比HCl中H—Cl键(填“强”或“弱”)____ 。
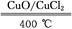 2Cl2+2H2O
2Cl2+2H2O已知:ⅰ.反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
ⅱ.

(1)反应A的热化学方程式是
(2)断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)氨气是一种重要化合物,在工农业生产、生活中有着重要应用。已知:断裂 键需吸
键需吸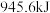 能量,断裂
能量,断裂 键需吸收
键需吸收 能量,形成
能量,形成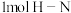 键可放出
键可放出 能量。试写出
能量。试写出 的电子式:
的电子式:___________ 。若生成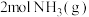 ,热量变化是
,热量变化是___________ (吸收、放出)___________ kJ。
(2)一种用于潜艇的液氨-液氧燃料电池原理示意图如图所示。
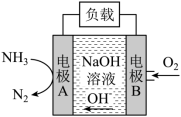
①该燃料电池工作时能量转化关系为___________ 。
②电极B上发生的电极反应式为___________ 。
(3)①已知25℃、 时,
时, 甲烷完全燃烧生成液态水放出
甲烷完全燃烧生成液态水放出 热量,则该条件下1mol
热量,则该条件下1mol 完全燃烧放出的热量为
完全燃烧放出的热量为___________ kJ。
②一种甲烷燃料电池,用强碱做电解质。其负极反应式为___________ ,随着电池不断放电,负极附近溶液的
___________ 。(填“增大”、“减小”或“不变”)。
(1)氨气是一种重要化合物,在工农业生产、生活中有着重要应用。已知:断裂
 键需吸
键需吸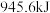 能量,断裂
能量,断裂 键需吸收
键需吸收 能量,形成
能量,形成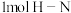 键可放出
键可放出 能量。试写出
能量。试写出 的电子式:
的电子式: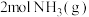 ,热量变化是
,热量变化是(2)一种用于潜艇的液氨-液氧燃料电池原理示意图如图所示。

①该燃料电池工作时能量转化关系为
②电极B上发生的电极反应式为
(3)①已知25℃、
 时,
时, 甲烷完全燃烧生成液态水放出
甲烷完全燃烧生成液态水放出 热量,则该条件下1mol
热量,则该条件下1mol 完全燃烧放出的热量为
完全燃烧放出的热量为②一种甲烷燃料电池,用强碱做电解质。其负极反应式为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】生活中离不开化学。运用化学知识回答下列问题。
(1)已知H—H键的键能为436 kJ·mol-1,Cl—Cl键的键能为243 kJ·mol-1,H—Cl键的键能为431 kJ·mol-1,则H2(g) +Cl2(g)=2HCl(g)的反应热为_______ 。
(2)NH4Al(SO4)2在食品加工中是一种合法的食品添加剂,它还是一种净水剂,其净水的理由是_______ (用化学方程式回答)。
(3)龋齿是有机酸使牙齿中的Ca5(PO4)3(OH)溶解造成的。使用含氟牙膏会使其转化为Ca5(PO4)3F抵抗酸的腐蚀,含氟牙膏能使牙断中Ca5(PO4)3(OH)转化为Ca5(PO4)3F的理由是:溶解度Ca5(PO4)3(OH)_______ Ca5(PO4)3F(填“﹥”或“﹤”)。
(4)目前民用电池的主要成分是碱性锌锰电池,该电池的总反应式为:Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2,该电池放电时,负极的电极反应式为_______
(1)已知H—H键的键能为436 kJ·mol-1,Cl—Cl键的键能为243 kJ·mol-1,H—Cl键的键能为431 kJ·mol-1,则H2(g) +Cl2(g)=2HCl(g)的反应热为
(2)NH4Al(SO4)2在食品加工中是一种合法的食品添加剂,它还是一种净水剂,其净水的理由是
(3)龋齿是有机酸使牙齿中的Ca5(PO4)3(OH)溶解造成的。使用含氟牙膏会使其转化为Ca5(PO4)3F抵抗酸的腐蚀,含氟牙膏能使牙断中Ca5(PO4)3(OH)转化为Ca5(PO4)3F的理由是:溶解度Ca5(PO4)3(OH)
(4)目前民用电池的主要成分是碱性锌锰电池,该电池的总反应式为:Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2,该电池放电时,负极的电极反应式为
您最近一年使用:0次



