已知亚磷酸 是具有强还原性的二元弱酸,可被银离子氧化为磷酸。
是具有强还原性的二元弱酸,可被银离子氧化为磷酸。
 亚磷酸与银离子反应的离子方程式为
亚磷酸与银离子反应的离子方程式为______ 。
 向亚磷酸溶液中滴加氢氧化钠溶液至中性,写出所得溶液中电荷守恒方程式
向亚磷酸溶液中滴加氢氧化钠溶液至中性,写出所得溶液中电荷守恒方程式______ 。
 某温度下,
某温度下, 的亚磷酸溶液的pH为
的亚磷酸溶液的pH为 ,即c(H+)=3.9×10-2,则该温度下亚磷酸的一级电离平衡常数
,即c(H+)=3.9×10-2,则该温度下亚磷酸的一级电离平衡常数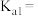
______ 。 亚磷酸第二级电离忽略不计,结果保留两位有效数字
亚磷酸第二级电离忽略不计,结果保留两位有效数字
 是具有强还原性的二元弱酸,可被银离子氧化为磷酸。
是具有强还原性的二元弱酸,可被银离子氧化为磷酸。 亚磷酸与银离子反应的离子方程式为
亚磷酸与银离子反应的离子方程式为 向亚磷酸溶液中滴加氢氧化钠溶液至中性,写出所得溶液中电荷守恒方程式
向亚磷酸溶液中滴加氢氧化钠溶液至中性,写出所得溶液中电荷守恒方程式 某温度下,
某温度下, 的亚磷酸溶液的pH为
的亚磷酸溶液的pH为 ,即c(H+)=3.9×10-2,则该温度下亚磷酸的一级电离平衡常数
,即c(H+)=3.9×10-2,则该温度下亚磷酸的一级电离平衡常数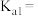
 亚磷酸第二级电离忽略不计,结果保留两位有效数字
亚磷酸第二级电离忽略不计,结果保留两位有效数字
更新时间:2020-09-26 22:17:55
|
相似题推荐
填空题
|
适中
(0.65)
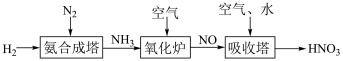
【推荐1】氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题: 的说法中,不正确的是___________(填字母)。
的说法中,不正确的是___________(填字母)。
(2) 易溶于水,标准状况下,用充满
易溶于水,标准状况下,用充满 的烧瓶做喷泉实验(如图),引发喷泉的方法是
的烧瓶做喷泉实验(如图),引发喷泉的方法是___________ 。___________ 。
(4)工厂生产出的浓硝酸可用铝槽车或铁槽车来运输,是因为在常温下,浓硝酸能使铝、铁等发生___________ 现象,说明浓硝酸具有很强的___________ 性。
(5)“吸收塔”尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的污染,可用以下两种方法处理:
①可用ClO2将氮氧化物转化成 。向含ClO2的溶液中加入NaOH溶液调节至碱性,ClO2转化为去除氮氧化物效果更好的NaClO2,再通入NO气体进行反应。碱性条件下NaClO2去除NO反应的离子方程式为
。向含ClO2的溶液中加入NaOH溶液调节至碱性,ClO2转化为去除氮氧化物效果更好的NaClO2,再通入NO气体进行反应。碱性条件下NaClO2去除NO反应的离子方程式为___________ 。
②氨转化法。已知7mol氨恰好能将含NO和NO2共6mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为___________ 。
 的说法中,不正确的是___________(填字母)。
的说法中,不正确的是___________(填字母)。A.工业合成 需要在高温、高压、催化剂下进行 需要在高温、高压、催化剂下进行 |
B. 可用来生产碳铵和尿素等化肥 可用来生产碳铵和尿素等化肥 |
C. 可用浓硫酸或无水氯化钙干燥 可用浓硫酸或无水氯化钙干燥 |
D. 受热易分解,须置于冷暗处保存 受热易分解,须置于冷暗处保存 |
 易溶于水,标准状况下,用充满
易溶于水,标准状况下,用充满 的烧瓶做喷泉实验(如图),引发喷泉的方法是
的烧瓶做喷泉实验(如图),引发喷泉的方法是
(4)工厂生产出的浓硝酸可用铝槽车或铁槽车来运输,是因为在常温下,浓硝酸能使铝、铁等发生
(5)“吸收塔”尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的污染,可用以下两种方法处理:
①可用ClO2将氮氧化物转化成
 。向含ClO2的溶液中加入NaOH溶液调节至碱性,ClO2转化为去除氮氧化物效果更好的NaClO2,再通入NO气体进行反应。碱性条件下NaClO2去除NO反应的离子方程式为
。向含ClO2的溶液中加入NaOH溶液调节至碱性,ClO2转化为去除氮氧化物效果更好的NaClO2,再通入NO气体进行反应。碱性条件下NaClO2去除NO反应的离子方程式为②氨转化法。已知7mol氨恰好能将含NO和NO2共6mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】利用图,可以从不同角度研究含氯物质的性质及其转化关系,图中甲~辛均含氯元素。回答下列问题:

(1)丙的化学式为______ ;丁属于______ (“酸性”或“碱性”)氧化物。
(2)图中甲、乙、丁、戊中,属于电解质的是_____ (填化学式);根据氯元素的化合价判断,乙物质的性质______ (填标号)。
a.只有氧化性 b.既有氧化性又有还原性 c.只有还原性
(3)物质己的化学式为HClO4,电解甲溶液制备己的化学反应为:甲+H2O 己+H2↑(未配平),配平后参与反应的甲与H2O的微粒个数之比是
己+H2↑(未配平),配平后参与反应的甲与H2O的微粒个数之比是_____ 。
(4)庚是家庭中常用消毒液的有效成分NaClO,用乙制取庚的化学方程式为_____ 。NaClO溶液中显碱性原因:______ (用离子方程式表示)。
(5)辛在MnO2催化下受热分解可用于制备氧气,每生成1.204×1024氧气分子,转移e-的个数为______ 。

(1)丙的化学式为
(2)图中甲、乙、丁、戊中,属于电解质的是
a.只有氧化性 b.既有氧化性又有还原性 c.只有还原性
(3)物质己的化学式为HClO4,电解甲溶液制备己的化学反应为:甲+H2O
 己+H2↑(未配平),配平后参与反应的甲与H2O的微粒个数之比是
己+H2↑(未配平),配平后参与反应的甲与H2O的微粒个数之比是(4)庚是家庭中常用消毒液的有效成分NaClO,用乙制取庚的化学方程式为
(5)辛在MnO2催化下受热分解可用于制备氧气,每生成1.204×1024氧气分子,转移e-的个数为
您最近一年使用:0次
【推荐3】Ⅰ.胶体是一种常见的分散系,回答下列问题。
①胶体是指分散质粒子大小在_________________ nm之间的分散系。
②向Fe(OH)3胶体中加入盐酸的现象是_________________________________ 。
Ⅱ.①FeCl3溶液用作蚀刻铜箔制造电路板的工艺,其离子方程式为_________________________ 。
②高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,反应的离子方程式为___________________________ 。
III.(1)过氧化氢H2O2(氧的化合价为﹣1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。
①对于下列A~D涉及H2O2的反应,填写空白:
A.Na2O2+2HCl=2NaCl+H2O2 B.Ag2O+H2O2=2Ag+O2+H2O
C.2H2O2=2H2O+O2 D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
H2O2既体现氧化性又体现还原性的反应是_________ (填代号)。
②在稀硫酸中,KMnO4和H2O2能发生氧化还原反应。
氧化反应:H2O2﹣2e﹣=2H++O2↑
还原反应:MnO4—+5e﹣+8H+=Mn2++4H2O
写出该氧化还原反应的离子方程式:_________________________________
(2)在K2Cr2O7+14HCl=2KCl+3Cl2↑+7H2O+2CrCl3的反应中,有0.3 mol电子转移时生成Cl2的体积为______ L(标准状况)
①胶体是指分散质粒子大小在
②向Fe(OH)3胶体中加入盐酸的现象是
Ⅱ.①FeCl3溶液用作蚀刻铜箔制造电路板的工艺,其离子方程式为
②高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,反应的离子方程式为
III.(1)过氧化氢H2O2(氧的化合价为﹣1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。
①对于下列A~D涉及H2O2的反应,填写空白:
A.Na2O2+2HCl=2NaCl+H2O2 B.Ag2O+H2O2=2Ag+O2+H2O
C.2H2O2=2H2O+O2 D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
H2O2既体现氧化性又体现还原性的反应是
②在稀硫酸中,KMnO4和H2O2能发生氧化还原反应。
氧化反应:H2O2﹣2e﹣=2H++O2↑
还原反应:MnO4—+5e﹣+8H+=Mn2++4H2O
写出该氧化还原反应的离子方程式:
(2)在K2Cr2O7+14HCl=2KCl+3Cl2↑+7H2O+2CrCl3的反应中,有0.3 mol电子转移时生成Cl2的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】 时,三种酸的电离平衡常数如下:
时,三种酸的电离平衡常数如下:
回答下列问题:
(1)一般情况下,当温度升高时,
______ 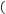 填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变” 。
。
(2)下列四种离子结合质子能力由大到小的顺序是______  填序号
填序号 ;
;
a、CO32- b、ClO- c、CH3COO- d、HCO3-
(3)下列反应不能发生的是______  填序号
填序号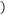
a.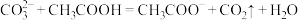
b.
c.
d.
(4)用蒸馏水稀释 的醋酸,下列各式表示的数值随水量的增加而增大的是
的醋酸,下列各式表示的数值随水量的增加而增大的是______  填序号
填序号 ;
;
a. b.
b.  c.
c. d.
d.
(5)体积均为10mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如图所示。
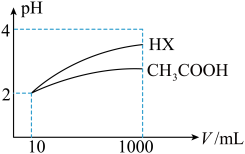
则HX的电离平衡常数______ 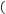 填“大于”、“等于”或“小于”,下同
填“大于”、“等于”或“小于”,下同 醋酸的电离平衡常数;稀释后,HX溶液中水电离出来的c(H+)
醋酸的电离平衡常数;稀释后,HX溶液中水电离出来的c(H+)______ 醋酸溶液中水电离出来的c(H+),理由是___________ 。
 时,三种酸的电离平衡常数如下:
时,三种酸的电离平衡常数如下:| 化学式 |  |  | HClO |
| 电离平衡常数 |  |  , , |  |
回答下列问题:
(1)一般情况下,当温度升高时,

 填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变” 。
。(2)下列四种离子结合质子能力由大到小的顺序是
 填序号
填序号 ;
;a、CO32- b、ClO- c、CH3COO- d、HCO3-
(3)下列反应不能发生的是
 填序号
填序号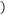
a.
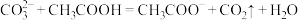
b.

c.

d.

(4)用蒸馏水稀释
 的醋酸,下列各式表示的数值随水量的增加而增大的是
的醋酸,下列各式表示的数值随水量的增加而增大的是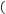 填序号
填序号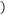 ;
;a.
 b.
b.  c.
c. d.
d.
(5)体积均为10mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如图所示。

则HX的电离平衡常数
 填“大于”、“等于”或“小于”,下同
填“大于”、“等于”或“小于”,下同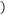 醋酸的电离平衡常数;稀释后,HX溶液中水电离出来的c(H+)
醋酸的电离平衡常数;稀释后,HX溶液中水电离出来的c(H+)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】 溶液和盐酸中的
溶液和盐酸中的 均为
均为 ,请根据下列操作回答问题:
,请根据下列操作回答问题:
(1)取 溶液,加入等体积的水,
溶液,加入等体积的水, 的电离平衡(
的电离平衡(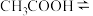
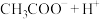 )
)______________ (填“向左”“向右”或“不”)移动;另取 溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中
溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中 的值将
的值将_______________ (填“增大”“减小”或“无法确定”)。
(2)相同条件下,取等体积的 溶液和盐酸,各稀释100倍。稀释后的溶液,其氢离子浓度大小关系为
溶液和盐酸,各稀释100倍。稀释后的溶液,其氢离子浓度大小关系为 溶液
溶液_________________ (填“>”“<”或“=”)盐酸。
(3)取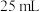 的
的 溶液,加入等体积
溶液,加入等体积 的NaOH溶液,反应后溶液中
的NaOH溶液,反应后溶液中 、
、 的大小关系为
的大小关系为
_________________ (填“>”“<”或“=”) 。
。
 溶液和盐酸中的
溶液和盐酸中的 均为
均为 ,请根据下列操作回答问题:
,请根据下列操作回答问题:(1)取
 溶液,加入等体积的水,
溶液,加入等体积的水, 的电离平衡(
的电离平衡(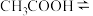
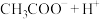 )
) 溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中
溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中 的值将
的值将(2)相同条件下,取等体积的
 溶液和盐酸,各稀释100倍。稀释后的溶液,其氢离子浓度大小关系为
溶液和盐酸,各稀释100倍。稀释后的溶液,其氢离子浓度大小关系为 溶液
溶液(3)取
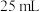 的
的 溶液,加入等体积
溶液,加入等体积 的NaOH溶液,反应后溶液中
的NaOH溶液,反应后溶液中 、
、 的大小关系为
的大小关系为
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知亚磷酸(H3PO3)的结构如图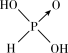 ,具有强还原性的弱酸,可以被银离子氧化为磷酸。
,具有强还原性的弱酸,可以被银离子氧化为磷酸。
(1)已知亚磷酸可由PCl3水解而成,请写出相应的离子方程式____________ ;
(2)Na2HPO3是________ (填“正盐”或“酸式盐”);
(3)亚磷酸与银离子反应时氧化剂与还原剂的物质的量之比为______________ ;
(4)某温度下,0.10mol•L-1的H3PO3溶液的pH为1.6,即c(H+)=2.5×10-2mol•L-1,该温度下H3PO3的一级电离平衡常数Ka1=___________________ ;(H3PO3第二步电离忽略不计,结果保留两位有效数字)
(5)向H3PO3溶液中滴加NaOH溶液至中性,所得溶液中:c(Na+)_____ c(H2PO3-)+2c(HPO32-)(填“>”、“<”或“=”);
(6)向某浓度的亚磷酸中滴加NaOH溶液,其pH与溶液中的H3PO3、H2PO3-、HPO32-的物质的量分数a(X)(平衡时某物种的浓度与整个物种浓度之和的比值)的关系如图所示。

以酚酞为指示剂,当溶液由无色变为浅红色时,发生主要反应的离子方程式是_________________________ 。
 ,具有强还原性的弱酸,可以被银离子氧化为磷酸。
,具有强还原性的弱酸,可以被银离子氧化为磷酸。(1)已知亚磷酸可由PCl3水解而成,请写出相应的离子方程式
(2)Na2HPO3是
(3)亚磷酸与银离子反应时氧化剂与还原剂的物质的量之比为
(4)某温度下,0.10mol•L-1的H3PO3溶液的pH为1.6,即c(H+)=2.5×10-2mol•L-1,该温度下H3PO3的一级电离平衡常数Ka1=
(5)向H3PO3溶液中滴加NaOH溶液至中性,所得溶液中:c(Na+)
(6)向某浓度的亚磷酸中滴加NaOH溶液,其pH与溶液中的H3PO3、H2PO3-、HPO32-的物质的量分数a(X)(平衡时某物种的浓度与整个物种浓度之和的比值)的关系如图所示。

以酚酞为指示剂,当溶液由无色变为浅红色时,发生主要反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,有浓度均为 的下列4种溶液:①
的下列4种溶液:① 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液
溶液
(1)这4种溶液 由大到小的顺序是
由大到小的顺序是______ (填序号)。
(2)①中各离子浓度由大到小的顺序是______ 。
(3)④的水解平衡常数
______  。
。
(4)若向等体积的③和④中滴加盐酸至呈中性,则消耗盐酸的体积③______ ④(填“﹥”、“﹤”、“=”)。
(5)25℃时,测得 和
和 的混合溶液的
的混合溶液的 ,则
,则 约为
约为______ 。向 溶液中通入少量
溶液中通入少量 ,则发生反应的离子方程式为:
,则发生反应的离子方程式为:______ 。
 的下列4种溶液:①
的下列4种溶液:① 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液
溶液 |  |  |
 |   |  |
 由大到小的顺序是
由大到小的顺序是(2)①中各离子浓度由大到小的顺序是
(3)④的水解平衡常数

 。
。(4)若向等体积的③和④中滴加盐酸至呈中性,则消耗盐酸的体积③
(5)25℃时,测得
 和
和 的混合溶液的
的混合溶液的 ,则
,则 约为
约为 溶液中通入少量
溶液中通入少量 ,则发生反应的离子方程式为:
,则发生反应的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列水溶液中的离子反应与平衡相关问题:
(1)一定温度下,向NH3·H2O中加入NH4Cl固体,NH3·H2O的电离平衡将_______ 移动(填“向正反应方向”、“向逆反应方向”或“不发生”),NH3·H2O的电离平衡常数_______ (填“增大”、“减小”或“不变”)。
(2)明矾化学式为KAl(SO4)2·12H2O,其净水原理用离子方程式表示为_______ 。
(3)室温下,将pH=2的HCl与pH=12的NH3·H2O混合至呈中性,则c(Cl-)_______ c(NH )(填“>”、“<”或“=”)。
)(填“>”、“<”或“=”)。
(4)用HCl标准液滴定NaOH溶液时。
①用_______ (填仪器名称)量取25.00 mLNaOH溶液,图中,盛装待测液后排气泡动作正确的是_______ (填序号)。
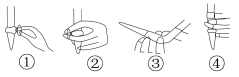
②下列操作(其他操作正确)造成测定结果偏低的是_______ (填字母)。
A.振荡过程中,锥形瓶内液体飞溅出瓶外
B.滴定起始时仰视读数
C.锥形瓶水洗后未干燥
D.酸式滴定管尖端部分有气泡,滴定后消失
(1)一定温度下,向NH3·H2O中加入NH4Cl固体,NH3·H2O的电离平衡将
(2)明矾化学式为KAl(SO4)2·12H2O,其净水原理用离子方程式表示为
(3)室温下,将pH=2的HCl与pH=12的NH3·H2O混合至呈中性,则c(Cl-)
 )(填“>”、“<”或“=”)。
)(填“>”、“<”或“=”)。(4)用HCl标准液滴定NaOH溶液时。
①用

②下列操作(其他操作正确)造成测定结果偏低的是
A.振荡过程中,锥形瓶内液体飞溅出瓶外
B.滴定起始时仰视读数
C.锥形瓶水洗后未干燥
D.酸式滴定管尖端部分有气泡,滴定后消失
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈___ 性(填“酸”、“中”或“碱”,下同),溶液中c(Na+)__ c(CH3COO-)(填“>”、“=”或“<”下同)。
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈__ 性,溶液中c(Na+)____ c(CH3COO-)。
(3)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈__ 性,醋酸体积__ 氢氧化钠溶液体积。
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈
(3)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈
您最近一年使用:0次



