已知放热反应: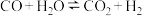 ,起始温度为600℃,在甲、乙、丙三个容积均为4L的恒容绝热(与外界没有热量交换)的密闭容器中分别充入不同物质的量的起始气体(如图所示),开始发生反应,甲容器达到平衡时用时10s,平衡时
,起始温度为600℃,在甲、乙、丙三个容积均为4L的恒容绝热(与外界没有热量交换)的密闭容器中分别充入不同物质的量的起始气体(如图所示),开始发生反应,甲容器达到平衡时用时10s,平衡时 的物质的量为0.6mol。回答下列问题:
的物质的量为0.6mol。回答下列问题:
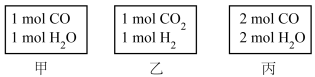
(1)甲容器0~10s内用CO表示的平均反应速率为__________ ,CO的转化率为__________ 。
(2)甲容器达到平衡时体系温度__________ (填“>”“<”或“=”)600℃,乙容器达到平衡时,容器内的温度低于甲容器,可能的原因为__________ 。
(3)下列说法能说明乙容器达到平衡状态的是__________(填序号)。
(4)丙容器达到平衡所需的时间__________ 10s(填“>”“<”或“=”),原因是__________ 。
(5)达到平衡后保持温度不变,向丙容器中通入2molNe,此时反应的速率将__________ (填“增大”“减小”或“不变”)。
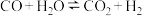 ,起始温度为600℃,在甲、乙、丙三个容积均为4L的恒容绝热(与外界没有热量交换)的密闭容器中分别充入不同物质的量的起始气体(如图所示),开始发生反应,甲容器达到平衡时用时10s,平衡时
,起始温度为600℃,在甲、乙、丙三个容积均为4L的恒容绝热(与外界没有热量交换)的密闭容器中分别充入不同物质的量的起始气体(如图所示),开始发生反应,甲容器达到平衡时用时10s,平衡时 的物质的量为0.6mol。回答下列问题:
的物质的量为0.6mol。回答下列问题: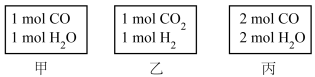
(1)甲容器0~10s内用CO表示的平均反应速率为
(2)甲容器达到平衡时体系温度
(3)下列说法能说明乙容器达到平衡状态的是__________(填序号)。
A.每消耗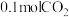 ,同时生成 ,同时生成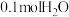 |
| B.容器内CO的体积分数不再改变 |
C.CO、 、 、 和 和 的物质的量之比为1:1:1:1 的物质的量之比为1:1:1:1 |
| D.容器内温度不再变化 |
(5)达到平衡后保持温度不变,向丙容器中通入2molNe,此时反应的速率将
更新时间:2023-06-15 15:38:17
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某温度时,在2L恒容容器中X、Y、Z三种物质随时间的变化关系曲线如图所示。
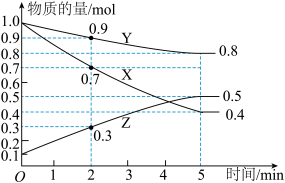
(1)由图中的数据分析,该反应的化学方程式为___ 。
(2)反应开始至2min、5min时,Z的平均反应速率分别为___ 、___ 。
(3)5min后Z的生成速率___ (填“大于”“小于”或“等于”)5min末Z的生成速率。

(1)由图中的数据分析,该反应的化学方程式为
(2)反应开始至2min、5min时,Z的平均反应速率分别为
(3)5min后Z的生成速率
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某温度时,在2L恒容密闭容器中,发生反应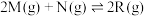 ,A、B气体的物质的量随时间变化的曲线如图,回答下列问题:
,A、B气体的物质的量随时间变化的曲线如图,回答下列问题:

(1)B为_____ (填“M”“N”或“R”)。
(2)Q点时,正、逆反应速率的大小关系为v正_____ (填“>”“<”或“=”)v逆,该点R的物质的量为_____ mol(保留两位有效数字)。
(3)0~4min内,该反应的平均反应速率v(M)=_____  。
。
(4)平衡时N的转化率为_____ ,若降低温度,则该反应的正反应速率_____ (填“加快”“减慢”或“不变”)。
(5)如图为氢氧燃料电池的构造示意图。

①氧气从_____ (填“a”或“b”)口通入;电池工作时, 向
向_____ (填“X”或“Y”)极移动。
②某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,则电池工作时负极电极反应式为_____ 。当电路中转移0.4mol电子时,理论上正极通入的气体在标准状况下的体积为_____ L。
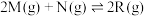 ,A、B气体的物质的量随时间变化的曲线如图,回答下列问题:
,A、B气体的物质的量随时间变化的曲线如图,回答下列问题:
(1)B为
(2)Q点时,正、逆反应速率的大小关系为v正
(3)0~4min内,该反应的平均反应速率v(M)=
 。
。(4)平衡时N的转化率为
(5)如图为氢氧燃料电池的构造示意图。

①氧气从
 向
向②某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,则电池工作时负极电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】碘及其化合物在生产生活中有重要作用。
(1)单质碘可与氢气反应生成碘化氢。将物质的量比为2:1的氢气和碘蒸气放入密闭容器中进行反应:H2(g)+I2(g)⇌2HI(g),反应经过5分钟测得碘化氢的浓度为0.1mol·L-1,碘蒸气的浓度为0.05mol·L-1。
①前5分钟平均反应速率v(H2)=____ ,H2的初始浓度是____ 。
②下列能说明反应已达平衡状态的是____ 。(填序号)
a.氢气的生成速率等于碘化氢的消耗速率
b.单位时间内断裂的H—H键数目与断裂的H—I键数目相等
c.c(H2):c(I2):c(HI)=1:1:2
d.2v(I2)正=v(HI)逆
e.反应混合体系的颜色不再发生变化
(2)某小组同学在室温下进行“碘钟实验”:将浓度均为0.01mol·L-1的H2O2、H2SO4、KI、Na2S2O3溶液及淀粉混合,一定时间后溶液变为蓝色。
已知:“碘钟实验”的总反应的离子方程式为H2O2+2S2O +2H+=S4O
+2H+=S4O +2H2O
+2H2O
反应分两步进行:
反应A:……
反应B:I2+2S2O =2I-+S4O
=2I-+S4O
①反应A的离子方程式是____ 。
②为探究溶液变蓝快慢的影响因素,进行实验I、II(溶液浓度均为0.01mol·L-1)
溶液从混合时的无色变为蓝色的时间:实验I是30min、实验II是40min。实验II中,x、y、z所对成的数值分别是____ ;对比实验I、II,可得出的实验结论是____ 。
(1)单质碘可与氢气反应生成碘化氢。将物质的量比为2:1的氢气和碘蒸气放入密闭容器中进行反应:H2(g)+I2(g)⇌2HI(g),反应经过5分钟测得碘化氢的浓度为0.1mol·L-1,碘蒸气的浓度为0.05mol·L-1。
①前5分钟平均反应速率v(H2)=
②下列能说明反应已达平衡状态的是
a.氢气的生成速率等于碘化氢的消耗速率
b.单位时间内断裂的H—H键数目与断裂的H—I键数目相等
c.c(H2):c(I2):c(HI)=1:1:2
d.2v(I2)正=v(HI)逆
e.反应混合体系的颜色不再发生变化
(2)某小组同学在室温下进行“碘钟实验”:将浓度均为0.01mol·L-1的H2O2、H2SO4、KI、Na2S2O3溶液及淀粉混合,一定时间后溶液变为蓝色。
已知:“碘钟实验”的总反应的离子方程式为H2O2+2S2O
 +2H+=S4O
+2H+=S4O +2H2O
+2H2O反应分两步进行:
反应A:……
反应B:I2+2S2O
 =2I-+S4O
=2I-+S4O
①反应A的离子方程式是
②为探究溶液变蓝快慢的影响因素,进行实验I、II(溶液浓度均为0.01mol·L-1)
| 用量试剂 | H2O2溶液 | H2SO4溶液 | Na2S2O3溶液 | KI溶液(含淀粉) | H2O |
| 实验I | 5 | 4 | 8 | 3 | 0 |
| 实验II | 5 | 2 | x | y | z |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某合成气的主要成分是一氧化碳和氢气,可用于合成甲醚等清洁燃料。由天然气获得该合成气过程中可能发生的反应有
①CH4(g)+H2O(g) CO(g)+3H2(g) ΔH1=+206.1 kJ·mol-1
CO(g)+3H2(g) ΔH1=+206.1 kJ·mol-1
②CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH2=+247.3 kJ·mol-1
2CO(g)+2H2(g) ΔH2=+247.3 kJ·mol-1
③CO(g)+H2O(g) CO2(g)+H2(g) ΔH3
CO2(g)+H2(g) ΔH3
请回答下列问题:
(1)在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图1所示。

反应进行的前5 min内,v(H2)=___________ ;10 min时,改变的外界条件可能是___________ 。
(2)如图2所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等。在相同温度下发生反应②,并维持反应过程中温度不变。已知甲容器中CH4的转化率随时间的变化如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图象___________ 。

①CH4(g)+H2O(g)
 CO(g)+3H2(g) ΔH1=+206.1 kJ·mol-1
CO(g)+3H2(g) ΔH1=+206.1 kJ·mol-1②CH4(g)+CO2(g)
 2CO(g)+2H2(g) ΔH2=+247.3 kJ·mol-1
2CO(g)+2H2(g) ΔH2=+247.3 kJ·mol-1③CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH3
CO2(g)+H2(g) ΔH3请回答下列问题:
(1)在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图1所示。

反应进行的前5 min内,v(H2)=
(2)如图2所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等。在相同温度下发生反应②,并维持反应过程中温度不变。已知甲容器中CH4的转化率随时间的变化如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图象

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】一定条件下2L的密闭容器中,反应aA(g)+bB(g)⇌cC(g)+dD(g)达到平衡。
(1)若起始时A为lmol,反应2min达到平衡,A剩余0.4mol,则在0~2min内A的平均反应速率为______ mol/(L·min)
(2)在其他条件不变的情况下,扩大容器体积,若平衡向逆反应方向移动,则a+b_____ c+d(选填“>”、“<”或“=”),v逆_____ (选填“增大”、“减小”或“不变”)
(3)若反应速率(v)与时间(t)的关系如图所示,则缩小容器体积时导致t1时刻及以后速率发生变化示意图为____ ?

(1)若起始时A为lmol,反应2min达到平衡,A剩余0.4mol,则在0~2min内A的平均反应速率为
(2)在其他条件不变的情况下,扩大容器体积,若平衡向逆反应方向移动,则a+b
(3)若反应速率(v)与时间(t)的关系如图所示,则缩小容器体积时导致t1时刻及以后速率发生变化示意图为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】磷酸铁(FePO4·2H2O,难溶于水的米白色固体)可用于生产药物、食品添加剂和锂离子电池的正极材料,实验室可通过下列实验制备磷酸铁。
(1)称取一定量已除去油污的废铁屑,加入稍过量的稀硫酸,加热、搅拌,反应一段时间后过滤。反应加热的目的是_______________________ 。
(2)向滤液中加入一定量H2O2氧化Fe2+ 。为确定加入H2O2的量,需先用K2Cr2O7标准溶液滴定滤液中 的Fe2+,离子方程式如下: Cr2O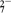 +6Fe2++14H+===2Cr3++6Fe3++7H2O
+6Fe2++14H+===2Cr3++6Fe3++7H2O
① 在向滴定管注入K2Cr2O7标准溶液前,滴定管需要检漏、________ 和________ 。
② 若滴定x mL滤液中的Fe2+,消耗a mol·L-1 K2Cr2O7标准溶液b mL,则滤液中c(Fe2+)=________ mol·L-1。
③ 为使滤液中的Fe2+完全被H2O2氧化,下列实验条件控制正确的是________ (填序号)。
A.加入适当过量的H2O2溶液
B.缓慢滴加H2O2溶液并搅拌
C.加热,使反应在较高温度下进行
D.用氨水调节溶液pH=7
(1)称取一定量已除去油污的废铁屑,加入稍过量的稀硫酸,加热、搅拌,反应一段时间后过滤。反应加热的目的是
(2)向滤液中加入一定量H2O2氧化Fe2+ 。为确定加入H2O2的量,需先用K2Cr2O7标准溶液滴定滤液中 的Fe2+,离子方程式如下: Cr2O
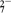 +6Fe2++14H+===2Cr3++6Fe3++7H2O
+6Fe2++14H+===2Cr3++6Fe3++7H2O① 在向滴定管注入K2Cr2O7标准溶液前,滴定管需要检漏、
② 若滴定x mL滤液中的Fe2+,消耗a mol·L-1 K2Cr2O7标准溶液b mL,则滤液中c(Fe2+)=
③ 为使滤液中的Fe2+完全被H2O2氧化,下列实验条件控制正确的是
A.加入适当过量的H2O2溶液
B.缓慢滴加H2O2溶液并搅拌
C.加热,使反应在较高温度下进行
D.用氨水调节溶液pH=7
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】工业废气二氧化碳催化加氢也可合成甲醇: ,在密闭容器中投入
,在密闭容器中投入 和
和 ,在不同条件下发生反应,实验测得平衡时甲醇的物质的量随温度、压强的变化如图所示。
,在不同条件下发生反应,实验测得平衡时甲醇的物质的量随温度、压强的变化如图所示。

(1)该反应的
_______ 0(填“>”“<”或“=”,下同)。
(2)M、N两点的化学反应速率:
_______ 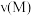 ,判断理由是
,判断理由是_______ 。
(3)为提高 的转化率,除可以改变温度和压强外,还可以采取的措施有
的转化率,除可以改变温度和压强外,还可以采取的措施有_______ 、_______ 。
(4)若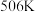 时,在
时,在 密闭容器中反应,达平衡时恰好处于图中M点,则N点对应的平衡常数
密闭容器中反应,达平衡时恰好处于图中M点,则N点对应的平衡常数
_______ (保留两位小数)。
 ,在密闭容器中投入
,在密闭容器中投入 和
和 ,在不同条件下发生反应,实验测得平衡时甲醇的物质的量随温度、压强的变化如图所示。
,在不同条件下发生反应,实验测得平衡时甲醇的物质的量随温度、压强的变化如图所示。
(1)该反应的

(2)M、N两点的化学反应速率:

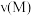 ,判断理由是
,判断理由是(3)为提高
 的转化率,除可以改变温度和压强外,还可以采取的措施有
的转化率,除可以改变温度和压强外,还可以采取的措施有(4)若
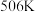 时,在
时,在 密闭容器中反应,达平衡时恰好处于图中M点,则N点对应的平衡常数
密闭容器中反应,达平衡时恰好处于图中M点,则N点对应的平衡常数
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】一定温度下,在2L的密闭容器中,M、N两种气体的物质的量随时间变化的曲线如图所示:
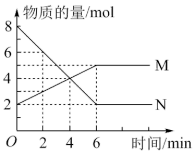
(1)反应的化学方程式为___________ 。
(2)反应达到平衡状态的时间是_______ min,该时间内的平均反应速率v(N)=_______ 。
(3)判断该反应达到平衡状态的依据是___________(填序号)。
(4)能加快反应速率的措施是___________(填序号)。

(1)反应的化学方程式为
(2)反应达到平衡状态的时间是
(3)判断该反应达到平衡状态的依据是___________(填序号)。
| A.该条件下,正、逆反应速率都为零 |
| B.该条件下,混合气体的密度不再发生变化 |
| C.该条件下,混合气体的压强不再发生变化 |
| D.条件下,单位时间内消耗2molN的同时,生成1molM |
| A.升高温度 |
| B.容器容积不变,充入惰性气体Ar |
| C.容器压强不变,充入惰性气体He |
| D.使用催化剂 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)根据图象填空:

①反应物是_______ ;生成物是_______ 。
②在2min内用A、B、C表示的化学反应速率分别为_______ 、_______ 、_______ 。
③该反应的化学方程式为_______ 。
(2)人工光合作用的途径之一就是在催化剂和光照条件下,将CO2和H2O转化为CH3OH,该反应的化学方程式为:2CO2(g)+4H2O(g) 2CH3OH(g)+3O2(g)。一定条件下,在2L密闭容器中进行上述反应,测得n(CH3OH)随时间的变化如下表所示:
2CH3OH(g)+3O2(g)。一定条件下,在2L密闭容器中进行上述反应,测得n(CH3OH)随时间的变化如下表所示:
①用CH3OH表示0~3 min内该反应的平均反应速率为_______ 。
②能说明该反应已达到平衡状态的是_______ 。
a.v正(H2O)=2v逆(CO2) b.n(CH3OH)∶n(O2)=2∶3
c.容器内密度保持不变 d.容器内压强保持不变
③反应达到平衡后,往容器中通入一定量的CO2,化学平衡向_______ 方向移动(填“正反应”或“逆反应”)

①反应物是
②在2min内用A、B、C表示的化学反应速率分别为
③该反应的化学方程式为
(2)人工光合作用的途径之一就是在催化剂和光照条件下,将CO2和H2O转化为CH3OH,该反应的化学方程式为:2CO2(g)+4H2O(g)
 2CH3OH(g)+3O2(g)。一定条件下,在2L密闭容器中进行上述反应,测得n(CH3OH)随时间的变化如下表所示:
2CH3OH(g)+3O2(g)。一定条件下,在2L密闭容器中进行上述反应,测得n(CH3OH)随时间的变化如下表所示:| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| n(CH3OH)/mol | 0.000 | 0.040 | 0.070 | 0.090 | 0.100 | 0.100 | 0.100 |
①用CH3OH表示0~3 min内该反应的平均反应速率为
②能说明该反应已达到平衡状态的是
a.v正(H2O)=2v逆(CO2) b.n(CH3OH)∶n(O2)=2∶3
c.容器内密度保持不变 d.容器内压强保持不变
③反应达到平衡后,往容器中通入一定量的CO2,化学平衡向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知反应:2NO2(红棕色) N2O4(无色) △H<0,在100℃时,将0.40mol NO2气体充入2L密闭容器中,每隔一段时间对该容器的物质进行测量,得到的数据如下表:
N2O4(无色) △H<0,在100℃时,将0.40mol NO2气体充入2L密闭容器中,每隔一段时间对该容器的物质进行测量,得到的数据如下表:
(1)100s后降低反应混合物的温度,混合气体的颜色_________ (填“变浅”、“变深”或“不变”)。
(2)20至40s内,v(NO2)=__________ mol/(L·s),100℃时该反应的平衡常数K =_____________ 。
(3)将一定量的NO2充入密闭注射器中,图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是______________
A.b点的操作是压缩注射器
B.c点与a点相比,c(NO2)增大,c(N2O4)减小
C.若密闭注射器为绝热容器,则T(b)>T(c)
D.d点时v(正)>v(逆)

(4)能说明反应2NO2(红棕色) N2O4(无色)达平衡的是
N2O4(无色)达平衡的是_________
A. 体系的颜色不变 B. 恒容条件下,气体的密度不变
C. 2v正(NO2)=v逆(N2O4) D. 混合气体的平均摩尔质量不变
 N2O4(无色) △H<0,在100℃时,将0.40mol NO2气体充入2L密闭容器中,每隔一段时间对该容器的物质进行测量,得到的数据如下表:
N2O4(无色) △H<0,在100℃时,将0.40mol NO2气体充入2L密闭容器中,每隔一段时间对该容器的物质进行测量,得到的数据如下表:| 时间/s n/mol | 0 | 20 | 40 | 60 | 80 | 100 |
| n(NO2) | 0.40 | a | 0.26 | c | d | e |
| n(N2O4) | 0.00 | 0.05 | b | 0.08 | 0.08 | 0.08 |
(1)100s后降低反应混合物的温度,混合气体的颜色
(2)20至40s内,v(NO2)=
(3)将一定量的NO2充入密闭注射器中,图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是
A.b点的操作是压缩注射器
B.c点与a点相比,c(NO2)增大,c(N2O4)减小
C.若密闭注射器为绝热容器,则T(b)>T(c)
D.d点时v(正)>v(逆)

(4)能说明反应2NO2(红棕色)
 N2O4(无色)达平衡的是
N2O4(无色)达平衡的是A. 体系的颜色不变 B. 恒容条件下,气体的密度不变
C. 2v正(NO2)=v逆(N2O4) D. 混合气体的平均摩尔质量不变
您最近一年使用:0次

 2HI(g)△H<0.写出下列条件下反应速率的变化(填“增大”,“减小”或“不变”)
2HI(g)△H<0.写出下列条件下反应速率的变化(填“增大”,“减小”或“不变”) 2SO3,当其他条件不变时,只改变一个条件,将生成SO3的反应速率的变化填入下表格里(填“增大”、“ 减小”或“不变”)。
2SO3,当其他条件不变时,只改变一个条件,将生成SO3的反应速率的变化填入下表格里(填“增大”、“ 减小”或“不变”)。

