对于反应:2SO2+O2 2SO3,当其他条件不变时,只改变一个条件,将生成SO3的反应速率的变化填入下表格里(填“增大”、“ 减小”或“不变”)。
2SO3,当其他条件不变时,只改变一个条件,将生成SO3的反应速率的变化填入下表格里(填“增大”、“ 减小”或“不变”)。
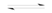 2SO3,当其他条件不变时,只改变一个条件,将生成SO3的反应速率的变化填入下表格里(填“增大”、“ 减小”或“不变”)。
2SO3,当其他条件不变时,只改变一个条件,将生成SO3的反应速率的变化填入下表格里(填“增大”、“ 减小”或“不变”)。| 编号 | 改变的条件 | 生成的SO3的速率 |
| ① | 降低温度 | |
| ② | 升高温度 | |
| ③ | 增大O2的浓度 | |
| ④ | 恒容下充入Ne | |
| ⑤ | 压缩体积 | |
| ⑥ | 使用催化剂 |
11-12高一下·辽宁盘锦·期中 查看更多[4]
(已下线)2011-2012学年辽宁省盘锦市二中高一下学期期中考试化学试卷2014-2015学年江西省上饶市横峰中学等四校高一6月月考化学试卷黑龙江省伊春市第二中学2016-2017学年高一下学期期末考试(理)化学试题人教版 高中化学 必修2 第二章 《化学反应与能量》 单元能力检测
更新时间:2017-07-24 04:39:15
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响,在常温下按照如下方案完成实验。
(1)催化剂能加快化学反应速率的原因_______ 。
(2)实验①和②的目的是_______ 。实验时由于较长时间没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是_______ 。
(3)写出实验③的化学反应方程式:_______ 。
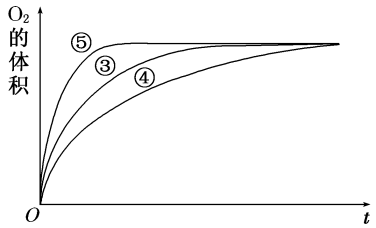
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图。分析如图能够得出的实验结论是_______ 。
| 实验编号 | 反应物 | 催化剂 |
| ① | 10 mL 2% H2O2溶液 | 无 |
| ② | 10 mL 5% H2O2溶液 | 无 |
| ③ | 10 mL 5% H2O2溶液 | 1 mL 0.1 mol • L-1 FeCl3溶液 |
| ④ | 10 mL 5% H2O2溶液+少量HCl溶液 | 1 mL 0.1 mol • L-1 FeCl3溶液 |
| ⑤ | 10 mL 5% H2O2溶液+少量NaOH溶液 | 1 mL 0.1 mol • L-1 FeCl3溶液 |
(2)实验①和②的目的是
(3)写出实验③的化学反应方程式:
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图。分析如图能够得出的实验结论是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.向体积为2 L的固定密闭容器中通入3 mol X气体,在一定温度下发生如下反应:2X(g) Y(g)+3Z(g)。经5 min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y表示的化学反应速率为
Y(g)+3Z(g)。经5 min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y表示的化学反应速率为____________ ,X的转化率为__________ ,Z的平衡浓度为_______________ 。
Ⅱ.一定温度下,反应N2(g)+O2(g) 2NO(g)在密闭容器中进行,回答下列措施对化学反应速率的影响(填“增大”“减小”或“不变”)。
2NO(g)在密闭容器中进行,回答下列措施对化学反应速率的影响(填“增大”“减小”或“不变”)。
(1)缩小体积使压强增大:__________ ;
(2)恒容充入N2:__________ ;
(3)恒容充入He:__________ ;
(4)恒压充入He:__________ 。
 Y(g)+3Z(g)。经5 min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y表示的化学反应速率为
Y(g)+3Z(g)。经5 min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y表示的化学反应速率为Ⅱ.一定温度下,反应N2(g)+O2(g)
 2NO(g)在密闭容器中进行,回答下列措施对化学反应速率的影响(填“增大”“减小”或“不变”)。
2NO(g)在密闭容器中进行,回答下列措施对化学反应速率的影响(填“增大”“减小”或“不变”)。(1)缩小体积使压强增大:
(2)恒容充入N2:
(3)恒容充入He:
(4)恒压充入He:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某同学为了探究锌与盐酸反应过程中的速率变化,他在100 mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气(气体体积已折算为标准状况下的体积),实验记录如下(累计值):
(1)反应速率最大的时间段是___________ (填“0~1 min”“1~2 min”“2~3 min”“3~4 min”或“4~5 min”),原因是___________ 。
(2)反应速率最小的时间段是___________ (填“0~1 min”“1~2 min”“2~3 min”“3~4 min“或“4~5min”),原因是___________ 。
(3)2~3 min时间段内,以盐酸的浓度变化表示该反应的速率为___________ 。
(4)如果反应太剧烈,为了减缓反应速率而又不减少产生氢气的量,该同学在盐酸中分别加入等体积的下列液体,你认为可行的是___________ (填序号)。
A.蒸馏水 B.NaCl溶液 C. 溶液 D.
溶液 D. 溶液
溶液
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL | 50 | 120 | 232 | 290 | 310 |
(1)反应速率最大的时间段是
(2)反应速率最小的时间段是
(3)2~3 min时间段内,以盐酸的浓度变化表示该反应的速率为
(4)如果反应太剧烈,为了减缓反应速率而又不减少产生氢气的量,该同学在盐酸中分别加入等体积的下列液体,你认为可行的是
A.蒸馏水 B.NaCl溶液 C.
 溶液 D.
溶液 D. 溶液
溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)一定温度下,反应 在密闭容器中进行,回答下列措施对化学反应速率的影响。(填“增大”“减小”或“不变”)
在密闭容器中进行,回答下列措施对化学反应速率的影响。(填“增大”“减小”或“不变”)
①缩小体积使压强增大:________ ;②恒容充入 :
:________ ;③恒压充入He:________ 。
(2)在恒温恒容条件下,可逆反应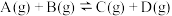 。判断该反应是否达到平衡的依据为
。判断该反应是否达到平衡的依据为________ (填正确选项前的字母)。
a.压强不随时间改变 b.气体的密度不随时间改变
c.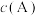 不随时间改变 d.单位时间里生成C和D的物质的量相等
不随时间改变 d.单位时间里生成C和D的物质的量相等
(3)一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
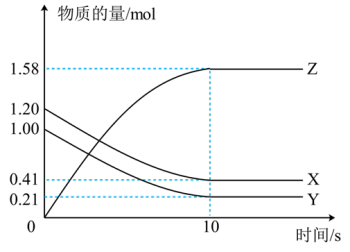
①从反应开始到10s时,用Z表示的反应速率为________ ,X的物质的量浓度减少了________ ,Y的转化率为________ 。
②该反应的化学方程式为________ 。
(1)一定温度下,反应
 在密闭容器中进行,回答下列措施对化学反应速率的影响。(填“增大”“减小”或“不变”)
在密闭容器中进行,回答下列措施对化学反应速率的影响。(填“增大”“减小”或“不变”)①缩小体积使压强增大:
 :
:(2)在恒温恒容条件下,可逆反应
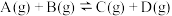 。判断该反应是否达到平衡的依据为
。判断该反应是否达到平衡的依据为a.压强不随时间改变 b.气体的密度不随时间改变
c.
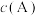 不随时间改变 d.单位时间里生成C和D的物质的量相等
不随时间改变 d.单位时间里生成C和D的物质的量相等(3)一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:

①从反应开始到10s时,用Z表示的反应速率为
②该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某温度时,在2 L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示。
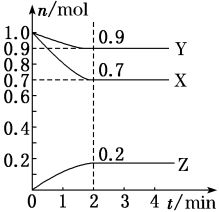
(1)由图中所给数据进行分析,该反应的化学方程式为___________________________ ;
(2)反应从开始至2分钟,用Z的浓度变化 表示的平均反应速率为v(Z)=________________ ;
(3)2min反应达平衡容器内混合气体的平均相对分子质量比起始时__________ (填增大、减小或不变);混合气体密度比起始时_________ (填增大、减小或不变)。
(4)将a mol X与b mol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n (X) = n (Y) =n (Z),则原混合气体中a : b =______________ 。
(5)下列措施能加快反应速率的是_____________ 。
A.恒压时充入He
B.恒容时充入He
C.恒容时充入X
D.及时分离出Z
E.升高温度
F.选择高效的催化剂
(6)下列说法正确的是___________ 。
A.升高温度改变化学反应的限度
B.已知正反应是吸热反应,升高温度平衡向右移动,正反应速率加快,逆反应速率减慢
C.化学反应的限度与时间长短无关 D.化学反应的限度是不可能改变的
E. 增大Y的浓度,正反应速率加快,逆反应速率减慢

(1)由图中所给数据进行分析,该反应的化学方程式为
(2)反应从开始至2分钟,用Z的浓度变化 表示的平均反应速率为v(Z)=
(3)2min反应达平衡容器内混合气体的平均相对分子质量比起始时
(4)将a mol X与b mol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n (X) = n (Y) =n (Z),则原混合气体中a : b =
(5)下列措施能加快反应速率的是
A.恒压时充入He
B.恒容时充入He
C.恒容时充入X
D.及时分离出Z
E.升高温度
F.选择高效的催化剂
(6)下列说法正确的是
A.升高温度改变化学反应的限度
B.已知正反应是吸热反应,升高温度平衡向右移动,正反应速率加快,逆反应速率减慢
C.化学反应的限度与时间长短无关 D.化学反应的限度是不可能改变的
E. 增大Y的浓度,正反应速率加快,逆反应速率减慢
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】乙烯(C2H4)是重要的化工原料,乙炔(C2H2)选择性加氢合成乙烯是科学家当前关注的热点。
(1)70℃时,反应 C2H2(g) +H2(g) C2H4(g) △H= -174 kJ • mol - 1在刚性容器中达到平衡。
C2H4(g) △H= -174 kJ • mol - 1在刚性容器中达到平衡。
①下列说法正确的是_________ (填标号).
A.选用合适的催化剂,可以增大平衡气体中C2H4的百分含量
B.投料时增大 的值,该反应的平衡常数K不变
的值,该反应的平衡常数K不变
C.通入一定量He,可以缩短反应达到平衡的时间
D.升高温度,正反应速率和逆反应速率都增大,K减小
②测得在某催化剂上生成乙烯的速率方程为v =0. 585 [ p( C2H2)] -0.36 • [ p( H2)]0.85,P(H2)—定时,若 p1(C2H2) >p2(C2H2),则 V1____ V2(填“>” “<”或“=”)。
(2)在催化剂作用下,110℃时按体积比V( C2H2): V( H2) =1: 4充入刚性容器中,发生反应C2H2 + H2=C2H4、C2H2 +2H2=C2H6。若乙炔完全反应时,乙烯的体积分数为20% ,则H2的转化率为_______ , C2H4的选择性为_______ ,( C2H4的选择性=
 100%)
100%)
(1)70℃时,反应 C2H2(g) +H2(g)
 C2H4(g) △H= -174 kJ • mol - 1在刚性容器中达到平衡。
C2H4(g) △H= -174 kJ • mol - 1在刚性容器中达到平衡。①下列说法正确的是
A.选用合适的催化剂,可以增大平衡气体中C2H4的百分含量
B.投料时增大
 的值,该反应的平衡常数K不变
的值,该反应的平衡常数K不变C.通入一定量He,可以缩短反应达到平衡的时间
D.升高温度,正反应速率和逆反应速率都增大,K减小
②测得在某催化剂上生成乙烯的速率方程为v =0. 585 [ p( C2H2)] -0.36 • [ p( H2)]0.85,P(H2)—定时,若 p1(C2H2) >p2(C2H2),则 V1
(2)在催化剂作用下,110℃时按体积比V( C2H2): V( H2) =1: 4充入刚性容器中,发生反应C2H2 + H2=C2H4、C2H2 +2H2=C2H6。若乙炔完全反应时,乙烯的体积分数为20% ,则H2的转化率为

 100%)
100%)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.某温度时,在一个10L的恒容容器中X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:_______ ;
(2)反应开始至2min,以气体X表示的平均反应速率为_______ ;
(3)平衡时混合气体的平均相对分子质量M2_______ (填“大于”,“小于”或“等于”下同)起始时的平均相对分子质量M1;
(4)将amolX与bmolY的混合气体发生上述反应,反应到某时刻各物质的量恰好满足: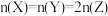 ,则气体X和气体Y的转化率之比为
,则气体X和气体Y的转化率之比为_______ 。
II.已知硫代硫酸钠溶液与稀硫酸反应的化学方程式为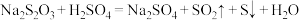 ,某学习小组探究一定条件下影响化学反应速率的因素,如下表所示:
,某学习小组探究一定条件下影响化学反应速率的因素,如下表所示:
(5)对比实验I、III的目的为:_______ 。若实验III、IV为证明浓度对速率的影响,则X=_______ ,Y=_______ 。

(2)反应开始至2min,以气体X表示的平均反应速率为
(3)平衡时混合气体的平均相对分子质量M2
(4)将amolX与bmolY的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:
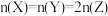 ,则气体X和气体Y的转化率之比为
,则气体X和气体Y的转化率之比为II.已知硫代硫酸钠溶液与稀硫酸反应的化学方程式为
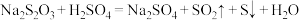 ,某学习小组探究一定条件下影响化学反应速率的因素,如下表所示:
,某学习小组探究一定条件下影响化学反应速率的因素,如下表所示:(5)对比实验I、III的目的为:
| 实验序号 | 温度 |  溶液 溶液 | 稀 |  | ||
 | 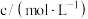 |  | 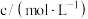 |  | ||
| I | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
| II | 25 | 5 | 0.2 | 5 | 0.2 | 10 |
| III | 35 | 5 | 0.1 | 10 | 0.1 | 5 |
| IV | 35 | 5 | 0.2 | X | 0.2 | Y |
您最近一年使用:0次
【推荐2】向2 L容器中充入1 mol CO2和2 mol H2,若只发生反应I:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H1=-51 kJ·mol-1,测得反应在不同压强、不同温度下,平衡混合物中CH3OH体积分数如图I所示,测得反应时逆反应速率与容器中c(CH3OH)关系如图II所示:

(1)图I中A、B、C三点对应的平衡常数K(A)、K(B)、K(C)由大到小的顺序排列为_______ ,图I中C点CO2的转化率为_______ 。
(2)图II中当x点平衡体系升高至某一温度时,反应可重新达平衡状态,新平衡点可能是_______ 。
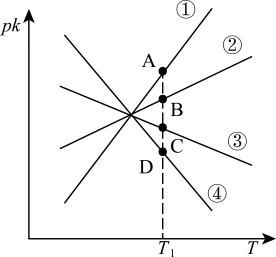
(3)反应II:CO(g)+H2O(g)⇌CO2(g)+H2(g)的正反应是放热反应,若其正、逆反应速率分别可表示为v正=k正c(CO)·c(H2O)、v逆=k逆c(CO2)·c(H2),k正、k逆分别为正、逆反应速率常数,c为物质的量浓度。则下图(pk=-lgk:T表示温度)所示①、②、③、④四条斜线中,能表示以pk正随T变化关系的是斜线_______ ,能表示pk逆随T变化关系的是斜线_______ ,图中A、B、C、D点的纵坐标分别为a+3、a+1、a-1、a-3,则温度T1时化学平衡常数K=_______ mol-1·L。

(1)图I中A、B、C三点对应的平衡常数K(A)、K(B)、K(C)由大到小的顺序排列为
(2)图II中当x点平衡体系升高至某一温度时,反应可重新达平衡状态,新平衡点可能是
(3)反应II:CO(g)+H2O(g)⇌CO2(g)+H2(g)的正反应是放热反应,若其正、逆反应速率分别可表示为v正=k正c(CO)·c(H2O)、v逆=k逆c(CO2)·c(H2),k正、k逆分别为正、逆反应速率常数,c为物质的量浓度。则下图(pk=-lgk:T表示温度)所示①、②、③、④四条斜线中,能表示以pk正随T变化关系的是斜线

您最近一年使用:0次
【推荐1】20世纪初德国化学家哈伯(F.Haber)发明工业合成氨,人工制出氮肥,粮食产量显著提高,为解决人类温饱做出重大贡献。回答下列问题:
(1)合成氨的原料H2主要来源于煤的综合利用,如煤的气化: (吸热反应),煤的气化反应过程中能量变化可表示为
(吸热反应),煤的气化反应过程中能量变化可表示为_______ (填字母)。 纳米复合物)能以太阳光为能源,使水分解获得
纳米复合物)能以太阳光为能源,使水分解获得 ,其原理如图所示。反应①的化学方程式是
,其原理如图所示。反应①的化学方程式是_______ 。_______ (填“极性键”或“非极性键”,下同),形成的化学键是_______ 。
②生成17gNH3时,该反应_______ (填“吸收”或“放出”)的能量为_______ kJ。
(1)合成氨的原料H2主要来源于煤的综合利用,如煤的气化:
 (吸热反应),煤的气化反应过程中能量变化可表示为
(吸热反应),煤的气化反应过程中能量变化可表示为
 纳米复合物)能以太阳光为能源,使水分解获得
纳米复合物)能以太阳光为能源,使水分解获得 ,其原理如图所示。反应①的化学方程式是
,其原理如图所示。反应①的化学方程式是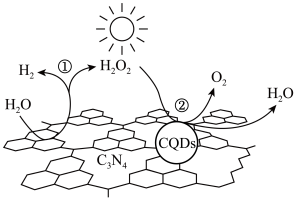
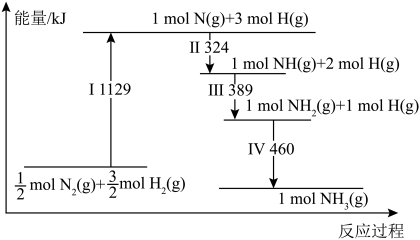
②生成17gNH3时,该反应
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】目前,科学家正在研究一种以乙烯作为还原剂的脱硝(NO)原理,其脱硝机理示意图如图1所示,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示。

(1)写出该脱硝原理总反应的化学方程式:____ 。
(2)为达到最佳脱硝效果,应采取的条件是____ 。

(1)写出该脱硝原理总反应的化学方程式:
(2)为达到最佳脱硝效果,应采取的条件是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】利用化学原理可以对工厂排放的废水进行有效检测与合理处理。
⑴染料工业排放的废水中含有大量有毒的NO2-,可在碱性条件下加入铝粉除去(加热处理后的废水会产生能使湿润的红色石蕊试纸变蓝的气体)。除去NO2-的离子方程式为 ▲ 。
⑵废水中的N、P元素是造成水体富营养化的关键因素,农药厂排放的废水中常含有较多的NH4+和PO43-,一般可以通过两种方法将其除去。
①方法一:将Ca(OH)2或CaO 投加到待处理的废水中,生成磷酸钙,从而进行回收。当处理后的废水中c(Ca2+)=2×10-7 mol/L时,溶液中c(PO43-)= ▲ mol/L。
(已知Ksp[Ca3(PO4)2]=2×10-33)
②方法二:在废水中加入镁矿工业废水,就可以生成高品位的磷矿石―鸟粪石,反应的方程式为Mg2++NH4++PO43-=MgNH4PO4↓。该方法中需要控制污水的pH为7.5~10,若pH高于10.7,鸟粪石的产量会大大降低。其原因可能为 ▲ 。与方法一相比,方法二的优点为 ▲ 。
⑶三氯乙烯在印刷、纺织等行业应用广泛,为了减少其对环境的影响,可将三氯乙烯在二氧化钛薄膜上催化降解,其反应的机理如下:
CCl2=CHCl +·Cl→·CCl2CHCl2
·CCl2CHCl2 + O2→·OOCCl2CHCl2
·OOCCl2CHCl2→·OCCl2CHCl2 + 1/2O2
·OCCl2CHCl2→CHCl2COCl +·Cl
该反应的总化学反应为 ▲ 。
⑴染料工业排放的废水中含有大量有毒的NO2-,可在碱性条件下加入铝粉除去(加热处理后的废水会产生能使湿润的红色石蕊试纸变蓝的气体)。除去NO2-的离子方程式为 ▲ 。
⑵废水中的N、P元素是造成水体富营养化的关键因素,农药厂排放的废水中常含有较多的NH4+和PO43-,一般可以通过两种方法将其除去。
①方法一:将Ca(OH)2或CaO 投加到待处理的废水中,生成磷酸钙,从而进行回收。当处理后的废水中c(Ca2+)=2×10-7 mol/L时,溶液中c(PO43-)= ▲ mol/L。
(已知Ksp[Ca3(PO4)2]=2×10-33)
②方法二:在废水中加入镁矿工业废水,就可以生成高品位的磷矿石―鸟粪石,反应的方程式为Mg2++NH4++PO43-=MgNH4PO4↓。该方法中需要控制污水的pH为7.5~10,若pH高于10.7,鸟粪石的产量会大大降低。其原因可能为 ▲ 。与方法一相比,方法二的优点为 ▲ 。
⑶三氯乙烯在印刷、纺织等行业应用广泛,为了减少其对环境的影响,可将三氯乙烯在二氧化钛薄膜上催化降解,其反应的机理如下:
CCl2=CHCl +·Cl→·CCl2CHCl2
·CCl2CHCl2 + O2→·OOCCl2CHCl2
·OOCCl2CHCl2→·OCCl2CHCl2 + 1/2O2
·OCCl2CHCl2→CHCl2COCl +·Cl
该反应的总化学反应为 ▲ 。
您最近一年使用:0次




