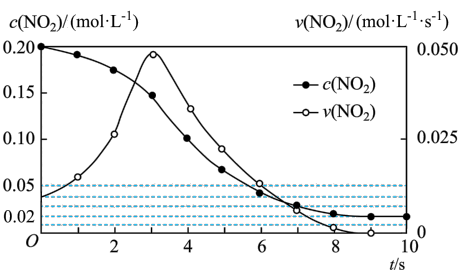
容积均为1 L的甲、乙两个容器,其中甲为绝热容器,乙为恒温容器。相同温度下,分别充入0.2 mol的NO2,发生反应:2NO2(g)  N2O4(g) ΔH<0,甲中NO2的相关量随时间变化如下图所示。0~3 s内,甲容器中NO2的反应速率增大的原因是
N2O4(g) ΔH<0,甲中NO2的相关量随时间变化如下图所示。0~3 s内,甲容器中NO2的反应速率增大的原因是___________
 N2O4(g) ΔH<0,甲中NO2的相关量随时间变化如下图所示。0~3 s内,甲容器中NO2的反应速率增大的原因是
N2O4(g) ΔH<0,甲中NO2的相关量随时间变化如下图所示。0~3 s内,甲容器中NO2的反应速率增大的原因是
2023高三·全国·专题练习 查看更多[2]
(已下线)04 常考题空4 平衡图像原因解释之温度、压强对平衡的影响 (解析)-备战2023年高考化学大题逐空突破系列(全国通用)(已下线)题型四 平衡图像原因解释-备战2024年高考化学答题技巧与模板构建
更新时间:2023-05-06 23:49:25
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】乙酸制氢具有重要意义,同时可能发生的反应如下:
热裂解反应: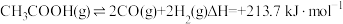
脱羧基反应:
完成下列问题:
(1)乙酸制氢时选择___________ (填“高压”或“常压”)有利于提高转化率。
(2)乙酸制直时温度与气体产率关系如图所示。
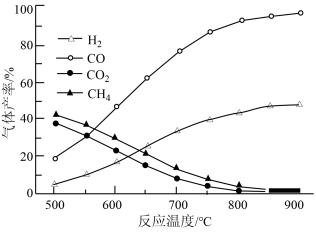
约650℃之前,脱羧基反应活化能低,速率快,故氢气产率低于甲烷;650℃之后氢气产率高于甲烷,理由是随若温度升高,热裂解反应速率加快,且___________ 。
(3)保持其他条件不变,在乙酸气中掺杂一定量水蒸气,氢气产率显著提高而CO的产率下降,请分析原因:___________ 。
热裂解反应:
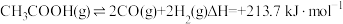
脱羧基反应:

完成下列问题:
(1)乙酸制氢时选择
(2)乙酸制直时温度与气体产率关系如图所示。

约650℃之前,脱羧基反应活化能低,速率快,故氢气产率低于甲烷;650℃之后氢气产率高于甲烷,理由是随若温度升高,热裂解反应速率加快,且
(3)保持其他条件不变,在乙酸气中掺杂一定量水蒸气,氢气产率显著提高而CO的产率下降,请分析原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】煤化工通常研究不同条件下 转化率以解决实际问题。已知在催化剂存在条件下反应:
转化率以解决实际问题。已知在催化剂存在条件下反应: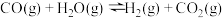 中
中 的平衡转化率随
的平衡转化率随 比例及温度变化关系如图所示:
比例及温度变化关系如图所示:
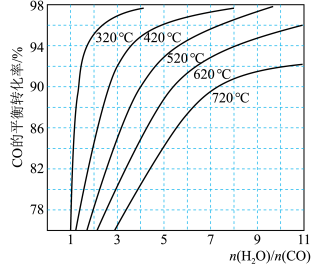
(1)上述反应的正反应是_______ (填“吸热”或“放热”)反应。
(2)若提高 比例,则该反应的平衡常数K会
比例,则该反应的平衡常数K会_______ (填“变大”“变小”或“不变”)。
(3)若降低温度,反应重新达到平衡,则
_______ (填“增大”“减小”或“不变”,下同); 转化率
转化率_______ 。
(4)在使用铁镁催化剂的实际流程中,一般采用 左右,采用此温度的原因是
左右,采用此温度的原因是_______ 。
 转化率以解决实际问题。已知在催化剂存在条件下反应:
转化率以解决实际问题。已知在催化剂存在条件下反应: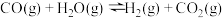 中
中 的平衡转化率随
的平衡转化率随 比例及温度变化关系如图所示:
比例及温度变化关系如图所示:
(1)上述反应的正反应是
(2)若提高
 比例,则该反应的平衡常数K会
比例,则该反应的平衡常数K会(3)若降低温度,反应重新达到平衡,则

 转化率
转化率(4)在使用铁镁催化剂的实际流程中,一般采用
 左右,采用此温度的原因是
左右,采用此温度的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某温度时,在一个2L的密闭容器中A、B、C三种气体物质的浓度随时间的变化曲线如图所示。根据图中数据,回答下列问题:
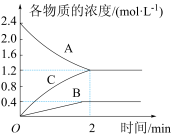
(1)该反应的化学方程式为___________ 。
(2)从开始至2min,B的平均反应速率为___________ ;平衡时,C的浓度为___________ ,A的转化率为___________ 。
(3)反应达平衡时体系的压强是开始时的___________ 倍(用分数表示)。
(4)下列叙述能说明该反应已达到化学平衡状态的是___________(填字母标号)。
(5)在某一时刻采取下列措施能使该反应速率减小的是___________(填字母标号)。

(1)该反应的化学方程式为
(2)从开始至2min,B的平均反应速率为
(3)反应达平衡时体系的压强是开始时的
(4)下列叙述能说明该反应已达到化学平衡状态的是___________(填字母标号)。
| A.B的体积分数不再发生变化 |
| B.相同时间内消耗3nmolA,同时消耗nmol的B |
| C.混合气体的总质量不随时间的变化而变化 |
| D.混合气体的密度不随时间的变化而变化 |
| A.增大压强 | B.降低温度 |
| C.体积不变,充入A | D.体积不变,从容器中分离出A |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某可逆反应: 平衡常数与温度关系如表所示:
平衡常数与温度关系如表所示:
(1)根据上述数据判断,该可逆反应的正反应是_______ (填“吸热”或“放热”)反应,理由是_______ 。
(2)为了增大X的转化率,宜采用的措施是_______(填写序号)
(3)440℃时,在2L密闭容器中,开始充入1mol X气体和3mol Y气体进行反应,在某时刻测得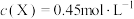 ,此时,反应是否达到平衡状态
,此时,反应是否达到平衡状态_______ (填“是”或“否”),简述理由:_______ 。
(4)在某容积固定的容器中进行上述反应,当X、Y起始物质的量一定时,仅改变一个外界条件对Z体积分数的影响如图所示(曲线Ⅰ为标准):
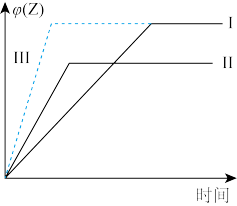
①曲线Ⅱ改变的条件是_______ 。
②曲线Ⅲ改变的条件是_______ 。
 平衡常数与温度关系如表所示:
平衡常数与温度关系如表所示:| 温度(℃) | 360 | 440 | 520 |
| K | 0.036 | 0.010 | 0.0038 |
(2)为了增大X的转化率,宜采用的措施是_______(填写序号)
| A.升高温度 | B.增大压强 | C.使用高效催化剂 | D.分离Z |
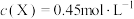 ,此时,反应是否达到平衡状态
,此时,反应是否达到平衡状态(4)在某容积固定的容器中进行上述反应,当X、Y起始物质的量一定时,仅改变一个外界条件对Z体积分数的影响如图所示(曲线Ⅰ为标准):

①曲线Ⅱ改变的条件是
②曲线Ⅲ改变的条件是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】2023年5月,中国神舟十六号载人飞船成功发射,三位航天员景海鹏、朱杨柱、桂海潮在天宫空间站开启长达半年的太空生活。航天员呼吸产生的CO2还可以利用Bosch反应:CO2(g)+2H2(g) C(s)+ 2H2O(g) 代替Sabatier反应。在250℃时,向体积为2L恒容密闭容器中通入2molH2和1molCO2发生Bosch反应,测得容器内气压变化如图所示。
C(s)+ 2H2O(g) 代替Sabatier反应。在250℃时,向体积为2L恒容密闭容器中通入2molH2和1molCO2发生Bosch反应,测得容器内气压变化如图所示。

(1)试解释容器内气压先增大后减小的原因:___________ 。
(2)该温度下Bosch反应的Kp=___________ (写出计算过程,Kp为用气体的分压表示的平衡常数,分压=气体的体积分数×体系总压)。
(3)在上图基础上画出其他条件相同,向体系加入催化剂时其压强随时间的变化曲线________ 。
 C(s)+ 2H2O(g) 代替Sabatier反应。在250℃时,向体积为2L恒容密闭容器中通入2molH2和1molCO2发生Bosch反应,测得容器内气压变化如图所示。
C(s)+ 2H2O(g) 代替Sabatier反应。在250℃时,向体积为2L恒容密闭容器中通入2molH2和1molCO2发生Bosch反应,测得容器内气压变化如图所示。
(1)试解释容器内气压先增大后减小的原因:
(2)该温度下Bosch反应的Kp=
(3)在上图基础上画出其他条件相同,向体系加入催化剂时其压强随时间的变化曲线
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某科研小组研究臭氧氧化-碱吸收法同时脱除SO2和NO的工艺,其氧化过程的反应原理及反应热、活化能数据如下:
反应I:NO(g)+O3(g) NO2(g)+O2(g)△H1=-200.9kJ·mol-1,E1=3.2kJ·mol-1
NO2(g)+O2(g)△H1=-200.9kJ·mol-1,E1=3.2kJ·mol-1
反应II:SO2(g)+O3(g) SO3(g)+O2(g)△H2=-241.6kJ·mol-1,E2=58kJ·mol-1
SO3(g)+O2(g)△H2=-241.6kJ·mol-1,E2=58kJ·mol-1
已知该体系中臭氧发生分解反应:2O3(g) 3O2(g)。
3O2(g)。
保持其他条件不变,每次向容积为2L的反应器中充入含2.0molNO、2.0molSO2的模拟烟气和4.0molO3,改变温度,反应相同时间后体系中NO和SO2的转化率如图所示:

(1)臭氧氧化过程不能有效地脱硫,但后续步骤“碱吸收”可以有效脱硫。写出利用氨水吸收SO3的离子方程式:___ 。
(2)由图可知相同温度下NO的转化率远高于SO2,其可能原因是___ 。
(3)若其他条件不变时,缩小反应器的容积,可提高NO和SO2的转化率,请解释原因:___ 。
(4)假设100℃时,P、Q均为平衡点,此时发生分解反应的O3占充入O3总量的10%,体系中剩余O3的物质的量是___ 。试分析反应II中SO2转化率随温度变化先增大后减小的可能原因:___ 。
反应I:NO(g)+O3(g)
 NO2(g)+O2(g)△H1=-200.9kJ·mol-1,E1=3.2kJ·mol-1
NO2(g)+O2(g)△H1=-200.9kJ·mol-1,E1=3.2kJ·mol-1反应II:SO2(g)+O3(g)
 SO3(g)+O2(g)△H2=-241.6kJ·mol-1,E2=58kJ·mol-1
SO3(g)+O2(g)△H2=-241.6kJ·mol-1,E2=58kJ·mol-1已知该体系中臭氧发生分解反应:2O3(g)
 3O2(g)。
3O2(g)。保持其他条件不变,每次向容积为2L的反应器中充入含2.0molNO、2.0molSO2的模拟烟气和4.0molO3,改变温度,反应相同时间后体系中NO和SO2的转化率如图所示:

(1)臭氧氧化过程不能有效地脱硫,但后续步骤“碱吸收”可以有效脱硫。写出利用氨水吸收SO3的离子方程式:
(2)由图可知相同温度下NO的转化率远高于SO2,其可能原因是
(3)若其他条件不变时,缩小反应器的容积,可提高NO和SO2的转化率,请解释原因:
(4)假设100℃时,P、Q均为平衡点,此时发生分解反应的O3占充入O3总量的10%,体系中剩余O3的物质的量是
您最近一年使用:0次



