金刚石和石墨为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时完全燃烧生成二氧化碳,1mol金刚石和石墨分别与O2反应,放出的热量如图所示,回答下列问题:
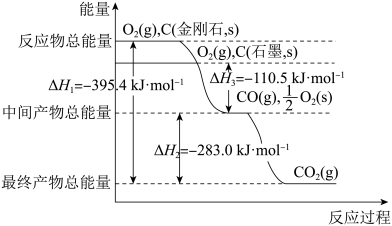
(1)金刚石、石墨与O2反应生成CO2均是_______ 反应(填“放热”或“吸热”),在通常状况下,金刚石和石墨的稳定性较大的是_______ (填“金刚石”或“石墨”);
(2)石墨的燃烧热△H=_______ kJ·mol-1,反应C(金刚石,s)=C(石墨,s)的反应热△H=_______ kJ·mol-1;
(3)12g石墨在一定量空气中燃烧,生成36g气体,该过程放出的热量为_______ kJ。

(1)金刚石、石墨与O2反应生成CO2均是
(2)石墨的燃烧热△H=
(3)12g石墨在一定量空气中燃烧,生成36g气体,该过程放出的热量为
更新时间:2021-08-02 10:56:10
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】回答问题:
(1)已知C(s、金刚石)+O2(g)=CO2(g) △H=-395.4 kJ·mol-1,C(s、石墨)+O2(g)=CO2(g) △H=-393.5 kJ·mol-1。则石墨中C-C键键能____ (填“大于”“小于”或“等于”)金刚石中C-C键键能。
(2)已知下列反应的反应热:
CH4(g)+H2O(g)=CO(g)+3H2(g) △H1=+206.2 kJ·mol-1
CH4(g)+CO2(g)=2CO(g)+2H2(g) △H2=-247.4 kJ·mol-1
则CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为____ 。
(1)已知C(s、金刚石)+O2(g)=CO2(g) △H=-395.4 kJ·mol-1,C(s、石墨)+O2(g)=CO2(g) △H=-393.5 kJ·mol-1。则石墨中C-C键键能
(2)已知下列反应的反应热:
CH4(g)+H2O(g)=CO(g)+3H2(g) △H1=+206.2 kJ·mol-1
CH4(g)+CO2(g)=2CO(g)+2H2(g) △H2=-247.4 kJ·mol-1
则CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请结合题中数据,写出对应的热化学方程式。
(1)航天燃料从液态变为固态,是一项重大的技术突破。铍是高效的火箭燃料,燃烧时放出巨大的能量,已知1kg金属铍完全燃烧生成BeO(s),放出62700kJ的热量;________________________ 。
(2)1mol CH4(g)和足量水蒸气反应生成CO气体和氢气,吸收216 kJ热量:_____________________ 。
(3)已知2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH=akJ/mol;CO(g)+2H2(g)=CH3OH(g) ΔH=bkJ/mol
试写出CH4和O2制取甲醇的热化学方程式:____________________ 。
(1)航天燃料从液态变为固态,是一项重大的技术突破。铍是高效的火箭燃料,燃烧时放出巨大的能量,已知1kg金属铍完全燃烧生成BeO(s),放出62700kJ的热量;
(2)1mol CH4(g)和足量水蒸气反应生成CO气体和氢气,吸收216 kJ热量:
(3)已知2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH=akJ/mol;CO(g)+2H2(g)=CH3OH(g) ΔH=bkJ/mol
试写出CH4和O2制取甲醇的热化学方程式:
您最近一年使用:0次
【推荐1】2SO2(g)+O2(g)=2SO3(g)反应过程中的能量变化如图所示。已知1 mol SO2(g)被氧化为1 mol SO3(g)的ΔH1=-99 kJ/mol。请回答下列问题:

(1) 图中A、C分别表示________ 、________ 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________ ;
(2) 图中ΔH=__________ kJ/mol;
(3) 已知单质硫的燃烧热为296 kJ·mol-1,计算由S(s)生成3mol SO3(g)的ΔH_______ 。

(1) 图中A、C分别表示
(2) 图中ΔH=
(3) 已知单质硫的燃烧热为296 kJ·mol-1,计算由S(s)生成3mol SO3(g)的ΔH
您最近一年使用:0次
【推荐2】工业上用CO生产燃料甲醇。一定温度和容积条件下发生反应:CO(g)+2H2(g)  CH3OH(g)。图1表示反应中的能量变化;请回答下列问题:
CH3OH(g)。图1表示反应中的能量变化;请回答下列问题:

(1)在图1中,曲线____ (填a或b)表示使用了催化剂;没有使用催化剂时,在该温度和压强条件下反应CO(g)+2H2(g)  CH3OH(g)的△H =
CH3OH(g)的△H =________ 。
(2)已知CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g)ΔH =-193kJ/mol,又知H2O(l)= H2O(g) ΔH =+44 kJ/mol,请写出32g的CH3OH(g)完全燃烧生成液态水的热化学方程式_______________________ 。
 CH3OH(g)。图1表示反应中的能量变化;请回答下列问题:
CH3OH(g)。图1表示反应中的能量变化;请回答下列问题:
(1)在图1中,曲线
 CH3OH(g)的△H =
CH3OH(g)的△H =(2)已知CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g)ΔH =-193kJ/mol,又知H2O(l)= H2O(g) ΔH =+44 kJ/mol,请写出32g的CH3OH(g)完全燃烧生成液态水的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题。
(1)如图是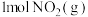 和
和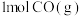 反应生成
反应生成 和
和 过程中的能量变化示意图。请写出
过程中的能量变化示意图。请写出 和
和 反应的热化学方程式
反应的热化学方程式__________ 。
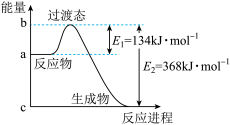
(2)用如图所示装置进行中和热的测定实验。
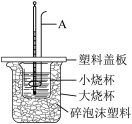
①仪器A的名称是__________ ,碎泡沫塑料的作用是__________ 。
②若实验过程中,未加塑料盖板,则实验测出的
__________ (填“偏大”或“偏小”或“无影响”)。
③理论上强酸强碱的中和热为 ,写出表示稀硫酸和稀
,写出表示稀硫酸和稀 溶液反应的中和热的热化学方程式
溶液反应的中和热的热化学方程式__________ 。
(3)甲醇是人们开发和利用的一种新能源。已知:


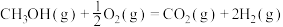
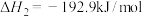
①甲醇蒸气完全燃烧生成二氧化碳气体和液态水的热化学方程式为__________ ;
② 的燃烧热为
的燃烧热为__________ 。
(1)如图是
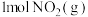 和
和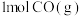 反应生成
反应生成 和
和 过程中的能量变化示意图。请写出
过程中的能量变化示意图。请写出 和
和 反应的热化学方程式
反应的热化学方程式
(2)用如图所示装置进行中和热的测定实验。

①仪器A的名称是
②若实验过程中,未加塑料盖板,则实验测出的

③理论上强酸强碱的中和热为
 ,写出表示稀硫酸和稀
,写出表示稀硫酸和稀 溶液反应的中和热的热化学方程式
溶液反应的中和热的热化学方程式(3)甲醇是人们开发和利用的一种新能源。已知:


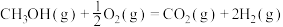
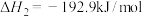
①甲醇蒸气完全燃烧生成二氧化碳气体和液态水的热化学方程式为
②
 的燃烧热为
的燃烧热为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】化学反应过程中释放或吸收的热量在生活、生产、科技及科学研究中具有广泛的应用。
(1)“神舟”系列火箭用偏二甲肼 作燃料,
作燃料, 作氧化剂,反应后产物无污染。
作氧化剂,反应后产物无污染。
已知:
反应1: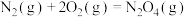
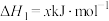 ;
;
反应2: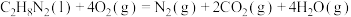
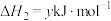 。
。
写出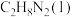 和
和 反应生成
反应生成 、
、 、
、 的热化学方程式:
的热化学方程式:_______ 。
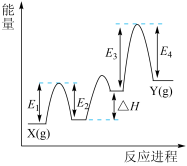
(2)已知某金属氧化物催化丙烷脱氢过程中,部分反应进程如图,则能 过程中的焓变为
过程中的焓变为_______ (列式表示)。
(3)已知,在25℃和101kPa下,部分化学键的键能数据如表所示。
①在25℃和101kPa下,工业合成氨的反应中每生成1mol 就会放出46kJ热量,在该条件下,向某容器中加入2mol
就会放出46kJ热量,在该条件下,向某容器中加入2mol 、6mol
、6mol 及合适的催化剂,充分反应后测得其放出的热量小于92kJ,原因可能是
及合适的催化剂,充分反应后测得其放出的热量小于92kJ,原因可能是_______ ,表中的a=_______ 。
②科学家发现了一种新的气态分子 (
(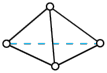 ),在25℃和101kPa下,
),在25℃和101kPa下, 转化为
转化为 的热化学方程式为
的热化学方程式为_______ ,此可知1mol 与1mol
与1mol 中能量更低的是
中能量更低的是_______ (填化学式)。
③已知:
 。甲烷是一种常用燃料,则表示甲烷的燃烧热的热化学方程式为
。甲烷是一种常用燃料,则表示甲烷的燃烧热的热化学方程式为_______ 。
(1)“神舟”系列火箭用偏二甲肼
 作燃料,
作燃料, 作氧化剂,反应后产物无污染。
作氧化剂,反应后产物无污染。已知:
反应1:
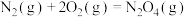
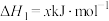 ;
;反应2:
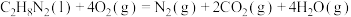
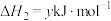 。
。写出
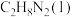 和
和 反应生成
反应生成 、
、 、
、 的热化学方程式:
的热化学方程式:(2)已知某金属氧化物催化丙烷脱氢过程中,部分反应进程如图,则能
 过程中的焓变为
过程中的焓变为
(3)已知,在25℃和101kPa下,部分化学键的键能数据如表所示。
| 化学键 | H—H | H—N | N≡N | O=O | C—H | C=O | H—O | N—N |
键能/( ) ) | 436 | 391 | a | 498 | 414 | 803 | 462 | 193 |
①在25℃和101kPa下,工业合成氨的反应中每生成1mol
 就会放出46kJ热量,在该条件下,向某容器中加入2mol
就会放出46kJ热量,在该条件下,向某容器中加入2mol 、6mol
、6mol 及合适的催化剂,充分反应后测得其放出的热量小于92kJ,原因可能是
及合适的催化剂,充分反应后测得其放出的热量小于92kJ,原因可能是②科学家发现了一种新的气态分子
 (
( ),在25℃和101kPa下,
),在25℃和101kPa下, 转化为
转化为 的热化学方程式为
的热化学方程式为 与1mol
与1mol 中能量更低的是
中能量更低的是③已知:

 。甲烷是一种常用燃料,则表示甲烷的燃烧热的热化学方程式为
。甲烷是一种常用燃料,则表示甲烷的燃烧热的热化学方程式为
您最近一年使用:0次
【推荐2】根据化学能和热能、电能相关的知识,请回答下列问题:
I.已知31g白磷(P4)变为31g红磷(P)时释放能量。上述变化属于__________ 变化(填“物理”或“化学”);稳定性白磷_________ 红磷(填“>”或“<”);
II.氢气是一种清洁能源,在我国航天工程中也有应用。
(1)已知1g氢气燃烧生成气态水放出热量121kJ,其中断裂1mol H—H键吸收436kJ,断裂1mol O=O键吸收496kJ,那么形成1mol H—O键放出热__ 。
(2)航天技术上使用的氢-氧燃料电池原理可以简单看作下图“氢-氧燃料电池的装置图” 则:
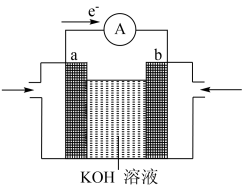
①a极为电池的______ (填“正极”或“负极”);溶液中OH-移向_______ 电极(填“a”或“b”)。
②放电时,b电极附近pH_______ 。(填增大、减小或不变)。
③如把H2改为甲烷,总反应为:CH4+ 2O2 + 2OH- = CO32- + 3H2O,则负极电极反应式为:_________ 。
I.已知31g白磷(P4)变为31g红磷(P)时释放能量。上述变化属于
II.氢气是一种清洁能源,在我国航天工程中也有应用。
(1)已知1g氢气燃烧生成气态水放出热量121kJ,其中断裂1mol H—H键吸收436kJ,断裂1mol O=O键吸收496kJ,那么形成1mol H—O键放出热
(2)航天技术上使用的氢-氧燃料电池原理可以简单看作下图“氢-氧燃料电池的装置图” 则:

①a极为电池的
②放电时,b电极附近pH
③如把H2改为甲烷,总反应为:CH4+ 2O2 + 2OH- = CO32- + 3H2O,则负极电极反应式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】碳是化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
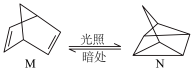
(1)有机物M经过太阳光照可转化成N,转化过程如下,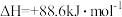 。则M、N相比,较稳定的是
。则M、N相比,较稳定的是_______
(2)已知 (l)的燃烧热为238.6kJ/mol,
(l)的燃烧热为238.6kJ/mol,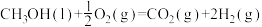
 ,则a
,则a_______ 238.6(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
(3)使 和
和 (g)通过灼热的炭层,生成HCl(g)和
(g)通过灼热的炭层,生成HCl(g)和 ,当有1mol
,当有1mol 参与反应时释放出145kJ热量,写出该反应的热化学方程式
参与反应时释放出145kJ热量,写出该反应的热化学方程式_______ 。
(4)火箭和导弹表面的薄层是耐高温物质。下列反应可制得耐高温材料,热化学方程式为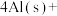
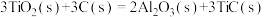
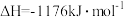 。反应过程中每转移1mol
。反应过程中每转移1mol 放出的热量为
放出的热量为_______ kJ。
(5)已知1mol燃料完全燃烧的数据分别为:
使用上述燃料最能体现“低碳经济”理念的是_______ 。
(6)乙基叔丁基醚(以ETBE表示)是一种性能优良的高辛烷值汽油调和剂。用乙醇与异丁烯(以IB表示)在催化剂HZSM—5催化下合成ETBE,反应的热化学方程式为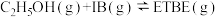
 。反应物被催化剂HZSM—5吸附的顺序与反应历程的关系如图所示,该反应的
。反应物被催化剂HZSM—5吸附的顺序与反应历程的关系如图所示,该反应的
_______ a ;反应历程的最优途径是
;反应历程的最优途径是
_______ (填“ ”、“
”、“ ”或“
”或“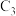 ”)。
”)。
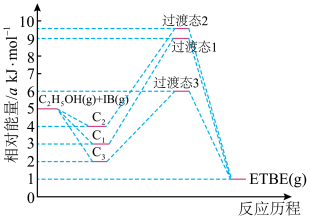
 表示先吸附乙醇,
表示先吸附乙醇, 表示先吸附异丁烯,
表示先吸附异丁烯,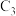 表示乙醇和异丁烯同时吸附
表示乙醇和异丁烯同时吸附
(1)有机物M经过太阳光照可转化成N,转化过程如下,
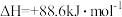 。则M、N相比,较稳定的是
。则M、N相比,较稳定的是
(2)已知
 (l)的燃烧热为238.6kJ/mol,
(l)的燃烧热为238.6kJ/mol,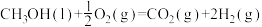
 ,则a
,则a ”、“
”、“ ”或“
”或“ ”)。
”)。(3)使
 和
和 (g)通过灼热的炭层,生成HCl(g)和
(g)通过灼热的炭层,生成HCl(g)和 ,当有1mol
,当有1mol 参与反应时释放出145kJ热量,写出该反应的热化学方程式
参与反应时释放出145kJ热量,写出该反应的热化学方程式(4)火箭和导弹表面的薄层是耐高温物质。下列反应可制得耐高温材料,热化学方程式为
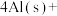
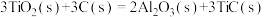
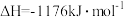 。反应过程中每转移1mol
。反应过程中每转移1mol 放出的热量为
放出的热量为(5)已知1mol燃料完全燃烧的数据分别为:
| 燃料 | 一氧化碳 | 甲烷 | 异辛烷(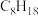 ) ) | 乙醇 |
 | 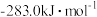 | 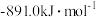 | 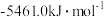 | 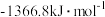 |
(6)乙基叔丁基醚(以ETBE表示)是一种性能优良的高辛烷值汽油调和剂。用乙醇与异丁烯(以IB表示)在催化剂HZSM—5催化下合成ETBE,反应的热化学方程式为
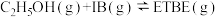
 。反应物被催化剂HZSM—5吸附的顺序与反应历程的关系如图所示,该反应的
。反应物被催化剂HZSM—5吸附的顺序与反应历程的关系如图所示,该反应的
 ;反应历程的最优途径是
;反应历程的最优途径是
 ”、“
”、“ ”或“
”或“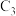 ”)。
”)。
 表示先吸附乙醇,
表示先吸附乙醇, 表示先吸附异丁烯,
表示先吸附异丁烯,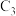 表示乙醇和异丁烯同时吸附
表示乙醇和异丁烯同时吸附
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】火箭推进器中盛有液态肼(N2H4)和氧气。当把0.2mol液态肼和足量氧气反应,生成氮气和水蒸气,放出128.8kJ的热量(相当于25℃、101kPa下测得的热量)。
(1)反应的热化学方程式为_____________________________________________ 。
(2)又已知H2O(l) = H2O(g)ΔH= +44kJ/mol。则16g液态肼与氧气生成液态水时放出的热量是____ kJ。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是__________________________________ 。
(1)反应的热化学方程式为
(2)又已知H2O(l) = H2O(g)ΔH= +44kJ/mol。则16g液态肼与氧气生成液态水时放出的热量是
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)已知:2H2(g)+O2(g)=2H2O(g) ΔH=−483.6kJ·mol−1,
查阅文献资料,化学键的键能如下表:
①合成氨反应的热化学方程式为______________ 。
②氨分解反应NH3(g)=1/2N2(g)+3/2H2(g)的活化能Ea1=300kJ·mol−1,则合成氨反应1/2N2(g)+3/2H2(g)=NH3(g)的活化能Ea2=___________ kJ·mol−1。
③氨气完全燃烧生成N2(g)和气态水的热化学方程式为___________________ 。
(2)研究氮氧化物与悬浮的大气中海盐粒子的相互作用时,涉及如下反应:
Ⅰ.2NO2(g)+NaCl(s)=NaNO3(s)+ClNO(g) ΔH1<0 Ⅱ.2NO(g)+Cl2(g)=2ClNO(g) ΔH2<0
则反应4NO2(g)+2NaCl(s)=2NaNO3(s)+2NO(g)+Cl2(g)的ΔH=___________ (用ΔH1、ΔH2表示)。
(1)已知:2H2(g)+O2(g)=2H2O(g) ΔH=−483.6kJ·mol−1,
查阅文献资料,化学键的键能如下表:
| 化学键 | H−H键 | N≡N键 | N−H键 |
| E/(kJ·mol−1) | 436 | 946 | 391 |
②氨分解反应NH3(g)=1/2N2(g)+3/2H2(g)的活化能Ea1=300kJ·mol−1,则合成氨反应1/2N2(g)+3/2H2(g)=NH3(g)的活化能Ea2=
③氨气完全燃烧生成N2(g)和气态水的热化学方程式为
(2)研究氮氧化物与悬浮的大气中海盐粒子的相互作用时,涉及如下反应:
Ⅰ.2NO2(g)+NaCl(s)=NaNO3(s)+ClNO(g) ΔH1<0 Ⅱ.2NO(g)+Cl2(g)=2ClNO(g) ΔH2<0
则反应4NO2(g)+2NaCl(s)=2NaNO3(s)+2NO(g)+Cl2(g)的ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.回答下列问题:
(1)在微生物作用的条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:

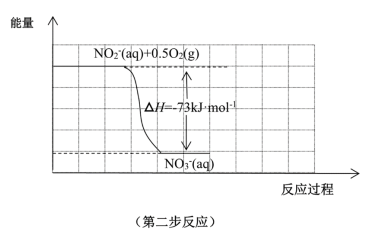
①第一步反应是____ (填“放热”或“吸热”)反应。
②1molNH (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是___ 。
(2)已知H2(g)+Br2(l)=2HBr(g) ΔH=-72kJ·mol-1,蒸发1molBr2(l)需要吸收的能量为30kJ,其他相关数据如表:
则表中a=____ 。
Ⅱ.工业生产硝酸的尾气中含有氮氧化物NOx(NO和NO2的混合物),对生态环境和人类健康带来较大的威胁。
(3)工业上可用氨催化吸收法处理NOx,反应原理如下:4xNH3+6NOx (2x+3)N2+6xH2O。某化学兴趣小组模拟该处理过程的实验装置如图:
(2x+3)N2+6xH2O。某化学兴趣小组模拟该处理过程的实验装置如图:
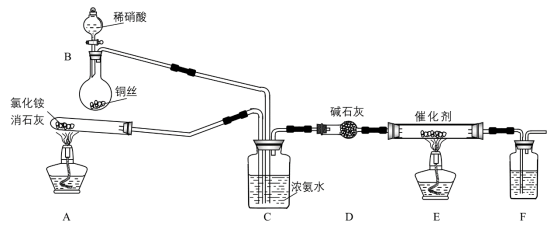
①装置E中发生反应的化学方程式为____ 。
②装置D中碱石灰的作用是____ 。
(4)工业上也常用Na2CO3溶液吸收法处理NOx。
已知:NO不能与Na2CO3溶液反应。
NO+NO2+Na2CO3=2NaNO2+CO2(Ⅰ)
2NO2+Na2CO3=NaNO2+NaNO3+CO2(Ⅱ)
当NOx被Na2CO3溶液完全吸收时,x的值不可能是____ (填字母)。
A.1.3 B.1.6 C.1.8
(1)在微生物作用的条件下,NH
 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:

①第一步反应是
②1molNH
 (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是(2)已知H2(g)+Br2(l)=2HBr(g) ΔH=-72kJ·mol-1,蒸发1molBr2(l)需要吸收的能量为30kJ,其他相关数据如表:
| 物质 | H2(g) | Br2(g) | HBr(g) |
| lmol分子中的化学键断裂时需要吸收的能量(kJ) | 436 | 200 | a |
Ⅱ.工业生产硝酸的尾气中含有氮氧化物NOx(NO和NO2的混合物),对生态环境和人类健康带来较大的威胁。
(3)工业上可用氨催化吸收法处理NOx,反应原理如下:4xNH3+6NOx
 (2x+3)N2+6xH2O。某化学兴趣小组模拟该处理过程的实验装置如图:
(2x+3)N2+6xH2O。某化学兴趣小组模拟该处理过程的实验装置如图:
①装置E中发生反应的化学方程式为
②装置D中碱石灰的作用是
(4)工业上也常用Na2CO3溶液吸收法处理NOx。
已知:NO不能与Na2CO3溶液反应。
NO+NO2+Na2CO3=2NaNO2+CO2(Ⅰ)
2NO2+Na2CO3=NaNO2+NaNO3+CO2(Ⅱ)
当NOx被Na2CO3溶液完全吸收时,x的值不可能是
A.1.3 B.1.6 C.1.8
您最近一年使用:0次



