完成下列问题。
(1)第十四届运动会于2021年9月15日在西安奥体中心体育场隆重开幕,00”后体坛新秀杨倩,带着我们共同的希望和梦想,点燃主火炬。火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料。试回答下列问题:
①如图是一定量丙烷完全燃烧生成CO2和1molH2O(l)过程中的能量变化图,图中的括号内应该填入___________ 。(“+”或“−”)
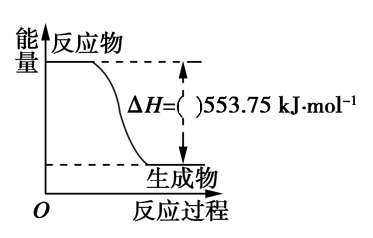
②写出表示丙烷燃烧热的热化学方程式:___________ 。
③二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1mol二甲醚完全燃烧生成CO2和液态水放出1455kJ热量。若1mol丙烷和二甲醚的混合气体完全燃烧生成CO2和液态水共放出1645kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为___________ 。
(2)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160kJ/mol
若用标准状况下4.48LCH4还原NO2生成N2,反应中转移的电子总数为___________ (用阿伏加德罗常数NA表示),放出的热量为___________ kJ。
(3)反应热大小比较(填“>”“<”或“=”)
A(g)+B(g)=C(g) ΔH1<0;A(g)+B(g)=C(l) ΔH2<0,则ΔH1___________ ΔH2
S(g)+O2(g)=SO2(g) ΔH1<0;S(s)+O2(g)=SO2(g) ΔH2<0,则ΔH1___________ ΔH2
C(s)+O2(g)=CO2(g) ΔH1<0;C(s)+ O2(g)=CO(g) ΔH2<0,则ΔH1
O2(g)=CO(g) ΔH2<0,则ΔH1___________ ΔH2
(1)第十四届运动会于2021年9月15日在西安奥体中心体育场隆重开幕,00”后体坛新秀杨倩,带着我们共同的希望和梦想,点燃主火炬。火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料。试回答下列问题:
①如图是一定量丙烷完全燃烧生成CO2和1molH2O(l)过程中的能量变化图,图中的括号内应该填入

②写出表示丙烷燃烧热的热化学方程式:
③二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1mol二甲醚完全燃烧生成CO2和液态水放出1455kJ热量。若1mol丙烷和二甲醚的混合气体完全燃烧生成CO2和液态水共放出1645kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为
(2)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160kJ/mol
若用标准状况下4.48LCH4还原NO2生成N2,反应中转移的电子总数为
(3)反应热大小比较(填“>”“<”或“=”)
A(g)+B(g)=C(g) ΔH1<0;A(g)+B(g)=C(l) ΔH2<0,则ΔH1
S(g)+O2(g)=SO2(g) ΔH1<0;S(s)+O2(g)=SO2(g) ΔH2<0,则ΔH1
C(s)+O2(g)=CO2(g) ΔH1<0;C(s)+
 O2(g)=CO(g) ΔH2<0,则ΔH1
O2(g)=CO(g) ΔH2<0,则ΔH1
更新时间:2021-10-11 20:00:32
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】已知一些烷烃的燃烧热如下表:
(1)热稳定性:正丁烷________ (填“>”或“<”)异丁烷。
(2)写出表示乙烷燃烧热的热化学方程式_____________________________________ 。
(3)相同物质的量的烷烃,碳原子数越多,燃烧放出的热量越_______ (填“多”或“少”)。
(4)有同学估计“正戊烷的燃烧热大约在3 540 kJ·mol−1左右”,你认为正确吗?______ 。理由是_______________________________________ 。
| 化合物 | 燃烧热/kJ·mol−1 | 化合物 | 燃烧热/kJ·mol−1 |
| 甲烷 | 891.0 | 正丁烷 | 2 878.0 |
| 乙烷 | 1 560.8 | 异丁烷 | 2 869.6 |
| 丙烷 | 2 221.5 | 异戊烷 | 3 531.3 |
(1)热稳定性:正丁烷
(2)写出表示乙烷燃烧热的热化学方程式
(3)相同物质的量的烷烃,碳原子数越多,燃烧放出的热量越
(4)有同学估计“正戊烷的燃烧热大约在3 540 kJ·mol−1左右”,你认为正确吗?
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)标准生成热指的是在某温度下,由处于标准状态的各种元素的最稳定的单质生成标准状态下 1mol 某纯物质的热效应,单位常用 kJ/mol表示,已知在 25℃的条件下:
①Ag2O(s)+2HCl(g)═2AgCl(s)+H2O(l)△H=-324.4 kJ/mol
②2Ag(s)+ O2(g)═Ag2O(s)△H=-30.56kJ/mol
O2(g)═Ag2O(s)△H=-30.56kJ/mol
③ H2(g)+
H2(g)+  Cl2(g)═HCl(g)△H=-92.21 kJ/mol
Cl2(g)═HCl(g)△H=-92.21 kJ/mol
④H2(g)+ O2(g)═H2O(l)△H=-285.6 kJ/mol
O2(g)═H2O(l)△H=-285.6 kJ/mol
则25℃时氯化银的标准生成热为________ kJ/mol;
(2)实验测得 64g 甲醇[CH3OH(l)]在氧气中充分燃烧生成 CO2气体和液态水时放出 1452.8kJ 的热量,则表示甲醇燃烧热的热化学方程式_________________ ;
(3)以甲烷、氧气为原料,KOH 为电解质,构成燃料电池,写出其负极的电极反应式:________ ;
(4)电解法制取有广泛用途的 Na2FeO4,工作原理如下图所示。
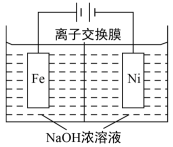
已知:Na2FeO4只在强碱性条件下稳定。
①Na2FeO4能够净水的主要原因是_______________ 。
②阳极电极反应式_______________ ;
③为使电解能较持久进行,应选用_______________ 离子交换膜(填“阴”或“阳”)。
①Ag2O(s)+2HCl(g)═2AgCl(s)+H2O(l)△H=-324.4 kJ/mol
②2Ag(s)+
 O2(g)═Ag2O(s)△H=-30.56kJ/mol
O2(g)═Ag2O(s)△H=-30.56kJ/mol③
 H2(g)+
H2(g)+  Cl2(g)═HCl(g)△H=-92.21 kJ/mol
Cl2(g)═HCl(g)△H=-92.21 kJ/mol④H2(g)+
 O2(g)═H2O(l)△H=-285.6 kJ/mol
O2(g)═H2O(l)△H=-285.6 kJ/mol则25℃时氯化银的标准生成热为
(2)实验测得 64g 甲醇[CH3OH(l)]在氧气中充分燃烧生成 CO2气体和液态水时放出 1452.8kJ 的热量,则表示甲醇燃烧热的热化学方程式
(3)以甲烷、氧气为原料,KOH 为电解质,构成燃料电池,写出其负极的电极反应式:
(4)电解法制取有广泛用途的 Na2FeO4,工作原理如下图所示。

已知:Na2FeO4只在强碱性条件下稳定。
①Na2FeO4能够净水的主要原因是
②阳极电极反应式
③为使电解能较持久进行,应选用
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)1.00 L 1.00 mol·L-1 H2SO4溶液与2.00 L 1.00 mol·L-1 NaOH溶液完全反应,放出114.6 kJ热量,该反应的中和热为________ ,表示其中和热的热化学方程式_________________________________ 。
(2)在25 ℃、101 kPa时,1.00 g C6H6(l)燃烧生成CO2(g)和H2O(l),放出41.8 kJ的热量,C6H6的燃烧热为________ kJ·mol-1,该反应的热化学方程式为_____________________________________ 。
(2)在25 ℃、101 kPa时,1.00 g C6H6(l)燃烧生成CO2(g)和H2O(l),放出41.8 kJ的热量,C6H6的燃烧热为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)甲醚(CH3OCH3)是一种无色气体,具有轻微的醚香味,其燃烧热为1455kJ/mol,写出甲醚燃烧的热化学方程式_____ ;已知H2(g)和C(s)的燃烧热分别是285.8kJ•mol﹣1、393.5kJ•mol﹣1;计算反应4C(s)+6H2(g)+O2(g)═2CH3OCH3(g)的反应热△H=______ ;
(2)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
若用标准状况下4.48L CH4还原NO2至N2,整个过程中转移的电子总数为________ (阿伏伽德罗常数用NA表示),放出的热量为________ kJ。
(3)在25 ℃、101 kPa时,1.00 g C6H6(l)燃烧生成CO2(g)和H2O(l),放出41.8 kJ的热量,则表示C6H6燃烧热的热化学方程式为_______________________________________ 。
(2)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
若用标准状况下4.48L CH4还原NO2至N2,整个过程中转移的电子总数为
(3)在25 ℃、101 kPa时,1.00 g C6H6(l)燃烧生成CO2(g)和H2O(l),放出41.8 kJ的热量,则表示C6H6燃烧热的热化学方程式为
您最近一年使用:0次
【推荐2】化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于吸热反应的是___________(填字母)。
(2)获取能量变化的途径
①通过化学键的键能计算。已知:
计算可得: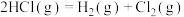 ∆H=
∆H=___________ kJ/mol
②通过盖斯定律可计算。已知在25℃、101kPa时:
I.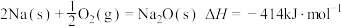
II.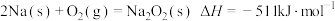
写出Na2O2与Na反应生成Na2O的热化学方程式:___________ 。
(3)以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如下图所示。
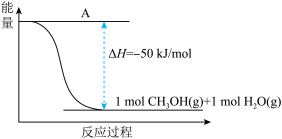
该反应需要加入铜-锌基催化剂。加入催化剂后,该反应的∆H___________ (填“变大”“变小”或“不变”)。
(4)有机物M经过太阳光光照可转化成N,转化过程如下:
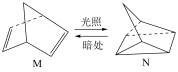
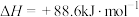
则M、N相比,较稳定的是___________ 。
(1)下列反应中,属于吸热反应的是___________(填字母)。
| A.NaOH与盐酸反应 | B.甲烷的燃烧反应 |
| C.Ba(OH)2∙8H2O与氯化铵反应 | D.锌与盐酸反应 |
(2)获取能量变化的途径
①通过化学键的键能计算。已知:
| 化学键种类 |  |  |  |
| 键能(kJ/mol) | 436 | 247 | 434 |
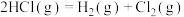 ∆H=
∆H=②通过盖斯定律可计算。已知在25℃、101kPa时:
I.
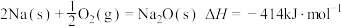
II.
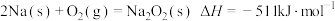
写出Na2O2与Na反应生成Na2O的热化学方程式:
(3)以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如下图所示。

该反应需要加入铜-锌基催化剂。加入催化剂后,该反应的∆H
(4)有机物M经过太阳光光照可转化成N,转化过程如下:

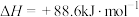
则M、N相比,较稳定的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】请完成下列有关非金属元素及其化合物的问题:
(1)氮及其化合物用途广泛。写出 的电子式:
的电子式:_______ 。
(2)将空气中的氮气转化为氮的化合物的过程称为固氮。下列能实现人工固氮的是_______(填字母)。
(3)肼 又称联氨,是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时负极的电极反应式是
又称联氨,是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时负极的电极反应式是_______ 。
(4)传统制备肼的方法,是以 氧化
氧化 ,制得肼的稀溶液。该反应的离子方程式是
,制得肼的稀溶液。该反应的离子方程式是_______ 。
(5)黑火药是中国古代的四大发明之一,其成分含有硝酸盐等,已知其爆炸反应为: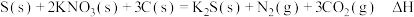
已知①碳的燃烧热为 ,
,
② ,
,
③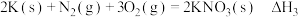 ;
;
则 为
为_______ (用含有 、
、 、
、 的代数式表示)。
的代数式表示)。
(6)铵盐常用作化肥,在实验室中检验 固体中含有
固体中含有 的实验方案为:
的实验方案为:_______ 。
(7)可以用氢氟酸刻蚀玻璃,氢氟酸发生反应的化学方程式是:_______ 。
(1)氮及其化合物用途广泛。写出
 的电子式:
的电子式:(2)将空气中的氮气转化为氮的化合物的过程称为固氮。下列能实现人工固氮的是_______(填字母)。
A. 和 和 在一定条件下反应生成 在一定条件下反应生成 | B.雷雨闪电时空气中的 和 和 化合生成NO 化合生成NO |
C. 经过催化氧化生成NO 经过催化氧化生成NO | D. 和 和 反应生成 反应生成 |
 又称联氨,是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时负极的电极反应式是
又称联氨,是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时负极的电极反应式是(4)传统制备肼的方法,是以
 氧化
氧化 ,制得肼的稀溶液。该反应的离子方程式是
,制得肼的稀溶液。该反应的离子方程式是(5)黑火药是中国古代的四大发明之一,其成分含有硝酸盐等,已知其爆炸反应为:
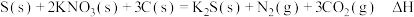
已知①碳的燃烧热为
 ,
,②
 ,
,③
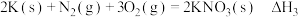 ;
;则
 为
为 、
、 、
、 的代数式表示)。
的代数式表示)。(6)铵盐常用作化肥,在实验室中检验
 固体中含有
固体中含有 的实验方案为:
的实验方案为:(7)可以用氢氟酸刻蚀玻璃,氢氟酸发生反应的化学方程式是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】热化学方程式中的ΔH实际上是热力学中的一个物理量,叫做焓变,其数值和符号与反应物和生成物的总能量有关,也与反应物和生成物的键能有关。
(1)已知反应CH3—CH3(g) → CH2=CH2(g)+H2(g),有关化学键键能如下。
试计算该反应的反应热___________________________
(2)已知H2(g)+Br2(l)=2HBr(g);ΔH=-72 kJ/mol。蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其它相关数据如下表:
则表中a为__________
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行理论推算。试依据下列热化学方程式,计算反应
2C(s)+2H2(g)+O2(g)=CH3COOH(l)的焓变ΔH=________ 。
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=-870.3 kJ·mol-1
②C(s)+O2(g)=CO2(g) ΔH2=-393.5 kJ·mol-1
③H2(g)+1/2O2(g)=H2O(l) ΔH3=-285.8 kJ·mol-1
(4)如下图Ⅰ所示表示的是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:___________________________________________________________________ 。
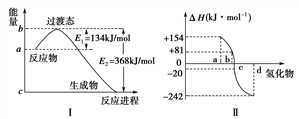
(5)图Ⅱ表示氧族元素中的氧、硫、硒(Se)、碲(Te)在生成氢化物时的焓变数据,根据焓变数据可确定a、b、c、d分别代表哪种元素,试写出硒化氢发生分解反应的热化学方程式:_____________________ 。
(6)已知:
①Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g);ΔH=-25 kJ·mol-1,
②3Fe2O3(s)+CO(g)===2Fe3O4(s)+CO2(g);ΔH=-47 kJ·mol-1,
③Fe3O4(s)+CO(g)===3FeO(s)+CO2(g);ΔH=+19 kJ·mol-1
请写出CO还原FeO的热化学方程式:__________________________ 。
(7) 火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。热化学方程式为:N2H4(l) + 2H2O2(l) == N2(g) + 4 H2O(g) △ H=-644.25 kJ/mol。又已知H2O (l) == H2O (g) ΔH=+ 44 kJ/mol。则64g液态肼
与液态双氧水反应生成液态水时放出的热量是_________________ kJ。
(8)焙烧产生的SO2可用于制硫酸。已知25 ℃、101 kPa时:
2SO2(g)+O2(g) 2SO3(g) ΔH1=-197 kJ·mol-1;
2SO3(g) ΔH1=-197 kJ·mol-1;
H2O(g)===H2O(l) ΔH2=-44 kJ·mol-1;
2SO2(g)+O2(g)+2H2O(g)===2H2SO4(l) ΔH3=-545 kJ·mol-1。
则SO3(g)与H2O(l)反应的热化学方程式是___________________ 。
(1)已知反应CH3—CH3(g) → CH2=CH2(g)+H2(g),有关化学键键能如下。
| 化学键 | C—H | C=C | C—C | H—H |
| 键能/kJ·mol-1 | 414.4 | 615.3 | 347.4 | 435.3 |
试计算该反应的反应热
(2)已知H2(g)+Br2(l)=2HBr(g);ΔH=-72 kJ/mol。蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其它相关数据如下表:
H2(g) | Br2(g) | HBr(g) | |
1 mol分子中的化学键断裂时需要吸收的能量(kJ) | 436 | a | 369 |
则表中a为
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行理论推算。试依据下列热化学方程式,计算反应
2C(s)+2H2(g)+O2(g)=CH3COOH(l)的焓变ΔH=
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=-870.3 kJ·mol-1
②C(s)+O2(g)=CO2(g) ΔH2=-393.5 kJ·mol-1
③H2(g)+1/2O2(g)=H2O(l) ΔH3=-285.8 kJ·mol-1
(4)如下图Ⅰ所示表示的是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:

(5)图Ⅱ表示氧族元素中的氧、硫、硒(Se)、碲(Te)在生成氢化物时的焓变数据,根据焓变数据可确定a、b、c、d分别代表哪种元素,试写出硒化氢发生分解反应的热化学方程式:
(6)已知:
①Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g);ΔH=-25 kJ·mol-1,
②3Fe2O3(s)+CO(g)===2Fe3O4(s)+CO2(g);ΔH=-47 kJ·mol-1,
③Fe3O4(s)+CO(g)===3FeO(s)+CO2(g);ΔH=+19 kJ·mol-1
请写出CO还原FeO的热化学方程式:
(7) 火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。热化学方程式为:N2H4(l) + 2H2O2(l) == N2(g) + 4 H2O(g) △ H=-644.25 kJ/mol。又已知H2O (l) == H2O (g) ΔH=+ 44 kJ/mol。则64g液态肼
与液态双氧水反应生成液态水时放出的热量是
(8)焙烧产生的SO2可用于制硫酸。已知25 ℃、101 kPa时:
2SO2(g)+O2(g)
 2SO3(g) ΔH1=-197 kJ·mol-1;
2SO3(g) ΔH1=-197 kJ·mol-1; H2O(g)===H2O(l) ΔH2=-44 kJ·mol-1;
2SO2(g)+O2(g)+2H2O(g)===2H2SO4(l) ΔH3=-545 kJ·mol-1。
则SO3(g)与H2O(l)反应的热化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】热值是指一定条件下单位质量的物质完全燃烧所放出的热量。已知H2(g)、CO(g)和CH3OH(l)的热值分别为143 kJ· g-1、10 kJ·g-1和23 kJ·g-1。请回答下列问题:
(1)写出CO燃烧反应的热化学方程式为_______ 。
(2)表示甲醇燃烧热的热化学方程式为_______ 。
(3)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为_______ 。
(1)写出CO燃烧反应的热化学方程式为
(2)表示甲醇燃烧热的热化学方程式为
(3)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】城市使用的燃料,现大多用煤气、液化石油气。煤气的主要成分是一氧化碳和氢气的混合气,它由煤炭与水(蒸气)反应制得,故又称水煤气。
(1)试写出制取水煤气的主要化学方程式___________________ 。
(2)液化石油气的主要成分是丙烷,丙烷燃烧的热化学方程式为:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-2 220.0 kJ•mol−1。已知CO气体燃烧的热化学方程式为:CO(g)+1/2O2(g)=CO2(g) ΔH=-283.0 kJ•mol−1。试比较相同物质的量的C3H8和CO燃烧,产生的热量比值约为_________ 。
(3)已知氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ•mol−1。试比较同质量的氢气和丙烷燃烧,产生的热量比值约为______ 。
(4)氢气是未来的能源,除产生的热量大之外,还具有的优点是___________________ 。
(1)试写出制取水煤气的主要化学方程式
(2)液化石油气的主要成分是丙烷,丙烷燃烧的热化学方程式为:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-2 220.0 kJ•mol−1。已知CO气体燃烧的热化学方程式为:CO(g)+1/2O2(g)=CO2(g) ΔH=-283.0 kJ•mol−1。试比较相同物质的量的C3H8和CO燃烧,产生的热量比值约为
(3)已知氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ•mol−1。试比较同质量的氢气和丙烷燃烧,产生的热量比值约为
(4)氢气是未来的能源,除产生的热量大之外,还具有的优点是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】完成下列问题
(1)已知CH3OH(l)的摩尔燃烧焓ΔH=-726.5 kJ·mol-1,CH3OH(l)+ O2(g)=CO2(g)+2H2(g) ΔH=-a kJ·mol-1,则a
O2(g)=CO2(g)+2H2(g) ΔH=-a kJ·mol-1,则a___________ (填“>”“<”或“=”)726.5。
(2)将Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145.0 kJ热量,写出该反应的热化学方程式:___________ 。
(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料:4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) ΔH=-1 176.0 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为___________ 。
(4)CO2与H2在某催化剂的作用下反应如图所示:
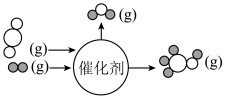
写出该反应的热化学方程式:___________ 。
(5)CO2催化加氢制CH3OH的一种反应历程如图所示(吸附在催化剂表面的物质用*标注,如CO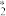 表示CO2吸附在催化剂表面)。
表示CO2吸附在催化剂表面)。
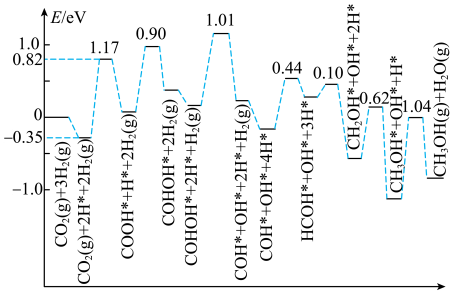
该反应历程中决速步反应的化学方程式为___________ 。
(1)已知CH3OH(l)的摩尔燃烧焓ΔH=-726.5 kJ·mol-1,CH3OH(l)+
 O2(g)=CO2(g)+2H2(g) ΔH=-a kJ·mol-1,则a
O2(g)=CO2(g)+2H2(g) ΔH=-a kJ·mol-1,则a(2)将Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145.0 kJ热量,写出该反应的热化学方程式:
(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料:4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) ΔH=-1 176.0 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为
(4)CO2与H2在某催化剂的作用下反应如图所示:

| 化学键 |  |  | 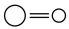 |  | 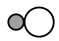 |
| 键能/(kJ·mol-1) | 436 | 326 | 803 | 464 | 414 |
(5)CO2催化加氢制CH3OH的一种反应历程如图所示(吸附在催化剂表面的物质用*标注,如CO
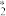 表示CO2吸附在催化剂表面)。
表示CO2吸附在催化剂表面)。
该反应历程中决速步反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】碳是形成化合物种类最多的元素,其单质及其化合物是人类生产生活的主要能源物质。已知: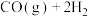
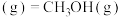
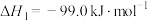 。
。
(1)该反应的熵变
_______ 0(填“>”“<”“=”),该反应自发进行的条件是_______ (填“低温”“高温”或“任意温度”)。
(2)反应
 ,则
,则
_______  (填“>”“<”“=”)。
(填“>”“<”“=”)。
(3)已知1g液态甲醇完全燃烧放出的热量为22.7kJ(298K、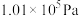 时测定)。写出该条件下表示甲醇燃烧热的热化学方程式
时测定)。写出该条件下表示甲醇燃烧热的热化学方程式_______ 。
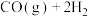
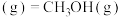
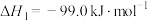 。
。(1)该反应的熵变

(2)反应

 ,则
,则
 (填“>”“<”“=”)。
(填“>”“<”“=”)。(3)已知1g液态甲醇完全燃烧放出的热量为22.7kJ(298K、
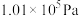 时测定)。写出该条件下表示甲醇燃烧热的热化学方程式
时测定)。写出该条件下表示甲醇燃烧热的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】中和热是一类重要的反应热,也是化学研究的重要课题。已知强酸稀溶液与强碱稀溶液发生反应生成1 mol H2O(l)的焓变为:ΔH1=-57.3 kJ/mol。
(1)下列各组试剂混合发生反应的离子方程式为H++OH-=H2O的是_______ (填字母)。
A.稀硫酸与氢氧化钡溶液
B.盐酸与氢氧化钠溶液
C.浓硫酸与氢氧化钠固体
D.硫酸氢钠溶液与氢氧化钾溶液
E.氢氧化镁溶于稀盐酸
(2)若稀硫酸与氢氧化钡稀溶液反应生成1 mol H2O(l),则反应放出的热量_______ (填“大于”“等于”或“小于”)57.3 kJ,原因是_______ (从化学键的角度简单解释即可)。
(3)若稀硫酸与氢氧化钠固体反应生成1 mol H2O(l),则反应放出的热量_______ (填“大于”“等于”或“小于”)57.3 kJ,原因是_______ 。
(4)醋酸(CH3COOH)是一种常见弱酸,醋酸与氢氧化钠稀溶液反应生成1 mol H2O(l) 的焓变为: ΔH2=a kJ/mol,则ΔH1和ΔH2的大小关系为ΔH1_______ ΔH2(填“>”“=”或“<”)。
(1)下列各组试剂混合发生反应的离子方程式为H++OH-=H2O的是
A.稀硫酸与氢氧化钡溶液
B.盐酸与氢氧化钠溶液
C.浓硫酸与氢氧化钠固体
D.硫酸氢钠溶液与氢氧化钾溶液
E.氢氧化镁溶于稀盐酸
(2)若稀硫酸与氢氧化钡稀溶液反应生成1 mol H2O(l),则反应放出的热量
(3)若稀硫酸与氢氧化钠固体反应生成1 mol H2O(l),则反应放出的热量
(4)醋酸(CH3COOH)是一种常见弱酸,醋酸与氢氧化钠稀溶液反应生成1 mol H2O(l) 的焓变为: ΔH2=a kJ/mol,则ΔH1和ΔH2的大小关系为ΔH1
您最近一年使用:0次



