请完成下列有关非金属元素及其化合物的问题:
(1)氮及其化合物用途广泛。写出 的电子式:
的电子式:_______ 。
(2)将空气中的氮气转化为氮的化合物的过程称为固氮。下列能实现人工固氮的是_______(填字母)。
(3)肼 又称联氨,是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时负极的电极反应式是
又称联氨,是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时负极的电极反应式是_______ 。
(4)传统制备肼的方法,是以 氧化
氧化 ,制得肼的稀溶液。该反应的离子方程式是
,制得肼的稀溶液。该反应的离子方程式是_______ 。
(5)黑火药是中国古代的四大发明之一,其成分含有硝酸盐等,已知其爆炸反应为: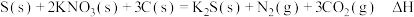
已知①碳的燃烧热为 ,
,
② ,
,
③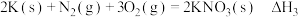 ;
;
则 为
为_______ (用含有 、
、 、
、 的代数式表示)。
的代数式表示)。
(6)铵盐常用作化肥,在实验室中检验 固体中含有
固体中含有 的实验方案为:
的实验方案为:_______ 。
(7)可以用氢氟酸刻蚀玻璃,氢氟酸发生反应的化学方程式是:_______ 。
(1)氮及其化合物用途广泛。写出
 的电子式:
的电子式:(2)将空气中的氮气转化为氮的化合物的过程称为固氮。下列能实现人工固氮的是_______(填字母)。
A. 和 和 在一定条件下反应生成 在一定条件下反应生成 | B.雷雨闪电时空气中的 和 和 化合生成NO 化合生成NO |
C. 经过催化氧化生成NO 经过催化氧化生成NO | D. 和 和 反应生成 反应生成 |
 又称联氨,是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时负极的电极反应式是
又称联氨,是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时负极的电极反应式是(4)传统制备肼的方法,是以
 氧化
氧化 ,制得肼的稀溶液。该反应的离子方程式是
,制得肼的稀溶液。该反应的离子方程式是(5)黑火药是中国古代的四大发明之一,其成分含有硝酸盐等,已知其爆炸反应为:
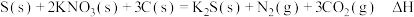
已知①碳的燃烧热为
 ,
,②
 ,
,③
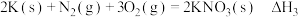 ;
;则
 为
为 、
、 、
、 的代数式表示)。
的代数式表示)。(6)铵盐常用作化肥,在实验室中检验
 固体中含有
固体中含有 的实验方案为:
的实验方案为:(7)可以用氢氟酸刻蚀玻璃,氢氟酸发生反应的化学方程式是:
更新时间:2023-06-26 19:08:07
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】已知:2Fe3++2I-= 2Fe2++I2,现有一种澄清透明的溶液中可能含有下列离子:K+、Fe3+、Ba2+、Al3+、NH4+、Cl-、I-、NO3-、HCO3-、SO32-、SO42-现做以下实验:
(1)将溶液滴在蓝色石蕊试纸上,试纸呈红色
(2)取少量溶液,加入用稀硝酸酸化的BaCl2溶液,产生白色沉淀
(3)将(2)中的沉淀过滤。由滤液中加入硝酸银溶液,产生白色沉淀
(4)另取溶液,逐滴加入氢氧化钠溶液至过量,只观察到有红棕色沉淀生成,且沉淀量不减少。由此可以推断:
溶液中肯定存在的离子有:_________________________________ 。
溶液中肯定不存在的离子有:________________________________ 。
溶液中还不能确定是否存在的离子有:___________________ 。
(1)将溶液滴在蓝色石蕊试纸上,试纸呈红色
(2)取少量溶液,加入用稀硝酸酸化的BaCl2溶液,产生白色沉淀
(3)将(2)中的沉淀过滤。由滤液中加入硝酸银溶液,产生白色沉淀
(4)另取溶液,逐滴加入氢氧化钠溶液至过量,只观察到有红棕色沉淀生成,且沉淀量不减少。由此可以推断:
溶液中肯定存在的离子有:
溶液中肯定不存在的离子有:
溶液中还不能确定是否存在的离子有:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分,用化学用语回答下列问题:
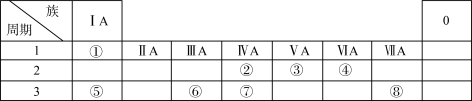
(1)化合物A是由⑤⑧两种元素构成的,用电子式表示其形成过程___________
(2)④、②元素形成的化合物的结构式__________
(3)②的最简单氢化物与氧气可以设计成燃料电池,写出在碱性条件下负极的电极方程式_____
(4)⑥的单质与⑤的最高价氧化物对应水化物的水溶液反应的离子方程式为:___________
(5)由①③⑧组成的M 物质中所含化学键的类型_________________
(6)M中的阳离子的鉴定方法是_______

(1)化合物A是由⑤⑧两种元素构成的,用电子式表示其形成过程
(2)④、②元素形成的化合物的结构式
(3)②的最简单氢化物与氧气可以设计成燃料电池,写出在碱性条件下负极的电极方程式
(4)⑥的单质与⑤的最高价氧化物对应水化物的水溶液反应的离子方程式为:
(5)由①③⑧组成的M 物质中所含化学键的类型
(6)M中的阳离子的鉴定方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】大气污染物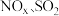 的脱除和利用可以保护大气环境。含氮废水中氨氮(以
的脱除和利用可以保护大气环境。含氮废水中氨氮(以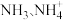 存在)和硝态氮(以
存在)和硝态氮(以 存在)会引起水体富营养化,需经处理后才能排放。
存在)会引起水体富营养化,需经处理后才能排放。
(1)空气中的 可在催化剂作用下被
可在催化剂作用下被 还原生成
还原生成 ,该反应的化学方程式是
,该反应的化学方程式是___________ 。
(2)工业上常在燃煤过程中加入 浆状物脱除
浆状物脱除 ,脱硫的产品
,脱硫的产品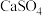 用于制造石膏,该脱硫反应的总化学方程式是
用于制造石膏,该脱硫反应的总化学方程式是___________ 。
(3)可以用天然海水吸收含硫烟气中 。根据如图所示的实验结果,为了提高一定浓度含硫烟气中
。根据如图所示的实验结果,为了提高一定浓度含硫烟气中 的吸收效率,下列措施正确的是
的吸收效率,下列措施正确的是___________ (填字母)。
B.减小通入含硫烟气的流速
C.减少天然海水的进入量
(4)利用微生物可对含氮废水进行处理,流程如图:___________ 。
②检验含氮废水中氨氮 是否除尽的实验操作是
是否除尽的实验操作是___________ 。
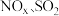 的脱除和利用可以保护大气环境。含氮废水中氨氮(以
的脱除和利用可以保护大气环境。含氮废水中氨氮(以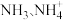 存在)和硝态氮(以
存在)和硝态氮(以 存在)会引起水体富营养化,需经处理后才能排放。
存在)会引起水体富营养化,需经处理后才能排放。(1)空气中的
 可在催化剂作用下被
可在催化剂作用下被 还原生成
还原生成 ,该反应的化学方程式是
,该反应的化学方程式是(2)工业上常在燃煤过程中加入
 浆状物脱除
浆状物脱除 ,脱硫的产品
,脱硫的产品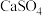 用于制造石膏,该脱硫反应的总化学方程式是
用于制造石膏,该脱硫反应的总化学方程式是(3)可以用天然海水吸收含硫烟气中
 。根据如图所示的实验结果,为了提高一定浓度含硫烟气中
。根据如图所示的实验结果,为了提高一定浓度含硫烟气中 的吸收效率,下列措施正确的是
的吸收效率,下列措施正确的是
B.减小通入含硫烟气的流速
C.减少天然海水的进入量
(4)利用微生物可对含氮废水进行处理,流程如图:
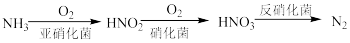
②检验含氮废水中氨氮
 是否除尽的实验操作是
是否除尽的实验操作是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】我国首创以铝组成的金属—海水—空气电池作为新型海水标志灯的能源,它以海水为电解质溶液,靠空气中的氧气使铝组成的金属不断氧化而产生电流。
(1)只要把灯放入海水中数分钟,就会发出耀眼的白光,则该电池的负极反应式为__________ ;
(2)电解法可制取碳的一种气态氢化物C2H4(如图所示)电极a接电源的__________ 极,该电极反应式为__________ ;
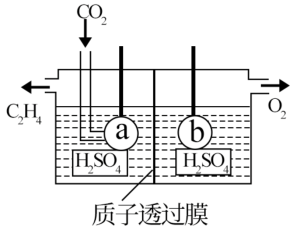
(3)将SO2气体通入BaCl2和HNO3的混合溶液中,生成白色沉淀和无色气体NO,有关反应的离子方程式为__________ ;
(4)处理NOx的一种方法是利用甲烷催化还原NOx,
已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)ΔH=-574kJ•mol-1;
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)ΔH=-1160kJ•mol-1
则甲烷直接将NO2还原为N2的热化学方程式为__________ ;
(5)H2O2在工业、农业、医药上都有广泛的用途。用碱性氢氧燃料电池可合成H2O2,具有效率高、无污染等特点。电池总反应式为H2+O2+OH-=H2O+ ,写出正极反应式
,写出正极反应式__________ 。
(1)只要把灯放入海水中数分钟,就会发出耀眼的白光,则该电池的负极反应式为
(2)电解法可制取碳的一种气态氢化物C2H4(如图所示)电极a接电源的

(3)将SO2气体通入BaCl2和HNO3的混合溶液中,生成白色沉淀和无色气体NO,有关反应的离子方程式为
(4)处理NOx的一种方法是利用甲烷催化还原NOx,
已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)ΔH=-574kJ•mol-1;
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)ΔH=-1160kJ•mol-1
则甲烷直接将NO2还原为N2的热化学方程式为
(5)H2O2在工业、农业、医药上都有广泛的用途。用碱性氢氧燃料电池可合成H2O2,具有效率高、无污染等特点。电池总反应式为H2+O2+OH-=H2O+
 ,写出正极反应式
,写出正极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.氧、硫、硒、碲均位于元素周期表的VIA族,其化合物在化工生产中有广泛应用。
(1)下列性质的递变顺序不正确 的是_____ (填字母)。
A.酸性:H2SeO4 > H2SeO3 B.非金属性:O > S > Se > Te
C.还原性:H2Te > H2Se > H2S > H2O D.热稳定性:H2O > H2Te > H2Se > H2S
E.沸点:H2Te > H2Se > H2S > H2O
(2)在常温下进行的置换反应X+W→Y+V中, H2O可以扮演不同的“角色”。已知X、Y是短周期主族元素形成的单质,W、V是化合物。
①若W是水,且作还原剂,反应的化学方程式为_____________________________________ 。
②若V是水,为还原产物,反应的化学方程式为_____________________________________ 。
(3)已知:液态CS2完全燃烧生成CO2、SO2气体,每转移3mol电子时放出269.2kJ热量。写出表示CS2(1)的燃烧热的热化学方程式:________________________________________ 。
(4)工业上,用S02还原TeC14溶液制备碲(Te),反应中氧化产物与还原产物的物质的量之比为____________ 。
Ⅱ.硫和氮的氧化物直接排放会引发严重的环境问题,请回答下列问题:
(1)下列环境问题主要由硫氧化物和氮氧化物的排放引发的是__________________ 。
A.全球变暖 B.酸雨 C.水体富营养化(水华) D.白色污染
(2)SO2的排放主要来自于煤的燃烧。常用石灰石脱硫,其产物可以做建筑材料。
已知:CaCO3(s)==CO2(g)+CaO(s) △H=+178.2 kJ·mol-1
SO2(g)+CaO(s)==CaSO3(s) △H=-402 kJ·mol-1
2CaSO3(s)+O2(g )==2CaSO4(s) △H=-234.2 kJ·mol-1
写出石灰石脱硫的热化学反应方程式_______________________________________ 。
(1)下列性质的递变顺序
A.酸性:H2SeO4 > H2SeO3 B.非金属性:O > S > Se > Te
C.还原性:H2Te > H2Se > H2S > H2O D.热稳定性:H2O > H2Te > H2Se > H2S
E.沸点:H2Te > H2Se > H2S > H2O
(2)在常温下进行的置换反应X+W→Y+V中, H2O可以扮演不同的“角色”。已知X、Y是短周期主族元素形成的单质,W、V是化合物。
①若W是水,且作还原剂,反应的化学方程式为
②若V是水,为还原产物,反应的化学方程式为
(3)已知:液态CS2完全燃烧生成CO2、SO2气体,每转移3mol电子时放出269.2kJ热量。写出表示CS2(1)的燃烧热的热化学方程式:
(4)工业上,用S02还原TeC14溶液制备碲(Te),反应中氧化产物与还原产物的物质的量之比为
Ⅱ.硫和氮的氧化物直接排放会引发严重的环境问题,请回答下列问题:
(1)下列环境问题主要由硫氧化物和氮氧化物的排放引发的是
A.全球变暖 B.酸雨 C.水体富营养化(水华) D.白色污染
(2)SO2的排放主要来自于煤的燃烧。常用石灰石脱硫,其产物可以做建筑材料。
已知:CaCO3(s)==CO2(g)+CaO(s) △H=+178.2 kJ·mol-1
SO2(g)+CaO(s)==CaSO3(s) △H=-402 kJ·mol-1
2CaSO3(s)+O2(g )==2CaSO4(s) △H=-234.2 kJ·mol-1
写出石灰石脱硫的热化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】工业制氢气的一个重要反应是:CO(s)+ H2O(g) ="=" CO2(g) + H2(g)
已知25℃时:C(石墨) +O2 (g) = CO2(g) △H1 =-394 kJ·mol-1
C(石墨) +1/2O2 (g) = CO (g) △H2 =-111 kJ·mol-1
H2(g) +1/2O2 (g)= H2O(g) △H3=-242kJ·mol-1
试计算25℃时CO(s)+ H2O(g) = CO2(g) + H2(g)的反应热_______ kJ·mol-1
已知25℃时:C(石墨) +O2 (g) = CO2(g) △H1 =-394 kJ·mol-1
C(石墨) +1/2O2 (g) = CO (g) △H2 =-111 kJ·mol-1
H2(g) +1/2O2 (g)= H2O(g) △H3=-242kJ·mol-1
试计算25℃时CO(s)+ H2O(g) = CO2(g) + H2(g)的反应热
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
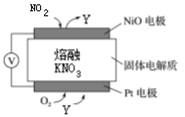
【推荐1】(1)通过NOx传感器可监测NOx的含量,其工作原理示意图如下图。回答下列问题:
①Pt电极上还需通入的气体是________ 。
②写出NiO电极的电极反应式:_____________________________________________ 。
(2)盐桥电池是一种比较普遍的原电池,该电池反应原理如下图所示。
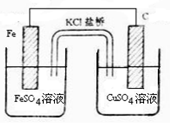
①负极电极反应式为________ 。
②当电路中通过电子为0.1mol时,两电极质量差为___ g,此时原电池电解质溶液的总质量与开始时电解质溶液总质量差值为___ g(不考虑溶液离子向盐桥移动)。
①Pt电极上还需通入的气体是
②写出NiO电极的电极反应式:

(2)盐桥电池是一种比较普遍的原电池,该电池反应原理如下图所示。

①负极电极反应式为
②当电路中通过电子为0.1mol时,两电极质量差为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】研究金属的腐蚀过程及防腐蚀对人们的日常生活有重大意义。
(1)如图中的铁棒若为纯铁,则其腐蚀过程属于_______ 腐蚀(选填“化学”或“电化学”)。
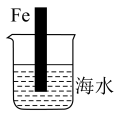
(2)若铁棒的含碳量为10.8%,浸入一段时间之后发现,越靠近烧杯底部发生电化学腐蚀就越轻微,该实验说明_______ 因素会影响铁的腐蚀速率;腐蚀时,正极的电极反应式为_______ 。(已知:海水pH约为8.1)
(1)如图中的铁棒若为纯铁,则其腐蚀过程属于

(2)若铁棒的含碳量为10.8%,浸入一段时间之后发现,越靠近烧杯底部发生电化学腐蚀就越轻微,该实验说明
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】电能是现代社会应用最广泛的能源之一
(1)某原电池装置如图所示:
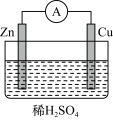
①其中,Zn电极为原电池的____ 极,电极反应式是_________
②Cu电极上发生的反应属于____ (填“氧化”或“还原”)反应,当铜表面析出4.48 L氢气(标准状况)时,导线中通过了___ mol电子。
③电子从___ 极流出(填Zn或者Cu,下同),阳离子移向___ 极。
(2)依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示:请回答下列问题:

①电极X的材料是______ ; 正极上发生的电极反应式为 ______________
②当导线中通过了0.1mol电子时,银棒增重____ g
(1)某原电池装置如图所示:

①其中,Zn电极为原电池的
②Cu电极上发生的反应属于
③电子从
(2)依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示:请回答下列问题:

①电极X的材料是
②当导线中通过了0.1mol电子时,银棒增重
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】化学与生产、生活息息相关。请回答以下问题。
(1)小苏打可用于治疗胃酸过多,写出该反应的离子方程式_______ 。
(2)合成氨工业化,对人类影响深远。工业上合成氨的化学方程式为_______ 。
(3)沾有水的铁锅在高温火焰上灼烧会发黑,该反应的化学方程式为_______ 。
(4)用碘水、淀粉等试剂检测葡萄酒中 的含量,写出相应的离子方程式
的含量,写出相应的离子方程式_______ 。
(5)洁厕剂的主要成分为盐酸。欲配制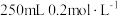 的盐酸,需要HCl的物质的量为
的盐酸,需要HCl的物质的量为_______ 。
(1)小苏打可用于治疗胃酸过多,写出该反应的离子方程式
(2)合成氨工业化,对人类影响深远。工业上合成氨的化学方程式为
(3)沾有水的铁锅在高温火焰上灼烧会发黑,该反应的化学方程式为
(4)用碘水、淀粉等试剂检测葡萄酒中
 的含量,写出相应的离子方程式
的含量,写出相应的离子方程式(5)洁厕剂的主要成分为盐酸。欲配制
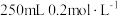 的盐酸,需要HCl的物质的量为
的盐酸,需要HCl的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】写出下列反应的化学方程式,是离子反应的写离子方程式
(1)工业上制备氨气反应的化学方程式___________
(2)铜和浓硫酸发生反应的化学方程式___________
(3)氨气催化氧化生成一氧化氮的化学方程式___________
(4)工业上制备漂白液发生反应的离子方程式___________
(5)将亚硫酸钠溶液滴入酸性高锰酸钾溶液中发生反应的离子方程式___________
(1)工业上制备氨气反应的化学方程式
(2)铜和浓硫酸发生反应的化学方程式
(3)氨气催化氧化生成一氧化氮的化学方程式
(4)工业上制备漂白液发生反应的离子方程式
(5)将亚硫酸钠溶液滴入酸性高锰酸钾溶液中发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氮肥的使用极大提高了粮食作物的产量,对解决世界粮食危机起到了不可或缺的作用,下面是几种通过氮的固定制备氮肥的方法。
(1)自然固氮:一种途径是通过雷电将空气中少量的氮气转化为含氮化合物(氮肥),主要转化途径如下(转化所需试剂及条件已略去):
 硝酸盐[如
硝酸盐[如 ]
]
①写出在空气中 转化为NO的化学方程式
转化为NO的化学方程式_______ 。
②将 转化为
转化为 ,列举两种不同类别的化合物M
,列举两种不同类别的化合物M_______ (写化学式)。
③若M是Cu单质,与稀硝酸反应也能生成硝酸盐,写出铜粉与稀硝酸反应的离子方程式_______ 。
(2)人工固氮:
①工业上以氮气和氢气为原料,在高温、高压和催化剂的条件下合成氨。该反应的化学方程式为_______ 。
②利用氨气与氧气在催化剂作用下生成NO,是工业制备硝酸的重要环节,该反应中NO是_______ (填“氧化产物”“还原产物”或“氧化产物和还原产物”)。
③利用氨气与二氧化碳在催化剂作用下合成重要氮肥尿素 ,尿素中N元素的化合价是
,尿素中N元素的化合价是_______ 。合成尿素的化学方程式_______ 。尿素在土壤中与水结合生成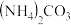 ,被植物吸收,有利于作物的生长。
,被植物吸收,有利于作物的生长。
(3)在微生物作用下实现 的转化,称为硝化过程。在一定条件下,
的转化,称为硝化过程。在一定条件下, 被
被 氧化成
氧化成 ,参加反应的
,参加反应的 和
和 的物质的量之比为
的物质的量之比为_______ 。由于 有毒,因此过量使用氮肥也会引起农作物大量减产,所以一定要合理科学使用。
有毒,因此过量使用氮肥也会引起农作物大量减产,所以一定要合理科学使用。
(4)有同学猜测,在 被细菌分解过程中,
被细菌分解过程中, 最终分解为
最终分解为 ,同时有
,同时有 生成。从化合价变化的角度分析有
生成。从化合价变化的角度分析有 生成的合理性
生成的合理性_______ 。
(1)自然固氮:一种途径是通过雷电将空气中少量的氮气转化为含氮化合物(氮肥),主要转化途径如下(转化所需试剂及条件已略去):
 硝酸盐[如
硝酸盐[如 ]
]①写出在空气中
 转化为NO的化学方程式
转化为NO的化学方程式②将
 转化为
转化为 ,列举两种不同类别的化合物M
,列举两种不同类别的化合物M③若M是Cu单质,与稀硝酸反应也能生成硝酸盐,写出铜粉与稀硝酸反应的离子方程式
(2)人工固氮:
①工业上以氮气和氢气为原料,在高温、高压和催化剂的条件下合成氨。该反应的化学方程式为
②利用氨气与氧气在催化剂作用下生成NO,是工业制备硝酸的重要环节,该反应中NO是
③利用氨气与二氧化碳在催化剂作用下合成重要氮肥尿素
 ,尿素中N元素的化合价是
,尿素中N元素的化合价是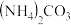 ,被植物吸收,有利于作物的生长。
,被植物吸收,有利于作物的生长。(3)在微生物作用下实现
 的转化,称为硝化过程。在一定条件下,
的转化,称为硝化过程。在一定条件下, 被
被 氧化成
氧化成 ,参加反应的
,参加反应的 和
和 的物质的量之比为
的物质的量之比为 有毒,因此过量使用氮肥也会引起农作物大量减产,所以一定要合理科学使用。
有毒,因此过量使用氮肥也会引起农作物大量减产,所以一定要合理科学使用。(4)有同学猜测,在
 被细菌分解过程中,
被细菌分解过程中, 最终分解为
最终分解为 ,同时有
,同时有 生成。从化合价变化的角度分析有
生成。从化合价变化的角度分析有 生成的合理性
生成的合理性
您最近一年使用:0次



