下表为元素周期表的一部分,用化学用语回答下列问题:
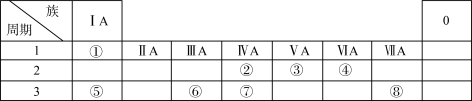
(1)化合物A是由⑤⑧两种元素构成的,用电子式表示其形成过程___________
(2)④、②元素形成的化合物的结构式__________
(3)②的最简单氢化物与氧气可以设计成燃料电池,写出在碱性条件下负极的电极方程式_____
(4)⑥的单质与⑤的最高价氧化物对应水化物的水溶液反应的离子方程式为:___________
(5)由①③⑧组成的M 物质中所含化学键的类型_________________
(6)M中的阳离子的鉴定方法是_______

(1)化合物A是由⑤⑧两种元素构成的,用电子式表示其形成过程
(2)④、②元素形成的化合物的结构式
(3)②的最简单氢化物与氧气可以设计成燃料电池,写出在碱性条件下负极的电极方程式
(4)⑥的单质与⑤的最高价氧化物对应水化物的水溶液反应的离子方程式为:
(5)由①③⑧组成的M 物质中所含化学键的类型
(6)M中的阳离子的鉴定方法是
更新时间:2019-05-31 09:22:42
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如下图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体体积在同温同压下测定)。试回答问题:
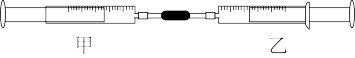
(1)实验1中发生反应的离子方程式为:___________ 。
(2)实验2反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入___________ 溶液中。
(3)实验3中能看见有白烟产生并生成一种气体(空气主要成分之一),该化学反应方程式___________ ,写出检验所得白色固体中阳离子的操作方法:___________ ,充分反应后甲针筒内剩余气体成分为___________ (填化学式)。

| 实验序号 | 甲针筒内物质 | 乙针筒内物质 |
| 1 | 溴水 | SO2 |
| 2 | H2S | SO2 |
| 3 | 15mLCl2 | 35mLNH3 |
(2)实验2反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入
(3)实验3中能看见有白烟产生并生成一种气体(空气主要成分之一),该化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氮元素及其化合物的转化关系如图所示:
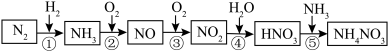
(1)反应①②③④⑤中不属于氧化还原反应的是___________ 。
(2)已知1mol氨气发生反应②,完全反应生成NO和水蒸气时放出226 kJ的热,该反应的热化学方程式是___________ 。
(3)汽车尾气净化装置中,气体在催化剂表面吸附与解吸作用的过程如图所示。

①该过程的中间产物是___________ 。
②催化转化过程中,理论上每生成1mol 时,转移的电子为
时,转移的电子为___________ mol。
(4)实验室中,浓硝酸需用棕色试剂瓶盛放,并置于冷暗处的原因是___________ 。
(5) 是农业生产中常用的一种氮肥。
是农业生产中常用的一种氮肥。
① 中氮元素的质量分数是
中氮元素的质量分数是___________ 。
②实验室中检验某种化肥是铵态氮肥的方法是___________ 。(写出操作步骤、现象和结论)

(1)反应①②③④⑤中不属于氧化还原反应的是
(2)已知1mol氨气发生反应②,完全反应生成NO和水蒸气时放出226 kJ的热,该反应的热化学方程式是
(3)汽车尾气净化装置中,气体在催化剂表面吸附与解吸作用的过程如图所示。

①该过程的中间产物是
②催化转化过程中,理论上每生成1mol
 时,转移的电子为
时,转移的电子为(4)实验室中,浓硝酸需用棕色试剂瓶盛放,并置于冷暗处的原因是
(5)
 是农业生产中常用的一种氮肥。
是农业生产中常用的一种氮肥。①
 中氮元素的质量分数是
中氮元素的质量分数是②实验室中检验某种化肥是铵态氮肥的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】细菌可以促使铁、氮两种元素进行化还原反应,并耦合两种元素的循环。

(1)氮循环中,属于氮的固定的有_______ (填字母序号,下同),属于氧化反应的有_______ 。
a. 转化为氨态氮 b.硝化过程 c.反硝化过程
转化为氨态氮 b.硝化过程 c.反硝化过程
(2)氮肥是水体中铵根的主要来源之一,铵根的电子式为_______ ,检验某固态氮肥中铵根的实验操作与相应的现象及结论为_______ 。
(3)铵态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移电子的物质的量为_______ 。
(4)土壤中的铁循环可用于水体脱氮(指将氮元素从水体中除去),用离子方程式说明利用土壤中的铁循环脱除水体中铵态氮的原理_______ 。
(5)实验室中也可以实现不同价态氮元素之间的转变,请写出符合以下要求的化学方程式:
① 转化为
转化为 :
:_______
②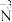 转化为
转化为 :
:_______

(1)氮循环中,属于氮的固定的有
a.
 转化为氨态氮 b.硝化过程 c.反硝化过程
转化为氨态氮 b.硝化过程 c.反硝化过程(2)氮肥是水体中铵根的主要来源之一,铵根的电子式为
(3)铵态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移电子的物质的量为
(4)土壤中的铁循环可用于水体脱氮(指将氮元素从水体中除去),用离子方程式说明利用土壤中的铁循环脱除水体中铵态氮的原理
(5)实验室中也可以实现不同价态氮元素之间的转变,请写出符合以下要求的化学方程式:
①
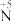 转化为
转化为 :
:②
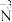 转化为
转化为 :
:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】按要求在横线上写出下列反应的离子方程式:
(1)将Al放入稀盐酸中:___________________ 。
(2)将Al放入NaOH溶液中:___________________ 。
(3)将Al2O3放入稀盐酸中:___________________ 。
(4)将Al2O3放入NaOH溶液中:___________________ 。
(5)将Al(OH)3放入稀盐酸中:___________________ 。
(6)将Al(OH)3放入NaOH溶液中:___________________ 。
(1)将Al放入稀盐酸中:
(2)将Al放入NaOH溶液中:
(3)将Al2O3放入稀盐酸中:
(4)将Al2O3放入NaOH溶液中:
(5)将Al(OH)3放入稀盐酸中:
(6)将Al(OH)3放入NaOH溶液中:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学与人类生活密切相关。请按要求,回答下列问题:
(1)生石灰可作食品干燥剂,它属于___________ (填“碱”、“盐”或“氧化物”)。
(2)将食品袋中的抗氧化剂还原铁粉投入食醋中,发现产生大量气泡,溶液变为浅绿色。请写出发生反应的离子方程式___________ 。
(3)洪涝灾害后,加入KAl(SO4)2·12H2O可使浑浊的水变澄清,该物质俗名为___________ ,因其溶于水生成___________ (化学式)而具有净水作用。
(4)铝粉和氢氧化钠混合物可用作下水道疏通剂,其主要原因为___________ (用化学方程式表示)。
(5)炒菜时,食盐不慎撒落在天然气火焰上,可能看到的现象为:___________ 。
(1)生石灰可作食品干燥剂,它属于
(2)将食品袋中的抗氧化剂还原铁粉投入食醋中,发现产生大量气泡,溶液变为浅绿色。请写出发生反应的离子方程式
(3)洪涝灾害后,加入KAl(SO4)2·12H2O可使浑浊的水变澄清,该物质俗名为
(4)铝粉和氢氧化钠混合物可用作下水道疏通剂,其主要原因为
(5)炒菜时,食盐不慎撒落在天然气火焰上,可能看到的现象为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题
(1)①基态Cu原子有______ 种不同能级的电子。
②N原子中最高能级的电子的电子云轮廓图为______ 。
③在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是___________ 。
(2)元素X位于第四周期,其基态原子有4个未成对电子,基态X2+的价电子排布式是________ ;X3+的价电子排布式为________ 。
(3)M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子,M元素基态原子的电子排布式为____ ,M+的价电子排布式为____ ,M2+的电子排布式为________ 。
(1)①基态Cu原子有
②N原子中最高能级的电子的电子云轮廓图为
③在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是
(2)元素X位于第四周期,其基态原子有4个未成对电子,基态X2+的价电子排布式是
(3)M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子,M元素基态原子的电子排布式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如右图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大。

(1)X位于元素周期表中第________ 周期第________ 族;W的基态原子核外有_____ 个未成对电子。
(2)Z的气态氢化物和溴化氢相比,较稳定的是______ (写化学式)。
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是__________________________________ 。

(1)X位于元素周期表中第
(2)Z的气态氢化物和溴化氢相比,较稳定的是
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】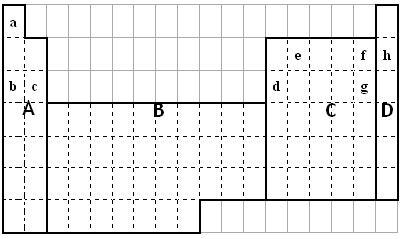
(1)在元素周期表上述四个区域中,单质均能导电的是 。
(a)A (b)B (c)C (d)D
(2)最外电子层只有圆球形电子云的主族元素在区域 中。
(a)A (b)B (c)C (d)D
(3)e形成的单质晶体可能为 。
A.离子晶体 B.分子晶体 C.原子晶体 D.金属晶体
(4)元素非金属性强弱比较有很多方法,其中f和g的非金属性强弱的研究方案中不可
行的是_________(填序号)。
①比较两种单质的颜色②比较氢化物的稳定性③依据两元素在周期表的位置④比较原子半径大小⑤比较最高价氧化物对应水化物的酸性
(5)请用一个化学方程式来说明b的金属性比d强________________

(1)在元素周期表上述四个区域中,单质均能导电的是 。
(a)A (b)B (c)C (d)D
(2)最外电子层只有圆球形电子云的主族元素在区域 中。
(a)A (b)B (c)C (d)D
(3)e形成的单质晶体可能为 。
A.离子晶体 B.分子晶体 C.原子晶体 D.金属晶体
(4)元素非金属性强弱比较有很多方法,其中f和g的非金属性强弱的研究方案中不可
行的是_________(填序号)。
①比较两种单质的颜色②比较氢化物的稳定性③依据两元素在周期表的位置④比较原子半径大小⑤比较最高价氧化物对应水化物的酸性
(5)请用一个化学方程式来说明b的金属性比d强________________
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表列出了①~⑨九种元素在周期表中的位置:
请按要求回答下列问题:
(1)上述元素中、金属性最强的是___________ (填元素名称),最高价氧化物对应水化物酸性最强的是___________ (写出酸的化学式)。
(2)由④、⑤、⑥三种元素形成的简单离子半径由大到小的顺序是_______ (用离子符号表示)。
(3)由元素②形成的单质的电子式为___________ ;元素⑤和⑧可形成化合物乙,请用电子式表示化合物乙的形成过程___________ 。
(4)元素③的最简单氢化物的化学式是___________ ,该氢化物在常温下与元素⑨发生反应的化学方程式是___________ ,所得溶液的pH___________ 7。
(5)元素⑥的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是___________ 。
| 族周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | |||||||
(1)上述元素中、金属性最强的是
(2)由④、⑤、⑥三种元素形成的简单离子半径由大到小的顺序是
(3)由元素②形成的单质的电子式为
(4)元素③的最简单氢化物的化学式是
(5)元素⑥的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下列变化①碘的升华②烧碱熔化③氯化钠溶于水④氯化氢溶于水⑤氧气溶于水⑥氯化铵受热分解。
氯化铵的电子式是______________ ;未发生化学键破坏的是______________ (填序号,下同);仅发生离子键破坏的是______________ ;仅发生共价键破坏的是______________ ;既发生离子键又发生共价键破坏的是______________ 。
氯化铵的电子式是
您最近一年使用:0次



