氮肥的使用极大提高了粮食作物的产量,对解决世界粮食危机起到了不可或缺的作用,下面是几种通过氮的固定制备氮肥的方法。
(1)自然固氮:一种途径是通过雷电将空气中少量的氮气转化为含氮化合物(氮肥),主要转化途径如下(转化所需试剂及条件已略去):
 硝酸盐[如
硝酸盐[如 ]
]
①写出在空气中 转化为NO的化学方程式
转化为NO的化学方程式_______ 。
②将 转化为
转化为 ,列举两种不同类别的化合物M
,列举两种不同类别的化合物M_______ (写化学式)。
③若M是Cu单质,与稀硝酸反应也能生成硝酸盐,写出铜粉与稀硝酸反应的离子方程式_______ 。
(2)人工固氮:
①工业上以氮气和氢气为原料,在高温、高压和催化剂的条件下合成氨。该反应的化学方程式为_______ 。
②利用氨气与氧气在催化剂作用下生成NO,是工业制备硝酸的重要环节,该反应中NO是_______ (填“氧化产物”“还原产物”或“氧化产物和还原产物”)。
③利用氨气与二氧化碳在催化剂作用下合成重要氮肥尿素 ,尿素中N元素的化合价是
,尿素中N元素的化合价是_______ 。合成尿素的化学方程式_______ 。尿素在土壤中与水结合生成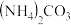 ,被植物吸收,有利于作物的生长。
,被植物吸收,有利于作物的生长。
(3)在微生物作用下实现 的转化,称为硝化过程。在一定条件下,
的转化,称为硝化过程。在一定条件下, 被
被 氧化成
氧化成 ,参加反应的
,参加反应的 和
和 的物质的量之比为
的物质的量之比为_______ 。由于 有毒,因此过量使用氮肥也会引起农作物大量减产,所以一定要合理科学使用。
有毒,因此过量使用氮肥也会引起农作物大量减产,所以一定要合理科学使用。
(4)有同学猜测,在 被细菌分解过程中,
被细菌分解过程中, 最终分解为
最终分解为 ,同时有
,同时有 生成。从化合价变化的角度分析有
生成。从化合价变化的角度分析有 生成的合理性
生成的合理性_______ 。
(1)自然固氮:一种途径是通过雷电将空气中少量的氮气转化为含氮化合物(氮肥),主要转化途径如下(转化所需试剂及条件已略去):
 硝酸盐[如
硝酸盐[如 ]
]①写出在空气中
 转化为NO的化学方程式
转化为NO的化学方程式②将
 转化为
转化为 ,列举两种不同类别的化合物M
,列举两种不同类别的化合物M③若M是Cu单质,与稀硝酸反应也能生成硝酸盐,写出铜粉与稀硝酸反应的离子方程式
(2)人工固氮:
①工业上以氮气和氢气为原料,在高温、高压和催化剂的条件下合成氨。该反应的化学方程式为
②利用氨气与氧气在催化剂作用下生成NO,是工业制备硝酸的重要环节,该反应中NO是
③利用氨气与二氧化碳在催化剂作用下合成重要氮肥尿素
 ,尿素中N元素的化合价是
,尿素中N元素的化合价是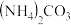 ,被植物吸收,有利于作物的生长。
,被植物吸收,有利于作物的生长。(3)在微生物作用下实现
 的转化,称为硝化过程。在一定条件下,
的转化,称为硝化过程。在一定条件下, 被
被 氧化成
氧化成 ,参加反应的
,参加反应的 和
和 的物质的量之比为
的物质的量之比为 有毒,因此过量使用氮肥也会引起农作物大量减产,所以一定要合理科学使用。
有毒,因此过量使用氮肥也会引起农作物大量减产,所以一定要合理科学使用。(4)有同学猜测,在
 被细菌分解过程中,
被细菌分解过程中, 最终分解为
最终分解为 ,同时有
,同时有 生成。从化合价变化的角度分析有
生成。从化合价变化的角度分析有 生成的合理性
生成的合理性
更新时间:2022-05-28 03:22:50
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】完成下列问题。
(1)现有以下物质:①NaCl晶体;②干冰;③液态的醋酸;④铜;⑤BaSO4固体;⑥蔗糖;⑦酒精;⑧熔融的KNO3;⑨HCl。以上物质能导电的是___________ ;以上物质属于电解质的是___________ 。
(2)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C 具有___________ (填“氧化性”或“还原性”)。
(3)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2,该反应的还原剂是___________ ,氧化剂是___________ 。
(4)查阅资料可知,铜和浓H2SO4共热,发生反应Cu+ 2H2SO4(浓) CuSO4+SO2↑+2H2O,该反应中氧化剂与还原剂的个数之比为
CuSO4+SO2↑+2H2O,该反应中氧化剂与还原剂的个数之比为___________ ,其中H2SO4在反应中表现___________ 。
(5)请配平反应方程式:____K2Cr2O7+____HCl _____KCl+____CrCl3+____Cl2+____H2O,
_____KCl+____CrCl3+____Cl2+____H2O,______ ,若反应中发生氧化反应的HCl个数为12,则反应中转移的电子数为___________ 个。
(1)现有以下物质:①NaCl晶体;②干冰;③液态的醋酸;④铜;⑤BaSO4固体;⑥蔗糖;⑦酒精;⑧熔融的KNO3;⑨HCl。以上物质能导电的是
(2)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C 具有
(3)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2,该反应的还原剂是
(4)查阅资料可知,铜和浓H2SO4共热,发生反应Cu+ 2H2SO4(浓)
 CuSO4+SO2↑+2H2O,该反应中氧化剂与还原剂的个数之比为
CuSO4+SO2↑+2H2O,该反应中氧化剂与还原剂的个数之比为(5)请配平反应方程式:____K2Cr2O7+____HCl
 _____KCl+____CrCl3+____Cl2+____H2O,
_____KCl+____CrCl3+____Cl2+____H2O,
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
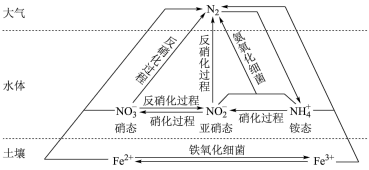
【推荐2】细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如下图所示。_______ (填字母序号)。
a. 转化为氨态氮 b.硝化过程 c.反硝化过程
转化为氨态氮 b.硝化过程 c.反硝化过程
(2)氮肥是水体中氨态氮的主要来源之一、
①氨气是生产氮肥的主要原料,工业合成氨的化学方程式为_______ 。
②检验氨态氮肥中 的实验方案是
的实验方案是_______ 。
(3)硝化过程中,含氮物质发生_______ (填“氧化”或“还原”)反应。
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生 氮气时,转移的电子的物质的量为
氮气时,转移的电子的物质的量为_______ mol。
(5)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式分别说明利用土壤中的铁循环脱除水体中氨态氮和硝态氮的原理:_______ 、_______ 。
a.
 转化为氨态氮 b.硝化过程 c.反硝化过程
转化为氨态氮 b.硝化过程 c.反硝化过程(2)氮肥是水体中氨态氮的主要来源之一、
①氨气是生产氮肥的主要原料,工业合成氨的化学方程式为
②检验氨态氮肥中
 的实验方案是
的实验方案是(3)硝化过程中,含氮物质发生
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生
 氮气时,转移的电子的物质的量为
氮气时,转移的电子的物质的量为(5)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式分别说明利用土壤中的铁循环脱除水体中氨态氮和硝态氮的原理:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】从物质类别和元素化合价两个维度研究物质的性质及转化是重要的化学学习方法。以下是氮元素的“价一类”二维图的部分信息。请回答下列问题:
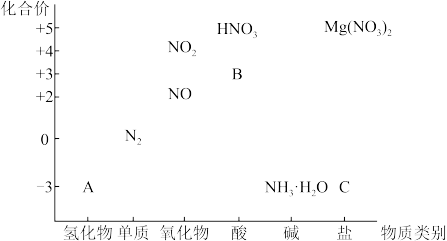
(1)亚硝酸(HNO2)在工业上用于有机合成,其在图中的字母标号为____ 。
(2)工业上制备A的化学方程式为____ ,检验C中含氮阳离子的方法是____ 。
(3)NO2溶于水发生反应3NO2+H2O=2HNO3+NO,若生成1molHNO3时,转移的电子数目为____ ,反应中NO2表现的性质为____ (填标号)。
A.只有氧化性 B.只有还原性 C.既有氧化性又有还原性
(4)Mg(NO3)2受热会分解,有同学猜想分解产物为MgO、NO2、N2,这种猜想不合理的理由是_____ 。

(1)亚硝酸(HNO2)在工业上用于有机合成,其在图中的字母标号为
(2)工业上制备A的化学方程式为
(3)NO2溶于水发生反应3NO2+H2O=2HNO3+NO,若生成1molHNO3时,转移的电子数目为
A.只有氧化性 B.只有还原性 C.既有氧化性又有还原性
(4)Mg(NO3)2受热会分解,有同学猜想分解产物为MgO、NO2、N2,这种猜想不合理的理由是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】I、氧化还原反应与离子反应在生产生活与科学实验中有重要作用,过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。根据下列反应回答问题:
A.
B.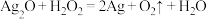
C.
D.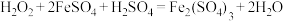
(1)上述反应中, 仅体现氧化性的反应是
仅体现氧化性的反应是______ (填字母序号,下同), 既体现氧化性又体现还原性的反应是
既体现氧化性又体现还原性的反应是______ , 、
、 、
、 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是______ 。
(2)某酸性反应体系中发生的一个属于氧化还原的离子反应,反应物和生成物共六种微粒: 、
、 、
、 、
、 、
、 、
、 ,则反应的离子方程式为
,则反应的离子方程式为______ 。
 、氯元素是中学化学中常见的重要非金属元素之一,氯元素的单质及其化合物在生产与生活中有着重要的用途,依据所学知识完成下列问题:
、氯元素是中学化学中常见的重要非金属元素之一,氯元素的单质及其化合物在生产与生活中有着重要的用途,依据所学知识完成下列问题:
(3)实验室利用 制备氯气的离子方程式是
制备氯气的离子方程式是______ :若多余的氯气用氢氧化钠溶液吸收,其离子方程式为______ 。
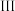 、
、 在实验室和工业上均有重要应用,其工业制备的部分工艺如下:
在实验室和工业上均有重要应用,其工业制备的部分工艺如下:
①将软锰矿(主要成分 )粉碎后,与
)粉碎后,与 固体混合,通入空气充分焙烧,生成暗绿色
固体混合,通入空气充分焙烧,生成暗绿色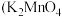 )
)
熔融态物质。
②冷却,将固体研细,用 溶液浸取,过滤,得暗绿色溶液。
溶液浸取,过滤,得暗绿色溶液。
③向暗绿色溶液中通入 ,溶液变为紫红色。
,溶液变为紫红色。
④将紫红色溶液蒸发浓缩,冷却结晶,过滤,洗涤,干燥,得 固体。
固体。
资料: 为暗绿色固体,在强碱性溶液中稳定,在近中性或酸性溶液中易发生歧化反应(
为暗绿色固体,在强碱性溶液中稳定,在近中性或酸性溶液中易发生歧化反应( 的化合价既升高又降低)。
的化合价既升高又降低)。
(4)①中生成 的化学方程式是
的化学方程式是______ 。
(5)②中浸取时用 溶液的原因是
溶液的原因是______ 。
(6)③中产生两种盐,写出③的方程式,并用单线桥标出电子转移______ 。
A.

B.
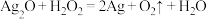
C.

D.
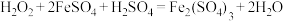
(1)上述反应中,
 仅体现氧化性的反应是
仅体现氧化性的反应是 既体现氧化性又体现还原性的反应是
既体现氧化性又体现还原性的反应是 、
、 、
、 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是(2)某酸性反应体系中发生的一个属于氧化还原的离子反应,反应物和生成物共六种微粒:
 、
、 、
、 、
、 、
、 、
、 ,则反应的离子方程式为
,则反应的离子方程式为 、氯元素是中学化学中常见的重要非金属元素之一,氯元素的单质及其化合物在生产与生活中有着重要的用途,依据所学知识完成下列问题:
、氯元素是中学化学中常见的重要非金属元素之一,氯元素的单质及其化合物在生产与生活中有着重要的用途,依据所学知识完成下列问题:(3)实验室利用
 制备氯气的离子方程式是
制备氯气的离子方程式是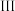 、
、 在实验室和工业上均有重要应用,其工业制备的部分工艺如下:
在实验室和工业上均有重要应用,其工业制备的部分工艺如下:①将软锰矿(主要成分
 )粉碎后,与
)粉碎后,与 固体混合,通入空气充分焙烧,生成暗绿色
固体混合,通入空气充分焙烧,生成暗绿色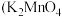 )
)熔融态物质。
②冷却,将固体研细,用
 溶液浸取,过滤,得暗绿色溶液。
溶液浸取,过滤,得暗绿色溶液。③向暗绿色溶液中通入
 ,溶液变为紫红色。
,溶液变为紫红色。④将紫红色溶液蒸发浓缩,冷却结晶,过滤,洗涤,干燥,得
 固体。
固体。资料:
 为暗绿色固体,在强碱性溶液中稳定,在近中性或酸性溶液中易发生歧化反应(
为暗绿色固体,在强碱性溶液中稳定,在近中性或酸性溶液中易发生歧化反应( 的化合价既升高又降低)。
的化合价既升高又降低)。(4)①中生成
 的化学方程式是
的化学方程式是(5)②中浸取时用
 溶液的原因是
溶液的原因是(6)③中产生两种盐,写出③的方程式,并用单线桥标出电子转移
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】通常情况下,氮气很不活泼,其原因是:N2分子内部具有N≡N结构,键能很大,不容易被破坏。
(1)在一定条件下也可以与其他物质反应,有两种气体,一种能够氧化N2,一种能够还原N2,请分别写出这两个反应的化学方程式:
①氧化N2:_______ ;
②还原N2:_______ 。
(2)Mg可以在N2中燃烧生成氮化镁,写出该反应的化学方程式_______ ,在该反应中N2表现_______ 性。
(3)已知氮化镁可以与水反应生成氢氧化镁和氨气,写出该反应的化学反应方程式_______ 。
(1)在一定条件下也可以与其他物质反应,有两种气体,一种能够氧化N2,一种能够还原N2,请分别写出这两个反应的化学方程式:
①氧化N2:
②还原N2:
(2)Mg可以在N2中燃烧生成氮化镁,写出该反应的化学方程式
(3)已知氮化镁可以与水反应生成氢氧化镁和氨气,写出该反应的化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现代文明中将 排放到大气的同时,又想方设法地把空气中的
排放到大气的同时,又想方设法地把空气中的 吞下去,但在空气中的
吞下去,但在空气中的 是很稳定的。长期田间劳作的人们发现玉米等作物和豆类作物“轮换种植”长势优越。
是很稳定的。长期田间劳作的人们发现玉米等作物和豆类作物“轮换种植”长势优越。
(1)上述文字中所提到的 ,其分子的电子式是
,其分子的电子式是___________ 。简述N2稳定的原因___________ 。
(2)玉米与豆类作物轮换种植时,玉米长势优越的原因是___________
 排放到大气的同时,又想方设法地把空气中的
排放到大气的同时,又想方设法地把空气中的 吞下去,但在空气中的
吞下去,但在空气中的 是很稳定的。长期田间劳作的人们发现玉米等作物和豆类作物“轮换种植”长势优越。
是很稳定的。长期田间劳作的人们发现玉米等作物和豆类作物“轮换种植”长势优越。(1)上述文字中所提到的
 ,其分子的电子式是
,其分子的电子式是(2)玉米与豆类作物轮换种植时,玉米长势优越的原因是___________
| A.玉米有固氮作用 | B.豆类作物有固氮作用 |
| C.大气固氮的作用 | D.人工合成氨的作用 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氮循环是自然界中一种重要的物质循环方式:
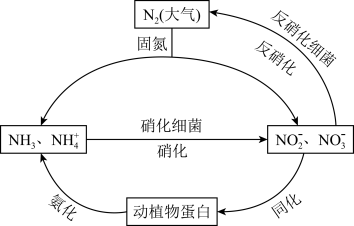
(1)化学与生产、生活和科技都密切相关。下列有关说法不正确的是___________ 。
A.硝化过程无需氧化剂参与
B.含有新冠病毒的飞沫分散在空气中形成的分散系为气溶胶
C.固氮过程中, 只做氧化剂
只做氧化剂
D.“落红不是无情物,化作春泥更护花”蕴含着自然界中的碳、氮循环
E.反硝化过程有助于弥补人工固氮对氮循环造成的影响
F.同化、氨化过程中,实现了氮元素在无机物和有机物之间的转化
(2)写出氮循环中 的电子式
的电子式___________ ,其空间构型是___________ 。写出 的检验方法
的检验方法___________ 。
(3)实验室用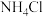 与
与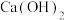 反应来制备
反应来制备 ,原理:
,原理:___________ (化学反应方程式)。在图中补上尾气处理装置(注明所用的化学物质的化学式)。___________
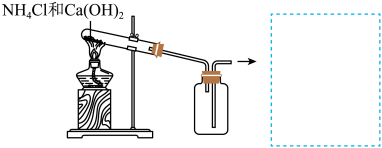
(4)通常我们把大气中游离态的氮转化为氮的化合物的过程称为氮的固定,主要有3种途径。如上① 称为
称为___________ ,②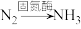 称为生物固氮,还有1种是工业固氮,其反应的化学方程式是
称为生物固氮,还有1种是工业固氮,其反应的化学方程式是___________ 。
(5)反硝化过程中, (C化合价:
(C化合价: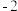 )可作为反应的还原剂。请将该反应的离子方程式补充完整:
)可作为反应的还原剂。请将该反应的离子方程式补充完整:___________ 。
___________ ___________
___________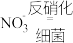 ___________
___________ ___________
___________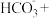 ___________
___________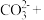 ___________。
___________。

(1)化学与生产、生活和科技都密切相关。下列有关说法不正确的是
A.硝化过程无需氧化剂参与
B.含有新冠病毒的飞沫分散在空气中形成的分散系为气溶胶
C.固氮过程中,
 只做氧化剂
只做氧化剂D.“落红不是无情物,化作春泥更护花”蕴含着自然界中的碳、氮循环
E.反硝化过程有助于弥补人工固氮对氮循环造成的影响
F.同化、氨化过程中,实现了氮元素在无机物和有机物之间的转化
(2)写出氮循环中
 的电子式
的电子式 的检验方法
的检验方法(3)实验室用
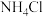 与
与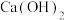 反应来制备
反应来制备 ,原理:
,原理:
(4)通常我们把大气中游离态的氮转化为氮的化合物的过程称为氮的固定,主要有3种途径。如上①
 称为
称为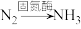 称为生物固氮,还有1种是工业固氮,其反应的化学方程式是
称为生物固氮,还有1种是工业固氮,其反应的化学方程式是(5)反硝化过程中,
 (C化合价:
(C化合价: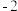 )可作为反应的还原剂。请将该反应的离子方程式补充完整:
)可作为反应的还原剂。请将该反应的离子方程式补充完整:___________
 ___________
___________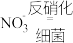 ___________
___________ ___________
___________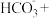 ___________
___________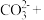 ___________。
___________。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】我国“蓝天保卫战”成果显著,肆虐的雾霾逐渐被遏止。科学家研究发现含氮化合物和含硫化合物在形成雾霾时与大气中的氨有关,转化关系如图所示:
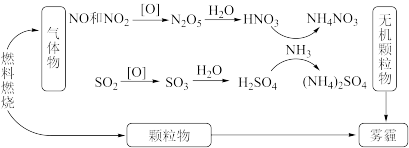
回答下列问题:
(1)从物质分类的角度看,图中的物质属于酸性氧化物的有_______ (写化学式)。
(2)写出 转化为
转化为 的化学方程式:
的化学方程式:_______ 。
(3)工业上合成氨的化学方程式为_______ 。
(4)实验室长期保存浓硝酸,需使用棕色试剂瓶,并放置在阴凉处,其原因为_______ (用化学方程式表示)。
(5)氨与一氧化氮(NO)在一定条件下反应可生成对空气无污染的物质,该反应的化学方程式为_______ 。

回答下列问题:
(1)从物质分类的角度看,图中的物质属于酸性氧化物的有
(2)写出
 转化为
转化为 的化学方程式:
的化学方程式:(3)工业上合成氨的化学方程式为
(4)实验室长期保存浓硝酸,需使用棕色试剂瓶,并放置在阴凉处,其原因为
(5)氨与一氧化氮(NO)在一定条件下反应可生成对空气无污染的物质,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氨气 是一种重要的化工原料,其中约80%用来生产各种氮肥。
是一种重要的化工原料,其中约80%用来生产各种氮肥。
(1)氨气的制备
①实验室通过加热 和
和 的混合物制取氨,该反应的化学方程式为
的混合物制取氨,该反应的化学方程式为_____ 。
实验室用该反应原理制取并收集一瓶干燥的氨气,从下图中选择合适的装置,其连接顺序为_____ 。(按从左到右的气流方向,用小写字母和箭头表示)
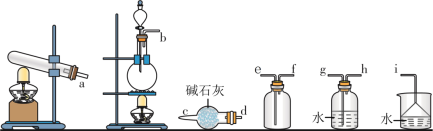
②工业上以氮气和氢气为原料合成氨,该反应的化学方程式为_____ ,氨气的电子式为_____ 。
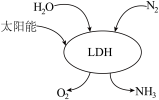
③我国科研团队借助一种固体催化剂(LDH),在常温、常压和可见光条件下合成了氨,其过程如图所示。该反应的化学方程式为_____ 。反应中每转移6mole⁻,生成NH3的物质的量为_____ mol。
(2)氮肥的制备和应用
主要转化途径如下(转化所需试剂及条件已略去):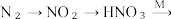 硝酸盐(如
硝酸盐(如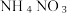 )。
)。
①写出 的化学方程式
的化学方程式_____ 。
②将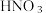 转化为
转化为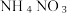 ,请你写出一个化合物
,请你写出一个化合物 的化学式
的化学式_____ 。
 是一种重要的化工原料,其中约80%用来生产各种氮肥。
是一种重要的化工原料,其中约80%用来生产各种氮肥。(1)氨气的制备
①实验室通过加热
 和
和 的混合物制取氨,该反应的化学方程式为
的混合物制取氨,该反应的化学方程式为实验室用该反应原理制取并收集一瓶干燥的氨气,从下图中选择合适的装置,其连接顺序为

②工业上以氮气和氢气为原料合成氨,该反应的化学方程式为
③我国科研团队借助一种固体催化剂(LDH),在常温、常压和可见光条件下合成了氨,其过程如图所示。该反应的化学方程式为

(2)氮肥的制备和应用
主要转化途径如下(转化所需试剂及条件已略去):
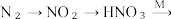 硝酸盐(如
硝酸盐(如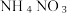 )。
)。①写出
 的化学方程式
的化学方程式②将
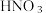 转化为
转化为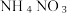 ,请你写出一个化合物
,请你写出一个化合物 的化学式
的化学式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】按照要求回答问题。
(1)硅是无机非金属材料的主角,Si在元素周期表中的位置___________ ,氮化硅是一种性能优异的无机非金属材料,化学式为___________ ,氮原子和硅原子通过___________ (填“离子键”或“共价键”)连接。建筑粘合剂和防火剂硅酸钠,可用 溶解在
溶解在 溶液中制备,反应的离子方程式为
溶液中制备,反应的离子方程式为___________ 。
(2)氨和硝酸是重要的化工产品,工业合成氨及制备硝酸的部分流程图如下
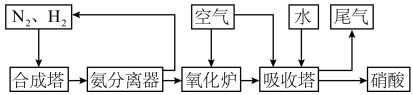
①合成塔中发生反应的化学方程式为___________ 。
②氧化炉中,标准状况下
 转化为
转化为 时转移的电子数目为
时转移的电子数目为___________ 。
③吸收塔中出来的尾气 和
和 ,通过调节其体积比,可用
,通过调节其体积比,可用 溶液完全吸收,生成硫酸盐或亚硝酸盐。
溶液完全吸收,生成硫酸盐或亚硝酸盐。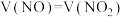 时,发生反应的化学方程式为
时,发生反应的化学方程式为___________ 。标准状况下22.4L仅含 和
和 的混合气被完全吸收,若
的混合气被完全吸收,若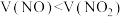 ,消耗
,消耗 的物质的是为
的物质的是为___________  。
。
(1)硅是无机非金属材料的主角,Si在元素周期表中的位置
 溶解在
溶解在 溶液中制备,反应的离子方程式为
溶液中制备,反应的离子方程式为(2)氨和硝酸是重要的化工产品,工业合成氨及制备硝酸的部分流程图如下

①合成塔中发生反应的化学方程式为
②氧化炉中,标准状况下

 转化为
转化为 时转移的电子数目为
时转移的电子数目为③吸收塔中出来的尾气
 和
和 ,通过调节其体积比,可用
,通过调节其体积比,可用 溶液完全吸收,生成硫酸盐或亚硝酸盐。
溶液完全吸收,生成硫酸盐或亚硝酸盐。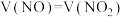 时,发生反应的化学方程式为
时,发生反应的化学方程式为 和
和 的混合气被完全吸收,若
的混合气被完全吸收,若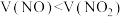 ,消耗
,消耗 的物质的是为
的物质的是为 。
。
您最近一年使用:0次



