氨气 是一种重要的化工原料,其中约80%用来生产各种氮肥。
是一种重要的化工原料,其中约80%用来生产各种氮肥。
(1)氨气的制备
①实验室通过加热 和
和 的混合物制取氨,该反应的化学方程式为
的混合物制取氨,该反应的化学方程式为_____ 。
实验室用该反应原理制取并收集一瓶干燥的氨气,从下图中选择合适的装置,其连接顺序为_____ 。(按从左到右的气流方向,用小写字母和箭头表示)
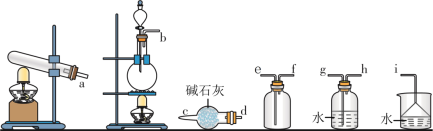
②工业上以氮气和氢气为原料合成氨,该反应的化学方程式为_____ ,氨气的电子式为_____ 。
③我国科研团队借助一种固体催化剂(LDH),在常温、常压和可见光条件下合成了氨,其过程如图所示。该反应的化学方程式为_____ 。反应中每转移6mole⁻,生成NH3的物质的量为_____ mol。
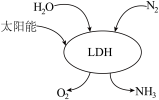
(2)氮肥的制备和应用
主要转化途径如下(转化所需试剂及条件已略去):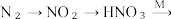 硝酸盐(如
硝酸盐(如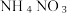 )。
)。
①写出 的化学方程式
的化学方程式_____ 。
②将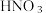 转化为
转化为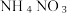 ,请你写出一个化合物
,请你写出一个化合物 的化学式
的化学式_____ 。
 是一种重要的化工原料,其中约80%用来生产各种氮肥。
是一种重要的化工原料,其中约80%用来生产各种氮肥。(1)氨气的制备
①实验室通过加热
 和
和 的混合物制取氨,该反应的化学方程式为
的混合物制取氨,该反应的化学方程式为实验室用该反应原理制取并收集一瓶干燥的氨气,从下图中选择合适的装置,其连接顺序为

②工业上以氮气和氢气为原料合成氨,该反应的化学方程式为
③我国科研团队借助一种固体催化剂(LDH),在常温、常压和可见光条件下合成了氨,其过程如图所示。该反应的化学方程式为

(2)氮肥的制备和应用
主要转化途径如下(转化所需试剂及条件已略去):
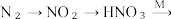 硝酸盐(如
硝酸盐(如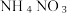 )。
)。①写出
 的化学方程式
的化学方程式②将
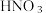 转化为
转化为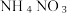 ,请你写出一个化合物
,请你写出一个化合物 的化学式
的化学式
更新时间:2024-04-02 13:49:56
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。

(1)A中装有Ca(OH)2和NH4Cl混合粉末,该反应的化学方程式是_____________________ 。
(2)B中加入的是______________ ,其作用是______________________ 。
(3)实验时在C中观察到的现象是_____________________ ,发生反应的化学方程式是:_______________ 。
(4)E中收集到的物质是________ 。

(1)A中装有Ca(OH)2和NH4Cl混合粉末,该反应的化学方程式是
(2)B中加入的是
(3)实验时在C中观察到的现象是
(4)E中收集到的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氮及其化合物在生产生活中有广泛的应用,按要求回答下列问题:
I.氨气是重要的化工原料,回答下列问题:
(1)实验室制取 的化学方程式为
的化学方程式为___________ 。
(2)1909年化学家哈伯在实验室首次用单质合成了氨。2007年化学家格哈德埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,获得诺贝尔化学奖。用 、
、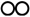 、
、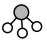 分别表示
分别表示 ,观察如图,判断符合在催化剂表面合成氨反应过程的顺序为___________。
,观察如图,判断符合在催化剂表面合成氨反应过程的顺序为___________。
II.氮氧化物是造成环境污染的主要原因之一,消除氮氧化物有多种方法。
(3)某学习小组设计如图装置,有效降低含氮化合物的排放,同时充分利用化学能,相同温度和压强下, 两电极产生气体的体积比为
两电极产生气体的体积比为___________ , 电极的电极反应方程式为
电极的电极反应方程式为___________ 。
I.氨气是重要的化工原料,回答下列问题:
(1)实验室制取
 的化学方程式为
的化学方程式为(2)1909年化学家哈伯在实验室首次用单质合成了氨。2007年化学家格哈德埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,获得诺贝尔化学奖。用
 、
、 、
、 分别表示
分别表示 ,观察如图,判断符合在催化剂表面合成氨反应过程的顺序为___________。
,观察如图,判断符合在催化剂表面合成氨反应过程的顺序为___________。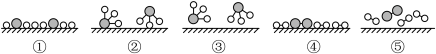
| A.②③④①⑤ | B.③②①④⑤ | C.③②④①⑤ | D.⑤④①②③ |
II.氮氧化物是造成环境污染的主要原因之一,消除氮氧化物有多种方法。
(3)某学习小组设计如图装置,有效降低含氮化合物的排放,同时充分利用化学能,相同温度和压强下,
 两电极产生气体的体积比为
两电极产生气体的体积比为 电极的电极反应方程式为
电极的电极反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某化学兴趣小组的同学利用下图所示实验装置进行某些气体的制备、性质探究等实验(图中夹持装置已省略)。
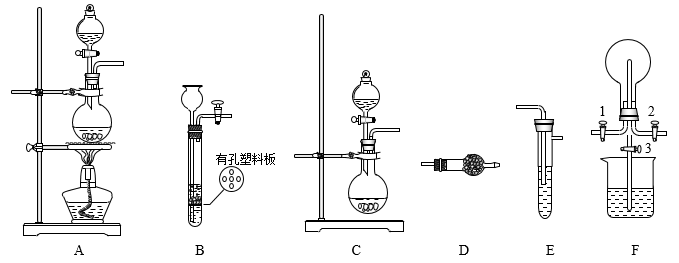
I.制备气体
(1)利用装置B可制取的气体有___________ (选填字母序号)。
a.CO2b.H2 c.SO2
II.探究Cl2与NH3的反应
(2)装置C与装置D连接可制取干燥的氨气,D装置内的药品是_______ ;装置A、E、D连接可制取纯净、干燥的Cl2,E装置的作用是___________ 。
(3)装置F可用于探究Cl2与NH3的反应。实验时打开开关1、3,关闭2,先向烧瓶中通入______ ,然后关闭3,打开2,向烧瓶中慢慢通入一定量的另一种气体。实验开始一段时间后,烧瓶内出现浓厚的白烟并在容器内壁凝结,该反应的化学方程式为___________ 。
III.探究某些物质的性质
(4)利用装置C、E可设计实验比较碳元素和硅元素的非金属性强弱,实验方案是___________ 。
(5)将装置B、C分别与装置F相连后,进行H2S与SO2反应的实验。烧瓶中发生反应的化学方程式为___________ 。

I.制备气体
(1)利用装置B可制取的气体有
a.CO2b.H2 c.SO2
II.探究Cl2与NH3的反应
(2)装置C与装置D连接可制取干燥的氨气,D装置内的药品是
(3)装置F可用于探究Cl2与NH3的反应。实验时打开开关1、3,关闭2,先向烧瓶中通入
III.探究某些物质的性质
(4)利用装置C、E可设计实验比较碳元素和硅元素的非金属性强弱,实验方案是
(5)将装置B、C分别与装置F相连后,进行H2S与SO2反应的实验。烧瓶中发生反应的化学方程式为
您最近一年使用:0次
【推荐1】氮元素是生命的基础。自然界中氨的循环过程如下图所示,请分析此图并回答问题:

(1)大气中的氮以___________ (填化学式)形式存在,图中共表示了___________ 种固氮的途径。
(2)由图可知,动植物体内的氮主要存在于蛋白质中,当动植物尸体发生了腐败时,往往会产生一种含氮的气体,其电子式为___________ 。
(3)土壤中的硝酸盐会被细菌分解。有一种脱氧硫杆菌能够利用土壤中的硫化物来分解硝酸盐,其主要化学原理如下: ,配平上述反应方程式,并标出电子转移的方向和数目。
,配平上述反应方程式,并标出电子转移的方向和数目。___________
(4)某同学写出下面三个不同价态的氮的化合物相互转换的关系(未配平):
a.NO+HNO3→N2O3+H2O
b.NH3+NO→HNO2+H2O
c.N2O4+H2O→HNO3+HNO2
其中你认为一定不可能实现的是___________ (填编号)。

(1)大气中的氮以
(2)由图可知,动植物体内的氮主要存在于蛋白质中,当动植物尸体发生了腐败时,往往会产生一种含氮的气体,其电子式为
(3)土壤中的硝酸盐会被细菌分解。有一种脱氧硫杆菌能够利用土壤中的硫化物来分解硝酸盐,其主要化学原理如下:
 ,配平上述反应方程式,并标出电子转移的方向和数目。
,配平上述反应方程式,并标出电子转移的方向和数目。(4)某同学写出下面三个不同价态的氮的化合物相互转换的关系(未配平):
a.NO+HNO3→N2O3+H2O
b.NH3+NO→HNO2+H2O
c.N2O4+H2O→HNO3+HNO2
其中你认为一定不可能实现的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】写出下列反应的化学方程式,是离子反应的写离子方程式
(1)工业上制备氨气反应的化学方程式___________
(2)铜和浓硫酸发生反应的化学方程式___________
(3)氨气催化氧化生成一氧化氮的化学方程式___________
(4)工业上制备漂白液发生反应的离子方程式___________
(5)将亚硫酸钠溶液滴入酸性高锰酸钾溶液中发生反应的离子方程式___________
(1)工业上制备氨气反应的化学方程式
(2)铜和浓硫酸发生反应的化学方程式
(3)氨气催化氧化生成一氧化氮的化学方程式
(4)工业上制备漂白液发生反应的离子方程式
(5)将亚硫酸钠溶液滴入酸性高锰酸钾溶液中发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
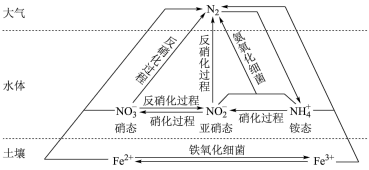
【推荐3】细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如下图所示。_______ (填字母序号)。
a. 转化为氨态氮 b.硝化过程 c.反硝化过程
转化为氨态氮 b.硝化过程 c.反硝化过程
(2)氮肥是水体中氨态氮的主要来源之一、
①氨气是生产氮肥的主要原料,工业合成氨的化学方程式为_______ 。
②检验氨态氮肥中 的实验方案是
的实验方案是_______ 。
(3)硝化过程中,含氮物质发生_______ (填“氧化”或“还原”)反应。
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生 氮气时,转移的电子的物质的量为
氮气时,转移的电子的物质的量为_______ mol。
(5)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式分别说明利用土壤中的铁循环脱除水体中氨态氮和硝态氮的原理:_______ 、_______ 。
a.
 转化为氨态氮 b.硝化过程 c.反硝化过程
转化为氨态氮 b.硝化过程 c.反硝化过程(2)氮肥是水体中氨态氮的主要来源之一、
①氨气是生产氮肥的主要原料,工业合成氨的化学方程式为
②检验氨态氮肥中
 的实验方案是
的实验方案是(3)硝化过程中,含氮物质发生
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生
 氮气时,转移的电子的物质的量为
氮气时,转移的电子的物质的量为(5)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式分别说明利用土壤中的铁循环脱除水体中氨态氮和硝态氮的原理:
您最近一年使用:0次



