从物质类别和元素化合价两个维度研究物质的性质及转化是重要的化学学习方法。以下是氮元素的“价一类”二维图的部分信息。请回答下列问题:
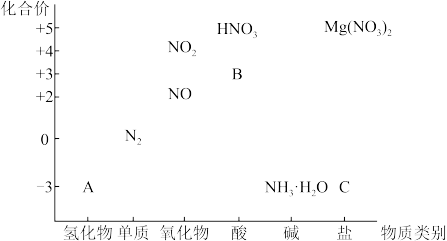
(1)亚硝酸(HNO2)在工业上用于有机合成,其在图中的字母标号为____ 。
(2)工业上制备A的化学方程式为____ ,检验C中含氮阳离子的方法是____ 。
(3)NO2溶于水发生反应3NO2+H2O=2HNO3+NO,若生成1molHNO3时,转移的电子数目为____ ,反应中NO2表现的性质为____ (填标号)。
A.只有氧化性 B.只有还原性 C.既有氧化性又有还原性
(4)Mg(NO3)2受热会分解,有同学猜想分解产物为MgO、NO2、N2,这种猜想不合理的理由是_____ 。

(1)亚硝酸(HNO2)在工业上用于有机合成,其在图中的字母标号为
(2)工业上制备A的化学方程式为
(3)NO2溶于水发生反应3NO2+H2O=2HNO3+NO,若生成1molHNO3时,转移的电子数目为
A.只有氧化性 B.只有还原性 C.既有氧化性又有还原性
(4)Mg(NO3)2受热会分解,有同学猜想分解产物为MgO、NO2、N2,这种猜想不合理的理由是
更新时间:2022-01-18 10:34:17
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】含铜元素的氧化还原反应在工业生产、环保及科研中有广泛的应用。
Ⅰ.碘化亚铜( )是难溶于水的白色固体。碘水因溶解碘单质而呈黄色。
)是难溶于水的白色固体。碘水因溶解碘单质而呈黄色。
已知:氧化性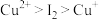 ,还原性
,还原性 。
。
(1) 可用于监测空气中是否含有汞(
可用于监测空气中是否含有汞( )蒸气:
)蒸气: (
( 为+2价)
为+2价) 。其中还原剂为
。其中还原剂为___________ ;每生成1个 原子,电子转移数目为
原子,电子转移数目为___________ 。
(2)久置于空气中的 溶液呈黄色,向其中加入一些铜粉,可使溶液黄色消失,黄色消失的反应的化学方程式为
溶液呈黄色,向其中加入一些铜粉,可使溶液黄色消失,黄色消失的反应的化学方程式为__________ 。
(3)根据物质氧化性还原性的强弱推测,在溶液中 和过量的
和过量的 反应的产物是
反应的产物是_____ 、___ 。
Ⅱ.氢化亚铜( )是一种难溶物质,不稳定,易分解,与稀盐酸反应能生成气体。
)是一种难溶物质,不稳定,易分解,与稀盐酸反应能生成气体。 在酸性条件下发生的反应是
在酸性条件下发生的反应是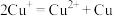 。
。
(4)“与稀盐酸反应能生成气体”的气体为___________ (填化学式)。
(5) 溶解在稀硫酸中反应的离子方程式为
溶解在稀硫酸中反应的离子方程式为___________ 。
Ⅰ.碘化亚铜(
 )是难溶于水的白色固体。碘水因溶解碘单质而呈黄色。
)是难溶于水的白色固体。碘水因溶解碘单质而呈黄色。已知:氧化性
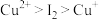 ,还原性
,还原性 。
。(1)
 可用于监测空气中是否含有汞(
可用于监测空气中是否含有汞( )蒸气:
)蒸气: (
( 为+2价)
为+2价) 。其中还原剂为
。其中还原剂为 原子,电子转移数目为
原子,电子转移数目为(2)久置于空气中的
 溶液呈黄色,向其中加入一些铜粉,可使溶液黄色消失,黄色消失的反应的化学方程式为
溶液呈黄色,向其中加入一些铜粉,可使溶液黄色消失,黄色消失的反应的化学方程式为(3)根据物质氧化性还原性的强弱推测,在溶液中
 和过量的
和过量的 反应的产物是
反应的产物是Ⅱ.氢化亚铜(
 )是一种难溶物质,不稳定,易分解,与稀盐酸反应能生成气体。
)是一种难溶物质,不稳定,易分解,与稀盐酸反应能生成气体。 在酸性条件下发生的反应是
在酸性条件下发生的反应是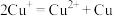 。
。(4)“与稀盐酸反应能生成气体”的气体为
(5)
 溶解在稀硫酸中反应的离子方程式为
溶解在稀硫酸中反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】良好生态环境是最普惠的民生福祉。治理大气污染物CO、NOX、SO2具有十分重要的意义。
(1)氧化还原法消除NOX的转化如下所示: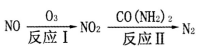 。反应I为NO+O3===NO2+O2,其还原产物是
。反应I为NO+O3===NO2+O2,其还原产物是_________ 。反应Ⅱ中,氧化剂与还原剂的物质的量之比为__________ 。
(2)吸收SO2和NO获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素)。

装置Ⅱ中,酸性条件下NO被Ce4+氧化的产物主要是NO3-和NO2-,请写出生成等物质的量的NO3-和NO2-时的离子方程式_______________ 。装置III中发生反应的离子方程式为_________________ 。
(3)已知进入装置IV的溶液中NO2-的浓度为a mol·L-1,要使1L该溶液中NO2-完全转化为NH4NO3,至少需向装置IV中通入标准状况下的氧气____ L(用含a代数式表示)。
(1)氧化还原法消除NOX的转化如下所示:
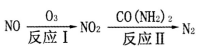 。反应I为NO+O3===NO2+O2,其还原产物是
。反应I为NO+O3===NO2+O2,其还原产物是(2)吸收SO2和NO获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素)。

装置Ⅱ中,酸性条件下NO被Ce4+氧化的产物主要是NO3-和NO2-,请写出生成等物质的量的NO3-和NO2-时的离子方程式
(3)已知进入装置IV的溶液中NO2-的浓度为a mol·L-1,要使1L该溶液中NO2-完全转化为NH4NO3,至少需向装置IV中通入标准状况下的氧气
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】2022年6月,搭载神舟十四号载人飞船的长征二号F遥十四运载火箭,在酒泉卫星发射中心成功发射。火箭用偏二甲肼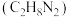 作燃料,四氧化二氮
作燃料,四氧化二氮 作推进剂,点燃后两者反应生成3种常见无污染物质。已知:常温下,
作推进剂,点燃后两者反应生成3种常见无污染物质。已知:常温下, 为无色液体,易溶于水;
为无色液体,易溶于水; 有剧毒,熔点为
有剧毒,熔点为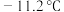 ,沸点为21.2℃。
,沸点为21.2℃。
(1) 的摩尔质量为
的摩尔质量为______ ,请写出 和
和 发生反应的化学方程式:
发生反应的化学方程式:______ , 作
作______ (填“氧化剂”或“还原剂”)。
(2) 与水可发生反应:
与水可发生反应: ,请用双线桥法表示该反应中电子转移的方向和数目:
,请用双线桥法表示该反应中电子转移的方向和数目:______ 。
(3)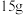
 中含有的N原子数为
中含有的N原子数为______ ,与______ g 中含有的N原子数相同。
中含有的N原子数相同。
(4)常温下,将 a%的
a%的 水溶液跟
水溶液跟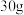 b%的
b%的 水溶液混合,得到的溶液密度为
水溶液混合,得到的溶液密度为 ,设
,设 的摩尔质量为
的摩尔质量为 ,则混合后的溶液中
,则混合后的溶液中 的质量分数为
的质量分数为______ (用含字母的式子表示,下同),混合后溶液的物质的量浓度为______ 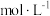 。
。
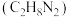 作燃料,四氧化二氮
作燃料,四氧化二氮 作推进剂,点燃后两者反应生成3种常见无污染物质。已知:常温下,
作推进剂,点燃后两者反应生成3种常见无污染物质。已知:常温下, 为无色液体,易溶于水;
为无色液体,易溶于水; 有剧毒,熔点为
有剧毒,熔点为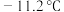 ,沸点为21.2℃。
,沸点为21.2℃。(1)
 的摩尔质量为
的摩尔质量为 和
和 发生反应的化学方程式:
发生反应的化学方程式: 作
作(2)
 与水可发生反应:
与水可发生反应: ,请用双线桥法表示该反应中电子转移的方向和数目:
,请用双线桥法表示该反应中电子转移的方向和数目:(3)
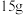
 中含有的N原子数为
中含有的N原子数为 中含有的N原子数相同。
中含有的N原子数相同。(4)常温下,将
 a%的
a%的 水溶液跟
水溶液跟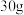 b%的
b%的 水溶液混合,得到的溶液密度为
水溶液混合,得到的溶液密度为 ,设
,设 的摩尔质量为
的摩尔质量为 ,则混合后的溶液中
,则混合后的溶液中 的质量分数为
的质量分数为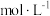 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】完成下列填空
(1)现有下列八种物质:①纯硝酸、②NaHSO4晶体、③熔融的NaCl、④CO2、⑤金属铝、⑥Ba(OH)2固体、⑦氢氧化铁胶体、⑧氨水
a.上述八种物质中,属于电解质且在给定条件下能导电有____ (填序号,下同)。属于非电解质,但溶于水能导电的有___ 。
b.有两种物质在水溶液中反应的离子方程式为H++OH-=H2O,该反应的化学方程式为:___ 。
c.向Ba(OH)2溶液中滴加NaHSO4溶液至溶液呈中性,该反应的离子方程式为:____ 。
(2)向盛有沸水的烧杯中滴加饱和FeCl3溶液,继续加热可制得Fe(OH)3胶体。
①欲验证FeCl3溶液已转化为胶体的实验方法是___ 。
②利用如图所示装置可除去Fe(OH)3胶体中的杂质,实验中需不断____ 。

(3)在室温下,发生下列几种反应:①16H++10Z-+2XO =2X2++5Z2+8H2O②2A2++B2=2A3++2B-③2B-+Z2=B2+2Z-
=2X2++5Z2+8H2O②2A2++B2=2A3++2B-③2B-+Z2=B2+2Z-
a.在溶液中以下反应:8H++5A2++XO =X2++5A3++4H2O能否发生?
=X2++5A3++4H2O能否发生?___ (填“是”或“否”)。
b.要氧化除去含有A2+、Z-、B-混合溶液中的A2+,应加入___ (所需物质在以上方程式中寻找)。
(1)现有下列八种物质:①纯硝酸、②NaHSO4晶体、③熔融的NaCl、④CO2、⑤金属铝、⑥Ba(OH)2固体、⑦氢氧化铁胶体、⑧氨水
a.上述八种物质中,属于电解质且在给定条件下能导电有
b.有两种物质在水溶液中反应的离子方程式为H++OH-=H2O,该反应的化学方程式为:
c.向Ba(OH)2溶液中滴加NaHSO4溶液至溶液呈中性,该反应的离子方程式为:
(2)向盛有沸水的烧杯中滴加饱和FeCl3溶液,继续加热可制得Fe(OH)3胶体。
①欲验证FeCl3溶液已转化为胶体的实验方法是
②利用如图所示装置可除去Fe(OH)3胶体中的杂质,实验中需不断

(3)在室温下,发生下列几种反应:①16H++10Z-+2XO
 =2X2++5Z2+8H2O②2A2++B2=2A3++2B-③2B-+Z2=B2+2Z-
=2X2++5Z2+8H2O②2A2++B2=2A3++2B-③2B-+Z2=B2+2Z-a.在溶液中以下反应:8H++5A2++XO
 =X2++5A3++4H2O能否发生?
=X2++5A3++4H2O能否发生?b.要氧化除去含有A2+、Z-、B-混合溶液中的A2+,应加入
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据要求,回答下列问题:
(1)写出离子反应方程式“Ba2+ + SO = BaSO4↓”对应的化学反应方程式
= BaSO4↓”对应的化学反应方程式__________ 。
(2)反应“2Na + O2 Na2O2”,氧化产物是
Na2O2”,氧化产物是____ ;产物中O的化合价为__ 。
(3)维生素C 又称“抗坏血酸”,能帮助人体将食物中摄取的不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C 具有_____ 。(填氧化性或还原性)
(4)某混合物中可能含有可溶性硫酸盐、碳酸盐及硝酸盐。为了检验其中是否含有硫酸盐,某同学取少量混合物溶于水后,向其中加入_____ 溶液,再加入______ 溶液发现有白色沉淀生成,并由此得出该混合物中含有硫酸盐的结论。
(1)写出离子反应方程式“Ba2+ + SO
 = BaSO4↓”对应的化学反应方程式
= BaSO4↓”对应的化学反应方程式(2)反应“2Na + O2
 Na2O2”,氧化产物是
Na2O2”,氧化产物是(3)维生素C 又称“抗坏血酸”,能帮助人体将食物中摄取的不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C 具有
(4)某混合物中可能含有可溶性硫酸盐、碳酸盐及硝酸盐。为了检验其中是否含有硫酸盐,某同学取少量混合物溶于水后,向其中加入
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】NaClO广泛用作水处理剂及漂白剂。
已知:25℃时NaClO溶液中HClO、ClO-的物质的量分数随pH的分布如下图所示。
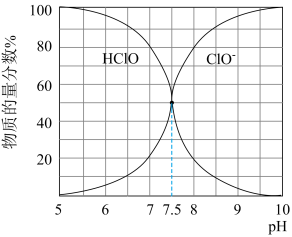
(1)工业上将Cl2通入 的NaOH溶液中制备NaClO。
的NaOH溶液中制备NaClO。
①NaClO属于______ (填“酸”、“盐”、“氧化物”),制备NaClO的离子方程式为_______ 。
②取少量pH=9时的溶液加入稀硫酸,发生离子方程式除了 外,还有
外,还有______ 。
③若反应温度过高会生成副产物NaClO3,写出该反应的离子方程式并用双线桥标明电子转移的方向和数目_______ ,该反应中氧化剂与还原剂的物质的量之比是_____ 。
(2)含NaClO消毒液与洁厕剂(含有盐酸)会产生有毒气体,写出该反应的离子方程式______ 。
已知:25℃时NaClO溶液中HClO、ClO-的物质的量分数随pH的分布如下图所示。

(1)工业上将Cl2通入
 的NaOH溶液中制备NaClO。
的NaOH溶液中制备NaClO。①NaClO属于
②取少量pH=9时的溶液加入稀硫酸,发生离子方程式除了
 外,还有
外,还有③若反应温度过高会生成副产物NaClO3,写出该反应的离子方程式并用双线桥标明电子转移的方向和数目
(2)含NaClO消毒液与洁厕剂(含有盐酸)会产生有毒气体,写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氮元素是植物不可缺少的一种主要营养元素。游离态的N分子不能被大多数植物直接吸收,植物吸收和利用效果最好的是 和
和 。回答下列问题:
。回答下列问题:
(1)氮的固定包含人工固氮和___________ ;人工固氮中工业合成氨的化学方程式为___________ 。
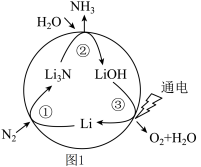
(2)一种新型人工固氮的原理如图1所示,这种固氮方式的总反应方程式为___________ (反应条件省略);反应①②③中属于氧化还原反应的是___________ (填编号)。
(3)碳酸氢铵作肥料时,要遵循“五不施”原则。其中有“烈日当空不施”,原因是___________ (用化学方程式表示)。
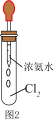
(4)自然界中的微生物也可将氮的化合态NH3转化为游离态的N2,在实验室可用Cl2实现此过程。如图2所示,试管中集满干燥的Cl2,迅速用胶塞塞紧,滴入足量浓氨水。开始时,试管内发生反应:2NH3+3Cl2=N2+6HCl,并产生白烟。白烟的化学式为___________ ,将反应后的试管浸入水中并倒立,在水下打开胶塞,最终进入试管内的水约占试管总体积的___________ 。
 和
和 。回答下列问题:
。回答下列问题:(1)氮的固定包含人工固氮和
(2)一种新型人工固氮的原理如图1所示,这种固氮方式的总反应方程式为

(3)碳酸氢铵作肥料时,要遵循“五不施”原则。其中有“烈日当空不施”,原因是
(4)自然界中的微生物也可将氮的化合态NH3转化为游离态的N2,在实验室可用Cl2实现此过程。如图2所示,试管中集满干燥的Cl2,迅速用胶塞塞紧,滴入足量浓氨水。开始时,试管内发生反应:2NH3+3Cl2=N2+6HCl,并产生白烟。白烟的化学式为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】A、B、C、D、E为中学化学常见的单质或化合物,其相互转化关系如下图所示(反应条件和部分产物已略去)。
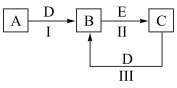
(1)若气体A的水溶液呈碱性,气体B在空气中会变为红棕色,反应II的其中一种产物能引起温室效应。
①A的电子式为___________ 。
②反应I的化学方程式是___________ 。反应II的化学方程式是___________ 。
(2)若A是常用于呼吸面具中的淡黄色固体,D是常见的温室气体,C中的阴、阳离子均为10电子微粒。
①A中阳离子与阴离子的个数比是___________ ;C中所含化学键的类型是___________ 。
②若工业上用E制作漂白粉,写出反应II的离子方程式:___________ 。

(1)若气体A的水溶液呈碱性,气体B在空气中会变为红棕色,反应II的其中一种产物能引起温室效应。
①A的电子式为
②反应I的化学方程式是
(2)若A是常用于呼吸面具中的淡黄色固体,D是常见的温室气体,C中的阴、阳离子均为10电子微粒。
①A中阳离子与阴离子的个数比是
②若工业上用E制作漂白粉,写出反应II的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求写出反应的化学方程式:
(1)木炭加入到热的浓硝酸中有无色和红棕色气体生成_______
(2)加热条件下铜加入到浓硫酸中_______
(3)氯化铵固体和氢氧化钠固体混合加热______
(4)二氧化硫与硫化氢混合有黄色物质生成_______
(1)木炭加入到热的浓硝酸中有无色和红棕色气体生成
(2)加热条件下铜加入到浓硫酸中
(3)氯化铵固体和氢氧化钠固体混合加热
(4)二氧化硫与硫化氢混合有黄色物质生成
您最近一年使用:0次



