NaClO广泛用作水处理剂及漂白剂。
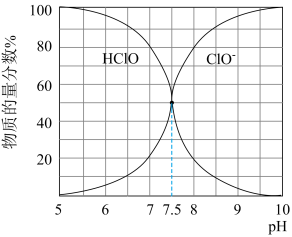
已知:25℃时NaClO溶液中HClO、ClO-的物质的量分数随pH的分布如下图所示。
(1)工业上将Cl2通入 的NaOH溶液中制备NaClO。
的NaOH溶液中制备NaClO。
①NaClO属于______ (填“酸”、“盐”、“氧化物”),制备NaClO的离子方程式为_______ 。
②取少量pH=9时的溶液加入稀硫酸,发生离子方程式除了 外,还有
外,还有______ 。
③若反应温度过高会生成副产物NaClO3,写出该反应的离子方程式并用双线桥标明电子转移的方向和数目_______ ,该反应中氧化剂与还原剂的物质的量之比是_____ 。
(2)含NaClO消毒液与洁厕剂(含有盐酸)会产生有毒气体,写出该反应的离子方程式______ 。
已知:25℃时NaClO溶液中HClO、ClO-的物质的量分数随pH的分布如下图所示。

(1)工业上将Cl2通入
 的NaOH溶液中制备NaClO。
的NaOH溶液中制备NaClO。①NaClO属于
②取少量pH=9时的溶液加入稀硫酸,发生离子方程式除了
 外,还有
外,还有③若反应温度过高会生成副产物NaClO3,写出该反应的离子方程式并用双线桥标明电子转移的方向和数目
(2)含NaClO消毒液与洁厕剂(含有盐酸)会产生有毒气体,写出该反应的离子方程式
更新时间:2024-01-06 10:09:32
|
相似题推荐
【推荐1】Ⅰ.(1)已知反应:①SO3+H2O=H2SO4
②Cl2+H2O=HCl+HClO
③2F2+2H2O=4HF+O2
④2Na+2H2O=2NaOH+H2↑
⑤2Na2O2+2H2O=4NaOH+O2↑
⑥CaCO3+ CO2+H2O= Ca(HCO3)2
上述反应中不属于氧化还原反应的有_________ (填序号,下同);H2O被氧化的是____ ,H2O被还原的是__________ ,属于氧化还原反应,但其中的H2O既不被氧化,又不被还原的是___________ 。
(2)用双线桥表示下列反应电子转移情况
① KClO3 + 6HCl(浓)= KCl + 3Cl2↑+ 3H2O
__________________________________
② 3KOH + P4 + 3H2O = 3KH2PO2 + PH3↑
___________________________________
Ⅱ.(1)配平下列反应方程式
①请将5种物质N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,并配平其反应。__________ +__________ →__________ +__________ +__________ +____ N2O↑
②在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,配平其反应。
____ CuO+___ NH4Cl 
____ Cu+___ CuCl2+___ N2↑+___ H2O。
(2)已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
①含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此时被氧化的离子是_______ ,被氧化的离子的物质的量分别是_______________ 。
②若向含a mol FeI2和b mol FeBr2的溶液中通入c mol Cl2,当I-、Fe2+、Br-完全被氧化时,c为_______ (用含a、b的代数式表示)。
②Cl2+H2O=HCl+HClO
③2F2+2H2O=4HF+O2
④2Na+2H2O=2NaOH+H2↑
⑤2Na2O2+2H2O=4NaOH+O2↑
⑥CaCO3+ CO2+H2O= Ca(HCO3)2
上述反应中不属于氧化还原反应的有
(2)用双线桥表示下列反应电子转移情况
① KClO3 + 6HCl(浓)= KCl + 3Cl2↑+ 3H2O
② 3KOH + P4 + 3H2O = 3KH2PO2 + PH3↑
Ⅱ.(1)配平下列反应方程式
①请将5种物质N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,并配平其反应。
②在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,配平其反应。

(2)已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
①含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此时被氧化的离子是
②若向含a mol FeI2和b mol FeBr2的溶液中通入c mol Cl2,当I-、Fe2+、Br-完全被氧化时,c为
您最近一年使用:0次
【推荐2】实验室里迅速制备少量氯气可利用如下反应:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,此反应不需加热,常温下就可以迅速进行,而且对盐酸的浓度要求不高。
(1)该反应中,氧化剂是________ ,还原剂是________ 。
(2)当参加反应的氧化剂的物质的量是1mol时,被氧化的还原剂的物质的量是________ ,产生的氯气在标准状况下的体积为________ ,电子转移数目为________ 。
(3)氯化氢在该反应过程中表现出的化学性质有________ 。
A 酸性B 还原性C 氧化性D 挥发性
(1)该反应中,氧化剂是
(2)当参加反应的氧化剂的物质的量是1mol时,被氧化的还原剂的物质的量是
(3)氯化氢在该反应过程中表现出的化学性质有
A 酸性B 还原性C 氧化性D 挥发性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】把Cl2通入浓氨水中,发生如下反应:3Cl2 + 8NH3 = 6NH4Cl + N2
(1)用双线桥表示反应的电子转移方向和数目:____ 。
(2)发生化学反应的Cl2与NH3的分子数之比为:__________ ,反应中发生电子转移的Cl2与NH3的分子数之比为:_____ 。
(3)写出NH4Cl在溶液中的电离方程式_________ ,在其溶液中分散质粒子的直径范围为_______ 。
(4)若反应中有6.8克氨发生氧化反应,则反应中生成氮气的质量为_______ 。
(1)用双线桥表示反应的电子转移方向和数目:
(2)发生化学反应的Cl2与NH3的分子数之比为:
(3)写出NH4Cl在溶液中的电离方程式
(4)若反应中有6.8克氨发生氧化反应,则反应中生成氮气的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知1L某溶液中含有FeI2和FeBr2两种溶质,分析知Fe2+、I-、Br-的物质的量比为1:1:1。取出1/10体积该混合溶液进行氧化还原反应滴定。发现吸收3.36L(标况下)的氯气,溶液中的溶质离子刚好完全被氧化到I2、Br2、Fe3+。请回答:
(1)试写出此时先后发生的离子方程式__________ 、__________ 、__________ 。
(2)求混合溶液中各溶质的物质的量浓度______________ 。
(3)若向原混合溶液中通入氯气,当溶液中I-有一半被氧化,通入的氯气在标况下体积约为________ 升?
(4)当溶液中Br-有一半被氧化时,通入的氯气在标况下所占体积又是________ 升?此时溶液中溶质的物质的量浓度约为________ ?
(1)试写出此时先后发生的离子方程式
(2)求混合溶液中各溶质的物质的量浓度
(3)若向原混合溶液中通入氯气,当溶液中I-有一半被氧化,通入的氯气在标况下体积约为
(4)当溶液中Br-有一半被氧化时,通入的氯气在标况下所占体积又是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】三氟化氮(NF3)是一种无色、无味的气体,它是微电子工业技术的关键原料之一。
(1)三氟化氮可由氨气和氟气反应得到:4NH3+3F2=NF3+3NH4F。NH3的电子式为_______ ,反应中氨气显示的化学性质有_____________ ,当有17.0g氨气发生反应时,转移电子的物质的量为_______ 。
(2)在潮湿的空气中,NF3能与水蒸气发生反应,产物有HF、NO和一种酸,则被氧化与被还原元素原子的物质的量之比为___________ ,NF3、F2、NO三种气体氧化性由弱到强的顺序为____________ 。
(3)三氟化氮在空气中泄漏时,很容易被发现,依据的现象是_______________________ 。
(4)NCl3的结构类似NF3,但NCl3中N元素显-3价,NCl3遇水发生反应,且反应为非氧化还原反应,该反应的化学方程式为______________________________ 。
(1)三氟化氮可由氨气和氟气反应得到:4NH3+3F2=NF3+3NH4F。NH3的电子式为
(2)在潮湿的空气中,NF3能与水蒸气发生反应,产物有HF、NO和一种酸,则被氧化与被还原元素原子的物质的量之比为
(3)三氟化氮在空气中泄漏时,很容易被发现,依据的现象是
(4)NCl3的结构类似NF3,但NCl3中N元素显-3价,NCl3遇水发生反应,且反应为非氧化还原反应,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)铁钉在氯气中被锈蚀为棕褐色物质FeCl3,而在盐酸中生成浅绿色的FeCl2溶液。在Cl2、Cl-、H+中,具有氧化性的是____________ ,其中氧化性最强的是____________ 。
(2)盐酸在不同的反应中可以分别表现出酸性、氧化性和还原性。现在有如下三个反应,请写出盐酸在三个反应中分别起何种作用:
①Zn+2HCl===ZnCl2+H2↑____________________ ;
②NaOH+HCl===NaCl+H2O__________________ ;
③2HCl H2↑+Cl2↑
H2↑+Cl2↑________________________ 。
(3)铁钉在氯气中被锈蚀成棕褐色物质FeCl3,而在盐酸中生成浅绿色溶液(FeCl2);向浓盐酸中滴加KMnO4溶液产生淡黄绿色气体(Cl2)。在Cl2、H+、 中,
中,__________________ 氧化性最强。
(4)高锰酸钾与氢溴酸溶液可以发生下列反应:2KMnO4+16HBr===5Br2+2MnBr2+2KBr+8H2O。其中还原剂是________________ 。若消耗15.8 g氧化剂,则被氧化的还原剂的质量是______________ g。HBr的作用是____________________ 。
(2)盐酸在不同的反应中可以分别表现出酸性、氧化性和还原性。现在有如下三个反应,请写出盐酸在三个反应中分别起何种作用:
①Zn+2HCl===ZnCl2+H2↑
②NaOH+HCl===NaCl+H2O
③2HCl
 H2↑+Cl2↑
H2↑+Cl2↑(3)铁钉在氯气中被锈蚀成棕褐色物质FeCl3,而在盐酸中生成浅绿色溶液(FeCl2);向浓盐酸中滴加KMnO4溶液产生淡黄绿色气体(Cl2)。在Cl2、H+、
 中,
中,(4)高锰酸钾与氢溴酸溶液可以发生下列反应:2KMnO4+16HBr===5Br2+2MnBr2+2KBr+8H2O。其中还原剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求答题。
I.写出下列化学反应方程式
(1)工业合成氨_______ 。
(2)浓硝酸见光分解的反应_______ 。
II.用化学知识可以解决环境污染,请回答下列问题:
(3)汽车尾气中的CO、 在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出NO被CO还原的化学方程式:
在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出NO被CO还原的化学方程式:_______ 。
(4)用氨可将氮氧化物转化为无毒气体,例如 ,该反应中氧化产物与还原产物的质量之比为
,该反应中氧化产物与还原产物的质量之比为_______ 。
(5)工业尾气中氮的氧化物常采用碱液吸收法处理。
① 被烧碱溶液吸收时,生成两种钠盐,其物质的量之比为1∶1,写出该反应的化学方程
被烧碱溶液吸收时,生成两种钠盐,其物质的量之比为1∶1,写出该反应的化学方程_______ 。
②NO与 按物质的量之比为1∶1被足量NaOH溶液完全吸收后只得到一种钠盐,该钠盐的化学式是
按物质的量之比为1∶1被足量NaOH溶液完全吸收后只得到一种钠盐,该钠盐的化学式是_______ 。
I.写出下列化学反应方程式
(1)工业合成氨
(2)浓硝酸见光分解的反应
II.用化学知识可以解决环境污染,请回答下列问题:
(3)汽车尾气中的CO、
 在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出NO被CO还原的化学方程式:
在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出NO被CO还原的化学方程式:(4)用氨可将氮氧化物转化为无毒气体,例如
 ,该反应中氧化产物与还原产物的质量之比为
,该反应中氧化产物与还原产物的质量之比为(5)工业尾气中氮的氧化物常采用碱液吸收法处理。
①
 被烧碱溶液吸收时,生成两种钠盐,其物质的量之比为1∶1,写出该反应的化学方程
被烧碱溶液吸收时,生成两种钠盐,其物质的量之比为1∶1,写出该反应的化学方程②NO与
 按物质的量之比为1∶1被足量NaOH溶液完全吸收后只得到一种钠盐,该钠盐的化学式是
按物质的量之比为1∶1被足量NaOH溶液完全吸收后只得到一种钠盐,该钠盐的化学式是
您最近一年使用:0次
【推荐2】高铁酸盐是一种新型、高效、多功能绿色水处理剂,工业上可用湿法制备高铁酸钾: 。
。
(1) 中铁元素的化合价为
中铁元素的化合价为___________ ,在该反应中氧化剂与还原剂的物质的量之比为___________ ,氧化产物是___________ 。
(2)请用双线桥表示反应中电子转移情况:___________ 。
(3)根据化合价,推测 能和下列___________反应(填序号)。
能和下列___________反应(填序号)。
(4)在下列中,水既不作氧化剂又不作还原剂是___________(填序号)。
 。
。(1)
 中铁元素的化合价为
中铁元素的化合价为(2)请用双线桥表示反应中电子转移情况:
(3)根据化合价,推测
 能和下列___________反应(填序号)。
能和下列___________反应(填序号)。| A.KMnO4 | B.SO2 | C.H2S | D.O2 |
A.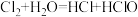 | B. |
C. | D. |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】判断下列实验操作是否正确。
1.保存硫酸亚铁溶液需加入铁钉和少量硫酸。(_______)
2.金属钠保存在装有煤油的玻璃塞广口瓶中。(_______)
3.溴化银固体保存在棕色玻璃塞广口瓶中。(_______)
4.保存浓硝酸需用带橡胶塞的棕色细口瓶。(_______)
5.氢氟酸或浓硝酸存放在带橡胶塞的棕色玻璃瓶中。(_______)
6.汽油或煤油存放在带橡胶塞的棕色玻璃瓶中。(_______)
7.碳酸钠溶液或氢氧化钙溶液存放在配有磨口塞的棕色玻璃瓶中。(_______)
8.氯水或硝酸银溶液存放在配有磨口塞的棕色玻璃瓶中。(_______)
9.取用少量白磷时,应在水中切割白磷,剩余的白磷立即放回原试剂瓶中。(_______)
10.做完铜与浓硫酸反应实验后的试管,立即用大量水冲洗。(_______)
11.取用一小块钠后,剩余的钠放到垃圾桶里。(_______)
12.燃着的酒精灯被打翻,引起失火,应立即用水浇灭。(_______)
13.少量浓硫酸沾在皮肤上,应立即用氢氧化钠溶液冲洗。(_______)
14.用氢气还原氧化铜时,应先通一会儿氢气,再加热氧化铜。(_______)
15.金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理。(_______)
16.有大量的氯气泄漏时,应用肥皂水浸湿的软布捂住鼻孔,并迅速离开现场。(_______)
17.不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上2%~5%的硼酸溶液。(_______)
18.用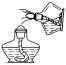 方法点燃酒精灯。(_______)
方法点燃酒精灯。(_______)
19.用 配制硫酸溶液。(_______)
配制硫酸溶液。(_______)
20.用 制备氢气并检验H2的可燃性。(_______)
制备氢气并检验H2的可燃性。(_______)
1.保存硫酸亚铁溶液需加入铁钉和少量硫酸。(_______)
2.金属钠保存在装有煤油的玻璃塞广口瓶中。(_______)
3.溴化银固体保存在棕色玻璃塞广口瓶中。(_______)
4.保存浓硝酸需用带橡胶塞的棕色细口瓶。(_______)
5.氢氟酸或浓硝酸存放在带橡胶塞的棕色玻璃瓶中。(_______)
6.汽油或煤油存放在带橡胶塞的棕色玻璃瓶中。(_______)
7.碳酸钠溶液或氢氧化钙溶液存放在配有磨口塞的棕色玻璃瓶中。(_______)
8.氯水或硝酸银溶液存放在配有磨口塞的棕色玻璃瓶中。(_______)
9.取用少量白磷时,应在水中切割白磷,剩余的白磷立即放回原试剂瓶中。(_______)
10.做完铜与浓硫酸反应实验后的试管,立即用大量水冲洗。(_______)
11.取用一小块钠后,剩余的钠放到垃圾桶里。(_______)
12.燃着的酒精灯被打翻,引起失火,应立即用水浇灭。(_______)
13.少量浓硫酸沾在皮肤上,应立即用氢氧化钠溶液冲洗。(_______)
14.用氢气还原氧化铜时,应先通一会儿氢气,再加热氧化铜。(_______)
15.金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理。(_______)
16.有大量的氯气泄漏时,应用肥皂水浸湿的软布捂住鼻孔,并迅速离开现场。(_______)
17.不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上2%~5%的硼酸溶液。(_______)
18.用
 方法点燃酒精灯。(_______)
方法点燃酒精灯。(_______)19.用
 配制硫酸溶液。(_______)
配制硫酸溶液。(_______)20.用
 制备氢气并检验H2的可燃性。(_______)
制备氢气并检验H2的可燃性。(_______)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Cl2通入70℃的NaOH水溶液中,发生氧化—还原反应,反应完成后,测得溶液中NaClO与NaClO3的物质的量之比为4∶1,则:
(1)配平溶液中所发生反应的化学方程式:____ Cl2+______ NaOH=____ NaCl+____ NaClO3+_____ NaClO+____ ____
(2)反应中的氧化产物为_________________ 。
(3)已知生成0.1mol NaClO,反应中转移的电子总数是__________ mol,若溶液的体积正好为100mL,则溶液中NaCl的物质的量浓度为________ mol/L。
(1)配平溶液中所发生反应的化学方程式:
(2)反应中的氧化产物为
(3)已知生成0.1mol NaClO,反应中转移的电子总数是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某工厂在山坡坑道的仓库里贮有氯气钢瓶。某天,有一只贮有氯气的钢瓶损坏,造成氯气泄漏,在场工人采取以下措施,请选择。
(1)①处理该钢瓶的方法正确的是_______ 。
A.钢瓶推到坡下的小河里 B.把钢瓶丢到深坑里,用石灰填埋 C.把钢瓶扔到农田中
②若在场工人没有防毒面具,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是_______ 。
A.NaOH B.NaCl C.Na2CO3
(2)为了探究HClO的漂白性,某同学设计了如图的实验:

①将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是_______ ;氯水可作为漂白剂,起主要作用的是氯水中含有的_______ (用化学式表示)。
②为防止氯气尾气污染空气,可用NaOH溶液吸收多余的氯气,原理是_______ (化学方程式);根据这一原理,工业上常用廉价的石灰乳吸收制得漂白粉,漂白粉的有效成分是_______ (填化学式)。
(1)①处理该钢瓶的方法正确的是
A.钢瓶推到坡下的小河里 B.把钢瓶丢到深坑里,用石灰填埋 C.把钢瓶扔到农田中
②若在场工人没有防毒面具,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是
A.NaOH B.NaCl C.Na2CO3
(2)为了探究HClO的漂白性,某同学设计了如图的实验:

①将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是
②为防止氯气尾气污染空气,可用NaOH溶液吸收多余的氯气,原理是
您最近一年使用:0次



