完成下列问题。
(1)现有以下物质:①NaCl晶体;②干冰;③液态的醋酸;④铜;⑤BaSO4固体;⑥蔗糖;⑦酒精;⑧熔融的KNO3;⑨HCl。以上物质能导电的是___________ ;以上物质属于电解质的是___________ 。
(2)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C 具有___________ (填“氧化性”或“还原性”)。
(3)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2,该反应的还原剂是___________ ,氧化剂是___________ 。
(4)查阅资料可知,铜和浓H2SO4共热,发生反应Cu+ 2H2SO4(浓) CuSO4+SO2↑+2H2O,该反应中氧化剂与还原剂的个数之比为
CuSO4+SO2↑+2H2O,该反应中氧化剂与还原剂的个数之比为___________ ,其中H2SO4在反应中表现___________ 。
(5)请配平反应方程式:____K2Cr2O7+____HCl _____KCl+____CrCl3+____Cl2+____H2O,
_____KCl+____CrCl3+____Cl2+____H2O,______ ,若反应中发生氧化反应的HCl个数为12,则反应中转移的电子数为___________ 个。
(1)现有以下物质:①NaCl晶体;②干冰;③液态的醋酸;④铜;⑤BaSO4固体;⑥蔗糖;⑦酒精;⑧熔融的KNO3;⑨HCl。以上物质能导电的是
(2)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C 具有
(3)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2,该反应的还原剂是
(4)查阅资料可知,铜和浓H2SO4共热,发生反应Cu+ 2H2SO4(浓)
 CuSO4+SO2↑+2H2O,该反应中氧化剂与还原剂的个数之比为
CuSO4+SO2↑+2H2O,该反应中氧化剂与还原剂的个数之比为(5)请配平反应方程式:____K2Cr2O7+____HCl
 _____KCl+____CrCl3+____Cl2+____H2O,
_____KCl+____CrCl3+____Cl2+____H2O,
更新时间:2023-10-21 07:27:38
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】碳酸钠俗称纯碱,用途非常广泛,我国化学家侯德榜发明了“侯氏制碱法”,其具体流程如下,请回答下列问题:
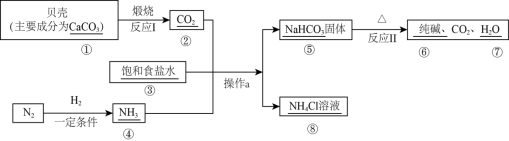
(1)图中涉及的①~⑧八种物质中,能导电的物质有_______ (填序号,下同),属于电解质的有_______ 。
(2)反应Ⅱ的化学方程式为_______ 。
(3)用离子方程式表示操作a制备NaHCO3的原理:_______ 。
(4)若向NaHCO3溶液中加入足量的Ba(OH)2,该反应的离子方程式为_______ 。
(5)若称取10.5g纯净的NaHCO3固体,加热一段时间后,剩余固体的质量为8.02g。如果把剩余的固体全部加入到含0.2mol HCl的盐酸中充分反应。求反应后溶液中剩余的H+的物质的量_______ (忽略因水电离产生的H+)。

(1)图中涉及的①~⑧八种物质中,能导电的物质有
(2)反应Ⅱ的化学方程式为
(3)用离子方程式表示操作a制备NaHCO3的原理:
(4)若向NaHCO3溶液中加入足量的Ba(OH)2,该反应的离子方程式为
(5)若称取10.5g纯净的NaHCO3固体,加热一段时间后,剩余固体的质量为8.02g。如果把剩余的固体全部加入到含0.2mol HCl的盐酸中充分反应。求反应后溶液中剩余的H+的物质的量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】以下为中学化学中常见的几种物质;①熔融KNO3;②醋酸;③C2H5OH;④CO2;⑤蔗糖;⑥5%的酒精;⑦KHCO3;⑧NaOH溶液;⑨稀盐酸;⑩Fe.回答下列问题:
(1)上述物质中属于电解质的有___________ (填序号,下同);属于非电解质的有___________ ;上述条件下能导电的有___________ ,写出⑦在水溶液中的电离方程式___________ 。
(2)已知写出下列反应的离子方程式:已知将SO2通入澄清石灰水的现象与CO2完全相同,也是先生成沉淀后沉淀溶解,请依次写出将SO2通入澄清石灰水至过量时生成沉淀和沉淀溶解的离子方程式___________ 、___________ 。
(3)碱式碳酸铜Cu2(OH)2CO3可以看作是Cu(OH)2和CuCO3按照1:1的比例组成的混合型化合物,写出它与足量盐酸反应的化学方程式:___________ 。
(4)已知Cl2O与CO2类似,都是可溶性酸性氧化物。由此可判断Cl2O与NaOH溶液反应生成的盐为___________
A. NaClO B. NaClO2 C.NaClO3
写出Cl2O与水反应的化学方程式___________ 。
(1)上述物质中属于电解质的有
(2)已知写出下列反应的离子方程式:已知将SO2通入澄清石灰水的现象与CO2完全相同,也是先生成沉淀后沉淀溶解,请依次写出将SO2通入澄清石灰水至过量时生成沉淀和沉淀溶解的离子方程式
(3)碱式碳酸铜Cu2(OH)2CO3可以看作是Cu(OH)2和CuCO3按照1:1的比例组成的混合型化合物,写出它与足量盐酸反应的化学方程式:
(4)已知Cl2O与CO2类似,都是可溶性酸性氧化物。由此可判断Cl2O与NaOH溶液反应生成的盐为
A. NaClO B. NaClO2 C.NaClO3
写出Cl2O与水反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】NaHSO4通常为晶体,易溶于水,它溶于水时电离出三种不同的离子,溶液显酸性。NaHSO4受热熔化时只能电离出两种不同的离子。
(1)NaHSO4在水溶液中的电离方程式为_____________________ 。
(2)NaHSO4在熔融状态下的电离方程式为_________________ 。
(3)下列说法中正确的是________(填字母)。
(4)NaHCO3在水溶液中只电离出两种不同的离子,其电离方程式为_______ 。
(1)NaHSO4在水溶液中的电离方程式为
(2)NaHSO4在熔融状态下的电离方程式为
(3)下列说法中正确的是________(填字母)。
| A.NaHSO4属于酸 |
| B.NaHSO4属于盐 |
| C.NaHSO4属于电解质 |
| D.NaHSO4溶液能与Zn反应生成氢气 |
您最近一年使用:0次
【推荐1】氧化还原反应原理在研究物质性质及方面具有重要价值。
(1)化合价是学习氧化还原反应的基础。写出以下几种物质中加点元素的化合价。
NaC l_________ 、H2O 2___________ 、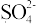
_____________ 、I 2____________ 。
(2)氨催化氧化制硝酸的反应是4NH3+5O2 4NO+6H2O,该反应中,氧化剂是
4NO+6H2O,该反应中,氧化剂是______ (填化学式,下同),被氧化的物质是_________ 。若反应中消耗了4molNH3,则生成NO的物质的量为______ mol。
(1)化合价是学习氧化还原反应的基础。写出以下几种物质中加点元素的化合价。
Na
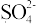
(2)氨催化氧化制硝酸的反应是4NH3+5O2
 4NO+6H2O,该反应中,氧化剂是
4NO+6H2O,该反应中,氧化剂是
您最近一年使用:0次
【推荐2】(I)有以下10种物质,请回答下列问题:(填序号)
①石墨 ②氯化钠 ③蔗糖 ④稀硫酸 ⑤NaHSO4溶液 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧冰醋酸 ⑨氯化氢 ⑩铜
(1)其中能导电的是_______ ;属于电解质的是______ ;属于非电解质的是_______ 。
(2)写出物质④和⑦反应的离子方程式:___________ 。
(3)写出过量的物质⑦和少量的物质⑤发生反应的离子方程式:_________ 。
(II)用一种试剂除去下列各物质中的杂质(括号内的物质)。写出所用试剂及离子方程式。
(1)NaCl溶液(Na2CO3):试剂_______ 离子方程式_____________ 。
(2)FeSO4溶液(CuSO4):试剂_______ 离子方程式_____________ 。
(III)
(1)K2FeO4可用作水处理剂,它可由以下反应制得:
3Cl2+2Fe(OH)3+10KOH=2K2FeO4+6KCl+8H2O,当有1mol K2FeO4生成时转移的电子数目为________ 。
(2)4NH3+6NO=5N2+6H2O反应中氧化产物和还原产物物质的量之比为________ 。
①石墨 ②氯化钠 ③蔗糖 ④稀硫酸 ⑤NaHSO4溶液 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧冰醋酸 ⑨氯化氢 ⑩铜
(1)其中能导电的是
(2)写出物质④和⑦反应的离子方程式:
(3)写出过量的物质⑦和少量的物质⑤发生反应的离子方程式:
(II)用一种试剂除去下列各物质中的杂质(括号内的物质)。写出所用试剂及离子方程式。
(1)NaCl溶液(Na2CO3):试剂
(2)FeSO4溶液(CuSO4):试剂
(III)
(1)K2FeO4可用作水处理剂,它可由以下反应制得:
3Cl2+2Fe(OH)3+10KOH=2K2FeO4+6KCl+8H2O,当有1mol K2FeO4生成时转移的电子数目为
(2)4NH3+6NO=5N2+6H2O反应中氧化产物和还原产物物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知反应:Ⅰ .2K2CrO4+ H2SO4=K2Cr2O7+ K2SO4+ H2O
Ⅱ. Fe2(SO4)3+ 2HI =2FeSO4+ I2+ H2SO4
Ⅲ .K2Cr2O7+ 6FeSO4+7 H2SO4=3 Fe2(SO4)3+ Cr2(SO4)3+ K2SO4+ 7H2O
(1)上述三个反应中,属于非氧化还原反应的是____________ (填序号);
(2)Fe2(SO4)3、K2Cr2O7、I2的氧化性由强到弱的顺序为__________________________ ;
(3)反应Ⅱ中的还原产物是_________________________ ;
(4)在下式中标出电子转移的方向和数目:K2Cr2O7+ 6FeSO4+ 7H2SO4→________
(5)若用K2Cr2O7与HI反应,每生成12.7g I2生成,转移电子_______________ 个。
Ⅱ. Fe2(SO4)3+ 2HI =2FeSO4+ I2+ H2SO4
Ⅲ .K2Cr2O7+ 6FeSO4+7 H2SO4=3 Fe2(SO4)3+ Cr2(SO4)3+ K2SO4+ 7H2O
(1)上述三个反应中,属于非氧化还原反应的是
(2)Fe2(SO4)3、K2Cr2O7、I2的氧化性由强到弱的顺序为
(3)反应Ⅱ中的还原产物是
(4)在下式中标出电子转移的方向和数目:K2Cr2O7+ 6FeSO4+ 7H2SO4→
(5)若用K2Cr2O7与HI反应,每生成12.7g I2生成,转移电子
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】I.现有9种物质:①Na;②盐酸;③ ;④
;④ ;⑤空气;⑥
;⑤空气;⑥ ;⑦
;⑦ 胶体;⑧Na2O2;⑨CO
胶体;⑧Na2O2;⑨CO
(1)属于电解质的是_______ (用序号填空,下同);属于酸性氧化物的是_______ 。
(2)实验室中少量①通常保存在_____ 中;④在工业上大量用于_____ (写出一种用途即可)。
(3)⑧与⑥反应的化学方程式_______
(4)③是一种白色晶体,因受热易分解并产生气体适宜作膨松剂,请写出此物质受热分解的化学方程式_______ 。
Ⅱ.某种飞船以联氨 和
和 为动力源,发生反应:
为动力源,发生反应: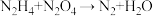 ,反应温度可高达
,反应温度可高达 ,回答下列问题。
,回答下列问题。
(5)①配平该方程式_______ 。
②该反应中,氧化产物与还原产物的质量之比为_______ 。
 ;④
;④ ;⑤空气;⑥
;⑤空气;⑥ ;⑦
;⑦ 胶体;⑧Na2O2;⑨CO
胶体;⑧Na2O2;⑨CO(1)属于电解质的是
(2)实验室中少量①通常保存在
(3)⑧与⑥反应的化学方程式
(4)③是一种白色晶体,因受热易分解并产生气体适宜作膨松剂,请写出此物质受热分解的化学方程式
Ⅱ.某种飞船以联氨
 和
和 为动力源,发生反应:
为动力源,发生反应: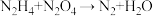 ,反应温度可高达
,反应温度可高达 ,回答下列问题。
,回答下列问题。(5)①配平该方程式
②该反应中,氧化产物与还原产物的质量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。
(1)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原
反应的关系”可用如图表达。
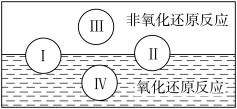
试写出有水参加的符合反应类型Ⅳ的一个化学方程式:_____________________________ ,其中水为________ 剂。
(2)氯化铵常用作焊接。如:在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为:___ CuO+____ NH4Cl 
____ Cu+____ CuCl2+____ N2↑+____ H2O。
①配平此氧化还原反应方程式。
②该反应中,被氧化的元素是______ (填元素名称),氧化剂是________ (填化学式)。
③反应中若产生0.2mol的气体,则有________ mol的电子转移。
(1)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原
反应的关系”可用如图表达。

试写出有水参加的符合反应类型Ⅳ的一个化学方程式:
(2)氯化铵常用作焊接。如:在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为:

①配平此氧化还原反应方程式。
②该反应中,被氧化的元素是
③反应中若产生0.2mol的气体,则有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】饮用水中常见的污染物有三氯乙酸(CCl3COOH)、 NO 等,难以直接氧化降解,可通过Fe/Cu微电池法、芬顿法等方法将污染物除去。
等,难以直接氧化降解,可通过Fe/Cu微电池法、芬顿法等方法将污染物除去。
(1)pH=4时,向含有三氯乙酸的水样中投入铁屑和铜屑,通过原电池反应生成的活性氢原子(H)将CCl3COOH脱氯后转化为CHCl2COOH。
①写出活性氢原子(H)与CCl3COOH反应的离子方程式:_______ 。
②铁屑和铜屑的总质量一定,改变铁屑和铜屑的质量比,水样中单位时间三氯乙酸的脱氯率如图1所示,当 大于4时,铁屑质量越大,脱氯率越低的原因是
大于4时,铁屑质量越大,脱氯率越低的原因是_______ 。

(2)取上述反应后的溶液,向其中加入H2O2,发生如图2所示转化,生成羟基自由基(·OH),·OH能将溶液中的CHCl2COOH等物质进一步脱氯除去。

①写出图2所示转化中反应Ⅱ的离子方程式:_______ 。
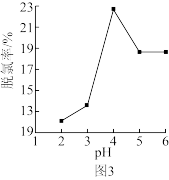
②控制水样的pH不同,所得脱氯率如图3所示,当pH>4后,脱氯率逐渐下降的原因是_______ 。
(3)石墨烯负载纳米铁能迅速有效地还原污水中的NO ,纳米铁还原废水中NO
,纳米铁还原废水中NO 的可能反应机理如图所示。
的可能反应机理如图所示。

①纳米铁还原NO 的过程可描述为
的过程可描述为_______ 。
②经检验,污水经处理后,水体中NO 、NO
、NO 浓度很小,但水中总氮浓度下降不明显,原因是
浓度很小,但水中总氮浓度下降不明显,原因是_______ 。
 等,难以直接氧化降解,可通过Fe/Cu微电池法、芬顿法等方法将污染物除去。
等,难以直接氧化降解,可通过Fe/Cu微电池法、芬顿法等方法将污染物除去。(1)pH=4时,向含有三氯乙酸的水样中投入铁屑和铜屑,通过原电池反应生成的活性氢原子(H)将CCl3COOH脱氯后转化为CHCl2COOH。
①写出活性氢原子(H)与CCl3COOH反应的离子方程式:
②铁屑和铜屑的总质量一定,改变铁屑和铜屑的质量比,水样中单位时间三氯乙酸的脱氯率如图1所示,当
 大于4时,铁屑质量越大,脱氯率越低的原因是
大于4时,铁屑质量越大,脱氯率越低的原因是
(2)取上述反应后的溶液,向其中加入H2O2,发生如图2所示转化,生成羟基自由基(·OH),·OH能将溶液中的CHCl2COOH等物质进一步脱氯除去。

①写出图2所示转化中反应Ⅱ的离子方程式:
②控制水样的pH不同,所得脱氯率如图3所示,当pH>4后,脱氯率逐渐下降的原因是

(3)石墨烯负载纳米铁能迅速有效地还原污水中的NO
 ,纳米铁还原废水中NO
,纳米铁还原废水中NO 的可能反应机理如图所示。
的可能反应机理如图所示。
①纳米铁还原NO
 的过程可描述为
的过程可描述为②经检验,污水经处理后,水体中NO
 、NO
、NO 浓度很小,但水中总氮浓度下降不明显,原因是
浓度很小,但水中总氮浓度下降不明显,原因是
您最近一年使用:0次



