氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。
(1)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原
反应的关系”可用如图表达。
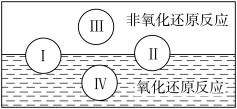
试写出有水参加的符合反应类型Ⅳ的一个化学方程式:_____________________________ ,其中水为________ 剂。
(2)氯化铵常用作焊接。如:在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为:___ CuO+____ NH4Cl 
____ Cu+____ CuCl2+____ N2↑+____ H2O。
①配平此氧化还原反应方程式。
②该反应中,被氧化的元素是______ (填元素名称),氧化剂是________ (填化学式)。
③反应中若产生0.2mol的气体,则有________ mol的电子转移。
(1)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原
反应的关系”可用如图表达。

试写出有水参加的符合反应类型Ⅳ的一个化学方程式:
(2)氯化铵常用作焊接。如:在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为:

①配平此氧化还原反应方程式。
②该反应中,被氧化的元素是
③反应中若产生0.2mol的气体,则有
更新时间:2019-11-14 19:30:19
|
相似题推荐
【推荐1】氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是____ (填写字母代号)

A.图A是煤的形成
B. 图B是卫星上的太阳能电池工作
C. 图C是简单机械织布
D. 图D是我国古代烧制陶器
(2)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”可用如图表达。

试写出有水参加的符合反应类型Ⅳ的一个化学方程式:_____ ,其中水为______ 剂。
(3)过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称;如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O2+H2O=A+NH3↑,试指出生成物A的化学式为___ ,并阐明H2O2被称为绿色氧化剂的理由是_______ 。
(4)氯化铵常用作焊接。如:在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为:____ CuO+___ NH4Cl
____ Cu+___ CuCl2+___ N2↑+___ H2O。
①配平此氧化还原反应方程式。
②该反应中,被氧化的元素是______ (填元素名称),氧化剂是____ (填化学式)。
③反应中若产生0.2mol的气体,则有_____ mol的电子转移。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是

A.图A是煤的形成
B. 图B是卫星上的太阳能电池工作
C. 图C是简单机械织布
D. 图D是我国古代烧制陶器
(2)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”可用如图表达。

试写出有水参加的符合反应类型Ⅳ的一个化学方程式:
(3)过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称;如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O2+H2O=A+NH3↑,试指出生成物A的化学式为
(4)氯化铵常用作焊接。如:在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为:

①配平此氧化还原反应方程式。
②该反应中,被氧化的元素是
③反应中若产生0.2mol的气体,则有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】离子反应是中学化学中重要的反应类型,请回答下列问题:
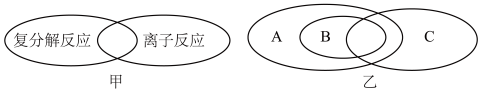
(1)人们常用图示的方法表示不同反应类型之间的关系,如复分解反应和离子反应可表示为下甲图。下乙图为离子反应、氧化还原反应和置换反应三者之间的关系。则表示离子反应、氧化还原反应、置换反应的字母分别是___________ 。
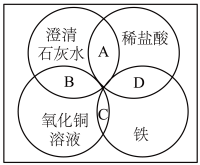
(2)铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见物质,四种物质间的反应关系如图所示,图中两圆相交部分(A、B、C、D)表示物质间的反应,请写出对应反应的离子方程式:
A:___________
B:___________
C:___________
D:___________
(3)离子方程式是重要的化学用语,下列是有关离子方程式的一些错误观点,请在下列表格中用相应的”离子方程式”否定这些观点,反应物从下列物质中选取︰ 。
。
(1)人们常用图示的方法表示不同反应类型之间的关系,如复分解反应和离子反应可表示为下甲图。下乙图为离子反应、氧化还原反应和置换反应三者之间的关系。则表示离子反应、氧化还原反应、置换反应的字母分别是

(2)铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见物质,四种物质间的反应关系如图所示,图中两圆相交部分(A、B、C、D)表示物质间的反应,请写出对应反应的离子方程式:
A:
B:
C:
D:

(3)离子方程式是重要的化学用语,下列是有关离子方程式的一些错误观点,请在下列表格中用相应的”离子方程式”否定这些观点,反应物从下列物质中选取︰
 。
。| 错误观点 | 离子程式 | |
| ① | 所有的离子方程式均可以表示一类反应 | |
| ② | 所有酸碱中和反应均可表示为: |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氧化还原反应在高中化学中是一类重要的反应类型。 、
、 、
、 、
、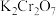 是中学化学中常用的氧化剂。回答下列问题:
是中学化学中常用的氧化剂。回答下列问题:
(1)下列基本反应类型中一定属于氧化还原反应的是___________(填字母)。
(2)实验室迅速制备少量氯气可利用如下反应:
 。上述反应中被氧化的元素为
。上述反应中被氧化的元素为___________ (填元素符号);还原产物为___________ (填化学式)。
(3) 溶液能与Cu反应制作印刷电路板,其制作原理可用
溶液能与Cu反应制作印刷电路板,其制作原理可用 表示。
表示。
①上式中X的化学式为___________ 。
②若有32g铜被氧化,则参与反应的 的质量为
的质量为___________ g。
③该反应的离子方程式为___________ 。
(4)已知方程式: 。用双线桥法标出电子转移的方向和数目
。用双线桥法标出电子转移的方向和数目___________ 。
(5)某反应的反应物与生成物有 、KCl、
、KCl、 、
、 、HCl(浓)、
、HCl(浓)、 ,已知氧化性:
,已知氧化性: ,写出并配平该化学方程式:
,写出并配平该化学方程式:___________ 。
 、
、 、
、 、
、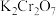 是中学化学中常用的氧化剂。回答下列问题:
是中学化学中常用的氧化剂。回答下列问题:(1)下列基本反应类型中一定属于氧化还原反应的是___________(填字母)。
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |

 。上述反应中被氧化的元素为
。上述反应中被氧化的元素为(3)
 溶液能与Cu反应制作印刷电路板,其制作原理可用
溶液能与Cu反应制作印刷电路板,其制作原理可用 表示。
表示。①上式中X的化学式为
②若有32g铜被氧化,则参与反应的
 的质量为
的质量为③该反应的离子方程式为
(4)已知方程式:
 。用双线桥法标出电子转移的方向和数目
。用双线桥法标出电子转移的方向和数目(5)某反应的反应物与生成物有
 、KCl、
、KCl、 、
、 、HCl(浓)、
、HCl(浓)、 ,已知氧化性:
,已知氧化性: ,写出并配平该化学方程式:
,写出并配平该化学方程式:
您最近一年使用:0次
【推荐1】医学上常用酸性高锰酸钾溶液和草酸溶液的反应来测定血钙的含量。回答下列问题:
( ) H++( ) MnO4-+( ) H2C2O4→( ) CO2↑+ ( ) Mn2++( ) ____
(1)配平以上离子方程式,并在横线中填上所需的微粒。
(2)该反应中的还原剂是_____________ (填化学式)。
(3)反应转移了0.4 mol电子,则消耗KMnO4的物质的量为_________ mol。
(4)测定血钙含量的方法是:取2.0mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①稀硫酸溶解CaC2O4沉淀的化学方程式是__________________________ 。
②溶解沉淀时______ (填“能”或“不能”)用稀盐酸,原因是________________ 。
③若消耗了1.0×10-4 mol·L-1的KMnO4溶液20.00 mL,则100 mL该血液中含钙_____ g。
(5)草酸系统命名为乙二酸,请写出乙二酸的结构简式_____________________ 。
(6)已知:Ka1(H2C2O4)=5.9×10—2,Ka2(H2C2O4)=6.4×10—5;Ka(HF)=3.53×10—4,请写出足量草酸(H2C2O4)与NaF溶液反应的化学方程式:______ 。
(1)配平以上离子方程式,并在横线中填上所需的微粒。
(2)该反应中的还原剂是
(3)反应转移了0.4 mol电子,则消耗KMnO4的物质的量为
(4)测定血钙含量的方法是:取2.0mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①稀硫酸溶解CaC2O4沉淀的化学方程式是
②溶解沉淀时
③若消耗了1.0×10-4 mol·L-1的KMnO4溶液20.00 mL,则100 mL该血液中含钙
(5)草酸系统命名为乙二酸,请写出乙二酸的结构简式
(6)已知:Ka1(H2C2O4)=5.9×10—2,Ka2(H2C2O4)=6.4×10—5;Ka(HF)=3.53×10—4,请写出足量草酸(H2C2O4)与NaF溶液反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】NOx是空气的污染物,废水中的氨氮(以NH3、NH 存在)和硝态氮(以NO
存在)和硝态氮(以NO 、NO
、NO 存在)会引起水体富营养化,需经处理后才能排放。
存在)会引起水体富营养化,需经处理后才能排放。
(1)电解氧化吸收法可将废气中的 NOx转变为NO 。电解 0.1 mol·L-1NaCl 溶液时,溶液中相关成分的浓度变化与电流强度的关系如图-1 所示。向 0.1 mol·L-1NaCl 溶液中通入 NO,测得电流强度与 NO 的脱除率的关系如图-2 所示。
。电解 0.1 mol·L-1NaCl 溶液时,溶液中相关成分的浓度变化与电流强度的关系如图-1 所示。向 0.1 mol·L-1NaCl 溶液中通入 NO,测得电流强度与 NO 的脱除率的关系如图-2 所示。
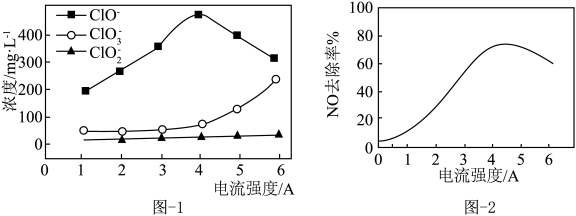
①电解NaCl溶液作吸收液时,若电流强度为4A,吸收NO 的反应离子方程式为_______ 。
②当电流强度大于 4A 后,NO去除率下降,其原因是_______ 。
(2)某氮肥厂处理氨氮废水的方案如图,回答下列问题:
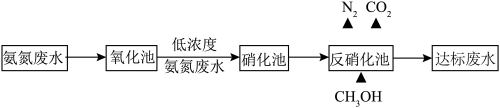
①“氧化池”中可用活性炭—臭氧可处理高浓度氨氮废水。氧化机理如图-3 所示。*表示吸附在活性炭表面的物种,·OH 为羟基自由基。其它条件不变,调节 pH,废水中氨氮去除率随 pH 的变化如图-4 所示。随 pH 增大氨氮去除率先明显增大后变化较小的可能原因是_______ 。

②“反硝化池”中发生的变化为:HNO3→ →N2。1 mol HNO3完全转化理论上消耗甲醇的质量为
→N2。1 mol HNO3完全转化理论上消耗甲醇的质量为_______ 。
(3)纳米Fe 可还原去除水中的硝酸盐污染物。
已知:i.纳米 Fe 具有很高的活性,易被氧化使表面形成氧化层
ii.纳米 Fe 将 还原为
还原为 的转化关系如下:
的转化关系如下:





①纳米 Fe 的制备原理:FeSO4+2NaBH4+6H2O=2B(OH)3+Fe+7H2↑+Na2SO4; 已知电负性 H>B,则该反应中氧化剂是_______ (填化学式) 。
②检验还原后的溶液中存在 的实验方法是
的实验方法是_______ 。
③溶液初始 pH 较低有利于 的去除,其可能的原因是
的去除,其可能的原因是_______ 。
 存在)和硝态氮(以NO
存在)和硝态氮(以NO 、NO
、NO 存在)会引起水体富营养化,需经处理后才能排放。
存在)会引起水体富营养化,需经处理后才能排放。(1)电解氧化吸收法可将废气中的 NOx转变为NO
 。电解 0.1 mol·L-1NaCl 溶液时,溶液中相关成分的浓度变化与电流强度的关系如图-1 所示。向 0.1 mol·L-1NaCl 溶液中通入 NO,测得电流强度与 NO 的脱除率的关系如图-2 所示。
。电解 0.1 mol·L-1NaCl 溶液时,溶液中相关成分的浓度变化与电流强度的关系如图-1 所示。向 0.1 mol·L-1NaCl 溶液中通入 NO,测得电流强度与 NO 的脱除率的关系如图-2 所示。
①电解NaCl溶液作吸收液时,若电流强度为4A,吸收NO 的反应离子方程式为
②当电流强度大于 4A 后,NO去除率下降,其原因是
(2)某氮肥厂处理氨氮废水的方案如图,回答下列问题:

①“氧化池”中可用活性炭—臭氧可处理高浓度氨氮废水。氧化机理如图-3 所示。*表示吸附在活性炭表面的物种,·OH 为羟基自由基。其它条件不变,调节 pH,废水中氨氮去除率随 pH 的变化如图-4 所示。随 pH 增大氨氮去除率先明显增大后变化较小的可能原因是

②“反硝化池”中发生的变化为:HNO3→
 →N2。1 mol HNO3完全转化理论上消耗甲醇的质量为
→N2。1 mol HNO3完全转化理论上消耗甲醇的质量为(3)纳米Fe 可还原去除水中的硝酸盐污染物。
已知:i.纳米 Fe 具有很高的活性,易被氧化使表面形成氧化层
ii.纳米 Fe 将
 还原为
还原为 的转化关系如下:
的转化关系如下:




①纳米 Fe 的制备原理:FeSO4+2NaBH4+6H2O=2B(OH)3+Fe+7H2↑+Na2SO4; 已知电负性 H>B,则该反应中氧化剂是
②检验还原后的溶液中存在
 的实验方法是
的实验方法是③溶液初始 pH 较低有利于
 的去除,其可能的原因是
的去除,其可能的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】在高锰酸钾固体上滴加浓盐酸,马上产生黄绿色气体。反应的化学方程式为:2KMnO4 + 16HCl=2KC1 + 2MnCl2 + 5C12↑+ 8H2O
回答下列问题:
(1)此反应中的氧化剂是____ ,当在标准状况下产生0.112L氯气,转移的电子数为____ mol。
(2)氯原子的核电荷数为______ ;氧原子的原子结构示意图_______ 。
(3)在KC1固体中存在的化学键是__________ ;写出H2O电子式_________ 。
(4)工业上用氯气与消石灰作原料制造漂粉精,此反应的化学方程式是_________ 。
(5)浓盐酸的溶质是氯化氢,用一个实验证明氯化氢极易溶于水。_________ 。
回答下列问题:
(1)此反应中的氧化剂是
(2)氯原子的核电荷数为
(3)在KC1固体中存在的化学键是
(4)工业上用氯气与消石灰作原料制造漂粉精,此反应的化学方程式是
(5)浓盐酸的溶质是氯化氢,用一个实验证明氯化氢极易溶于水。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】《我在故宫修文物》展示了专家精湛的技艺和对传统文化的热爱与坚守,也令人体会到化学方法在文物保护中的巨大作用。某博物馆修复出土铁器的过程如下:
(1)检测锈蚀产物
铁器在具有O2、________ 等环境中容易被腐蚀。
(2)分析腐蚀原理:一般认为,铁经过了如下腐蚀循环。
Ⅰ.Fe转化为Fe2+。
Ⅱ. FeO(OH)和Fe2+反应形成致密的Fe3O4保护层,Fe2+的作用是____ (填字母)。
a.氧化剂 b.还原剂 c.既不是氧化剂也不是还原剂
(3)研究发现,Cl-对铁的腐蚀会造成严重影响。化学修复:脱氯、还原,形成Fe3O4保护层,方法如下:
将铁器浸没在盛有0.5 mol·L-1 Na2SO3、0.5 mol·L-1 NaOH溶液的容器中,缓慢加热至60~90 ℃。一段时间后,取出器物,用NaOH溶液洗涤至无Cl-。
①检测洗涤液中Cl-的方法是________________________________________ 。
②脱氯反应:FeOCl+OH-===FeO(OH)+Cl-。离子反应的本质是离子浓度的减小,比较FeOCl与FeO(OH)溶解度的大小:________________ 。
③Na2SO3还原FeO(OH)形成Fe3O4的离子方程式是_____SO32-+______FeO(OH)===______SO42-+____Fe3O4+______H2O(将反应补充完全)。________
(1)检测锈蚀产物
| 主要成分的化学式 | |||
| Fe3O4 | Fe2O3·H2O | FeO(OH) | FeOCl |
铁器在具有O2、
(2)分析腐蚀原理:一般认为,铁经过了如下腐蚀循环。
Ⅰ.Fe转化为Fe2+。
Ⅱ. FeO(OH)和Fe2+反应形成致密的Fe3O4保护层,Fe2+的作用是
a.氧化剂 b.还原剂 c.既不是氧化剂也不是还原剂
(3)研究发现,Cl-对铁的腐蚀会造成严重影响。化学修复:脱氯、还原,形成Fe3O4保护层,方法如下:
将铁器浸没在盛有0.5 mol·L-1 Na2SO3、0.5 mol·L-1 NaOH溶液的容器中,缓慢加热至60~90 ℃。一段时间后,取出器物,用NaOH溶液洗涤至无Cl-。
①检测洗涤液中Cl-的方法是
②脱氯反应:FeOCl+OH-===FeO(OH)+Cl-。离子反应的本质是离子浓度的减小,比较FeOCl与FeO(OH)溶解度的大小:
③Na2SO3还原FeO(OH)形成Fe3O4的离子方程式是_____SO32-+______FeO(OH)===______SO42-+____Fe3O4+______H2O(将反应补充完全)。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】H2O2是重要的化学试剂,在实验室和实际生产中应用广泛。
(1)H2O2有一定的还原性,能使酸性KMnO4溶液褪色。
①写出反应的离子方程式:______________ 。
②实验室常用酸性KMnO4标准液测定溶液中H2O2的浓度,酸性KMnO4溶液应盛放在___________ (填“酸式”或“碱式”)滴定管中,判断到达滴定终点的现象是___________ 。
(2)①我们知道,稀硫酸不与铜反应,但在稀硫酸中加入H2O2后,则可使铜顺利溶解,写出该反应的离子方程式:___________ 。
②在“海带提碘”的实验中,利用酸性H2O2得到碘单质的离子方程式是___________ 。
③利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥Cr(Ⅲ)的处理工艺流程如图:
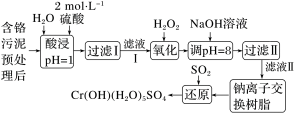
已知:硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。H2O2的作用是将滤液Ⅰ中的Cr3+转化为 ,写出此反应的离子方程式:
,写出此反应的离子方程式: ___________ 。
(3)H2O2是一种二元弱酸,写出其第一步电离的方程式:___________ ,它与过量的Ba(OH)2反应的化学方程式为________________ 。
(1)H2O2有一定的还原性,能使酸性KMnO4溶液褪色。
①写出反应的离子方程式:
②实验室常用酸性KMnO4标准液测定溶液中H2O2的浓度,酸性KMnO4溶液应盛放在
(2)①我们知道,稀硫酸不与铜反应,但在稀硫酸中加入H2O2后,则可使铜顺利溶解,写出该反应的离子方程式:
②在“海带提碘”的实验中,利用酸性H2O2得到碘单质的离子方程式是
③利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥Cr(Ⅲ)的处理工艺流程如图:

已知:硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。H2O2的作用是将滤液Ⅰ中的Cr3+转化为
 ,写出此反应的离子方程式:
,写出此反应的离子方程式: (3)H2O2是一种二元弱酸,写出其第一步电离的方程式:
您最近一年使用:0次

 2Na2S+
2Na2S+

