医学上常用酸性高锰酸钾溶液和草酸溶液的反应来测定血钙的含量。回答下列问题:
( ) H++( ) MnO4-+( ) H2C2O4→( ) CO2↑+ ( ) Mn2++( ) ____
(1)配平以上离子方程式,并在横线中填上所需的微粒。
(2)该反应中的还原剂是_____________ (填化学式)。
(3)反应转移了0.4 mol电子,则消耗KMnO4的物质的量为_________ mol。
(4)测定血钙含量的方法是:取2.0mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①稀硫酸溶解CaC2O4沉淀的化学方程式是__________________________ 。
②溶解沉淀时______ (填“能”或“不能”)用稀盐酸,原因是________________ 。
③若消耗了1.0×10-4 mol·L-1的KMnO4溶液20.00 mL,则100 mL该血液中含钙_____ g。
(5)草酸系统命名为乙二酸,请写出乙二酸的结构简式_____________________ 。
(6)已知:Ka1(H2C2O4)=5.9×10—2,Ka2(H2C2O4)=6.4×10—5;Ka(HF)=3.53×10—4,请写出足量草酸(H2C2O4)与NaF溶液反应的化学方程式:______ 。
(1)配平以上离子方程式,并在横线中填上所需的微粒。
(2)该反应中的还原剂是
(3)反应转移了0.4 mol电子,则消耗KMnO4的物质的量为
(4)测定血钙含量的方法是:取2.0mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①稀硫酸溶解CaC2O4沉淀的化学方程式是
②溶解沉淀时
③若消耗了1.0×10-4 mol·L-1的KMnO4溶液20.00 mL,则100 mL该血液中含钙
(5)草酸系统命名为乙二酸,请写出乙二酸的结构简式
(6)已知:Ka1(H2C2O4)=5.9×10—2,Ka2(H2C2O4)=6.4×10—5;Ka(HF)=3.53×10—4,请写出足量草酸(H2C2O4)与NaF溶液反应的化学方程式:
更新时间:2019-10-18 08:07:15
|
相似题推荐
【推荐1】回答下列问题
(1)在 、
、 、
、 、
、 、
、 、
、 中,只有氧化性的是
中,只有氧化性的是_____ ,只有还原性的是_____ ,既有氧化性又有还原性的是_____ 。
(2)某同学写出以下三个化学方程式(未配平):
①
②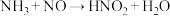
③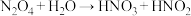
其中你认为一定不可能实现的是_____ 。
(3)下列三个氧化还原反应中,氧化性最强的物质是_____ 。(填化学式)
①
②
③ (浓)
(浓)
若溶质中 与
与 共存,为了氧化
共存,为了氧化 而
而 不被氧化,除单质外,还应用上述反应中的
不被氧化,除单质外,还应用上述反应中的_____ 作氧化剂。
(4)用双线桥标出方程式 中电子转移的方向和数目
中电子转移的方向和数目_____ ,并指出氧化产物与还原产物的质量比_____ 。
(1)在
 、
、 、
、 、
、 、
、 、
、 中,只有氧化性的是
中,只有氧化性的是(2)某同学写出以下三个化学方程式(未配平):
①

②
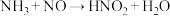
③
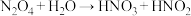
其中你认为一定不可能实现的是
(3)下列三个氧化还原反应中,氧化性最强的物质是
①

②

③
 (浓)
(浓)
若溶质中
 与
与 共存,为了氧化
共存,为了氧化 而
而 不被氧化,除单质外,还应用上述反应中的
不被氧化,除单质外,还应用上述反应中的(4)用双线桥标出方程式
 中电子转移的方向和数目
中电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】工业上利用电解饱和食盐水生产氯气(Cl2)、烧碱和氢气的化学方程式是:2NaCl + 2H2O 2NaOH + Cl2↑+ H2↑
2NaOH + Cl2↑+ H2↑
(1)用双线桥表示出电子转移的方向和数目______________ ,题干中反应改写成离子方程式是___________________________________
(2)电解食盐水的过程中,氧化产物是__________________________________
(3)电解食盐水要求对粗食盐水进行精制,以除去粗食盐水中含有的泥沙和SO42-、Ca2+,Mg2+等杂质离子。精制时依次加入氯化钡溶液、纯碱、烧碱,充分反应后过滤,在滤液中加入盐酸中和至中性。盐酸与滤液反应的离子方程式:____________________________
 2NaOH + Cl2↑+ H2↑
2NaOH + Cl2↑+ H2↑(1)用双线桥表示出电子转移的方向和数目
(2)电解食盐水的过程中,氧化产物是
(3)电解食盐水要求对粗食盐水进行精制,以除去粗食盐水中含有的泥沙和SO42-、Ca2+,Mg2+等杂质离子。精制时依次加入氯化钡溶液、纯碱、烧碱,充分反应后过滤,在滤液中加入盐酸中和至中性。盐酸与滤液反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)0.5 mol Na2CO3中含有___________ 个Na+。
(2)质量都是50 g的 HCl、NH3、CO2、O2四种气体,在相同温度和相同压强条件下,体积最大的是____________ 。
(3)配制90 mL 0.1 mol/L CuSO4溶液,需要CuSO4·5H2O________ g,下列操作会使所配溶液浓度偏低的是___________ 。
A.容量瓶洗涤干净后未干燥
B.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
C.定容时俯视刻度线 D.烧杯和玻璃棒未洗涤
(4)氧化还原反应3S+6KOH=2K2S+K2SO3+3H2O中,氧化剂与还原剂的物质的量之比为_____________ ,若反应中消耗了0.6molS,则反应中转移的电子为________ mol。
(2)质量都是50 g的 HCl、NH3、CO2、O2四种气体,在相同温度和相同压强条件下,体积最大的是
(3)配制90 mL 0.1 mol/L CuSO4溶液,需要CuSO4·5H2O
A.容量瓶洗涤干净后未干燥
B.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
C.定容时俯视刻度线 D.烧杯和玻璃棒未洗涤
(4)氧化还原反应3S+6KOH=2K2S+K2SO3+3H2O中,氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)K2FeO4是一种重要的净水剂,可用下列方法制得:2Fe(OH)3+3Cl2+10KOH=2K2FeO4+6KCl+8H2O,在该反应中,还原剂是________________ 。当反应中有1molK2FeO4生成时,消耗的Cl2在标况下的体积为_______________ ,转移电子的数目为________________ 。
(2)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式____________
(3)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:______________
(4)将钠、镁、铝各0.3mol分别放入100mL1mol·L-1的盐酸中,同温同压下产生的气体体积比是________________
(5)现有①铝 ②SiO2 ③熔融NaCl ④稀硫酸 ⑤KOH固体 ⑥FeSO4溶液 ⑦NH3 ⑧新制备的氢氧化铁胶体分散系 ⑨HCl ⑩Na2O2上述物质属于非电解质的有___________ (填序号)
(2)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式
(3)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:
(4)将钠、镁、铝各0.3mol分别放入100mL1mol·L-1的盐酸中,同温同压下产生的气体体积比是
(5)现有①铝 ②SiO2 ③熔融NaCl ④稀硫酸 ⑤KOH固体 ⑥FeSO4溶液 ⑦NH3 ⑧新制备的氢氧化铁胶体分散系 ⑨HCl ⑩Na2O2上述物质属于非电解质的有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】根据所学知识,回答下列问题:
(1)高铁酸钠(Na2FeO4)可作为高效、多功能水处理剂,其摩尔质量是__________ 。高铁酸钠可与水反应生成Fe(OH)3胶体、氢氧化钠和氧气,写出相应的离子方程式:_____________ 。
(2)戴维通过电解法首先制得了金属钠,随后几十年内,工业上采用铁粉和氢氧化钠高温熔融的方法制得钠蒸气,同时获得Fe3O4和氢气。写出该反应的化学方程式_____________ ,该反应中属于电解质但不属于氧化物的物质是________________ (填化学式),若制得22.4L(折算为标准状况下)钠蒸气,转移电子的数目为________________ 。
(3)漂白粉常用于饮水、污水、排泄物及被污染的环境消毒,其主要成分是氯化钙和次氯酸钙[Ca(ClO)2],有效成分为次氯酸钙。为测得某漂白粉的有效成分含量,称取A g漂白粉样品溶解,往所得溶液中通入CO2至不再产生沉淀为止,反应的化学方程式为Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO,若反应生成次氯酸(HClO)的物质的量为Kmol,则该漂白粉中有效成分的质量分数为___________ %(用含A、K的式子表示)。
(1)高铁酸钠(Na2FeO4)可作为高效、多功能水处理剂,其摩尔质量是
(2)戴维通过电解法首先制得了金属钠,随后几十年内,工业上采用铁粉和氢氧化钠高温熔融的方法制得钠蒸气,同时获得Fe3O4和氢气。写出该反应的化学方程式
(3)漂白粉常用于饮水、污水、排泄物及被污染的环境消毒,其主要成分是氯化钙和次氯酸钙[Ca(ClO)2],有效成分为次氯酸钙。为测得某漂白粉的有效成分含量,称取A g漂白粉样品溶解,往所得溶液中通入CO2至不再产生沉淀为止,反应的化学方程式为Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO,若反应生成次氯酸(HClO)的物质的量为Kmol,则该漂白粉中有效成分的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】G、Q、X、Y、Z均为氯的含氧化合物。我们不了解它们的化学式,但知道它们在一定条件下具有如下转化关系(未配平)
①G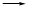 Q+NaCl
Q+NaCl
②Q +H2O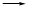 X+H2
X+H2
③Y+NaOH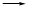 G+Q+H2O
G+Q+H2O
④Z+NaOH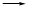 Q+X+H2O
Q+X+H2O
(1)这五种化合物中氯的化合价由高到低的顺序是______________ ;
(2)臭氧与二氧化氯作用,可以得到红色油状的六氧化二氯Cl2O6,遇有机物会爆炸。它与氢氧化钠溶液反应可得到氯的两种含氧酸盐,其离子方程式是:_________________ 。
(3)亚氯酸钠NaClO2,可以作漂白剂,在常温下不见光可以保存约1年。但在酸性条件下因为生成亚氯酸而发生分解反应:HClO2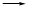 ClO2+H++Cl―+H2O,分解时,刚加入硫酸时的反应很慢,随后突然迅速放出气态的二氧化氯。写出配平的化学方程式
ClO2+H++Cl―+H2O,分解时,刚加入硫酸时的反应很慢,随后突然迅速放出气态的二氧化氯。写出配平的化学方程式____________________ 。
如果有2molHClO2发生反应,则转移电子的个数是_____ ,后期反应速率迅速加快的原因是______ 。
①G
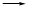 Q+NaCl
Q+NaCl ②Q +H2O
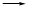 X+H2
X+H2③Y+NaOH
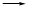 G+Q+H2O
G+Q+H2O ④Z+NaOH
 Q+X+H2O
Q+X+H2O(1)这五种化合物中氯的化合价由高到低的顺序是
(2)臭氧与二氧化氯作用,可以得到红色油状的六氧化二氯Cl2O6,遇有机物会爆炸。它与氢氧化钠溶液反应可得到氯的两种含氧酸盐,其离子方程式是:
(3)亚氯酸钠NaClO2,可以作漂白剂,在常温下不见光可以保存约1年。但在酸性条件下因为生成亚氯酸而发生分解反应:HClO2
 ClO2+H++Cl―+H2O,分解时,刚加入硫酸时的反应很慢,随后突然迅速放出气态的二氧化氯。写出配平的化学方程式
ClO2+H++Cl―+H2O,分解时,刚加入硫酸时的反应很慢,随后突然迅速放出气态的二氧化氯。写出配平的化学方程式如果有2molHClO2发生反应,则转移电子的个数是
| A.酸使亚氯酸的氧化性增强 | B.溶液中的氢离子还起了催化作用 |
| C.溶液中的氯离子还起了催化作用 | D.逸出的气体使反应生成物的浓度降低 |
您最近一年使用:0次
【推荐2】国家实施“青山绿水”工程,加大力度研究脱硫及脱氮处理技术意义重大。回答下列问题:
(1)某工厂拟综合处理工业废气(主要含 、
、 、
、 、NO、CO),主要采用石灰乳、NaOH溶液等试剂。下列物质中,属于电解质的是
、NO、CO),主要采用石灰乳、NaOH溶液等试剂。下列物质中,属于电解质的是___________ (填序号)。
① ②
② ③CO ④石灰乳 ⑤NaOH
③CO ④石灰乳 ⑤NaOH
(2)写出少量 通入NaOH溶液的离子方程式:
通入NaOH溶液的离子方程式:___________ 。
(3)可用碱液吸收氮氧化物( )
)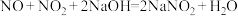 、
、
 。已知:NO与氢氧化钠溶液不反应。根据上述原理判断,将下列气体通入过量NaOH溶液中,反应结束后一定有剩余的是
。已知:NO与氢氧化钠溶液不反应。根据上述原理判断,将下列气体通入过量NaOH溶液中,反应结束后一定有剩余的是___________ (填字母)。
A.1mol NO和4mol B.1mol
B.1mol  和7mol NO C.6mol NO和4mol
和7mol NO C.6mol NO和4mol 
(4)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是硫酸。以下是二氧化硫形成酸雨的两种途径:
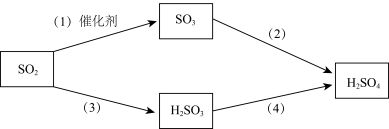
①请写出(1)中发生反应的化学方程式:___________ 。
②你认为减少酸雨产生的途径可采用的措施是___________ (填字母)。
A.少用煤作燃料 B.把工厂烟囱造高 C.燃料脱硫 D.在已酸化的土壤中加石灰 E.开发新能源
(5)利用 溶液可脱除二氧化硫,配平下列离子方程式:
溶液可脱除二氧化硫,配平下列离子方程式:_________

(6) 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,将烟气中
催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,将烟气中 转化为无污染气体。当
转化为无污染气体。当 与NO的物质的量之比为1:1时,每转化1mol该氮氧化物混合气体,需要消耗标准状况下
与NO的物质的量之比为1:1时,每转化1mol该氮氧化物混合气体,需要消耗标准状况下 的体积为
的体积为___________ L。
(1)某工厂拟综合处理工业废气(主要含
 、
、 、
、 、NO、CO),主要采用石灰乳、NaOH溶液等试剂。下列物质中,属于电解质的是
、NO、CO),主要采用石灰乳、NaOH溶液等试剂。下列物质中,属于电解质的是①
 ②
② ③CO ④石灰乳 ⑤NaOH
③CO ④石灰乳 ⑤NaOH(2)写出少量
 通入NaOH溶液的离子方程式:
通入NaOH溶液的离子方程式:(3)可用碱液吸收氮氧化物(
 )
)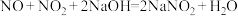 、
、
 。已知:NO与氢氧化钠溶液不反应。根据上述原理判断,将下列气体通入过量NaOH溶液中,反应结束后一定有剩余的是
。已知:NO与氢氧化钠溶液不反应。根据上述原理判断,将下列气体通入过量NaOH溶液中,反应结束后一定有剩余的是A.1mol NO和4mol
 B.1mol
B.1mol  和7mol NO C.6mol NO和4mol
和7mol NO C.6mol NO和4mol 
(4)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是硫酸。以下是二氧化硫形成酸雨的两种途径:

①请写出(1)中发生反应的化学方程式:
②你认为减少酸雨产生的途径可采用的措施是
A.少用煤作燃料 B.把工厂烟囱造高 C.燃料脱硫 D.在已酸化的土壤中加石灰 E.开发新能源
(5)利用
 溶液可脱除二氧化硫,配平下列离子方程式:
溶液可脱除二氧化硫,配平下列离子方程式:
(6)
 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,将烟气中
催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,将烟气中 转化为无污染气体。当
转化为无污染气体。当 与NO的物质的量之比为1:1时,每转化1mol该氮氧化物混合气体,需要消耗标准状况下
与NO的物质的量之比为1:1时,每转化1mol该氮氧化物混合气体,需要消耗标准状况下 的体积为
的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】根据信息完成下列方程式。
(1)KMnO4氧化废水中Mn2+生成MnO2的离子方程式为_______ 。
(2)NaAlH4与水发生氧化还原反应的化学方程式为_______ 。
(3)PbO2可由PbO与次氯酸钠溶液反应制得,该反应的离子方程式为_______ 。
(4)NaClO溶液与Ag反应的产物为AgCl、NaOH和O2,该反应的化学方程式为________ 。
(5)在45~50℃时向CuCl悬浊液中持续通入空气,得到碱式氯化铜[Cu2(OH)2Cl2•3H2O],该反应的化学方程式为________ 。
(1)KMnO4氧化废水中Mn2+生成MnO2的离子方程式为
(2)NaAlH4与水发生氧化还原反应的化学方程式为
(3)PbO2可由PbO与次氯酸钠溶液反应制得,该反应的离子方程式为
(4)NaClO溶液与Ag反应的产物为AgCl、NaOH和O2,该反应的化学方程式为
(5)在45~50℃时向CuCl悬浊液中持续通入空气,得到碱式氯化铜[Cu2(OH)2Cl2•3H2O],该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】人们日常生产生活与化学有着紧密的联系。
(1)现有常温下pH=2的盐酸(甲)和pH=2的醋酸溶液(乙),请根据下列操作回答:
①常温下, 溶液加水稀释,下列数值一定变小的是
溶液加水稀释,下列数值一定变小的是___________ (填字母)。
A.c(H+) B. C.
C.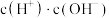 D.
D.
②取10mL乙溶液,加入少量无水CH3COONa固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中 的值将
的值将___________ (填“增大”“减小”或“无法确定”)。
③相同条件下,取等体积的甲、乙两溶液,分别与0.1mol/LNaOH溶液反应,消耗NaOH溶液的体积(甲)___________ (乙)(填“>”“<”或“=”)。
(2)已知水在25℃和100℃时,其电离平衡曲线如图所示:
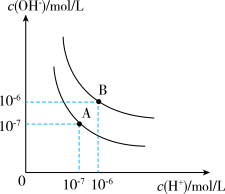
25℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,所得混合溶液的pH=7,则NaOH溶液与硫酸溶液的体积比为___________ 。
(3)已知:在25℃,有关弱电解质的电离平衡常数如下表有下表:
①CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为___________ 。
②同浓度的CH3COO-、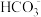 、
、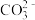 、ClO-结合H+的能力由强到弱的顺序为
、ClO-结合H+的能力由强到弱的顺序为___________ 。
③将少量CO2气体通入NaClO溶液中,写出反应的离子方程式:___________ 。
④将SO2通入该氨水中,当c(OH-)降至 时,溶液中的
时,溶液中的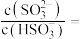
___________ 。
⑤下列微粒在溶液中不能大量共存的是___________ 。
A. 、
、 B.ClO-、
B.ClO-、 C.
C. 、
、 D.HClO、
D.HClO、
(1)现有常温下pH=2的盐酸(甲)和pH=2的醋酸溶液(乙),请根据下列操作回答:
①常温下,
 溶液加水稀释,下列数值一定变小的是
溶液加水稀释,下列数值一定变小的是A.c(H+) B.
 C.
C.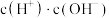 D.
D.
②取10mL乙溶液,加入少量无水CH3COONa固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中
 的值将
的值将③相同条件下,取等体积的甲、乙两溶液,分别与0.1mol/LNaOH溶液反应,消耗NaOH溶液的体积(甲)
(2)已知水在25℃和100℃时,其电离平衡曲线如图所示:

25℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,所得混合溶液的pH=7,则NaOH溶液与硫酸溶液的体积比为
(3)已知:在25℃,有关弱电解质的电离平衡常数如下表有下表:
| 弱电解质 | 电离常数(Ka) | |
| NH3·H2O | Kb=1.8×10-5 | |
| HClO | Kₐ=4.7×10-8 | |
| H2CO3 | Ka1=4.2×10-7 | Ka2=5.6×10-11 |
| H2SO3 | Ka1=1.54×10-2 | Ka2=1.02×10-7 |
| CH3COOH | Kₐ=1.7×10-5 | |
②同浓度的CH3COO-、
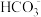 、
、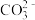 、ClO-结合H+的能力由强到弱的顺序为
、ClO-结合H+的能力由强到弱的顺序为③将少量CO2气体通入NaClO溶液中,写出反应的离子方程式:
④将SO2通入该氨水中,当c(OH-)降至
 时,溶液中的
时,溶液中的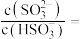
⑤下列微粒在溶液中不能大量共存的是
A.
 、
、 B.ClO-、
B.ClO-、 C.
C. 、
、 D.HClO、
D.HClO、
您最近一年使用:0次
填空题
|
适中
(0.65)
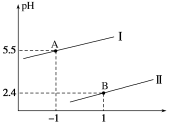
【推荐2】已知亚磷酸(H3PO3)为二元弱酸,常温下,向某浓度的亚磷酸溶液中逐滴加入一定物质的量浓度的KOH溶液,混合溶液的pH与离子浓度的关系如图所示。
lg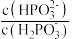 或lg
或lg
(1)写出亚磷酸电离的方程式:___________ 、___________ 。
(2)表示pH与lg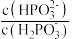 的变化关系的曲线是
的变化关系的曲线是___________ (填“Ⅰ”或“Ⅱ”)。
(3)根据图象计算亚磷酸的Ka1=___________ 。

lg
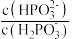 或lg
或lg
(1)写出亚磷酸电离的方程式:
(2)表示pH与lg
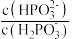 的变化关系的曲线是
的变化关系的曲线是(3)根据图象计算亚磷酸的Ka1=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】研究化学反应意义重大,请就下列现象和实质回答问题。
(1) 可用作白色颜料和阻燃剂等。在实验室中可利用
可用作白色颜料和阻燃剂等。在实验室中可利用 的水解反应制取
的水解反应制取 (
( 的水解分三步进行,中间产物有
的水解分三步进行,中间产物有 等),写出
等),写出 水解生成
水解生成 的水解反应方程式
的水解反应方程式______ 。
(2)次磷酸( )是一种弱酸,
)是一种弱酸, 溶液和足量
溶液和足量 溶液混合,所得溶液中阴离子只有
溶液混合,所得溶液中阴离子只有 、
、 两种。写出
两种。写出 溶液与
溶液与 溶液恰好完全中和的溶液中各离子浓度由大到小的顺序为
溶液恰好完全中和的溶液中各离子浓度由大到小的顺序为_______ 。
(3)已知 与
与 溶液反应生成
溶液反应生成 ,与稀硫酸反应生成
,与稀硫酸反应生成 ,写出
,写出 在水中的两种电离方程式
在水中的两种电离方程式_______ 、_______ 。
(4)一定温度下,用水吸收 气体时,溶液中水的电离平衡
气体时,溶液中水的电离平衡_______ 移动(填“向左”“向右”或“不”);若得到 的
的 溶液,试计算溶液中
溶液,试计算溶液中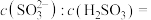
_______ (已知该温度下, 的电离常数:
的电离常数: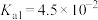 ,
, )。
)。
(5)某温度下, 的盐酸中
的盐酸中 ;该温度下
;该温度下 的
的 溶液与
溶液与 的
的 溶液混合后溶液的
溶液混合后溶液的 ,则
,则 与
与 溶液的体积比为
溶液的体积比为_______ 。
(6) 时,若向
时,若向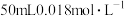 的
的 溶液中加入
溶液中加入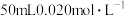 的盐酸,混合后溶液中的
的盐酸,混合后溶液中的 为
为______  (
( 时,
时, )。
)。
(1)
 可用作白色颜料和阻燃剂等。在实验室中可利用
可用作白色颜料和阻燃剂等。在实验室中可利用 的水解反应制取
的水解反应制取 (
( 的水解分三步进行,中间产物有
的水解分三步进行,中间产物有 等),写出
等),写出 水解生成
水解生成 的水解反应方程式
的水解反应方程式(2)次磷酸(
 )是一种弱酸,
)是一种弱酸, 溶液和足量
溶液和足量 溶液混合,所得溶液中阴离子只有
溶液混合,所得溶液中阴离子只有 、
、 两种。写出
两种。写出 溶液与
溶液与 溶液恰好完全中和的溶液中各离子浓度由大到小的顺序为
溶液恰好完全中和的溶液中各离子浓度由大到小的顺序为(3)已知
 与
与 溶液反应生成
溶液反应生成 ,与稀硫酸反应生成
,与稀硫酸反应生成 ,写出
,写出 在水中的两种电离方程式
在水中的两种电离方程式(4)一定温度下,用水吸收
 气体时,溶液中水的电离平衡
气体时,溶液中水的电离平衡 的
的 溶液,试计算溶液中
溶液,试计算溶液中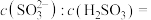
 的电离常数:
的电离常数: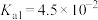 ,
, )。
)。(5)某温度下,
 的盐酸中
的盐酸中 ;该温度下
;该温度下 的
的 溶液与
溶液与 的
的 溶液混合后溶液的
溶液混合后溶液的 ,则
,则 与
与 溶液的体积比为
溶液的体积比为(6)
 时,若向
时,若向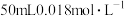 的
的 溶液中加入
溶液中加入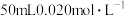 的盐酸,混合后溶液中的
的盐酸,混合后溶液中的 为
为 (
( 时,
时, )。
)。
您最近一年使用:0次

 Al2O3+2Fe
Al2O3+2Fe

